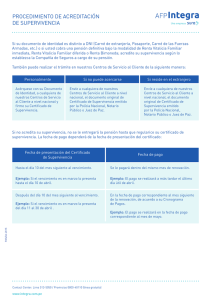
INFORME DEL V SEMINARIO DE LA FUNDACIÓN ECO SOBRE
Anuncio

1 INFORME DEL V SEMINARIO DE LA FUNDACIÓN ECO SOBRE BENEFICIO CLÍNICO DEL TRATAMIENTO MÉDICO: OBJETIVOS Y RESULTADOS EN CANCER, Transcriptor: Dr. J. A. Moreno Nogueira 2 3 INTRODUCCIÓN AL V SEMINARIO. El Prof. D. Joaquín Poch Broto Presidente de la RANM abrió el acto destacando la importancia del contenido del Seminario, cediendo la palabra al Dr. Carlos Camps Presidente de la Fundación ECO que agradece la acogida un año mas por parte de la Academia al permitir la celebración de este acto científico. Destaca la importancia del tema: Beneficio clínico en cáncer del tratamiento médico en la era de los nuevos fármacos. Señala que los parámetros habituales de medición de este beneficio requieren actualizarse para seleccionar adecuadamente a los pacientes, dado el elevado coste de las terapias dirigidas. El Dr. Vicente Guillen en nombre de los coordinadores del Seminario destaca el impacto social que significa el cáncer, por su frecuencia, morbimortalidad, costes terapéuticos etc. Insiste en la necesidad de revisar en profundidad lo que se conoce como beneficio clínico al ser una demanda real de los pacientes. MESA 1. MAGNITUD DEL BENEFICIO EN LAS TERAPIA INNOVADORAS. Presiden Dr. A. Antón y Dr. M. Provencio. 1.- ¿Cómo medimos el beneficio clínico y como cuantificamos los resultados? El ponente de la primera intervención fue el Dr. Emilio Esteban. Destaca la importancia de la medición del beneficio clínico, pero esto no será igual para el tumor localizado cuyos objetivos son la curación y en segundo lugar la supervivencia libre de enfermedad; mientras que en el tumor avanzado o diseminado la mayoría no curables, los objetivos son la supervivencia global o libre de progresión, pero sobre todo la mejoría sintomáticas o de la calidad de vida, factores que con frecuencia son olvidados en la practica clínica, siendo probablemente lo mas importante para el paciente. Tipos de Beneficio • Tumor Localizado: – Objetivo curación – Mejorar la supervivencia Libre de recurrencia • Tumor avanzado: – La mayoría no son curables y/o asociados a síntomas con influencia en la calidad de vida – Objetivo mejorar: • La Supervivencia (libre progresión/Global) • La Supervivencia libre de empeoramiento clínico/Calidad de vida Los ensayos en fase III sus objetivos son la supervivencia pero como ha dicho es poco relevante para un paciente de forma individual. Los ensayos en fase II el objetivo es la respuesta como parámetro clínico más usado y que se relaciona con el uso de una medicación, pero la sensación es si eso es realmente útil para el paciente. Más recientemente está surgiendo la valoración del alivio sintomático o mejoría de la calidad de vida que es lo que le interesa al paciente y que adquiere relevancia en los 4 estudios de estrategias terapéuticas equivalentes, con frecuencia con fines de registro de un determinado fármaco. El ponente hace un análisis histórico de los objetivos utilizados en Oncología para la valoración de resultados o beneficios. En la década de los años 1950s lo esencial que se valoraba eran las respuestas y era suficiente para que la FDA aprobara un fármaco. En la década de los 1980s la FDA incorpora para la aprobación de fármacos la mejoría en la supervivencia global o una mejoría sintomática o beneficio clínico. En la década de 1990s la FDA incorpora la valoración de la supervivencia libre de enfermedad (aprobación del tamoxifeno) y supervivencia libre de progresión (aprobación del cisplatino en cáncer de ovario). Sustituto-Subrogado (Surrogate) • • • • Supervivencia Libre de Progresión/Enfermedad Respuestas Objetivas (RO) Calidad de vida, alivio sintomático Predictores de respuesta (enriquecer la muestra) Ocaña A et al. J Clin Oncol 2010; 28(24)e420-e421 En la actualidad los médicos y especialistas se inclinan por valorar los denominados “surrogate” cuyos conceptos se basan en intentar lograr el objetivo primario para los pacientes que es el beneficio clínico. Comprenden la valoración de la supervivencia libre de progresión/enfermedad, respuestas objetivas, calidad de vida y alivio sintomático y más recientemente se han incorporado los predictores de respuesta. Estos sustitutos o “surrogate” tienen una clara ventaja: más rapidez en su análisis y acceso a drogas activas. Requiere menor número de pacientes/eventos. Clara relación entre agente y evento analizado y ventajas económicas Las desventajas serian la ausencia de una clara validación y dudosa influencia o correlación con la supervivencia global. Hasta ahora se ha seguido una valoración morfológica de la respuesta en las lesiones medibles (RC, RP, EE y EP), valoración que son el fundamento de los criterios RECITS que ya van por la segunda edición. Pero estos criterios objetivos de respuesta tienen un evidente grado de subjetividad por lo que se puede hablar de una serie de desventajas: necesidad de una lesión medible, variabilidad entre los observadores, el corte en la medida de respuesta es arbitrario, variabilidad según el momento en que se hace la evaluación lo que también es arbitrario y ausencia de información en las variaciones biológicas, vasculares o metabólicas que intervienen en la respuesta y supervivencia de los pacientes. Un estudio publicado en The Oncology de abril 2014 presenta un análisis de la relación entre los cambios en el tamaño del tumor y los resultados clínicos en pacientes tratados con anti-VEGF. Este análisis concluyó que la reducción ≥ 10% del tamaño de la lesión diana según criterios RECIST (respondedores) en la primera exploración tempana se asoció con resultados significativamente mejores, en comparación con la de los no respondedores que eran aquellos que no logran la reducción del 10%. El tiempo hasta fracaso del tratamiento (TFT) fue de 8,4 meses frente a 4,1 meses, y la 5 supervivencia global fue de 35 meses frente a 15 meses, ambos con p <0,01. Por el contrario, el umbral de RECIST -30% en la primera exploración no predice el resultado del paciente (TFT de 6,9 meses frente a 5,5 meses). Estos datos sugirieron que una reducción >10% en primera exploración podrían ser utilizado para las decisiones de tratamiento en cuanto a si se deben continuar las terapias anti-VEGF. Diferentes estudios sugieren que la modificación de los criterios de respuesta para capturar y clasificar las respuestas menores puede proporcionar una lectura más sensible del efecto terapéutico y potencialmente mejorar la precisión de la evaluación precoz de las drogas. La búsqueda del punto de corte óptimo puede ser un reto, ya que el umbral puede ser diferente para los mismos agentes en diferentes indicaciones o para diferentes agentes en la misma indicación. Las limitaciones técnicas, como la variabilidad de medida, también pueden limitar la elección de los umbrales que se pueden adoptar. Se están realizando esfuerzos por el comité RECIST para expandir la base de datos e incluir los grandes ensayos clínicos aleatorios de agentes dirigidos. Un paso mas es una valoración biológica, molecular, dinámica y metabólica mediante estudios que utilizan la tomografía por emisión de positrones con fluorodeoxiglucosa (FDG-PET), con el plan de evaluar y actualizar las directrices y criterios para cumplir con las necesidades de desarrollo de fármacos y atención de los pacientes en la era de las nuevas terapias. Un estudio en cáncer de pulmón avanzado tratados con erlotinib y utilizando como metodología de valoración el PET-TAC a las tres semanas, una reducción del >10% tiene beneficios significativos en relación a la supervivencia global y en definitiva al beneficio clínico de los pacientes, frente a los que no lograron una reducción de ese 10%. Existen clasificaciones validadas que miden precisamente este tipo de valoraciones metabólicas y en relación con las puramente morfológicas. Criterios morfológicos y Metabólicos para el tratamiento y valoración de la respuesta (2) (1) 1. Choi H et al. J Clin Oncol 2007. 25: 1753-1759 2. Young H et al. Eur J Cancer 1999. 35: 1773-1782 Estos hechos ponen de manifiesto que la observación de la reducción del tumor por debajo del umbral de los criterios RECIST puede estar asociada con un beneficio clínico 6 significativo, y que la flexibilidad en el cambio de tamaño tumoral considerada en las modificaciones futuras de los criterios de respuesta. debe ser Un hecho que con frecuencia los oncólogos olvidan es mirar la cara de los pacientes y preguntarles por su calidad de vida que es una interpretación subjetiva, pero que valora de forma general que siente y le pasa al paciente e incluso valora el medio donde está el paciente. Esta valoración de calidad de vida puede hacerse simplemente con herramientas como el PS o con una simple escala de valoración analógica o de una forma más compleja como el Q-TWIST o FACT-C. Calidad de vida (CDV) Métodos de medición Concepto • Experiencia sensorial y emocional agradable o no • Escalas de estado general (Karnofsky, WHO, ECOG) • Multidimensional: componentes físicos, emocionales, sociales y cognitivos • Escalas analógicas visuales • FLIC (Funcional Living Index of Cancer) • EORTC (QLQ-C30)(Quality of life questionaire- Core 30) • FACT-G (Functional Assessment of Cancer) • Q-TWIST (CDV ajustada x tiempo sin síntomas ni toxicidad) • • Requiere una evaluación subjetiva del propio paciente Concepto no estático; requiere varias mediciones y un momento adecuado Medidas que son dinámicas y que requieren hacerse varias veces en el curso evolutivo del paciente. Son valoraciones con transformación numérica, las dos primeras de una forma muy simple y mucho más complejas p.e. Q-TWIS. Es una forma de hacer objetiva numéricamente lo que siente el paciente y en definitiva la calidad de vida. Un estudio en cáncer de pulmón tratado con Gefitinib 500 mg vs. 250 mg, tenía como objetivo principal la calidad de vida. En dicho estudio se muestra la dosis de Gefitinib 250 mg es una dosis adecuada para el tratamiento del cáncer de pulmón, pero sobre todo el estudio nos señala que los pacientes que responden tienen una mejor calidad de vida y además una mejor supervivencia global. Este trabajo nos dice que la valoración de la calidad de vida es un buen sustituto de otros parámetros como la respuesta y supervivencia. En una diapositiva el ponente ha recogido numerosos trabajos con diversos de tumores, sometidos a tratamientos comparativos, cuyo objetivo primario era la HR como medida de la magnitud del beneficio clínico expresado en forma de supervivencia libre de progresión o de la supervivencia global. Antes la medida era por el valor de “p”, pero eso incluía la probabilidad de falsos positivos, por lo que es mas fiable la HR. Su valor para la supervivencia global se sitúa en 0.75 y para la SLP en 050 - 0.60. 7 Magnitud del beneficio Clínico (δ) • Tamaño en la diferencia entre dos tratamientos en el endpoint pre-establecido • Historicamente era la significación estadística (p) • Actualmente se centra en la HR: – 3 meses (HR 0,75) para SG – 4-6 meses (HR 0,5) para SLP En la actualidad el objetivo de los trabajos es la HR como magnitud del beneficio clínico o de la supervivencia. En el trabajo FLEX que compara QT+Cetuximab vs. Cetuximab en pacientes con cáncer de pulmón, es una muestra de la no fiabilidad del valor de “p”. Este trabajo tenia como objetivo la SG con un HR de 0.80 y en el análisis estadístico dio un resultado significativo con una p=0.044 para Cetuximab, sin embargo no se cumplió la HR por lo que el estudio no encontró diferencias entre ambos brazos. Otra cosa distinta es cuando existe enriquecimiento o selección de los pacientes como ocurre en la combinación de dos trabajos LUX-Lung 3 y 6, donde hay enriquecimiento de pacientes por la presencia de mutación en EGFR y donde se comparaba Afitinib vs. Quimioterapia y cuyo objetivo primario era la SG. En el grupo con mutación la p=0.0001 y una HR de 0.59, por lo que resulta significativo para Afitinib. En el grupo sin mutación no existieron diferencias en SG (p=0.1600. HR 1.25). Relacionado con todo lo anterior es importante el análisis coste-utilidad de un agente en el tratamiento de los pacientes, se relaciona año de vida ajustado por calidad de vida (AVAC – QALY). La valoración por una entidad no oficial lo ha cifrado en 30.000 euros, por año de vida ganado, en relación con la riqueza del país, sin embargo en una encuesta realizada con 60 especialistas el 60% no están de acuerdo y que probablemente esta valoración llegara hasta los 100.000 - 160.000 euros. La conclusiones se resumen en el cuadro siguiente: Conclusiones • • • • El estándar de oro sigue siendo la Supervivencia, pero relacionada con: – CDV-alivio sintomático – Coste Sustitutos nuevos como la valoración metabólica o biológica de respuesta: – Más adecuados para terapia dirigida – Relación temprana con el beneficio clínico • Supervivencia • CDV y alivio sintomático Enriquecimiento de la población Magnitud del beneficio clínico (HR 0,5-0,75) Muchas gracias por la atención prestada. 8 2.- Magnitud del beneficio clínico en cáncer de mama. El ponente de esta intervención fue el Dr. Joan Albanell que destaca una publicación reciente del JCO (20 de abril de 2014) titulada “American Society of Clinical Oncology Perspective: Raising the Bar for Clinical Trials by Defining Clinically Meaningful Outcomes”. Señala que los ensayos clínicos sobre el cáncer se han dedicado para investigar agentes o regímenes en pacientes seleccionados para el estudio, selección basada principalmente en la histología del tumor y en las características clínicas. Este enfoque, cuando tiene éxito, con frecuencia solo detecta pequeñas mejoras en la supervivencia global (OS), probablemente reflejando el impacto de los agentes con una eficacia modesta en un subconjunto de la población del estudio que no es fácilmente identificable. Recientemente, las terapias dirigidas se administran a los pacientes seleccionados por biomarcadores lo que han producido mejoras sustanciales en los resultados en diversos tipos de cáncer. A medida que mejoramos nuestra capacidad para identificar las vías moleculares del cáncer, es razonable anticipar que los regímenes altamente eficaces, dirigidos molecularmente serán introducidos para su uso en pacientes que puedan ser identificados de manera prospectiva y con alta probabilidad de beneficiarse del tratamiento. Todo este proceso ha sido lento, costoso y empírico. Por todo ello los ensayos clínicos deben cambiar y adaptase a la nueva era molecular del tratamiento del cáncer. En este estudio se señala que el Comité de Investigación del Cáncer de ASCO, convocó cuatro grupos de trabajo para enfermedades específicas en el diseño de futuros ensayos clínicos que den lugar a resultados clínicamente significativos para los pacientes, es decir, mejorar significativamente la supervivencia, la calidad de la vida o ambos. Todos los grupos de trabajo seleccionaron como el criterio principal de valoración la SG, sin que ello signifique una disminución del valor de la supervivencia libre de progresión (PFS) y de otros criterios de valoración para las determinadas situaciones clínicas. Esto es especialmente cierto en los tipos de cáncer que a menudo producen síntomas relacionados con la enfermedad progresiva, por ejemplo, las metástasis óseas dolorosas, donde una prolongación significativa de la SLP puede representar una paliación significativa y una mejora de la calidad de vida. Por lo tanto, el uso de PFS como un punto final clínicamente significativo puede ser apropiado en la configuración particular de cada cáncer y de hecho, ha sido aceptado por las autoridades reguladoras en muchas ocasiones en la aprobación de fármacos. 9 En relación al diseño de ensayos clinicos de cáncer de mama, centraron el problema en subtipo triple negativo metastásico previamente no tratados, en 1ª línea, con una media de SG basal de 18 meses, consideraron que el objetivo primario seria un incremento de la SG de 4.5 a 6 meses, una HR de 0.75 – 0.80 y como objetivo secundario una SLP de 4 meses y una tasa de mejoría de la supervivencia al año del 63% al 71%. Los grupos de trabajo reconocieron las dificultades de valoración de la SG, tales como la necesidad de un seguimiento más prolongado y el potencial efecto de confusión de las terapias postestudio. Los grupos discutieron la necesidad de equilibrar los riesgos y beneficios de la terapia para definir un resultado clínicamente significativo en cada contexto clínico. Abriendo otras posibilidades, los ensayos clinicos pueden ser diseñados para que demuestren resultados clínicamente significativos sin afectar a la SG, pero con mucha menor toxicidad y no inferioridad de resultados en comparación con las terapias existentes. Un tema de discusiones del grupo de trabajo fue la calidad de vida, y todos estuvieron de acuerdo en que la calidad de vida es difícil de medir e interpretar, incluso utilizando instrumentos validados. Más recientemente el interés se ha desplazado a la carga de síntomas específicos del paciente y seria adecuado disponer de instrumentos validados para la evaluación de una serie de síntomas específicos relacionados con el cáncer. Los síntomas de los pacientes derivados de la progresión del cáncer y la tolerabilidad de las toxicidades relacionadas con el tratamiento son de vital importancia cuando se considera si un nuevo tratamiento produce un resultado clínicamente significativo para los pacientes. Sin embargo, se acordó en general que las mejoras relativas en la mediana de la SG de al menos el 20%, son necesarios para definir una mejoría clínicamente significativa en el resultado. Los grupos de trabajo piensan que el ejercicio descrito aquí inspire a los investigadores a subir el listón en un esfuerzo para avanzar de forma significativa la atención del cáncer., pero destacando que no son normas de obligado cumplimiento, pero si son perspectivas de futuro. Supervivencia libre de progresión como endpoint en ensayos clínicos CMM A FAVOR EN CONTRA •Requiere menos pacientes y tiempo •No se afecta por terapia o supervivencia post-progresión •Beneficio clínico per se • • No hay correlación clara con SG Difícil de medir (investigador o comité central) Sesgos medición (p.ej. según régimen) • Supervivencia Global Medida ‘gold standard’ de beneficio clínico A FAVOR EN CONTRA • • • • Objetivo Medida fácil y fiable Indicación clara de beneficio clínico • Requiere mayor muestra y seguimiento Efecto de terapias posteriores y cross-over 10 En cáncer de mama metastásico ha existido un gran debate sobre si el objetivo principal debe ser la SG o la SLP., existiendo criterios a favor y en contra. El ponente recomienda recordar como en el estudio de D. Slamon de 2001 que comparaba Taxol vs. Taxol+Herceptin, la mediana de supervivencia para el grupo de Taxol fue de 18-20 meses. El objetivo de estos es para demostrar al final los progresos en supervivencia que se han logrado. El ponente centra ahora su intervención en los estudios con fármacos biológicos recientes, en especial los resultados en pacientes con HER 2 negativo tratados con bevacizumab o con everolimus. En el trabajo que compara paclitaxel vs. paclitaxel+bevacizumab las diferencias en el beneficio clínico expresado en SLP es claramente significativo, con una mediana de supervivencia de 5.9 meses frente a 11.8 meses. En el estudio con Exemestano vs. Evelolimus+Examestano ocurre algo similar con una mediana de SLP de 4.1 meses frente a 10.6 meses. Estos datos permitieron la aprobación en Europa, si bien las diferencias en SG no eran significativas pero esto no era el objetivo primario de los estudios. Incremento significativo de PFS en ensayos pivotales de Bevacizumab y Everolimus (PEP: PFS) Bevacizumab 1L RE+ IANE previo Everolimus Incremento significativo de SG en ensayos pivotales en HER2+ (PEP: SLP y SG) CLEOPRATA Pertuzumab 1ºL HER2+ EMILIA T-DM1 2ºL HER2+ Estudios recientes en pacientes con cáncer de mama metastásico HER2 positivo ha sido diseñados con suficiente poder estadístico para tener como objetivos primarios la SG y la SLP cosa frecuente de observar en las publicaciones. Hablando solo de la SG, en el estudio CLEOPATRA en 1º línea se comparaba Pertuzumab+Trastuzumab+Docetaxel vs. Placebo+Trastuzumab+Docetaxel las diferencias eran significativas a favor del grupo de investigación con una mediana de supervivencia de mas de 50 meses, muy diferente a los 20 meses en el estudio de de D. Slamon del 2001. 11 Las diferencias son claras con beneficios clinicos significativos. Algo similar ocurre en el estudio EMILIA en 2ª línea que comparaba Lapatinib+capecitabina+T-DM1 vs. Lapatrinib+capecitabina con medianas de supervivencias de 30.9 vs. 25.1 meses. Tratamientos estos con una excelente tolerancia que es otro componente indudables del beneficio clínico. Solo unas palabras en relación al tratamiento adyuvante del cáncer de mama localizado con diferentes combinaciones que incluyen quimioterapia, trastuzumab, hormonoterapia, con unos beneficios incuestionables y una RH de 0.48 a 0.87, dando lugar a una disminución de las recaídas y a un incremento de las curaciones. Un tema innovador es la reglamentación de aprobación acelerada de la FDA de fármacos basado en objetivos “surrogate”. La FDA puede conceder aprobación de comercialización de un nuevo producto sobre la base de ensayos clínicos adecuados y bien controlados que establezcan que el medicamento tiene efecto basado en objetivos secundarios con razonables probabilidades de predecir un beneficio clínico. La pregunta es que se puede hacer con la pRC: ¿Se debe considerar que la pCR tiene una probabilidad razonable predecir un benéfico clinico? Seria una forma de lograr aprobaciones aceleradas de indudable valor en el tratamiento neoadyuvante de cáncer de mama. La FDA en las aprobaciones aceleradas requiere posterior confirmación de beneficios. Esta aprobación acelerada es una evidente ventaja ya que puede significar años de vida ganados y vidas salvadas, pero tiene sus riesgos, una vez aprobado el producto que no se logren los beneficios clínicos esperados y se exponen a los pacientes a efectos tóxicos sin tener certeza de estos beneficios. Lo importante en el caso del cáncer de mama es la selección de pacientes de alto riesgo, como población para justificar esta aprobación acelerada. 12 La FDA señala las pacientes de alto riesgo para estos estudios neodyuvante con nuevos fármacos de aprobación acelerada, considera candidatas a las que tienen un riesgo absoluto de recaída de mas del 20%. En la tabla de la FDA se pueden apreciar los grupos considerados de alto riesgo, teniendo en cuenta estadios, grado histológico, receptores hormonales, HER2+, Triple Negativo etc. En estos grupos podría estar justificado el uso de nuevos fármacos para una aprobación acelerada con seguimiento posterior. Pertuzumanb fue aprobado de forma acelerada por la FDA para pacientes HER2+ por la existencia de una correlación entre pRC y SLE especialmente en las pacientes con HER2+ HR - , y en triple negativo. Todo esto está tanbien apoyado por diversos estudios neobyuvantes que comparan tratamiento de QT+ Trastuzumab donde se ha logrado un incremento de las pRC y una mejor SLE, especialmente en HER2+RH-.El estudio NEOSPHERE compara Pertuzumab y Trastuzumab + docetaxel demostró un incremento de las pRC especialmente en el grupo de Pertuzumab+Trastuzumab+Docetaxel (47/107), superior a Trastuzumab+Docetaxel. Este estudio permitió la aprobación acelerada por la FDA en el tratamiento neoadyuvante de cáncer e mama HER2+, pero con un seguimiento confirmatorio. Estos resultados apoyan hacer nuevos estudios en tratamientos adyuvantes. Estudios como el CLEOPATRA en cáncer de mama metastásico también es un apoyo en el uso de Pertuzumab en la neoadyuvancia y especialmente el estudio en curso APHINITY que utiliza pertuzumab en combinación con quimioterapia y trastuzumab como tratamiento adyuvante en pacientes con cáncer de mama HER2-positivo. Par terminar el ponente hace un resumen de las conclusiones que figuran en el cuadro siguiente. Conclusiones • • • • • La supervivencia de las pacientes con CMM está aumentando significativamente, sobretodo en enfermedad HER2+ (18 meses año 2000 - > 50 meses año 2010), con menos toxicidad durante fases prolongadas. Los niveles de beneficio de fármacos biológicos aprobados está en línea con la perspectiva ASCO (en ‘CMTN’). Debe delimitarse muy bien si el endpoint es PFS, SG o ambos, y juzgar los resultados en base al endpoint. En el tratamiento adyuvante se consiguen ganancias incrementales significativas, que aumentan tasas de curación. Surge el nuevo paradigma de la aprobación acelerada de fármacos en contexto neoadyuvante, en base a incremento RCp, datos en CMM, y estudios adyuvantes en curso. Muchas gracias por la atención prestada. 13 3.- Magnitud del beneficio clínico en cáncer de pulmón. El siguiente ponente es el Dr. Bartomeu Massuti, donde destaca inicialmente que el Contenido exposición • • • • • • • • Comentarios terminológicos Beneficio vs costes; evaluación economica Resultados globales en cáncer de pulmón Estrategias tratamiento dirigido en cáncer de pulmón Evaluación beneficios terapias anti-EGFR y antiALK Impacto global del cáncer de pulmón Aprobación fármacos en cáncer de pulmon Conclusiones cáncer de pulmón es donde se presentan los peores resultados por ello su intervención es en cierto modo reivindicativa para mejorar dichos resultados. También hace destacar que hablar de beneficios es hablar de costes por lo que se puede desdibujar el concepto de beneficio. Al hablar de beneficio, señala el ponente, existe una perversión del lenguaje ya que se pueden estar refiriendo a diferentes cosas. En una búsqueda del beneficio clínico del Google Scholar, se encontró 2.240.000 citaciones en cáncer y de ellas 1.580.000 se refería a cáncer de pulmón lo que hace poner en duda a que se refiere beneficio clínico. ¿Para el paciente?, ¿Para el tumor? ¿Beneficio social o individual? La realidad es que tiene un coste y no se puede eludir hablar de él, siendo lo mas inmediato el coste oportunidad que implica consecuencias de una elección y una reflexión sobre las opciones no elegidas, y todo esto en la problemática cada vez mas importante de definir cada vez mejor el valor en cuidados de salud. Técnicas de evaluación económica • Análisis Coste/Beneficio (ACB) • Análisis Coste/Efectividad (ACE) (unidades objetivas) • Análisis Coste/Utilidad (ACU) (unidades subjetivas) • Fundamento ético de la eficiencia Valores individuales, base de los valores sociales Utilitarismo, base de la evaluación económica • Variables Costes: Coste de oportunidad Efectos: Cambios en el estado de salud: Beneficio? • Relación Coste-Efecto: El ACB y el ACE En relación a la evaluación economía el ponente hace solo unos comentarios. En primer lugar el análisis coste/benicio al ser lo que más se aproxima al beneficio clínico. En segundo lugar el análisis coste /efectividad se mide por unidades objetivas en lo que son los resultados. En tercer lugar el análisis coste/utilidad que tiene un componente subjetivo en su medida como son los cuestionarios de calidad de vida. Indudablemente la evaluación económica tiene un fundamento ético de la eficiencia y combina valores individuales base de los valores sociales y con el utilitarismo, base de la evaluación económica. Por tanto se tiene que jugar con las variables costes y efectos, base de las 14 decisiones de salud. Por todo ello no se puede hablar de beneficios sino se tiene en cuenta todo este escenario de coste/beneficio, coste/ efectividad y coste/ utilidad. Básicamente las evaluaciones nos permiten comparar las alternativas y las consecuencias con la utilización de los recursos disponibles, lo que sería la base de nuestras decisiones o las de un Servicio de Salud. Análisis coste/beneficio • Evaluación de acciones alternativas en términos de sus consecuencias, con el fin de maximizar los beneficios sociales netos del uso de los recursos, o el bienestar social • Un proyecto debe llevarse a cabo si y sólo si sus beneficios sociales exceden a los costes sociales, es decir, si su beneficio social neto es positivo • VAN = [( Bi - Ci ) /(1 + d)i ] Centrándonos en el cáncer de pulmón se debe destacar que la supervivencia relativa a cinco años en la Unión Europea (2012-2013) es de un 13%, lejos de la supervivencia de los tumores que han sido incluidos en esta mesa redonda. La mortalidad también referida a la EU-27 es de 1.314.230 casos totales de cáncer (H: 737.747. M: 576.487), correspondiendo al cáncer de pulmón 269.610 casos (H: 186.970. M: 82.640). Observando las curvas de mortalidad hombres/mujeres se aprecia una clara disminución en los hombres y un incremento en las mujeres, justificado por el cambio en el hábito de fumar. El coste de todos los tipos de cáncer por persona en relación al poder adquisitivo en la EU-27 es de 102 euros y en España de 90 euros. En relación al cáncer de pulmón el coste por persona en la EU-27 es de 8 euros y en España de 5 euros, costes que están por debajo de las otras neoplasias incluidas aquí en esta mesa, lo que se explica por una menor supervivencia del cáncer de pulmón. Un incremento de supervivencia significa sin duda un incremento de costes. En definitiva el coste por cáncer de pulmón por persona en España es inferior al resto de países de nuestro entorno. En una publicación del “The Washington Post” señala las tasas de incidencia y mortalidad en los EE.UU., la edad media de diagnostico y muerte (70/72) pero sobre todo lo que quiere destacar el ponente de esta publicación es que el cáncer de pulmón recibe menor subvención por parte del INC para la investigación a pesar de suponer unas perdidas de 2 millones de años de vida. Mucha menor subvención que el cancer de prostata que es menos devastador para la población. El cáncer de mama recibe el doble de financiación a pesar que en términos de años de vida perdidos tiene solo un tercio del cáncer de pulmón. Por todo esto el ponente dijo que su intervención era también reivindicativa. En el cáncer de pulmón en la última década han pasado muchas cosas y que están sintetizadas en la figura en el texto. La mediana de supervivencia era antes de menos de 6 meses y en la actualidad esta media de supervivencia es de 2 años, pero solo en una 15 población seleccionada o minoritaria que debe ser identificada previamente con unos costes determinados. Evolución terapéutica en Cáncer Pulmón avanzado: S XXI Quimioterap . plateau1 1L Bevacizumab + CP vs CP3 Segunda línea terapéutica 2000 2005 1LM Cont Pem vs 1L 1LM Plac / M Pem_Bev Gefitinib vs CP en swicht Pem 7 Crizotinib ie ALK + EGFR MUT+ 5 vs placebo 1L 1L 1LM 1L Erlotinib Erlotinib EGFR Erlotinib vs vs QT CPem vs CG4 6 8 MUT+ EGFR Mut placebo 2006 CP = carboplatin paclitaxel CPem = cisplatin pemetrexed CG = cisplatin gemcitabine 2008 2009 2010 2013 1. Schiller, et al. NEJM 2002; 2. Sheppard, et al. NEJM 2005; 3. Sandler, et al. NEJM 2006 4. Scagliotti, et al. JCO 2008; 5. Ciuleanu, et al. Lancet 2009; 6. Rossell, et al. NEJM 2009 7. Mok, et al. NEJM 2009; 8. Cappuzzo, et al. Lancet Oncol 2010; 9. Sandler, et al. JTO 2010 En un estudio francés con mas de 10.000 pacientes en los que se han estudiado las mutaciones en cáncer de pulmón no escamoso, solo aproximadamente han sido tratados con fármacos dirigidos comercializados y no de investigación, menos de un 15%. De las mutaciones detectadas sólo las de EGFR y EML4-ALK pueden actualmente estar tratadas de forma dirigida. Mutation driven therapy presently benefits only a subgroup of the overall population BIOMARKERS FRANCE: driver mutations in 10,000 patients with non-squamous NSCLC Of the alterations detected, only EGFR Mut and EML4-ALK can currently be targeted therapeutically Results expressed in % on available analyses Barlesi, et al. ASCO 2013 16 En un trabajo en JAMA de 2014 se analiza el impacto y las limitaciones de los tratamientos dirigidos sobre dianas determinadas. Este estudio comprende tres grupos, el primero tratado con terapias dirigidas, un segundo grupo con mutaciones sin tratamiento de terapias dirigidas y un tercer grupo sin mutaciones , la mediana de supervivencia era claramente superior para el primer grupo lo que es significativo de la importancia de la selección de pacientes para el uso de las terapia dirigidas. Ahora el ponente aborda la evaluación beneficios de las terapias anti-EGFR y antiALK. La primera mutación estudiada son las del EGFR y por tanto mejor conocidas. Su frecuencia es diferente según las áreas lo que plantea problemas de costes para los distintos piases a la hora de establecer los planes de salud. El primer estudio fue el IPASS donde se comparaba Gefitinib vs. Carboplatino/ Paclitaxel en un grupo de población general de cáncer de pulmón y otro grupo con mutaciones de EGFR. La SLP en el primer grupo, los tratados con Gefitinib tenían una HR de 0.741 (p<0.0001), pero mucho mas evidente el grupo con mutaciones con una HR de 0.40 (p<0.001). EGFR mutations IPASS: SUPERVIVENCIA LIBRE DE PROGRESIÓN POBLACIÓN GLOBAL MUTACIÓN EGFR POSITIVA Probabilidad 1.0 de SLP Gefitinib (n=132) Carboplatino / paclitaxel (n=129) 1.0 Probability of progression-free survival 0.8 0.6 5.7 m 0.4 0.2 5.8 m 0.0 At risk : Gefitinib Carboplatin / paclitaxel 0 609 608 4 363 412 8 212 118 12 76 22 16 24 3 HR (95% CI) = 0.741 (0.651-0.845) p<0.0001 20 5 1 Months 0.8 0.6 0.4 0.2 0.0 At risk : Gefitinib 0 4 132 8 108 12 Months 71 16 31 20 11 24 3 0 HR (95% CI)= 0.48 (0.36-0.64) P<0.0001 Primary Cox analysis with covariates HR <1 implies a lower risk of progression on gefitinib . Mok T. et al. NEJM 2009 Sep 3;361(10):947-57 Otros estudios como el NEJ002, el OPTIMAL, WJTOG3405 y el ICOGEN reproducen los resultados en SLP y en respuestas sin evidenciarse incrementos de la SG., datos que se pueden observar en la tabla siguiente. 17 La presencia de la mutación de EGFR (M +) define un subtipo diferente de NSCLC, sensible a EGFR TKIs1: (Erlotinib, Gefitinib). Las mutaciones mas sensibles son las deleciones del 19 y L858R, que representan el ~ 90% de los casos Los inhibidores TK del EGFR son el tratamiento estándar de primera línea en NSCLC EGFR M +, que muestra la mejora de la PFS y de la ORR en 7 ensayos aleatorios, pero no hubo diferencia en la SG vs. quimioterapia con dobletes de platino y esto es Trial EURTAC OPTIMAL ENSURE IPASS NEJ002 WJTOG3405 FIRST-SIGNAL TKI Erlotinib Erlotinib Erlotinib Gefitinib Gefitinib Gefitinib Gefitinib PFS HR 0.47 (0.28, 0.78) ind 0.16 (0.10, 0.26) inv 0.42 (0.27,0.66) ind 0.48 (0.36, 0.64) inv 0.30 (0.22, 0.41) ind 0.49 (0.34, 0.71) inv 0.54 (0.27, 1.1) inv OS HR 0.93 (0.64, 1.35) 1.04 (0.69, 1.58) n/a 1.00 (0.76, 1.33) 0.89 (0.63, 1.24) 1.25 (0.88, 1.78) 1.04 (0.50, 2.18) un tema de debate. Solo un estudio presentado en ASCO 2014, una especie de metanálisis donde compara pacientes con mutaciones activadas, tratados con quimioterapia vs. Afitinib, procedentes de dos estudios LUX-Lung 3+6 (631 p.), se observa una mejoría de la SG, con una mediana en meses de 24. 3 vs. 27.3, con una HR0.81 y una p=0.0374. Pero para complicar más las cosas los beneficios clínicos en SG se encuentra solo en la deleción del 19 y no del 21 (L858R). El posible impacto poblacional de las terapias anti-EGFR se pueden observar en el estudio japonés de Tacaño et al (JCO 2008) y que se representa mas abajo. POBLACIÓN GLOBAL 18.1 m 12.5 m EGFR M+ EGFR M- 27.2 m 13.2 m 10.4 m 13.6 m Takano T et al JCO 2008 También es importante al hablar de beneficios, considerar el impacto de estos fármacos en la Calidad de Vida debido y los efectos secundarios, efectos secundarios que son 18 menores por lo que se conserva mejor dicha Calidad de Vida. La quimioterapia se asocia a una mayor tasa de toxicidad grado 3-4, más eventos adversos serios asociados al tratamiento, mayores reducciones de dosis y discontinuación del tratamiento. Los pacientes que reciben un ITK anti-EGFR tienen una mejoría significativa en Calidad de Vida. Ahora tenemos que pasar al análisis económico de las terapias anti-EGFR y siguiendo los datos presentados en ASCO 2013, comentar que el tratamiento de primera línea con Erlotinib versus quimioterapia resultó en un aumento de 0,60 años de vida ganados o 0,44 años de vida ganados (QALYs) respectivamente ajustados por calidad, Los costos totales medios fueron $ 59.300 en el brazo de erlotinib y $ 17.800 en el grupo de quimioterapia, que arroja una ratio coste-efectividad incremental (ICER) de 98.338 dólares con un 53% de probabilidad de ser rentable en una disposición a pagar (WTP) de 100.000 dólares QALY. Probablemente esto no es asumible en sociedades europeas, pero si se consideran 1º y 2º línea el coste entra dentro de límites que podrían ser aceptables en Europa. En resumen el tratamiento con erlotinib en primera línea de NSCLC con EGFR-positivo existe un aumento de los costos, pero también un aumento sustancial de los QALY, por lo que la terapia personalizada puede ser rentable. El estudio EURTAC, presentado en el Congreso Internacional sobre Cáncer de Pulmón del 2013 viene a decir lo mismo, que el coste de 1ª línea es elevado de 28.491 euros con erlotinib y de 10.773 con quimioterapia. Tras progresión la 2ª línea el coste es de 38.947 euros con erlotinib frente a 66.163 con quimioterapia. La media total del coste es de 67.438 euros para erlotinib frente a 76.937 para quimioterapia. Según criterios europeos existe un 82% de probalidad de ser coste efectivo, si bien existen diferencias de costes entre los diversos piases. En un diagrama de dispersión de ICER, la probabilidad de tener un coste menor de € 30.000 = 90,2% Un ejemplo comparativo entre Francia, Italia y España, se observa las diferencias de precios, sin diferencias en la utilidad, con un coste incremental (ICER) negativo en los tres países. 19 Incremental cost/utility ratio according to the 3 countries France Italy Spain Cost difference -9,498 -7,806 -7,466 Utility difference 0.117 0.117 0.117 negative negative negative ICER 36 O16: Economics TKIs– A Vergnenegre El ponente expone la problemática de las mutaciones de ALK, mucho más complejas, resultando mas difícil la individualización. Los resultados en estudios en fase 1 con Crizotinib, la mediana de la SLP fue 9.7 meses (95% CI: 8.2, 14.7). Cuando Crizotinib se usaba en 1ª línea la mediana de PFP era de 18.3 meses (95% CI: 8.3– not reached), lo que representaba unos resultados sorprendentes en el pequeño subgrupo de pacientes con mutaciones de ALK. También en un estudio en fase I se analizo la SG, a un año era del 87.4% y a 2 años del 74%, sin haberse alcanzado la mediana de supervivencia. Estos datos son muy significativos. En cuanto a la segunda linea en el estudio PROFILE 1007 ALK+, tratados en primera linea con asociaciones de platino, se comparó Crizotinib 250 mg/12h (173 p.) vs. Pemetrexed 500 mg/m2 o Docetaxel 75 mg/m2, cada 21 días (174 p.), y como objetivo principal la supervivència libre de progresión (SLP). Para el grupo Grizotinb era de 7.7 meses y para el de quimioterpia solo de 3 meses. La tasa de respuesta objetivas era del 65% frente a solo un 20% y las tasas de control de la enfermedad del 94% vs. 66%. Estos datos corfiman la eficacia de una terapia dirigida cuando existe selección de pacientes en este caso por mutaciones de ALK. El estudio de la calidad de vida demostró la existencia de un cambio partiendo de la valoración basal, claramente superior al grupo de quimioterapia. Lo mismo ocurria cuando se analizaba el tiempo hasta el deterioro en calidad de vida (ver figura). Con Crizotinib también existe una mejoría de sintomas generales como la astenia, disnea y la tos que participan en una mejor calidad de vida y en definitiva mayor beneficio clínico, lo que se mantiene mas de un año y medio. En relación a la supervivencia Global en pacientes ALK + es superior en los pacientes tratados con crizotinib frente a quimioterapia. Los pacientes ALK + no tratados con crizotinib tienen un pronóstico similar a los pacientes “wild-type”. 20 Crizotinib vs QT 2ª línea: CDV PROFILE 1007 CALIDAD DE VIDA Cambio en Calidad de Vida desde la basal Tiempo hasta el deterioro en Calidad de Vidad Shaw et al NEJM 2013 Existen datos de Crizotinib en relación al coste/efectividad en un estudio canadiense publicado en el JCO abril de 2014. Un análisis costo/efectividad se realizó mediante un modelo de Markov desde la perspectiva canadiense de salud pública. En pacientes con NSCLC avanzado y AKL positivo, la primera línea con Crizotinib proporcionó 0.379 QALY adicionales que costó 95.043 dólares en comparación con la atención estándar y produjo un ICER de 250.632 dólares por QALY ganado. Siendo la causa de todo este incremento el coste del medicamento. Por todo ello se consideró no rentable por el alto costo en medicamentos y una baja frecuencia de biomaecadores positivos en la población con cáncer de pulmón. El ponente vuelve a reclamar más investigación para cáncer de pulmón, por lo que supone en cuanto a resultados y por su impacto social. Comenta que los QALY pudieran tener un precio a pagar diferente dependiendo del impacto de la enfermedad en la sociedad, si bien hay coste básico para los Servicios de Salud. También debe considerarse en relación a los QALY la mayor innovación terapéutica y los beneficios sociales que producen. Debe existir por tanto un precio negociado sobre la base del coste básico por QALY. Finalmente el ponente aborda el tema de la aprobación de fármacos por la FDA en el cáncer de pulmón donde se tiene en cuenta el diseño del ensayo y los objetivos del mismo, en casi todos es la supervivencia si bien hay alguno donde es la respuesta. Todos estos datos se pueden ver n el cuadro siguiente. 21 Aprobaciones FDA en CBP Contains Nonbinding Recommendations Draft — Not for Implementation 106 Table 1: Regulatory Experience With New Drug Approvals for the Treatment of NSCLC Drug First-Line Inoperable/Metastatic NSCLC Vinorelbine monotherapy Vinorelbine in combination with cisplatin Docetaxel in combination with cisplatin Gemcitabine in combination with cisplatin Bevacizumab in combination with paclitaxel/carboplatin1 Paclitaxel in combination with cisplatin Pemetrexed in combination with cisplatin1,2,3 Trial Design Approval Endpoints Open-label, randomized, active-controlled trial vs. 5FU/leucovorin Open-label, randomized, active-controlled trial vs. cisplatin Open-label, randomized, active-controlled trial, docetaxel/cisplatin vs. vinorelbine/cisplatin (1) Open-label, randomized, active-controlled trial vs. gemcitabine (2) Open-label, randomized, active-controlled trial, gemcitabine + cisplatin vs. etoposide + cisplatin Open-label, randomized, active-controlled trial vs. paclitaxel/ carboplatin OS, ORR OS, ORR OS, TTP, ORR Open-label, active-controlled, dose-ranging, randomized, three-arm trial, paclitaxel (135 mg/m2)/cisplatin vs. paclitaxel (250 mg/m2)/cisplatin vs. etoposide/cisplatin Open-label, active-controlled, randomized trial; pemetrexed/cisplatin vs. gemcitabine/cisplatin TTP, ORR, OS OS TTP, ORR OS OS Maintenance Therapy Pemetrexed in patients whose disease has not Randomized, double-blind, placebo-controlled trial OS progressed after four cycles of platinum-based 1 first-line chemotherapy Erlotinib in patients whose disease has not Randomized, double-blind, placebo-controlled trial OS progressed after four cycles of platinum-based first-line chemotherapy Second-Line NSCLC Docetaxel Randomized, placebo-controlled trial, docetaxel vs. best supportive care OS, TTP, ORR Erlotinib Randomized, placebo-controlled trial, erlotinib vs. best supportive care OS, TTP, ORR 1,2 Pemetrexed Randomized, open-label trial vs. docetaxel Durable ORR, Decreased Toxicity Third-Line NSCLC Erlotinib Randomized, placebo-controlled trial Erlotinib vs. best supportive care OS, TTP, ORR Gefitinib2,4 Single-arm trial Durable ORR Partially or Completely Obstructing Endobronchial Tumor NSCLC and Microinvasive Endobronchial NSCLC in Nonsurgical Candidates Porfimer sodium and photodynamic therapy Randomized, open-label, active-controlled trial vs. YAG laser Improvement in disease-related symptoms 107 108 109 110 111 1 Limited to non-squamous, non-small cell lung cancer. Accelerated approval. Because the approval was based on a subgroup of patients, confirmatory evidence in the subgroup from an on-going study was required under the accelerated approval. 4 Subsequent studies did not confirm clinical benefit; indication will be withdrawn in 2011 (press release http://www.astrazeneca-us.com/search/?itemId=12045633 accessed March 11, 2011). 2 3 Nuevos fármacos se incorporan al arsenal terapéutico del cáncer de pulmón tales como 4 el Ceritinib en pacientes pretratados con Crizotinib y translocación ALK y el Ramucirumab, con beneficios significativos y que en la actualidad están en estudios iniciales. Las conclusiones del ponente figuran en la tabla siguiente: Conclusiones • • • • • • • Alto impacto socio-económico del cáncer de pulmón Cáncer de pulmón área de investigación prioritaria en cáncer La evaluación coste-beneficio y coste-eficiencia en cáncer de pulmón moduladas por impacto de la enfermedad y baja supervivencia Supervivencia y CDV factores determinantes para definición beneficio Limitaciones EE CC clásicos para evidenciar beneficios en tratamientos individualizados. Criterios específicos de evaluación e implicaciones éticas para subpoblaciones minoritarias; consideración cribado Valor y precio de los fármacos determinantes en la evaluación económica Alianzas sociales Muchas gracias por la atención prestada. 22 4.-Magnitud del beneficio clínico en cáncer colorrecta. El Dr. M. Benavides abordó el tema de la “Magnitud del beneficio clínico en cáncer colorrectal” y parte del hecho que la definición de beneficio clinico es un tema complicado y sin unanimidad sobre el mismo como observó en la primera ponencia. El Centra su ponencia en el cáncer colorrectal metastásico considerando las mutaciones de RAS y otras mutaciones, para valorar el beneficio de terapias dirigidas. La supervivencia a cinco años es del 55% en España algo por encima del resto de países europeos según datos del EUROCARE-5. La cirugía de las metástasis especialmente hepáticas y en segundo lugar pulmonar y peritoneal ha participado en la mejoría de la supervivencia, incluso de curaciones. Cirugía metástasis Curación ? Tras la 1ª cirugía - Supervivencia global: 41.5% a 5 años - Supervivencia global: 26% a 10 años LiverMetSurvey. Statistics 2008 En los estudios básicos cuando llega por primera vez un paciente a la consulta el ponente considera esencial las determinaciones de KRAS e incluso BRAF por lo menos hasta ahora. Junto a esto indudablemente conocer comorbilidades, PS, 23 dependencia, preferencias del paciente y CdV. Posibilidades de resección del tumor primario y de la resecabilidad de la enfermedad metastásica. Finalmente se debe considerar las opciones de tratamiento local y sistémico, esquemas y toxicidades, duración / y la necesidad o no del mantenimiento. En cáncer colorrectal metastásico hay aprobados en 1ª línea tres anticuerpos monoclonales; en primer lugar el Bevacizumab un antiangiogénicos que bloquea el VGRF. No tiene marcador biológico de selección por lo que puede indicarse en todos los casos con EGFR mutado o no. Los otros anticuerpos monoclonales son Cetuximab y Panitumumab indicados en los casos de EGFR no mutado que es la base de selección de pacientes. En estos casos también puede ser utilizado en Bevacizumab. Esto es lo que ha estado haciéndose desde 2008 hasta mediados del 2013. Los estudios en fase III realizados para Bevacizumab no se tenían en cuenta la mutación o no de KRAS. Fases III independientes de RAS Desde 2008 hasta mediados 2013 MUTADO K-Ras ~ 45% Quimioterapia ± antiVEGF Desde mediados 2013 INCLUYENDO BRAF ? RAS Exón 2 KRAS exones 2-3-4 NRAS exones 2-3-4 NATIVO ~55% Quimioterapia ± antiEGFR MUTADO Quimioterapia ± anti-VEGF ~ 55-60% Quimioterapia NATIVO + INCLUYENDO BRAF ? anti-EGFR o Bevacizumab ~40-45% ??? Desde el año pasado se hacen determinaciones de mutaciones de KRAS en exones 2-34 y mutaciones de NRAS exones 2-3-4 porque detecta aproximadamente un 15-20% de casos mutados y que se suman al grupo mutado con la sola determinación de KRAS exón 2. Según el estado mutacional se hacen las indicaciones terapéuticas como figuran en el cuadro anterior. El ponente se centrará solo en el grupo nativo (40-45%) para su análisis del beneficio clinico dado que en ellos se centra el tratamiento con anticuerpos monoclonales antiEGFR y también el anti-VGFR. Los ensayos en fase III (1ª Línea): Quimioterapia ± anti-EGFR en Kras / RAS wt, tales como el estudio CRYSTAL con FOLFIRI ± Cetuximab y el estudio PRIME con FOLFOX4 ± Panitumumab que se comparaban a un brazo de quimioterapia solo, siendo demostrativos los beneficios de la terapia anti-EGFR. En el estudio CRYSTAL RAS wt, la tasa de RR era 66.3% vs. 38.5% (p=0.0001). La SLP de 11.8 m. vs. 8.4 m. (HR de 0.56. p=0.002 La SG de 28.4 m. vs. 20.2 m. (HR de 0.69. p=0.008). En el estudio PRIME las tasas de RR en Kras exón 2 wt, era del 55% vs. 48% (p=0.043). La SLE en RAS wt era de 10.1 m. vs. 7.9 m. (HR: 0.78 y p= 0.0006) y la SG de 26.0 m. vs. 20.2 m. (HR: 0.78. p= 0.043). En estos estudios se pudo ver la mejoría de la RR, SLE y SG cuando se identificaban los casos de mutaciones en exón 3 y 4 de KRAS y los de NRAS. Por tanto a los pacientes sin mutaciones hay que ofrecerle la terapia antiEGFR. 24 En la actualidad existen tres estudios que enfrentan en 1ª línea los anti-EGFR y los anti-VGFR más quimioterapia. Los resultados se pueden apreciar en la tabla siguiente: Kras exon 2 wt N RR (%) RAS wt mPFS mOS N PEAK Folfox + Panitumumab vs Folfox 10.9 vs. 10.1 34.2 vs. 24.3 Bevacizumab HR:0.62 285 57.8 vs. 53.5 HR:0.87 170 (Fase II) p.353 p.009 L.S. Schwartzberg J Clin Oncol 2014 FIRE-3 Folfiri + 10.0 vs. 10.3 28.7 vs. 25.0 Cetuximab vs Folfiri +592 62 vs. 58 HR:1.06 HR:0.77 342 p.54 p.017 Bevacizumab Stintzing S ASCO GI 2014 CALGB 80405 Folfox o Folfiri + 10.8 vs. 10.4 29.9 vs. 29.0 Cetuximab vs Folfox o Folfiri +1140 HR:1.04 HR:0.92 p.55 p.925 Bevacizumab A. Veenok ASCO 2014 RR(%) mPFS 13.0 vs. 63.6 vs. 60.5 HR:0.65 p.029 mOS 9.541.3 vs. 28.9 HR:0.63 p.058 10.4 vs. 10.2 33.1 vs. 25.6 65.5 vs. 59.6 HR:0.93 HR:0.7 p.32 p.54 p.011 - - - En los dos primeros estudios los datos del global RAS wt son superiores cuando se comparan con KRAS exón 2wt. También debe señalarse que los resultados con antiEGFR son superiores a los anti-VGFR. El tercer estudio CALGB 80405 presentado en ASCO de 2014 debería haber contestado a la pregunta de superioridad del anticuerpo monoclonal, pero solo se presentaron los datos de KRAS exón 2 wt., sin diferencias en SLP y SG, pero habrá que esperar a su publicación definitiva para conocer realmente los datos. Por tanto seguimos sin saber realmente y Cetuximab es realmente superior a Bevacizumab hasta que no tengamos los resultados del último estudio. El ponente pasó a exponer otras mutaciones en cáncer colorrectal donde hay múltiples vías de señalización, así en la vía de EGFR está RAS y BRAF, estando mutado este aproximadamente en el 50% de los casos. Los pacientes sin mutación de RAS y sin mutación de BRAF al ser tratados con anti-EGFR presentan mejor SLP y SG. 25 Nicolantonio, F. et al. JCO november 2008. Los pacientes con RAS no mutado y BRAF mutado serán del grupo no respondedores. Datos que fueron observados en los estudios CRISTA y OPUS (E. Van Cutsem et al. J Clin Oncol 2011). Lo mismo ocurre con los estudios COIN y CAIRO. En el estudio PRIME para la aprobación de Panitumumab (P), donde un grupo era tratado con P+FOLFOX4 vs. FOLFOX4, los pacientes con WT RAS/WT BRAF presentaban una SG de 28.3 m. (HR =0.74), y los que eran WT RAS/MT BRAF la SG era solo de 10.5 m (Oliner K, et al. J Clin Oncol 31, 2013 (suppl; abstr 3511). En el estudio FIRE-.3 la presencia de mutaciones BRAF venia a confirmar los hechos ya conocidos de la respuesta según existieran o no mutaciones de RAS para el tratamiento con anti-EGFR. En definitiva pacientes con WT RAS con BRAF mutado no serian candidatos a tratamiento con anti-EFGR. En ASCO 2014 se han presentado otros estudios con BRAF mutado como aparece en tabla siguiente y con el uso de nuevos fármacos para esta población especifica. Estudios en BRAF MUTADOS. ASCO 2014 Dabrafenib + Trametimib + Panitumumab Axitinib Tivantinib + Cetuximab Dabrafenib + Trametimib Vemurafenib + CPT-11 + Cetuximab Encorafenib + Cetuximab ± Inhibidor PI3KCA Vemurafenib ± Cetuximab La heterogeneidad tumoral analizada en el artículo de NEJM del 8 de marzo 2012 es una dificultad para identificar los biomarcadores que apoyen el tratamiento individualizado. Posiblemente las biopsias liquidas puedan ayudar a identificarlos a pesar de los cambios mutacionales que aparecen en los tumores. 26 JCO. 20.Feb. 2014 L. Diaz and A. Bardelli En el algoritmo sobre cáncer colorrectal metastático se intenta establecer los pacientes que se benefician de la terapia anti-EGFR. Es indudable que pacientes con WT RAS, si presentan mutaciones en BRAF y/o PI3KCA mutados y/o perdida de PTEN tienen pocas probabilidades de responde a los anti-EGFR. RAS NATIVO BRAF nativo PIK3CA nativo BRAF y/o PI3KCA mutados y/o perdida de PTEN PTEN expresado Alta probabilidad de beneficio clínico a antiEGFR Muy baja probabilidad de beneficio clínico a antiEGFR En este sentido, también están los estudios del TTD denominados VENUS 1 y VENUS 2, basando la indicación terapéutica según sus características moleculares. Para terminar el ponente expone una diapositiva donde se ven los logros alcanzados en cáncer colorrectal metastásico en supervivencia como una expresión del beneficio clínico. 27 Slide 30 Presented By Alan Venook at 2014 ASCO Annual Meeting Muchas gracias por la atención prestada 5.- Magnitud del beneficio clínico en cáncer de próstata. Esta última ponencia es sobre “Magnitud del beneficio clínico en cáncer de próstata” abordada por el Dr. Enrique Grande que destaca la magnitud del problema por la alta incidencia anual con 2.979.970 (43%) casos a uno de enero de 2014 y que pasaran a ser 4.194.190 (45%) casos en 2024 (De Sanctis CE, et al. CA CANCER J CLIN 2014). Las tasas de mortalidad por cáncer de próstata es aproximadamente de 258.000 casos en todo el mundo según datos de Globocam 2008, siendo la séptima causa de muerte por cáncer entre los hombres (5,8% del total de fallecimientos por tumores malignos). Se trata de un tumor con altísima incidencia, especialmente en países desarrollados, pero con una mortalidad moderada. El ponente hace destacar que esta neoplasia debe ocupar un lugar destacado a la hora incrementar la investigación sobre el mismo. También hace destacarla necesidad de tratar al cáncer de próstata en fase avanzada, especialmente al cáncer de próstata resistente a la castración y donde mas avances se han producido. 28 En la figura que aparece ahora en el texto están los avances de los últimos años. Inicialmente representado por el acido zolodrónico y por el docetaxel, pero mas recientemente se han incorporado cuatro nuevos fármacos (fondo verde), que tendremos que saber posicionarlos adecuadamente y medir la magnitud de su beneficio clínico. Opciones de Tratamiento para los Pacientes de Cáncer de Próstata Resistente a la Castración (CPRC) Cabazitaxel Enzalutamida Ácido Zoledrónico Denosumab Abiraterona Radium 223 Docetaxel Sipuleucel T Todo ello parte de los conocimientos recientes en biología molecular de esta neoplasia, especialmente la vía de los receptores de andrógenos implicados en los cambios evolutivos de la transición epitelio-mesenquima y en el proceso de metastatización. Evolución Natural del Cáncer de Próstata Radium 223 Quimioterapia Deprivación Androgénica Post-Quimioterapia Pre-Quimioterapia Docetaxel Cabazitaxel Tratamiento Local Abiraterona Enzalutamida PSA Asintomático No Metastásico Sensible a la Castración Sintomático Metastásico Resistente a la Castración Esta evolución puede ser observada en el siguiente esquema, desde sus inicios a la fase avanzada y el lugar que pueden ocupar los diferentes fármacos, tras la quimioterapia con docetaxel en fase resistente a la castración, y valorar su beneficio clínico. En primer lugar está el Cabazitaxel, un nuevo taxano que inhibe la polimerización de los 29 microtúbulos impidiendo la division celular, pero sobre todo impide que la señalización de la vía de los androgenos penetre en el nucleo celular y ponga en marcha mecanismos como la proliferación celular y cambios en el microambiente tumoral. El Cabazitaxel mejora los resultados del Mitoxantrone en relación a la SG en el estudio TROPIC (HR 0.70. p=0.0001). Cabazitaxel TROPIC Supervivencia Global con Abiraterona: COU301 15.1 m. 14.8 m vs 10.9 m HR 0.65 (95%CI, 0.54 to 0.77) P<0.001 12.7 m De Bono JS et al. N Engl J Med 2011 En la realidad las diferencias son solo de unos 3 meses como expresión del beneficio clínico. La Abiterona impide la síntesis de andrógenos por bloque de la CYP17 hidroxilasa y de la CYP 17 liasa. Los resultados con Abiterona+Prednisona en el trabajo COU-301 frente a Placebo + Prednisona es de 14.8 m vs. 10.9 m. HR 0.65 (95%CI, 0.54 - 0.77). p<0.001. El beneficio es de 4 meses en SG. El tercer fármaco es la Enzalutamida un nuevo antiandrógeno que actúa bloqueando la señalización del complejo andrógeno-receptor al núcleo. El beneficio cuando se compara con placebo fue de 18.4 m vs. 13.6 con HR de 0.65. p <0.0001, es decir un incremento de la SG de unos 5 meses lo que representa un dato importante en estos tumores resistentes a la castración. Supervivencia Global con Enzalutamida: AFFIRM 18.4 months 13.6 months Scher HI, et al. N Engl J Med 2012 30 Está claro que estos tres fármacos inducen un importante beneficio clínico a nuestros pacientes. Sin embargo debemos valorar aquí también el Docetaxel porque marcó una época en el tratamiento del cáncer de próstata resistente a los andrógenos. Dos estudios muestran el beneficio clínico de este fármaco. El estudio SWOG-16 con docetaxel + estramustina vs. Mitoxantrone + prednisona mostró una SG de 17.5 m. vs. 15.6 m. con p=0.02. El segundo estudio TAX-327 comparaba docetaxel vs. Mitoxantrone, con una SG de 18.9 m. vs. 16.5 m. (HR 0.76. p<0.001). En definitiva el beneficio clínico era de unos dos meses. Un nuevo elemento aparece en el escenario del tratamiento del cáncer de próstata y se puede poner antes o después del Docetaxel, se refiere al Radium 223 que emite radiaciones α que actúan sobretodo en la capa de osteoclastos. Es importante destacar que el 90% de los casos tienen metástasis óseas, además de en otros órganos, pues bien el uso de radium 223 en el estudio ALSYMPCA mejora la SG, en 14.9 m. vs. 11.3 m. en el grupo placebo con una HR 0.70 y p<0.001. (Parker C, et al. N Engl J Med. 2013). Además y es un hecho importante, retrasa los eventos óseos, como fracturas, dolores y el uso de radioterapia. En definitiva todo esto representa beneficio clínico no solo en SG. Otro hecho destacable el uso de Abiterona o de Enzalutamida antes del uso de quimioterapia (Docetaxel). Así el estudio COU-302 que compara Abiterona + prednisona vs. Prednisona, la SG fue de 35.3 m. vs. 30.1 m. con HR 0.79 y p=0.0151. Hay una mejoría no claramente significativa desde el punto de vistas estadístico pero si desde el punto de vista clínico. Además se pudo ver un retraso en el dolor relacionado con el cáncer, retraso en el inicio de la quimioterapia, mejoría de la CdV, retraso en el uso de radioterapia etc., objetivos que juegan un papel importante en el beneficio clínico. El estudio PREVAIL con Enzalutamida vs. Placebo encontró un incremento de la SG media de 32.4 m. vs. 30.2 m. con HR 0.71 y p< 0.001 y un retraso en el inicio de la quimioterapia de 28.0 m. vs. 10.8 m. HR 0.35 p< 0.0001. (Beer TM, et al. N Engl J Med 2014).. En resumen estos dos medicamentos están impactando en la SG de los pacientes y en definitiva de una forma global en el beneficio clínico. Evolución Natural del Cáncer de Próstata Radium 223 CHAARTED: Doc + TDA Quimioterapia Deprivación Androgénica Post-Quimioterapia Pre-Quimioterapia Docetaxel Cabazitaxel Abiraterona Tratamiento Local Abiraterona Enzalutamida Enzalutamida PSA Asintomático No Metastásico Sensible a la Castración Sintomático Metastásico Resistente a la Castración 31 Datos procedentes de ASCO 2014 señalan que Docetaxel se puede asociar a la deprivación androgenita desde un principio. El estudio CHAARTEDE tiene el objetivo fue evaluar el beneficio de la quimioterapia hormonal inicial para cáncer de próstata metastásico con aleatorización 1: 1 TDA (Terapia Deprivación de Androgenos) solo o TDA + Docetaxel a75mg / m 2 cada 3 semanas. Los factores de estratificación fueron alto volumen (HV) frente a un volumen bajo (LV) de enfermedad (HV: metástasis viscerales y / o 4 o más metástasis óseas). El objetivo principal fue la SG y el estudio fue diseñado para evaluar una mejora del 33.3% en la mediana de SG. Los resultados de eficacia aparecen en la tabla siguiente. TDA + D mejora la SG sobre TDA en hombres con alta masa (HV). Es necesario un mayor seguimiento para los casos con LV. Intención de tratar el análisis PSA <0,2 a los 12 meses TDA 9,4% La mediana de SG (mos) N = 790 42.3 N = 520-HV 32.2 NR ** N = 270 -LV TDA + D 19,7% Valor P <0,0001 Razón de riesgos (95% CI *) 52.7 49.2 NR 0.0006 0.0012 0.0836 0,63 (0,48, 0,62 (0,46, 0,58 (0,31, 1,08) 0,82) 0,83) En el cuadro siguiente se resumen todo lo que conocemos de cáncer de próstatas en los 10 últimos años, especialmente se refiere al objetivo principal la SG que oscila entre los 2 a 13.6 meses lo que representa un optimo beneficio clínico, recorriendo las diferentes etapas del tratamiento de esta neoplasia. Finalmente en dos figuras se hace una representación de la secuenciación del tratamiento del cáncer de próstata lo que no está teniendo en cuenta las diferentes agencias. Supervivencia Global en Cáncer de Próstata Esquema Año de Aprobación Docetaxel vs. mitoxantrone 2004 Abiraterona vs. placebo 2012 Indicación Pre-Docetaxel Pre-Docetaxel Mediana de Diferencia de medianas Supervivencia Global (m) de SG (m) 0.76 19.2 vs 16.3 2.9 0-75 35.3 vs 30.1 5.2 0.70 32.4 vs 30.2 (est) 2.2 (est) Enzalutamida vs. placebo 2014 Sipuleucel vs. placebo 2010 Pre- y PostDocetaxel 0.78 25.8 vs 21.7 4.1 Radium 223 vs. placebo 2013 Pre- y PostDocetaxel 0.69 14 vs 11.2 2.8 Enzalutamida vs. placebo 2012 PostDocetaxel Cabazitaxel vs. mitoxantrone Abiraterona/pred. vs. placebo/prednisona Docetaxel/TDA vs. TDA Pre-Docetaxel HR 0.63 18.4 vs 13.6 4.8 2010 PostDocetaxel 0.70 15.1 vs 12.7 2.4 2011 PostDocetaxel 0.65 14.8 vs 10.9 3.9 2014 Inicio 0.61 57.6 vs 44 13.6 El paciente debe beneficiarse de la adecuada secuenciación del tratamiento. 32 Secuenciación del Tto. del CPRC hasta 2010 CPRC Metastásico Paucisintomático Beneficio Clínico Segunda Maniobra Hormonal No demostrado Beneficio Clínico CPRC Metastásico Paucisintomático Post-Docetaxel CPRC Sintomático Docetaxel Mitoxatrone MTS 3 meses No demostrado CPRC Sintomático Mitoxatrone MTS 3 meses No demostrado Post-Docetaxel No demostrado Beneficio Clínico Docetaxel + DA 13 meses Enzalutamida 2.2 meses Abiraterona 5.2 meses Radium 223 4.6 meses Docetaxel 3 meses Enzalutamida 4.8 meses Abiraterona 4 meses Cabazitaxel 2.5 meses Radium 223 3.1meses Esto es lo que teníamos en los últimos 10 años, después en 2014 ya tenemos mas líneas de tratamiento que con evidencia I, que han logrado un incremento de la SG, objetivo primario y representativo del beneficio clínico. El Comité Multidisciplinar de Tumores Urológicos es clave en el diseño de la estrategia terapéutica y donde el oncólogo es una pieza mas del mismo pero imprescindible. Estos comités son para el ponente el primer paso en el beneficio clínico. ¿Qué hacemos en España? El grupo SOGUS pondrá en marcha un estudio para identificar que pacientes se benefician más con las nuevas terapias e identificar marcadores biológicos, realización de biopsias liquidas, marcadores biológicos circulantes, alteraciones moleculares que rigen a estos tumores, en conjunto un adecuado seguimiento con el objetivo indudable del beneficio clínico de los pacientes. Muchas gracias por la atención prestada. 33 DISCUSION DE LA 1ª MESA. Transcriptor: Dr. J. A. Moreno Nogueira Presidencia de la Mesa. Dr. A. Antón; Dr. M. Provencio. Discusores: Dr. M. de la Puente y Dr. J. Feliú Dr. A. Antón y Dr. M. Provencio: abre el turno de preguntas. Agradece a los ponentes el esfuerzo realizado y Dr. M. de la Puente: Para abrir la discusión plantea en primer lugar el concepto de gasto global en la asistencia ya que el gasto farmacéutico es solo una parte y seria mas lógico hablar de gasto por enfermedad donde comprende no solo el gasto farmacológico sino también el diagnostico y todo aquellos gastos nesarios para la asistencia adecuada del paciente. En segundo lugar plantea también y aquí quiere hacer participar a los médicos en este caso a los oncólogos, en la autorización de un determinado fármaco que a lo mejor solo causa un beneficio/supervivencia de semanas, pero su coste puede ser de 40.000-45.000 euros. ¿Es lógico autorizar su financiación? El paciente oncológico es un enfermo crónico que supone consumo de otros recursos terapéuticos de soporte y diagnósticos que engrosan el coste. Habría que discutir el coste global. Dr. A. Antón: Plantea como organizador que el objetivo del seminario es el Beneficio Clínico y que debe diferenciarse del Beneficio estadístico, si bien son conceptos interrelacionados. En España se ha cuantificado en 30.000 euros por año de vida ganados, ¿pero por que esta cifra y no otra? Para justificar el uso de un nuevo fármaco aprobado, habría que diferenciar entre los diversos tumores porque los beneficios clínicos son diferentes. Es distinto el cáncer de próstata al cáncer de pulmón p.e. Si un fármaco sobrepasa un dintel de precio, la petición debería ser individual y discutida. Dr. M. Provencio: Plantea que en la discusión del Beneficio Clínico debe distinguir los argumentos científicos de los económicos. A los oncólogos se les pide en los ensayos clínicos unos objetivos primarios y secundarios, donde además existen diferencias. Se pregunta si en un fármaco diana aprobado se debe exigir todo esto. También habría que preguntar a la sociedad que coste está dispuesto asumir a través de los impuestos, en la calidad asistencial. Dr. J. Feliú: El beneficio clínico por lo expuesto esta mañana se interpreta de diferentes formas, para unos es la SG, otros la SLE, las respuestas, la CdV etc. Tiene que haber un consenso para que sea igual para todos. Si embargo hay diferencias entre los tumores, con bases estadísticas, no es lo mismo hablar de beneficio clínico en un cáncer de próstata que de un cáncer de pulmón. Pacientes con perspectivas de vivir menos de un año, la HR seria exigible un valor de 0.5, sin embargo para supervivencias de 2-3 años la HR debería ser de 0.70. Se pregunta también quien debe definir el Beneficio Clínico, a lo mejor el paciente, la sociedad, las Agencias Reguladoras etc. Dr. Emilio Ignacio García, Presidente de la Sociedad Española de Calidad Asistencial quiere aportar que los avances en nuevos fármacos en oncología son abrumadores, por eso los estudios existentes son de eficacia y no de efectividad en relación al coste de fármacos y saber que España es uno de los países con más prescripciones de toda Europa…… Dr. Emilio Esteban. Es imposible valorar ahora la efectividad, habría que cambiar nuestros modelos de investigación. Se tendría que hacer un estudio epidemiológico retrospectivo para poder valorar efectividad., es decir si un fármaco tiene realmente 34 impacto en la supervivencia. Por eso debemos seguir utilizando subrogados como objetivos de nuestra investigación. Dr. M. Provencio: Se dirige al Dr B. Massuti diciéndole que los nuevos medicamentos innovadores que ya están posicionados, como elegir entre ellos, ya que incluso tienen la misma o parecida HR si bien hay quien utiliza DMT. Dr. B. Massuti: Por las reglas de mercado la competencia haría bajar los precios mejorando el coste/efectividad, pero no parece que esto pueda ocurrir. Seria de mayor utilidad la búsqueda alianzas posiblemente entre la propia industria, órganos oficiales para poner unos precios adecuados ya que parecen están hinchados sabiendo que es una investigación de riesgo. Dr. E. Díaz Rubio. Esta mañana se ha hablado de beneficio estadístico más que de beneficio clínico realmente. Hay fármacos con beneficios muy claros, pero otros no, p.e. erlotinib en cáncer de páncreas que mostraba un beneficio de 15 días. ¿La pregunta es cual es beneficio mínimo aceptable? Dr. E. Esteba: Contesta al DR. Díaz Rubio y señala que aquí es donde debemos aplicar el coste utilidad o QALY, donde una minima ventaja estadística se traduce en algo difícil de compensar por la sociedad. Debemos hacernos una pregunta ¿cuanto está dispuesta a pagar la sociedad procedente de los impuestos en gastos de sanidad o en alguno de sus aspectos mas particulares?. Ningún partido político lleva esto en sus programas. Ese beneficio estadístico del valor de “p” y de HR debe tener una magnitud suficiente ya que ello se traduce en precios o gastos. Si costara 5 euros no se estaría hablando de esto aquí de los 15 días de erlotinib en cáncer de páncreas, ese beneficio seria suficiente. Dr. E. Grande: Se debe ser exigentes y las Agencias Reguladoras también. No sabe cual es el HR que seria un punto importante de discusión. Una vez aprobado por la Agencia Reguladora al haberse logrado el objetivo principal, después se debe ser más permisivo para su uso. No es lógico cambiar el HR y ser más exigentes a la hora de la indicación por el oncólogo, dificultado enormemente su uso. No puede ser que una compañía farmacéutica negocie unas condiciones de objetivos /HR o subrogados) con la Agencia Reguladora, después de cumplir esos objetivos dicha agencia ponga obstáculos para su aprobación y uso. Dr. Díaz Rubio: Es verdad que las negociaciones de la Industria Farmacéutica con las Agencias Reguladores son las que ponen el precio fármaco. A veces se aprueba un fármaco que en la negociación se acordó un HR de 0.70 pero sale 0.81 y una “p” de 0.005 y el estudio se continua y se aprueba. Esto no es razonables se debería mantener lo pactado. Dr. J. Albanell: Se pide concreción, yo creo que un beneficio en 6 meses en el tiempo a la progresión o en la supervivencia del fármaco en cuestión debería incorporarse y si además se tolera mejor que el estándar, mas justificado. Todo esto está evolucionando tan rápidamente que la industria farmacéutica y los estados llegaran al acuerdo de una disminución de precios. Se ha visto en los últimos años que ganancias incrementales de ese tipo, en la actualidad estamos hablando de importantes avances en supervivencia en cáncer colorrectal, cáncer de próstata etc. Dr. M. de la Puente: Hace la pregunta de cuantas veces los oncólogos vais a visitar al gerente del hospital para la gestión de un proceso de un determinado paciente o cuantas veces vais para incluir un determinado fármaco para un paciente con un tumor que a lo mejor tiene una supervivencia de un mes o menos. El oncólogo tiene que llevar la gestión “in situ”. Tiene que participar no solo en la gestión del servicio sino también del hospital. 35 Hemos sido un país de prescriptores y no de investigadores lo cual debe cambiar. En los últimos cuatro meses el número de nuevos fármacos es muy importante y su coste no puede ser asumido por un país. Deberá ser gestionado de alguna forma entre todos. Dr. M. Provencio: ¿Debemos los oncólogos gestionar la indicación ultima de un fármaco tras haber sido aprobada por la Agencia del Medicamento? Esto da lugar a una falta de equidad entre comunidades e incluso hospitales. Seria la Agencia del Medicamento la que debe decir si se aprueba o no, o si se financia o no. No se debe dejar la decisión para el ultimo, el oncólogo. Dr. M de la Puente: Dice que el debate no es la Agencia del Medicamento. Pone un ejemplo: Abiterona + Docetaxel ha sido aprobado en 1ª línea del cáncer de próstata metastásico. ¿Según su coste se puede aprobar según sus resultados con 4 meses de mejora de la supervivencia? El problema no es aprobar o no aprobar, sino gestionar, lo que se complica por la existencia de 17 CC.AA. Dra. Cristina Abendaño: Presidenta de la Sociedad Española de Farmacología Clínica señala que la definición de beneficio clínico es para aprobación o financiación de un fármaco. El circuito es Agencia Europea del Medicamento, Ministerio de Sanidad, CC.AA., Hospital, gerente, medico y paciente. Realmente deberían valer solo dos criterios, la Agencia Europea del Medicamento y el Servicio Nacional de Salud colectivamente y que pagamos entre todos, para poder utilizar un determinado fármaco. Seria una decisión colectiva a nivel de todo el Sistema Nacional de Salud y no estaría a nivel del hospital. Dr. A. Antón: El problema es que tenemos 17 S.N.S o 17 pagadores en el área de la salud y esto es un gran problema ya que se está afectando es la equidad. Hay CC.AA que aceptan determinados fármacos y en otras no e incluso entre hospitales de una misma CC.AA: e incluso de la propia ciudad. Hacer unos cuatro - cinco años los servicios o el jefe de servicio desconocía los costos por fármacos o por procesos, por ello en la actualidad se tienen que implicar mas en la gestión. El desconocimiento de los costos en salud en general plantea un gran problema para gestión. No conocemos lo que cuesta un paciente en cada hospital, no hay una informática homogénea, no hay transparencia en todos estos datos, por ello cada uno intenta arreglar como puede las cosas para poder disponer en este caso de los nuevos fármacos. Dr. G. López Vivanco: Su experiencia es que en su hospital solo le han dejado gestionar la pobreza como la estancia media u otras circunstancias, pero nunca la posibilidad de gestión de fármacos. El aceptar un cierto fármaco obedecía más a criterios de conveniencia, de amiguismos que a otra cosa. Comenta también que en el caso de la Abiterona es un buen fármaco que puede llevar a una amplia supervivencia en el cáncer de próstata metastásico. No debemos salir de esta Reunión con la creencia que éramos más felices con el 5FU. Dr. C. Camps: Quiere destacar que hablar de fármacoeconomía es hablar de costes partido por beneficios. Esta Reunión lo que pretendía es hablar de beneficios no de costes aunque ello sea difícil de separar. Cuando se habla con un gerente nos dice que vamos a gastar tanto por un beneficio de solo 2-3 meses. La realidad es que hay que explicarles a estos gerentes la importancia de esos beneficios en toda la historia natural de un cáncer como aquí se ha comentado, en relación a los logros en supervivencia p. e. en el cáncer de mama de 18 a 50 meses y ello ha sido paso a paso. Este es el objetivo de la Reunión saber explicar estos beneficios aunque sean pequeños y no tanto hablar de costes. Dr. B. Massuti: Quiere hacerle recordar al Dr. M. de la Puente que si bien este país es muy prescriptor, la media del gasto sanitario está por debajo de la media de los países 36 de la OCDE e incluso en ciertas neoplasias mas abajo aun. Es cierto que tenemos margen para ser más eficientes pero también habría que exigir esa eficiencia a otras áreas sociales. Dr. M. de la Puente: Se reafirma, somos un país de prescriptores. No duda del beneficio de 4 meses, pero a veces se ponen 3ª y 4ª líneas de tratamiento en pacientes muy deteriorados, ancianos etc. La pegunta: ¿Habrá que seleccionar los pacientes? Dr. J. Albanell: A veces los oncólogos parece que tenemos que pedir perdón por querer lo mejor para los pacientes, lo que resulta increíble. Quiere destacar una frase que no recuerda quien la dijo “Un millón de muertes es una estadística y una muerte es un drama”.Los oncólogos vemos los pacientes uno a uno y sabemos que unos pacientes se beneficiaran poco y vivirán menos, consumirán menos tratamientos y ocasionaran menos gastos, pero otros serán largos supervivientes con buena calidad de vida. La supervivencia global es objetivo principal. Dr. M Provencio: Es una pregunta: ¿Todos los médicos pueden poner de todo y en todos los sitios poner de todo? Dr. A. Antón: Está claro que no puede ser así. Es un tema debatido ya en el seno de la Fundación. Dr. M. Codes: Decía el Dr. Vivancos que administraba la pobreza, en Andalucía se administra la miseria. La sostenibilidad del sistema no debe ser poner al medico al frente del paciente. Para una aprobación de un medicamento en su hospital se reúne la Comisión Permanente constituida por el Directo Medico poco conocedor de la Ontología y al jefe de Farmacia que solo quieren gastar menos y el problema de no conceder el fármaco lo derivan para que el oncólogo informe al paciente. La sostenibilidad del sistema tiene que estar a otras alturas, esa información de denegación la tiene que dar otro. Esto la Fundación ECO debería comunicárselo a todos los Gerentes. Dr. A. Antón. Esto ocurre en más comunidades y la sostenibilidad del sistema es un hecho más amplio que la prescripción de fármacos. Debemos buscar aliados y que los farmacéuticos no son nuestros enemigos. Esta Reunión pretende analizar el Beneficio Clínico y explicarlo para así facilitar probablemente las autorizaciones. No tenemos que implicarnos en problemas éticos, políticos o sociales, pero indudablemente el que debe explicar esto hechos es el político y no nosotros. Dr. M. de la Puente: Explica que en su hospital en esa comisión estaba el oncólogo y hematólogo y las autorizaciones eran firmadas por todos los miembros. Esto se ha trasladado a otros hospitales. Es un tema para reinventarse. Dr. M. Codes: En su hospital se niegan absolutamente a la presencia de un oncólogo en la comisión. Dr. C. Camps: Volviendo al Beneficio Clínico tema de la Reunión. ¿Al Dr. Massuti ¿Cuál es el beneficio clínico mínimo con fármacos no diana y con fármacos diana en el cáncer de pulmón? Dr. B. Massuti: Cree que se debe tenerse en cuenta la magnitud de la población y matiza que el resultado estaría en función de la 1ª, 2ª línea, pero sin recurrir a criterios fijos. De acuerdo con el Dr. Díaz Rubio el beneficio clínico debería al final establecerse entre el oncólogo y el paciente. Contestando a una pegunta anterior señala la existencia de una Economía de Escala que desde su punto de vista ya seria aceptable y en segundo lugar la Calidad. La asistencia en España ha ido en dirección contraria precisamente de la Economía de Escala y la Calidad. Dr. G. Vivancos: Todos sabemos que un ensayo clínico positivo no significa beneficio clínico. Meternos en lo que es beneficio clínico puede ser complejo ya que cada estudio, 37 cada tumor, cada paciente puede tener un dato de beneficio clínico. Tenemos que tener las ideas claras sobre esto. Las reuniones donde se toman decisiones se basan en el axioma “la ausencia de evidencia no es evidencia de nada” y en base a eso se toman muchas decisiones. Finalmente el producto sanitario es difícil de vender y el beneficio clínico es parte de este producto. Dr. J. Pérez Gil: En la actualidad es asesor de la Fundación ECO y señala que en el área que estamos hay beneficios, sin embargo en otras áreas como las enfermedades neurodegenerativas no se ven. Por tanto es un hecho positivo. Por otra parte cuando se hizo una evaluación del gasto sanitario en el País Vasco se pudo ver que el 33% era debido a los ingresos. Si se hace una buena gestión en esto, se colabora con la sostenibilidad del sistema. Una forma de mejorarlo es la adecuada coordinación entre los diferentes estamentos, desde el hospital a la asistencia primaria. En la planificación que haga este país, mas que crear hospitales está en como gestionemos y mejoremos los ingresos que representan el 33% del gasto. Decir también que un 5% de la población hacen 1/3 del gasto sanitario, son los pacientes crónicos. Dr. A. Anton: Quiere introducir un nuevo aspecto y pregunta al Dr. Albanell que hablando de la eficiencia, independiente del beneficio clínico, está el alto coste de los medicamentos y esto es importante. La Industria farmacéutica justifica por los gastos de investigación, sin embargo no todo el mundo está de acuerdo. Por todo esto la FDA y otras agencias quieren acortar este tiempo o buscar otros objetivos subrogados y disminuir el coste del fármaco. Un ejemplo de ello fueron los resultados esperanzadores de Lapatinib en neoadyuvancia en cáncer de mama, pero estos resultados no se han confirmado en la adyuvancia. Que opinas, como lo ves. Dr. J. Albanell: Considera que no se debe aprobar un fármaco por el resultado de un solo estudio en neoadyuvancia que se ha realizado en un contexto especial. En el caso de Lapatinib creo que hace falta antes un ensayo clínico en HER2 positivo frente a un tratamiento estándar. Aprobar fármacos de forma acelerada hay que analizar todos los datos en conjunto de la enfermedad metastásica. Es cierto que no aprobar de forma acelerada p.e. este fármaco mencionado nos pone en situación difícil porque si al final se aprueba hemos dejado de tratar enfermas. Nos supone una situación de riesgo. Dr. A. de Lorenzo: Se ha hablado mucho de los ensayos clínicos y del beneficio clínico relacionado con los fármacos. Creo que se deben aclarar conceptos como hizo p.e. el Dr. Esteban al definir el tiempo libre de empeoramiento. Considera que la Fundación ECO debería promover la comunicación en relación a la investigación y la calidad de la misma y llegar hasta al papel que juega el paciente en la definición del beneficio clínico. Dr. E. Esteban: Volvemos al punto de partida, cual es el beneficio clínico que debemos buscar. Aquí se enfrenta la Medicina a la Economía o convivimos con la Economía, ya que siempre tenemos que estar ofreciendo la oportunidad a nuestros pacientes. El Sistema Sanitario es un seguro que pagamos entre todos y se debe saber cuanto se destina a ese Sistema Sanitario y ellos deben decirnos hasta donde podemos llegar en el gasto y ahí entra de nuevo el Beneficio Clínico subjetivo o estadístico. Todo esto requiere una transformación numérica, significa dinero y se debe saber cuanto está dispuesta la sociedad a invertir en salud. Dr. J. Albanell: Hace poco invitamos hablar al Dr. Antonio Rivas que lleva 18 años en EE.UU. trabajando en inmunología y melanomas siendo un referente mundial. Nos dijo que pronto el tratamiento de los tumores seria inmunoterapia+quimioterapia y se le pregunto si eso era sostenible. Contestó que si las cosas funcionan y son eficaces y cambian el contexto, se impondrán y usaran. El ejemplo que puso fue el de la penicilina que no se sabían si seria costo/eficaz y al final se impuso su uso. Si hay grandes beneficios y con la colaboración de todos se impondrá. 38 Dr. Emilio Ignacio García: Proporciona algunos datos, desde el comienzo de la crisis el Sistema Sanitario se ha retrotraído aproximadamente en 15.000 millones de euros. Antes de la crisis el gobierno invertía en Sanidad 70.000 millones de euros que nos es caro en relaciona a los beneficios que proporciona y en referencia a otros países. Sin embargo de los 500.000 profesionales sanitarios que había, se han perdido 80.000 y en el ultimo informe se nos dice que somos ineficientes en un 25% (20.000 millones de euros) por lo que tenemos capacidad para mejorar. Dr. J. Feliú: Las últimas editoriales están endureciendo los criterios de beneficio clínico en cuanto a supervivencia global. Esto como reacción a que en los ensayos clínicos para alcanzar resultados p.e. de un mes o mes y medio de beneficio lo que se hacia era aumentar el numero de pacientes a incluir y así alcanzar la HR con una p<0.05. Todo esto tiene sus pros y sus contras ya que no se debe perder las perspectivas de los pequeños avances. En cáncer de colon con las nuevas terapias y con HR de 0.75-0.87 se ha conseguido pasar de 18 a 29 meses de supervivencia. Lo importante es la perspectiva global de lo que se ha conseguido poco a poco y que ha permitido aumentar la supervivencia global de los pacientes. Dr. M. de la Puente: Como Gerente tengo poco mas que añadir, quiero que nos entendáis y compartir mas tiempo juntos ya que no hay mas capacidad económica. En la aprobación de nuevos fármacos tendrá que ser el gobierno central el que diga hasta donde se llega. Añade si en todos los hospitales hay que tratar todo, como señalando la existencia de unidades de referencia. Dr. A. Antón: Esto daría para otra mesa. La Fundación ECO toma nota de todo esto y señala la importancia de la acreditación de las unidades de referencia. Agradece la asistencia a todos y pasa la palabra al Dr. M. Provencio. Dr. M. Provencio: Quiero recordar una encuesta en los años noventa entre médicos y personal de enfermería donde se preguntaba si estaría dispuesto a recibir quimioterapia según unos beneficios. Los médicos oncólogos y el personal de enfermería de oncología eran los más rigurosos en la exigencia de beneficios. Esto es la practica diaria del oncólogo caracterizado por su exigencia. También se debe tener en cuenta el tipo de tumor y el uso de nuevos fármacos. En conjunto todo eso ha permitido tener amplias supervivencias que antes eran imposibles. Un ejemplo es el Imatinib en la LMC, donde su aprobación fue en la respuesta molecular y muchos de estos pacientes están curados. Dr. A. Antón: Da por finalizada la mesa redonda. 39 PREMIO FUNDACION ECO 2014. 40 INFORME DEL V SEMINARIO DE LA FUNDACIÓN ECO SOBRE BENEFICIO CLÍNICO DEL TRATAMIENTO MÉDICO. Transcriptor: Dr. J. A. Moreno Nogueira 41 MESA 2. OPTIMIZACION DEL BENEFICIO CLINICO. ¿QUE PAPEL JUEGAN LOS DIFERENTES ACTORES? Presiden Dra. Cristina Grávalos y Dr. Guillermo López Vivanco. El Dr. G. López Vivancos hace la presentación de esta 2ª mesa sobre “Optimización del Beneficio Clínico”, definiendo que es la optimización, “buscar la mejor manera de hacer las cosas” y esto debemos de aplicarlo para lograr el mejor Beneficio Clínico. Esta aproximación se realiza con la participación de los diferentes componentes que de alguna manera juegan un papel importante en lograr dicho beneficio. La Dra. Cristina Grávalos hace la primera presentación. 1.- Los grupos cooperativos. Esta ponencia la desarrolla el Dr. Antonio González Presidente del Grupo Español de Investigación Cáncer de Ovario (GEICO) y comienza definiendo lo que es un grupo cooperativo ¿Qué Qué es un Grupo Cooperativo de Oncologí Oncología? • Organización en red sin ánimo de lucro. • Formada por médicos oncólogos, y en general especialistas de otras disciplinas. • Cuyo fin principal es promover y desarrollar investigación clinica y traslacional. • Habitualmente académica. • Habitualmente multidisciplinar. • Habitualmente independiente. • Con el objetivo de aumentar las tasas de curación de los distintos tipos de tumores. El desarrollo de los grupos cooperativos ha sido en los últimos veinte años, habiendo incluido numerosos pacientes en los diversos ensayos clínicos. Los Grupos Cooperativos en Cifras 45.000 pacientes incluidos en EC! • 16 Grupos Cooperativos • 1995 año de constitución de los primeros GC (GECP, GEICAM, SOLTI, TTD) • 45.000 pacientes incluidos en EC. • 85.000 pacientes incluidos en estudios observacionales, epidemiológicos, investigación básica y traslacional. • 572 artículos científicos (81% internacionales) • 925 abstracs en congresos (78% internacionales) Se han incluido en ensayos clínicos unos 130.000 pacientes en diferentes etapas, destacando las fases II y III. Por todo ello no se puede separar la investigación en 42 nuestro país de los grupos cooperativos. Estos grupos independientes de los ensayos tienen otras funciones como la formación. Todos los grupos desarrollan simposios, cursos etc. en el ámbito nacional e internacional. Por ellos los grupos cooperativos participan activamente en la formación continuada de los oncólogos médicos. Los grupos tienen relación con las asociaciones de pacientes, elaboran guías clínicas con impacto en el día a día del oncólogo. También, financian becas para el desarrollo de la excelencia y la investigación. Un hecho importante es la relación de los Grupos Cooperativos con la SEOM, para lo cual firmaron un convenio el 8 de mayo 2012 para permitir el desarrollo de investigación independiente. Esto es así porque los grupos cooperativos no tienen la entidad jurídica suficiente para ser interlocutores frente a la administración, pero si las tienen las sociedades científicas. Ello permite a una comisión mixta con SEOM ser interlocutor frente a las autoridades Sanitarias. Convenio 8 de mayo de 2012 SEOM-GC Objetivo: Fomentar investigación Clínica independiente en Oncología Médica en España Comisión Mixta GC-SEOM Objetivo: Constituirse en interlocutor común frente a autoridades sanitarias en lo referente a investigación clínica independiente Composición •Presidente/a SEOM •Vicepresidente/a SEOM •Vocal de JD SEOM •3 Presidentes de GC más representados (GECP, GEICAM, TTD) Presidentes de otros GC (carácter rotatorio) consideró que lo mejor era Cuando el •3 ponente se planteó hablar en este Seminario hablar de su “libro” de lo que hace su grupo cooperativo (GEICO). Considera que el cáncer ginecológico es poco frecuente, solo el 10% del cáncer de la mujer, el 6% cáncer de endometrio y solo un 3% el cáncer de ovario. Por esto es necesario absolutamente trabajar en grupos cooperativos para la investigación clínica. Los estándares de tratamiento han salido del trabajo conjunto, un hospital solo no tiene capacidad de reclutamiento para llevar a cabo estos estudios. Casi todos estos estándares han salido del grupo cooperativo COG de los EE.UU que es muy activo. Estos son unos ejemplos de su producción científica: CAP vs. CP; Cisplatin Dose Intensity (DI); IP-Cisplatin vs. IV-Cisplatin; Cisplatin-Paclitaxel vs. Cisplatin-Cyclophosphamide (1996); Carboplatin (AUC 9) vs. IP-Cisplatin – Paclitaxel; Sequential Single-Agente vs Combination etc. ¿Que ha aportado el grupo GEICO (1999) y que ha supuesto para nuestro país? Ha proporcionado cohesión entre los grandes hospitales y los pequeños, ha permitido compartir conocimiento, metodología de trabajo y aproximarse a los programas de I+D. El grupo también ha tenido una visión internacional perteneciendo al principal grupo europeo ENGOT que es una red europea de ensayos clínico y todo esto dentro de un grupo mayor mundial denominado “Gynecolgic Cáncer Intergroup” (GCI). Así hemos participado en el estudio ICON7 para la aprobación del bevacizumab en cáncer de ovario y con el grupo GOG para demostrar los beneficios de bevacizumab en cáncer de cervix recurrente o metastásico. GEICO está también colaborando en el estudio NOVA con bevacizumab en el tratamiento neoadyuvante del cáncer de ovario. Sabemos que es útil en 1ª línea, pero se quiere demostrar si es también útil en una fase 43 anterior. En definitiva se ha contribuido al cambio de la práctica clínica en estos tumores ginecológicos en nuestro país. Los grupos cooperativos pueden ser útiles para la industria farmacéutica en el desarrollo de trabajos académicos, fruto de esto ha sido el estudio PENELOPE presentado en ASCO 2014, sobre el tratamiento con pertuzumab mas quimioterapia en cáncer de ovario resistente que tiene una alteración molecular especifica. También, puede ser al revés que trabajos académicos o colaboraciones que le interesen a la industria farmacéutica, siendo por tanto una forma de cooperación. Así tenemos el estudio SOLO-2 (ENGOT-OV21) sobre Olaparib en cáncer de ovario y el estudio sobre Noraparib vs placebo en pacientes con cáncer de ovario platino-sensibles (ENGOTOV16). También están para contestar a preguntas terapéuticas que a lo mejor no tiene interés o poco interés para la industria farmacéutica. Un ejemplo es el estudio INOVATYON STUDY que investiga si una combinación sin cisplatino en pacientes con recaída entre 6-12 meses puede tener impacto en la supervivencia. El fármaco investigado en este caso es Yondelis aprobado para otras indicaciones. También pueden intervenir en estudios que no tienen nada que ver con la industria farmacéutica como es el caso del AGO-OVAR OP-4 que pretende evaluar la cirugía citorreductora de forma “randomizada” en pacientes con cáncer de ovario cisplatino sensibles. Indudablemente el marco para este tipo de estudios es el grupo cooperativo. El ponente termina con las siguientes conclusiones: Conclusiones Los Grupos Cooperativos • Red de investigación clínica de excelencia que ha permitido una cohesión inter-territorial y acceso a I+D a hospitales y pacientes. • Marco natural e idóneo para la investigación clínica independiente y desarrollo de estrategias de tratamiento centradas en el paciente. • Sin coste extra para la administración. Muchas gracias. 44 2.- Las sociedades científicas. El Dr. Alfredo Carrato expresidentes de la SEOM aborda el tema de las sociedades científicas en cuanto a la optimización de los resultados. Las sociedades juegan un papel importante en la innovación y en la incorporación de esta innovación a la cartera de servicios de las estructuras sanitarias. Las sociedades científicas tienen que responder a las expectativas de los profesionales y de la propia sociedad y el entorno exigir que los mejores profesionales puedan dar su opinión en la materia de que se trate. La Sociedad Científica debe estar en todos los foros donde se estudie y analice los nuevos fármacos. Si se va hablar de crónicos, el cáncer es una enfermedad crónica y debe estar presente la Sociedad Científica en el debate de todo aquello que afecta al cáncer y en especial en el de los nuevos fármacos, su eficiencia e indicaciones según patologías y también debe estar presente en un foro como este. Debe ser garante de que el beneficio clínico llegue a los pacientes. La Sociedad Científica debe estar presente en las CC.AA., en el Ministerio y en todos aquellos organismo donde se debata sobre el cáncer. No debe esperar a que le llamen, debe ser proactivo y provocar su participación en todos esos foros y dar el carácter de profesionalidad y de calidad científica. El beneficio que debe traer la innovación tiene que ser avalado por la sociedad científica, valorando su eficacia, indicaciones etc., tanto en el área de la epidemiología, cirugía, diagnóstico o de la terapéutica. Se debe propiciar los encuentros entre los miembros de la sociedades científica, y los otros actores de organismo decisorios, pacientes, industria farmacéutica, sociedades de farmacia, etc., que forman en conjunto multidisciplinar y profesionalizado, lo que indudablemente afecta a nuestro sistema sanitario Además se debe exigir transparencia completa para que sea creíble y represente la opinión de todos los componentes. Hoy estamos ante un problema económico, pero existen posibilidades de hacer frente. Sabemos que un tercio del gasto farmacéutico se debe al gasto de la hospitalización de pacientes, y se conoce que el 50% de ellos podrían ser dados de alta, unos derivados a los hospitales de día, otros externalizando las exploraciones que están en espera etc. Este ahorro de recursos podrían emplearse en nuevas estrategias como la robótica quirúrgica, radioterapia en 3D, nuevos fármacos etc. Hoy la gente vive más y eso cuesta dinero. P.e. un cáncer de mama metastásico puede vivir diez o más años, pero eso cuesta mucho dinero y dentro de una población envejecida. Nuestro país es la 5ª potencia económica de Europa y creo que debe dar a sus pacientes la posibilidad de un tratamiento excelente. 45 Hay que organizar la asistencia sanitaria, no todos los servicios u hospitales pueden tratar de todo. Determinadas patologías menos prevalentes deberían concentrase en determinados servicios, con el objetivo de optimizar los recursos y una mayor excelencia. Otro hecho que destaca el ponente es que los hospitales cierran a las tres de la tarde por lo que esto debe reorganizarse y rentabilizar los recursos disponibles. Hay que hacer estudios económicos no solo el coste farmacéutico, interesa saber el gasto por paciente, pero también teniendo en cuenta que si el paciente como consecuencia de este tratamiento más o menos caro se incorpora a su puesto de trabajo, debe contabilizarse en la valoración económica. La profesionalización de todos estos retos es la respuesta. Las sociedades científicas deben profesionalizarse y llevar una línea continua y coherente que cubra las expectativas de la sociedad y lograr una excelencia que derive hacia nuestros pacientes, en el momento actual ya que estamos viviendo una realidad dinámica a la que debemos adaptarnos y que se están incorporando nuevas expectativas, nuevos actores como consecuencia de esa realidad dinámica. Está bien jugar a ser Gerentes o Presidentes, pero se les debe exigir también una profesionalización al igual que a todas las sociedades científicas ya que tienen la gran responsabilidad de lograr la excelencia para nuestros pacientes. Muchas gracias. 3.- La gerencia hospitalaria. Dr. Ricardo Herranz desempeña el cargo de director gerente del Hospital Gregorio Marañón de Madrid, y nos señala lo que es un gerente de hospital. El papel del gerente es la de ser director de una organización e integración de todos los agentes participantes. Tiene además un papel de representación y la dirección ejecutiva y de la toma de decisiones debidamente informadas y teniendo en cuenta objetivos claramente definidos que le permitan tomar esas decisiones. Se hace la pegunta ¿Qué es lo que tiene que dirigir un gerente? En primer lugar los recursos asistenciales y logísticos. En segundo lugar los recursos humanos y materiales para poder dar un servicio sanitario optimo a los pacientes. En tercer lugar gerenciar la ciencia, el conocimiento y la técnica. La evidencia científica para él es dirigir los recursos verdaderos hacia los pacientes y que deben ser fiables y al alcance de las 46 posibilidades económicas. Saber que hay mucha presunta ciencia y poca innovación. Finalmente dirigir o administrar los recursos económicos. El gerente tiene que coordinar o dirigir lógicamente para nuestros pacientes. Tenemos que procurar curarlos, cuidarlos y ante todo servirles con la máxima calidad. El paciente oncológico es un paciente especial y así lo consideramos, estigmatizado por su enfermedad, si bien ya no tanto en la actualidad. El paciente debe ser ensalzado como persona y ser humano. En el hospital tienen un programa de atención integral al paciente oncológico no referente al carácter científico o técnico, sino a otros aspectos que los pacientes aprecian enormemente. Contempla como facilitarles el acceso al sistema, atención VIP hasta que sea llamado a consultas u hospital de día, programas de atención de peluquería, maquillaje etc. Se está remodelando toda el área de asistencia oncológica del Hospital Gregorio Marañón para mejorar las posibilidades de la atención técnica y social. El gerente tiene también que dirigir para la sostenibilidad de la organización. Sabemos que cualquier organización que quiera sobrevivir tendrá que gestionarse los recursos para poder pagar sus gastos. Se debe hacer política de mercado, marketing etc., ya que ninguna organización que no cuide su sostenibilidad no podrá durar mucho tiempo. El beneficio clínico me sugiere muchas preguntas y dudas. Es un concepto heterogéneo o poco homogéneo, que tiene un aspecto técnico, social y económico. El ponente señala que para él el concepto de beneficio clínico es “liquido” porque se adapta a todo. El oncólogo es el protagonista asistencial dentro del hospital. El ponente destaca que es la estrella, que busca el beneficio clínico para el paciente, es el que asigna recursos y toma decisiones y por tanto es un gestor de los recursos. Asume riesgos y decide gastos del presupuesto. Si se gasta en una cosa deja de gastarse en otra y esto debe saberse. El beneficio clínico • • • • El oncólogo (Medico Gestor). Protagonista asistencial - Busca el beneficio clínico para el paciente - Asigna recursos – Decisiones de gestión ¿Qué es el beneficio Clínico? – ¿Cómo se toman las decisiones? – ¿Con qué evidencia? – ¿Y el paciente – la familia? • ¿Obtiene la información que le interesa o que necesita? • ¿Es libre para decidir? – ¿Es beneficio una pequeña ganancia clínica a cambio de importantes incrementos de costes? ¿Qué es para la gerencia el beneficio clínico? Esta pregunta lleva a como se toman las decisiones, con que evidencia, con que influencias. También a preguntarse si el paciente y la familia tienen una adecuada información, si es libre el paciente para decidir y si decide libremente lo que le interesa. Finalmente si es beneficio de una pequeña ganancia clínica a cambio de importantes incrementos del coste. Estas son decisiones que se toman todos los días muchas veces y las toman personas que deberían tener adecuada formación y preparación que justifiquen estas decisiones. 47 El ponente añade que ellos no forman adecuadamente a sus profesionales científicamente y en estas áreas sometidas a debate. El profesional debe tomar estas decisiones con objetividad, con una evidencia clara y formación científica. Desde la gerencia se tiene una manera distinta de ver las cosas, ya que el gerente lo es de todo el hospital. Las estancias de Oncología representan el 8.81% de todo el hospital, las consultas externas el 8.48% y el Hospital de Día el 47.84%. El gasto de farmacia en Oncología en 2012y 2013 fue del 15% y en 2014 hasta mayo del 13%. La visión de la gerencia es global y posiblemente difiere de la visión desde el Servicio de Oncología. Debemos de ver de forma integral lo que sucede al paciente oncológico, desde el primer síntoma hasta su curación o desenlace final. También debe verse la integración del proceso oncológico en la organización hospitalaria en su conjunto, intentando buscar la máxima eficiencia de los recursos utilizados. Visión desde la Gerencia Otra mirada a la atención oncológica hospitalaria El servicio de oncología vs. el hospital Visión global – Ampliación de foco La visión del proceso oncológico en su integralidad - Visión integral del proceso oncológico - Integración de los procesos oncológicos en la organización asistencial hospitalaria. - El proceso y los subprocesos - El beneficio “integral” como composición del beneficio de las partes . Desarrollo equilibrado . Sinergias - Gestión del proceso completo - “Máxima relevancia para los pacientes” El paciente oncológico durante su paso el hospital hace muchas cosas y durante mucho tiempo, acude a consultas externas, hospital de día, radioterapia, quimioterapia, cirugía, pruebas diagnósticas, laboratorio etc., es de los pacientes que más utilizan los servicios hospitalarios. De tal manera que el beneficio integral sea la composición del beneficio de todas las partes, es decir de todos los pasos que el paciente ha dado por el hospital, y esto debe estar equilibrado, pues al final el paciente tiene una visión integral de todo el proceso. Puede darse el caso de insatisfacción por el trato personal o los tiempos de espera que no influyen en su proceso y máxima satisfacción por el resto de los pasos. Esto debe estar equilibrado e integrado para ser lo más satisfactorio para el paciente. El paciente es único y el proceso también. Unas cuantas ideas. Habla sobre las 3º,4,º y 5º líneas de tratamiento para llegar a proponer que el Oncólogo es como un mago que aparece y desaparece, pero lo cierto es que está durante gran parte del proceso, pero llega un momento en que debe pasar a un segundo plano y pasar de forma precoz al paciente a la medicina paliativa para un mejor conocimiento con estos nuevos profesionales y el propio paciente y colaboren en el control de sus síntomas. 48 Algunas ideas Optimización de los recursos • • El Oncólogo y los dispositivos asistenciales oncológicos – Quimioterapia 3ª y 4ª línea – Oncólogo como “mago” – Aparición relevante – Protagonista clínico – Desaparición oportuna – “Transición precoz” a la medicina paliativa(ASCO) – Auditoría de calidad de la CE de CPP en HGU “Gregorio Marañón” Iniciativas útiles con aportación de recursos – Potenciación de EE.CC – Aportación del EE.CC -- Aportación del Hospital En el Hospital Universitario Gregorio Marañón ya existe desde hace unos cuatro años una consulta para paso precoz de los pacientes dependiente de Cuidados Paliativos, con magníficos resultados y que próximamente serán presentados los datos de una auditoria.. Manifiesta que esto les supone a los pacientes un beneficio importante con una mejoría de la supervivencia, de la calidad de vida, mejor control de síntomas, el paciente y familia son más conscientes de la situación real, proporciona una reducción de la carta del cuidador, y evita las penalidades de unas quimioterapias agresivas y los costes de la misma. En los EE.UU. el 20% de las quimioterapias se ponen en las dos últimas semanas de la vida del paciente con unas ganancias de 20-80 días con peor calidad de vida, y esto se debe a las excesivas expectativas del paciente y a la falta de pericia de los oncólogos al valorar la situación real del paciente. El paso precoz es el paso previo del paciente a los Cuidados Paliativos de forma definitiva. La consulta precoz se entiende como un hecho menos amenazante, y que todavía se pueden hacer cosas. Son consultas difíciles y complicadas, una mezcla de honestidad, honradez, rigor, firmeza en el tratamiento y siempre con esperanza. Una última idea es la necesidad de incrementar los recursos, lo mejor indudablemente. Potenciar los ensayos clínicos que reportan ingresos para diferentes retribuciones, pero el hospital también aporta mucho, más o menos remunerados según los casos. El número de ensayos clínicos en oncología han ido creciendo y en 2014 hasta junio, 28 estudios, esto también ha inducido una facturación creciente que en el periodo señalado anteriormente fue 713.821 euros. El hospital se ha beneficiado además al evitar el gasto del consumo de determinados fármacos. Es una buena política especialmente en un momento de crisis. Muchas gracias. 49 4.- Los servicios de farmacia. El ponente Dr. José Luis Poveda aborda dentro de esta Mesa Redonda, el tema de los Servicios de Farmacia y señala que el farmacéutico es parte del equipo multidisciplinar formado por gerentes, directores económicos, oncólogos y otros agentes que tienen que decidir de tratar o no tratar en relación a la autorización de los nuevos fármacos. Hace unas reflexiones iniciales, en primer lugar sobre el beneficio clínico y señala como ejemplo que en el 2012, solo un fármaco de los 13 aprobados por la FDA producía unas ganancias en supervivencia superiores a 2 meses. Cuando hablamos del nivel de evidencia, básicamente son IIA y es la evidencia que hay. El ponente además considera que hay evidencia en algunos grupos de población pero no en otros en orden a la edad y sería necesario incorporar datos genéticos a los estudios, por lo que existe un “Gap” con determinadas poblaciones que sería necesario revisar. En cuanto a los Cuidados Paliativos ya ha sido expuesto en la anterior ponencia, pero es un tema que hay que plantear desde el punto de vista de la eficiencia o mejor aún de si se están proporcionando los mejores cuidados a los pacientes, en algunos casos señala el ponente que pueden dar mejores resultados que el tratamiento más específico del cáncer. Otro tema son los tratamientos calificados como “end-of-life” donde el NICE ha aprobado algunos tratamientos de esta naturaleza aplicando una ponderación de 1.6 para los AVAC ganados. La realidad en cuanto al coste de los fármacos, independiente de los factores que influyen, es en definitiva la sociedad la que tiene que determinar cuánto está dispuesta a pagar y esto no está hecho. En relación a los IPT (Informes Posicionamiento Terapéutico), muchos pendientes de publicarse; en cáncer hay uno de cada tres, es decir el 33%, por tanto hay un arsenal de reserva optimo y queda saber en qué entorno terapéutico y económico se deben hacer. Tenemos incertidumbre en numerosas indicaciones terapéuticas y es importante decidir cuál es el mejor tratamiento para los pacientes. Grado de incertidumbre en las decisiones terapéuticas para decidir El “mejo” tratamiento para un paciente. • Muchas situaciones clínicas no tienen nivel de evidencia I. • Existe cierta controversia sobre “end points” y el valor δ • El período de latencia entre diseño y resultados hace perder validez externa a algunos EC. • La significación clínica y/o estadística 50 • • • • Rara vez hay comparaciones directas. Frecuentemente los tratamientos más activos se asocian con mayor toxicidad. “Gap” eficacia/efectividad. Población geriátrica Factores favorecen el sobre-tratamiento. Optimizar tratamientos. Para el ponente en la Oncología del siglo XXI, hace destacar la necesidad de favorecer a los pacientes con tratamientos basados en la evidencia, con las medidas de efectividad y siguiendo indicadores de procesos. La Oncología de siglo XXI • • • • Todos los agentes debemos favorecer el acceso a los (escasos) tratamientos basados en la evidencia • Industria: coste relacionado con su valor • Transparencia Administración Sanitaria • Equipo asistencial: consenso. No derrochar recursos Para la mayoría de los casos: terapia centrada en el paciente Medida de resultados de efectividad: • CER (comparative effectiveness research • Datos locales • Big Data Indicadores de proceso El ponente no hablará de los beneficios, quiere referirse ahora a los riesgos principalmente del tratamiento oncológico y sobre todo como poder reducirlos lo que significa indudablemente un beneficio para los pacientes. Sabemos que la quimioterapia antineoplásica es una terapia de riesgo por la complejidad de los esquemas y porque intervienen numerosos actores, por eso el sistema y los pacientes lo consideran una terapia poco segura. El número de pacientes y de tratamientos es muy elevado y hay que asegurarles la seguridad del tratamiento: principios activos, dosis, concentración, vías y velocidad de administración, tratamiento de soporte, esterilidad etc. Se debe ser consciente del riesgo que corre el paciente pero también el personal sanitario como consecuencia de errores. Si no se logran beneficios con una opción terapéutica no deben ser sometidos riesgos. Otro paso importante es la garantía del circuito farmacoterapéutica desde la prescripción hasta su terminación con la administración y el seguimiento del paciente. Prescripción electrónica Validación Farmacéutica Preparación PACIENTE Dispensación Administración 51 La programación de la administración debe ser electrónica y hay abandonar el papel, a pesar que numerosos hospitales la mantienen. El formato electrónico nos permite asegurar prescripción a tiempo real, integración con otros sistemas de información, asistencia en la elección de tratamientos, individualización de la prescripción, programación del plan terapéutico, cálculo de dosis (datos antropométricos, función renal y/o hepática), alertas farmacoterapéutica (dosis máximas, intervalos nosológicos, ajuste de dosis según función renal, etc.). Esto permite una indudable seguridad al existir una validación farmacéutica. La implementación de la prescripción electrónica asistida supone una reducción del riesgo absoluto de errores de medicación de un 40,02% y una reducción del riesgo relativo de un 92,03% (Gramage Caro, T.; Bermejo Vicedo, T. y Benedi González, J. An. Real Acad. Farm. Vol 79, Nº 3, 2013, 450-464)., lo cual es demostrativo de la optimización del sistema, y desmonta la utilización del papel, que en su tiempo cumplió una importante función. Es difícil optimizar el beneficio si en el sistema utilizamos el papel donde existe un riesgo relativo del 92.03%. Otro hecho importante es la integración de este sistema con los laboratorios, con los sistemas de soporte, con la historia clínica electrónica etc. ¿Pero cuantos hospitales tienen esta optimización? No muchos, pero es un hecho necesario, un programa informático que es mucho más barato que otros gastos hospitalarios. Algo que tiene que ver con la validación es la capacitación, en EE.UU. existe una especialidad farmacéutica “Board of Pharmacy Specialties”. , siendo España el segundo país con más farmacéuticos especializados en Oncología. Más de 100 BCOP (Board Certified Oncology Pharmacist) en el año 2012. Los servicios de farmacia han intervenido en el desarrollo de esta especialización y ha sido la mejor forma de optimización de los resultados y en definitiva del beneficio, como aparece en la siguiente tabla. Validación Farmacéutica y Seguridad Doble evaluación independiente previa a preparación Identifica oportunidades de mejora de la farmacoterapia del paciente individual Detecta incidencias: situaciones potenciales de EM y/o PRM • Alertas predefinidas normalizadas • Alertas personalizadas Instaura acciones correctivas/preventivas En publicaciones para detectar errores de medicación con y sin validación se detectan diferencias sustanciales. En un estudio en el Hospital Universitario La Fe (Valencia) se detectaron 172 errores de medicación asociados a la prescripción y de estos 82 con una gravedad de 4 y que fueron solucionados. Si además agregamos al farmacéutico a los equipos asistenciales, cosa que no todos los hospitales hacen, se mejora no solo en términos de reducción de costes sino también en una mejor eficacia y seguridad del proceso, con una mayor tasa de detección de errores de medicamentos y una reducción del riesgo de morbilidad farmacoterapéutica. 52 En relación al tema de preparación y dispensación señalar que ya no valen tener solo las cabinas de flujo vertical al existir nuevas normas del Marco Legal Europeo y en las guías de buena práctica, que exigen condiciones de fabricación similares a las que tienen la industria farmacéutica. Hay que evitar la mínima contaminación microbiana o de partículas y pirógenos. Se deben tener las condiciones de control de partículas dentro y fuera de la cabina, control de temperatura, humedad y presión, disponer en definitiva de áreas blancas de biopeligrosos. Desde fuera de esta área, se ven señales de condiciones estándar (luz color verde) o de desviación de las condiciones estándar (luz color rojo), poniéndose en marcha los mecanismos de rectificación, lo que en definitiva es saber si nuestra practica es la correcta. Para todo esto se necesitan recursos. Cuando se hacen estudios sobre errores de medicación, se observa que son importantes como aparece en la figura siguiente. ERRORES DE MEDICACIÓN en la elaboración de citostáticos Aguiletta y cols. Aten Farm. 2011; 13:239‐243 Usar gravimetría que no se hace en todos los hospitales, y significa que se puede detectar un 5.3% aun 7.8% de desviación posológica de todo lo que se prepara, lo cual puede ser no significativo. Hay que incorporar tecnología en este sentido y código de barras. Hay que dar trazabilidad a todo el proceso para saber quién está haciendo las cosas, y demás preguntas que aparecen en figura siguiente. 53 Trazabilidad completa La dispensación y administración deben ser seguras, hoy se dispone de bombas de administración asistida integradas en el proceso de prescripción, dispensación y administración, con identificación del paciente, del personal de enfermería, ubicación, vía de administración, fármaco, etc. Todo esto es muy importante porque se pueden reducir los errores de administración en un 73% (reducción absoluta del riesgo 3.10.8/1000 dosis). De todos los que estamos aquí clínico, farmacéutico o gerente su objetivo es que los errores fueran cero. Pero las cosas no son así, sin embargo hay medios para reducir los errores. De cada 1000 errores potenciales relacionados con medicamentos, con las nuevas tecnologías podríamos reducir el error en un 95%, pero aun quedaría 48 de cada 1000 que podrían originar daños no deseables, y esta tecnología no está aún a disposición de todos los hospitales. Proceso Prescripción Validación Control Bombas electrónica farmacéutica gravimétrico inteligentes Reducción ↓ 40% Errores remanentes Proceso 600 ↓ 68% ↓ 7,8% ↓ 73% 192 177 48 Prescripción Validación Control Bombas electrónica farmacéutica gravimétrico inteligentes Reducción ↓ 95% Errores remanentes 48 En el Hospital Universitario La Fe de Valencia se considera que en la Unidad de Oncohematología por donde pasan diariamente 95 pacientes, hay una estimación de 54 1.9 errores de medicamentos al día y 694 al año y con toda la tecnología hay 34 errores de medicamentos al año y 10 pueden tener consecuencias importantes. Por último la participación del farmacéutico en el área de la monitorización de la adherencia al tratamiento, ya que cada vez más hay fármacos por vía oral. La adherencia del paciente oncológico en tratamiento con quimioterapia oral es del 75-80% al año de tratamiento y solo del 50-65% al quinto año de tratamiento. En cáncer de mama la no adherencia al tratamiento hormonal adyuvante se asocia a un incremento de la mortalidad y a una disminución de la supervivencia- En el caso de la LMC tratadas con imatinib la no adherencia al tratamiento produjo recaídas citogenéticas en pacientes en remisión. La reanudación del tratamiento indujo de nuevo la remisión de la enfermedad tras dos meses en los pacientes no cumplidores. En otro estudio sobre LMC e Imatinib, los pacientes no adherentes lograron menor tasa de respuesta citogenética completa (26% vs. 44%, p=0.004) y la supervivencia a los 5 años fue menor con respecto a los pacientes sin interrupción de la dosis (59.8% vs. 76.7%, p=0.011). Hay también estudios con tamoxifeno y con inhibidores de las aromatasas que nos confirman estos datos. Por tanto el farmacéutico dentro del equipo asistencia juega un papel importante en el área de la adherencia que influye mejorando resultados globales como hemos visto. Para finalizar resumiendo las aportaciones de los farmacéuticos han sido diversas. Han promovido cambios tecnológicos en el circuito para mejorar la seguridad, sin embargo no todos los hospitales están al mismo nivel. Han optimizado la preparación y mejorado la trazabilidad de todo el circuito farmacoterapéutico y finalmente han dado un valor añadido a la validación y dispensación (interacciones, adherencia, ajuste de dosis, medicación adyuvante, conciliación de tratamientos etc.), dando seguridad y disminuyendo los errores de medicación con un claro beneficio para los pacientes. Muchas gracias 5.- La industria farmacéutica. El Dr. José Ramón Luis –Yague comenzó hablando de una reunión que había tenido anteriormente, donde hizo según asistentes, un dibujo catastrofista, pero señala que es una realidad. La industria farmacéutica está íntimamente ligada al Sistema Nacional de Salud, si se despeña este sistema se despeña la industria farmacéutica, porque este es su negocio y los problemas existentes los tenemos que resolverlos entre todos. 55 La industria farmacéutica lo que hace es investigar, desarrollar y comercializar medicamentos que siempre aportan un beneficio. Los medicamentos siempre aportan y no se puede decir que hay una innovación poco relevante, hay una innovación disruptiva que ha cambiado el panorama de muchas enfermedades y otra innovación que hace subir peldaño a peldaño de una escalera y han supuesto poco a poco unos logros en supervivencia que no se vislumbraban hace 10 años y en el caso del cáncer ha sido espectacular. Esto es un trabajo de todos, investigadores, farmacéuticos y profesional médico que tiene la capacidad de diagnóstico y tratamiento reconocido por la sociedad y las autoridades sanitarias y además también la responsabilidad social y legal. A la industria farmacéutica lo que le corresponde es desarrollar los medicamentos con todas sus ventajas e inconvenientes. Es un proceso complejo como observamos en la figura siguiente: PROCESO DE I+D DE UN MEDICAMENTO. Descubrimiento + preclínica Fase I 52.2 meses 12.3 m. Fase II 26 m. Fase III 33.8 m. Aprobación 18.2 m. Total tiempo 146 m. ~12 años La investigación de nuevos medicamentos es un proceso arriesgado, complejo, largo, costoso y con una comercialización con fecha de caducidad. Arriesgado: De cada 10.000 moléculas investigadas solouna acabará siendo un medicamento comercializado. Complejo: Participan cientos de profesionales con la mas alta cualificación. Largo: La investigación y el desarrollo preclínico y clínico dura entre 10-15 años. Costoso: el gasto asciende a mas de 1.000 millones de euros. Caducidad: Los derechos de patente son de 10 años, a partir de su vencimiento puede autorizarse y comercializar EFG. Es un proceso arriesgado porque de cada 10.000 moléculas una sola acabara en medicamento, pero significa que el resto de las moléculas se desechan lo que supone un gasto importante. Cuando el fármaco sale al mercado tiene que pagar todo el proceso de desarrollo, siendo más complejo en los productos biológicos. El fármaco tiene fecha de caducidad a los 10 años por lo que da entrada a los genéricos que conducen a un abaratamiento en la prestación, pero se tiene que seguir con las inversiones. La disminución del coste de prestaciones farmacéuticas nos tendría que ayudar a pagar la innovación y no a pagar la sanidad. Una disminución del gasto de las prestaciones sanitarias lleva parejo una disminución de los presupuestos en sanidad de las CC.AA y por tanto menos dinero para la innovación y avances, en especial en el tratamiento del cáncer. ¿Por qué ha disminuido la inversión en I+D? Por disminución de las ventas, el mercado se ha contraído un 29%, que significa unos 4.000 millones de euros que es prácticamente el gasto farmacéutico hospitalario. Por la política de fomento del consumo de genéricos o principios activos no justificado ya que el precio de las macas originales son similares en la mayoría de los casos. Por las barreras a la innovación en las diferentes CC.AA lo que conduce a una falta de equidad indudable en la disponibilidad de fármacos en el tratamiento de los pacientes con cáncer. 56 Un trabajo publicado por una consultora donde se analizan 21 medicamentos innovadores contra el cáncer que representan el 80% de los tratamientos en oncología, se ha visto que entre el más dispensado y menos dispensado hay una diferencia del 42% y esto no se justifica por la lógica de la variabilidad de la práctica clínica. Es por otras razones como barreras a la innovación, con diferencias entre las distintas CC.AA. La esperanza que podían significar los Informes de Posicionamiento Terapéutico parece frustrarse ya que alguna comunidad ha dicho que los revisará favoreciendo la falta de equidad actual. La negativa del uso de un medicamento innovador por su coste a un paciente no es papel del médico o farmacéutico, debe proceder de otros noveles de decisión., por eso en este problema todos los protagonistas tenemos que ir juntos para darle una posible solución. La industria farmacéutica invirtió 972 millones de euros en I+D en 2012 (2.666.000 millones al día). La principal partida del gasto, 479 millones de euros, fue dedicada a ensayos clínicos y se invirtieron más de 140 millones de euros en investigación básica. La investigación IC realizada por la industria farmacéutica ha aumentado en un 86% en los últimos 9 años (258 millones en 2004). Todos estos datos son el resultado de una encuesta en los 200 laboratorios que están integrados en Farmaindustria, aunque no tenemos los últimos datos habrá una disminución de los recursos en un 3-8%, lo que supondrá disminución en la investigación del 20%. Analizando los datos del Proyecto Best, una amplia base de datos, las gráficas de 2013 en relación al número de ensayos (EE.CC), participaciones en los ensayos (PCEC. Hospitales que participan)) y pacientes previstos en las áreas de oncología y hepatología, se puede apreciar que en ese año tanto el número de ensayos como la participación en el área de oncología han caído bruscamente, particularmente en el porcentaje de pacientes. En hematología tanto los ensayos como participantes han tenido una tendencia creciente. El número de pacientes se encuentra estancado. Otros datos procedentes del Proyecto Best, es ver en que ensayos se estén participando, en oncología cerca del 12% son ensayos en fase Ia y que más del 60% de los ensayos en las dos áreas, son en fase temprana: Ia, Ib, y II, lo cual es un reconocimiento de nuestros investigadores y de la calidad de los centros hospitalarios. Existen otros indicadores importantes también procedentes del Proyecto Best en relación a tiempo y reclutamiento: 1) Envío del 1º paciente, mide el tiempo desde el primer contacto del promotor con el investigador y la entrada en el ensayo del primer paciente. 2) Envío de autorización. Este tiempo se mide desde el primer contacto hasta la aprobación del ensayo por los Comités Éticos y de Investigación (CEI) y de la Agencia Española de la realización de ensayos. Aquí existe un problema, la diversidad de CEI en el estado de las CC.AA. Una agrupación regional de estos CEI acortaría los tiempos de espera. 3) Visita de iniciación del primer paciente. 4) Tasas de reclutamiento. 5) Participaciones sin reclutamiento. Hay centros que entran en el ensayo, pero después no reclutan, lo cual ha ido aumentando. Esto es posible por las barreras que se interponen en el propio hospital o comunidad, pero más importante aunque el reclutamiento es competitivo, y hay países con más facilidades de reclutamiento. 6) Velocidad de reclutamiento 57 En definitiva viendo las curvas que eran ascendentes, en la actualidad son descendentes, lo que resta credibilidad a nuestros investigadores. La dispersión existente por la estructura del estado es un problema para investigación en España. El ponente muestra un diagrama de competitividad con los indicadores ya señalados. Valores mayor de 1 significa peor prestaciones. Este diagrama ha sido muy útil para saber dónde hay que mejorar y para la discusión con las autoridades sanitarias de las Comunidades. Para terminar se hace unas consideraciones sobre la valoración de indicadores: CONSIDERACIONES SOBRE LA VALORACION DE INDICADORES 1.- Los tiempos transcurridos desde el envío de los ensayos a los CEIC al reclutamiento del 1º paciente, han disminuido especialmente en Hematología. 2.- El tiempo desde el envío al CEIS a las autoridades AEMOS se encontraba estancado. Sin embrago en los últimos años ha aparecido un incremento. Destaca un fuerte aumento de Hematología en el 2013. 3.- El tiempo transcurrido desde la visita de inicio al reclutamiento del 1º paciente ha disminuido en los tres últimos años. 4.- La tasa de reclutamiento en Oncología se encuentra estancada alrededor del 80% en los últimos años. En el caso de Hematología hay un componente errático, en parte debido al escaso numero de casos. 5.- Las participaciones sin reclutamiento han crecido en Oncología, especialmente en el ultimo año. En Hematología se vuelve a manifestar su comportamiento errático: 50% sin reclutamiento en el 2011 a un 0% en el 2012 y a un 10% en 2013. En el resto del área en 2012 y especialmente en 2013 han crecido significativamente. 6.- En el ultimo año la velocidad de reclutamiento en Oncología se mantiene estable. En el resto de las áreas ha ido aumentando salvo en 2013 que tuvo una caída significativa Muchas gracias 58 DISCUSION DE LA 2ª MESA. Transcriptor: Dr. J. A. Moreno Nogueira Presidencia de la Mesa: Dra. Cristina Grávalos y Dr. Guillermo López Vivanco Discusores: Dr. Cesar Pascual, Dr. Emilio Alba Conejo, Dr. Carlos García Girón Dra. Cristina Grávalos y Dr. Guillermo López Vivanco: Agradecen a los ponentes el esfuerzo realizado y se abre el turno de preguntas. Dr. Cesar Pascual. Manifiesta tener muchas reflexiones de todo lo dicho esta mañana y por la tarde en este Seminario. Echa en falta que profesionales y sociedades científicas en 2014 continúen con una posición reivindicativa lastimera y de victimismo. Señala que se pide que la sociedad o estamentos políticos nos digan cuánto vale un QALY, y no se ha opinado ni se ha tomado decisiones sobre ese coste. El personal sanitario dedicado a la asistencia oncológica debe tomar posiciones sobre esto. Es muy común oír a muchos que el sistema sanitario no es sostenible y la realidad es que tiene un buen margen aun. En lugar de hablar de sostenibilidad habría que hablar de la utilidad de exploraciones hechas al final de la vida o de las 3ª o 4ª líneas de tratamiento oncológico; eso si es posicionarse. Todo esto aquí sí se puede discutir. Dr. Emilio Alba. Cada vez se habla con más claridad de los problemas que nos afectan. El compromiso es de todos y si bien al final es una cuestión política, esta tendrá que resolverse entre todos los que participan. Para él lo importante es decir prospectivamente que es el valor, que añade valor. Lo que añade valor se hace, y debe quitarse no que no tiene valor y con ello se haría una gran aportación a lo que disponemos en la actualidad. Muchos gerentes siempre nos hablan de 3º, 4º y 5º líneas de quimioterapia, pero ¿sabemos cuánto nos cuestan esas quimioterapias? No se sabe y considera que esto no es lo importante. El problema está al principio, cuestiona que se hace inicialmente: ¿Cuántas exploraciones diagnosticas? ¿Actos quirúrgicos? ¿Indicaciones de radioterapia que son baratas? Habría que analizar todo esto, no hay que focalizarlo todo en los fármacos. La industria farmacéutica también juega su papel, se debe pagar si el fármaco en cuestión aporta valor y no fijarse tanto en el gasto del desarrollo. El valor es una decisión social y política. Si aporta valor se aprueba y no hay nadie que impida su utilización. Sino aporta valor no debe aceptarse. Esto sería un incentivo para potenciar el desarrollo fármacos que aportan valor. Dr. Carlos García Girón. Inicia su intervención suscribiendo todo lo que ha dicho el Dr. E. Alba, pero quiere señalar además que el lenguaje que se utiliza es confuso y hablar de beneficio clínico por parte del paciente al que no se le suele preguntar, o el oncólogo, o el farmacéutico o los gerentes, seguro que tienen ideas y conceptos diferentes. Si se habla de calidad de vida, que se hace mucho, no tienen una definición clara de lo que es. Se habla del paciente y en muchas situaciones el paciente es el pretexto no una razón como debería de ser y de ello habla además cualquiera. Se habla también de recursos humanos que se cuantifica, pero habría que distinguir entre precio y valor. Los protagonistas han cambiado su discurso, los farmacéuticos hablan de beneficio clínico de un fármaco y el oncólogo del precio y el gerente habla de pacientes, que no significa lo que significa para el clínico. En resumen hay que definir de lo que hablamos, que queremos decir cuando hablamos y cuáles son nuestros interlocutores. El grado de preparación de todos estos actores no es el mismo. Por un lado está la formación del oncólogo bien definida, pero ¿dónde se forman los gerentes? ¿Dónde está esa escuela de formación de gerentes? ¿Tendrían un sistema MIR? Hacen un curso y ya 59 son gerentes capacitados. Finalmente decir que el que tiene el poder no tiene la responsabilidad y el poder se debe asociar a la responsabilidad, sino es muy fácil ejercer el poder. Dr. G. López Vivanco. Quiere decir algo sobre las cosas que ya han sido comentadas. En primer lugar ¿es libre el paciente para decidir o el oncólogo para decidir? Siempre hay una tercera persona que no está al frente del paciente y en base a que contenidos. También se ha hablado teniendo como fondo los costes, de las 3º y 4º líneas de tratamiento o los ingreso inadecuados, muchos de ellos por retraso en exploraciones complementarias o frecuentemente por problemas sociales, y considera que todo esto es anecdótico. Otro aspecto es la reclamación de los Cuidados Paliativos como parte de la Oncología ya que muchos servicios los hacen y lo hacen muy bien. Se plantea un problema ético en relación al uso de fármacos en los ensayos clínicos, que son eficientes desde el punto de vista de costes y resultados, pero que posteriormente no pueden ser usados en la práctica clínica al no ser aceptados. Dr. M. de la Puente. No se debe entrar en la polémica en la formación o capacitación del gerente o del oncólogo. En relación a los gastos insiste que hay que poner encima de la mesa todos los gastos, los farmacéuticos, los TAC, RMN a veces sin justificación, medicación no útil en el final de la vida etc. Para todo esto hay que compartir las decisiones. El gerente gestiona, pero el oncólogo también le tiene que dedicar un tiempo a gestionar. Es una labor de todos. Muestra un gran interés en la ponencia donde habló de los ensayos clínicos, especialmente en las fases iniciales. Finalmente define que los gerentes pueden ser dimitidos en cualquier momento incluido el político. Dr. J. R. Luis-Yague. Que difícil lo tienen los gerentes cuando tienen que administrar presupuestos cada vez más insuficientes. Los datos recientes de la OCDE señalan que el presupuesto sanitario es el 6.7% del producto interior bruto y bajando, ya que estos son los datos del 2011. Lo tienen difícil. En el valor de los medicamentos totalmente de acuerdo con lo dicho hasta ahora, pero el problema es cómo se evalúa, los economistas de un sistema de salud evalúan los costes sanitarios directos e indirectos, los tangibles y los intangibles. Por eso la evaluación total del coste puede ser desde una amplia perspectiva social o también considerando el coste de los antiguos fármacos y el de los actuales, si esto es así y es lo que actualmente se hace, tendremos muchos problemas. Dr. Ricardo Herranz. He pretendido en mi intervención hablar del paciente como persona, antes del diagnóstico, durante la quimioterapia o antes de morir. Indudablemente que cada uno es responsable de sus decisiones sobre todo de su dinero, si es público son otras cuentas. Es importante ahora hablar de oncología y no airear otras situaciones. Dr. Martín Algarra. Como ya se ha comentado es cierto que la expresión catártica puede ser adecuada como desahogo, pero no conduce a ningún sitio. Se debe aprovechar un foro como este donde oncólogos, farmacéuticos, gerentes, industria farmacéutica etc., hablan del beneficio clínico del tratamiento con fármacos que cambian el paradigma terapéutico de un paciente, pero no los podemos asumir o no sabemos asumirlos. Tenemos que tener foros como este donde debatir estos temas con la intención de proponer soluciones. Dr. A. Anton. La pregunta ya ha salido varias veces en el transcurso de este Seminario: ¿Quién pone precio a los AVAC/QALY? Es ponerle pecio a la vida, a los años de vida de un paciente. Esto ha sido debatido en diferentes escenarios de la 60 oncología sin llegar a un acuerdo. Podría ser la SEOM, o la sociedad de Gerentes. No lo tengo claro. NICE (Nacional Institute for Clinical Excellence), ya lo tiene hecho incluso para los últimos años de vida del paciente. Lo cierto es que tenemos entre todos tomar esta decisión para poder tener una base de referencia. Tenemos que tener una referencia del coste de vida ganado por año. Dr. Cesar Pascual. Estamos reclamando tener un NICE y a la espera que las Agencias de Evaluación Españolas lo hagan pero no lo hacen, el problema está que en el triángulo “coste-valor-precio”, solo el coste es objetivo, precio y valor es subjetivo, por ello sino tenemos NICE, serán las sociedades quien tenga que definirlo y buscar un amplio consenso social, ya que las administraciones irán a rastras por detrás y tenemos que tomar decisiones día a día, por lo que es importante tener un referente. Dr. Carlos Camps. En relación con los precios hay una publicación de la Fundación ECO en la revista de las sociedades científicas oncológicas, producto de una amplia consulta entre oncólogos de la Fundación y un amplio número de expertos, pudiendo ser la referencia para iniciar el trabajo. Ya que aquí están gerentes se está hablando mucho de los medicamentos pero no hay referencias a las reformas administrativas para mejorar la eficacia de los Servicios de Oncología de los grandes Hospitales Generales en relación a los retrasos diagnósticos, terapéuticos, diversas puertas de entrada etc. ¿Pueden decir algo sobre esto?. Dr. Cesar Pascual. Conocía la publicación a la que hace referencia el Dr. Camps y hay otras de autores españoles que han escrito algo sobre esto y de economistas de la salud, pero aún son poco consistentes para tener una base sólida real. Las organizaciones hospitalarias españolas son antiguas, se podría decir del siglo XIX en relación a una empresa moderna, por lo que se requieren modificaciones importantes. Se ha hecho algo con las Unidades de Gestión Clínica, pero creo que no solucionará los problemas. No es fácil y será a largo plazo. Dr. José Luis Poveda. Sin querer entrar en polémica de quien tiene que hablar de cada cosa, lo importante es hablar en los mismos términos para entendernos. Es importante que el oncólogo hable de Farmacoeconomía y que el farmacéutico pueda hablar de eficacia clínica, porque leyendo se informa uno. Lo importante es hablar y entendernos. La farmacia como servicio de soporte enseña que para avanzar en una profesión sanitaria es necesario hablar y colaborar. La crisis económica unas de las cosas que ha traído es la mayor conexión entre el clínico y el servicio de farmacia, no para recortar, sino para optimizar. Dr. G. López Vivanco. Un tema que ha salido y no se ha comentado es la “sostenibilidad del sistema”. Cree es un mensaje político para meter miedo. El problema es que el ciudadano deje de creer en el sistema, esto si es un peligro. El defiende el sistema público en el que siempre ha creído. Comenta el desarrollo equilibrado referido por el Dr. Ricardo Herranz y hace un planteamiento sobre un paciente: Un cáncer de próstata se opera con robótica “Da Vinci”; posteriormente las cosas no van bien y el paciente fallece, pero no se le ha podido dar Abiterona, solo por un problema de precio. ¿Se puede explicar esto? Dr. Alfredo Carrato. En contestación a las reflexiones del Dr. López Vivanco, poniendo los pies en el suelo y teniendo en cuenta lo que se ha dicho sobre el precio del AVAC, confianza en el sistema, sostenibilidad etc., la realidad es que vivimos sin un NICE que fue creado en Inglaterra hace tiempo, donde tienen una bolsa para financiar medicamentos innovadores aun no aprobados por ellos. No tenemos nada de esto. Además tenemos 17 CC.AA donde no se respeta lo que dice el Ministerio de Sanidad y poner precio a la vida en un foro de debate va a tener 17 precios diferentes. Será una barrera más y no una ayuda. 61 Dr. M. de la Puente. Hacemos lo que podemos en cada hospital. En el que dirige, el Hospital de Fuenlabrada, se ha reunificado en solo edificio toda la Oncología conexionando los servicios implicados, para optimizar y gestionar recursos. Dr. José Luis Poveda. Refiriéndose a la sostenibilidad, hay un informe del Banco de España reciente donde presenta el escenario del 2014 proyectado al 2050-60 y señala que en ese periodo de tiempo el gasto sanitario solo puede crecer entre 1.5-3.5 en términos de PIB. Entre 2003 y 2010 creció un 60%, por lo que no sabe si es sostenible pero si necesita una revaluación. En el mismo informe hace dos reflexiones que la contribución demográfica es pequeña en términos de costes sanitarios y en términos del PIB un 45% y un 50% en términos de residual que significa básicamente que si el PIB no crece en la misma proporción, el sistema se hace insostenible y solo queda trabajar en el residual, incrementando la eficiencia. Dr. G. López Vivanco. Lo que nos quiere decir es que la Empresa Pública de Sanidad es la unida que puede quebrar, ¿pero qué pasa con las otras empresas públicas?. Dr. José Luis Poveda. Los datos referidos del Banco de España, refrendados por el FMI y la OCDE, es lo que dicen y no los podemos cambiar. De las otras empresas públicas no conoce los datos. Dr. G. López Vivanco. Desde luego es necesario cambiar el modelo como ya se ha comentado en esta reunión. Desde luego no todo a todos pero nada a todos que es lo que está ocurriendo en muchos sitios ahora y eso no se sostiene y va en contra de la calidad e imagen del sistema sanitario. Dr. Emilio Alba. La eficiencia es esencial, hay muchas cosas que no son útiles y podrían dejar de hacerse. Le eficiencia es un deber moral de todos nosotros. La sostenibilidad no es una cuestión económica es política. Si la política dice que es sostenible lo será. Considera que el 2050 se le dedicará al gasto sanitario el 25% del PIB y se logrará por incremento de la productividad con las nuevas tecnológicas. El problema no es económico, es político. Dr. Carlos Camps. Volviendo a un terreno más próximo. En la Comunidad de Valencia los pequeños Servicios de Ontología gastan un 150% más en relación al número de casos, que los Servicios grandes. Estos temas administrativos son importantes y deben ser abordados incluso más que los medicamentos. ¿Debemos primar la dispersión o la convergencia en Servicios fuertes? Dr. Cesar Pascual. Él no se ha encontrado nunca en la situación de “nada a todos”. Otra cosa es optimizar recursos con sentido común. La primera barrera es el precio de los medicamentos innovadores, no es el gerente o la Agencia del Medicamento o la CC.AA.. Hay que pensar que el coste de la innovación es cara y la medicina individualizada será aun más cara, pero parece que todo nos lleva a eso. Hay que hacer un retorno de los costes. El fututo de la sostenibilidad no va a depender del precio de los fármacos, dependerá más de la dependencia y de cronicidad. Dra. Cristina Grávalos. Es una pregunta para el Dr. José Ramón Luis-Yague. Con los nuevos fármacos dirigidos a dianas moleculares, tienen que pasar estos por todas las fases del estudio o se podría pasar de la fase Ia, seleccionando bien a los pacientes, a la comercialización, lo que permitiría menor inversión en la investigación, abaratando los costes. Dr. J. R. Luis-Yague. Muy oportuna la pregunta, pero las cosas son así. Estamos intentado y colaborando con las CC.AA para hacer una red de biobancos que permitan hacer un buen genotipado y a la hora de diseñar un ensayo clínico, seleccionar bien a los pacientes diana lo que nos ayudaría a ser más efectivos y a abaratar los costes. El problema de la sostenibilidad es la solvencia y credibilidad. En la página “web” del Ministerio de Sanidad se puede consultar el presupuesto “per capita” en sanidad de 62 cada CC.AA, la horquilla va desde el País Vasco con 1537 euros a Andalucía con solo 978 y esto es un verdadero problema. La innovación ahorra, un ejemplo de ello es el tratamiento de la hepatitis C comparado con trasplante hepático. Dr…………………… Se han dado datos presupuestarios, cuando se ha dicho que el País Vasco y Navarra tienen más dotación que otros, la realidad es que cumplen el presupuesto y otros no. Cuando se compara el gasto real, las diferencias son menores. Sobre los QALY señala que en España no van a funcionar. Los anglosajones tiene muy claro la relación entre impuestos y gasto social, si quieren más inversión en sanidad, tienen que aumentar los impuestos. Tiene una concienciación mucho mayor en relación a los impuestos. Aquí eso no ocurre y muchos malos ejemplos políticos lo justifican. Dr. Ricardo Herranz. Un último matiz a la sostenibilidad y credibilidad. La sostenibilidad es un problema político, pero todo lo que es presupuestario es político, pero eso no nos disculpa. La sostenibilidad es tener organizaciones permanentes vinculadas a la eficiencia. Hacer las mismas cosas con el mejor resultado y a un menor coste, eso es lo que da credibilidad y permitirá la sostenibilidad. La gente piensa por ejemplo, que no cobrará la pensión pero es por falta de credibilidad en la organización, al pensar que dicha organización pueda desaparecer o no está garantizada su continuidad. Dr. G. López Vivanco. No hay duda que la sanidad privada está creciendo, lo que significativo de algo. Un individuo espera que cuando enferme sea atendido adecuadamente y no de otra manera. Cuando he hablado de “todo a todos o nada a todos” es una exageración pero las dos reflexiones señalan que en algunas situaciones se están dado ahora, y esta es una de razones de este Seminario. El problema no es que un medicamento valga 3000 euros o 50 euros, no estamos hablando de eso, estamos hablando del valor clínico. Se ha dicho si el fármaco es barato no estaríamos hablando de ello; sí estaríamos hablando porque lo importante es su valor clínico, su eficacia que no tiene nada que ver con el precio. Aquí solo se habla de los aspectos económicos. Dr. José Luis Poveda. La Dra. Cristina Grávalos lo ha dicho antes, no se duda de la eficacia de los medicamentos de lo que se duda es del precio relacionado con el valor clínico del medicamento y esto se puede ver desde un punto de vista social o individual. Desde el punto de vista individual no hay duda, tres meses de vida, son tres meses de su vida, pero desde el punto de vista social las cosas pueden verse de otra forma y dudarse del valor-precio de esa supervivencia. Otro tema es el acceso al medicamento. Habría que ver la transparencia y variabilidad de los resultados por hospitales, servicios de oncología y tipo de pacientes, lo que nos daría una idea de si es solo el medicamento el que da la variabilidad. Dra. Cristina Grávalos. Cuando se habla de supervivencia, se está hablando de mediana, unos viven más y otros menos, lo que habría que identificar cuáles son los pacientes que se benefician más, por encima de la mediana. En definitiva la selección optima de pacientes. Dr. Carlos García Girón. La pregunta es a los gerentes en la medida que representan a la administración. Hablamos de AVAC que es una medición del Reino Unido que tienen sus criterios y gastan menos en sanidad, pero los hemos incorporado. Se habla de los 30.000 euros por año de vida ganado como referencia, pero la pregunta es si un AVAC de 60.000 euros, rango donde se mueven los oncólogos como punto de referencia sería aceptable para la administración y no tener esa barrera de los 30.000 euros. 63 Dr. M. de la Puente. Yo en mi hospital no planteo que cuesta un tratamiento o medicamento, si es 60.000 e. o 70.000e o 30.000 e, la decisión se toma entre el oncólogo que solicita, el servicio de farmacia, la dirección médica y el gerente. Los oncólogos forman parte de la solución del problema, los gerentes no son el problema, formamos parte para la solución del problema, el gerente no pone precio. Debemos ser coparticipantes. Dr. Cesar Pascual. Lo que queremos es un criterio objetivo común para todos. Si tenemos una cifra de 60.000 o 70.000 euros o la que sea, giraríamos en torno a ese valor, así evitaríamos las diferencias, al igual que poner un criterio, p.e. 120.000 euros al final de la vida. Eso evitaría diferencias o estar pensando si te equivocas, etc. Nosotros también sentimos tomar una determinada decisión, por eso debemos tener criterios objetivos. Dr. José Luis Poveda. Todo esto tiene sentido si se incorpora a la cartera básica de servicios que debe tener un carácter garantista y finalista. Si no es finalista una CC.AA o las que sean, no lo cumplirán, póngase el precio que se ponga. Detrás de una aprobación con un determinado número de pacientes póngase un presupuesto que sea finalista. Si no es así, lo único que hace es incorporarse a la cartera de servicios pero no quiere decir que se incorpore a los pacientes, de ahí las diferencias entre comunidades e incluso hospitales. Por lo tanto si el presupuesto no es finalista, el precio que se ponga no tiene un valor real. Dr. Emilio Alba. Esto es lo que pasó cuando se transfirió la Sanidad a las CC.AA, no se hizo de forma finalista y gastan el presupuesto en lo que quieren, es un error en el diseño, por eso es un problema político de difícil resolución. Dr. José Luis Poveda. Para ver algún aspecto positivo, cree que se está haciendo alguna aproximación como es el “techo de gastos” en relación con el número de pacientes por cada CC.AA. y esto posiblemente nos ayude. Dr. J. R. Luis-Yague. Estamos hablando de un criterio para incluir una prestación farmacéutica en el Sistema Nacional de Salud. Aquí tenemos también criterios como el Informe de Posicionamiento Terapéutico, el coste efectividad, la aportación al PIB, y esto no es indiscriminado, pero no todo entra en la cartera básica de servicios. Otra cosa es lo que ocurre en la calle y en las CC.AA. por lo que vamos a tener un problema más. Cree que el camino es la valoración de los costes-efectividad, con los costes directos e indirectos. Dra. Cristina Grávalos. Da las gracias a los ponentes, a los discusores y a los asistentes, cerrando la mesa redonda. 64 CONCLUSIONES. Dr. E. Díaz Rubio (Presidente de la Comisión Científica de la Fundación ECO). Me corresponde hacer las conclusiones, pero no me atrevería a tanto después de lo visto aquí en el debate, tanto por la mañana como por la tarde. No haré ni siquiera unas consideraciones, lo que haré más bien es unas reflexiones sobre lo discutido y de la situación en la que nos encontramos y a donde vamos evolucionando con los retos que tenemos encima de la mesa. La Fundación ECO está formada por oncólogos médicos que han querido discutir sobre el tema del “beneficio clínico” que nosotros podemos generar en el paciente con cáncer, y por tanto es desde nuestra perspectiva. Lo que se ha discutido hoy aquí está más en relación con el tratamiento médico y no tanto con el proceso, quizás esta sería una primera reflexión y es posible que más adelante tengamos que trabajar sobre el proceso para saber lo que se refiere al beneficio y lo que se refiere a los costes en relación con nuestras actuaciones sobre el paciente. Hoy lo que hemos discutido es sobre el tratamiento médico y ese era el núcleo de la discusión. Los oncólogos médicos estamos asistiendo a un cambio importante en los últimos años en lo referente a la historia natural de la enfermedad cancerosa. Hay más de 220 variedades de cáncer y cuando hablamos de una no tiene nada que ver con otra. Lo que estamos viendo ahora es que hay pacientes que con el tratamiento médico se curan, otros tienen grandes supervivencias 8-9 años, otros sin embargo tienen supervivencias más cortas de 2-3 meses y otros se logra un incremento de la supervivencia libre de progresión sin aumento de la supervivencia global lo que representa un área muy distinta; finalmente en otros tenemos que buscar mejorar la calidad de vida y eso implica en la mayoría de los casos la utilización de fármacos. Otro de los escenarios en el que estamos actuando es en la adyuvancia y neoadyuvancia y, como ven, no siempre nos estamos moviendo en las 3º, 4º o 5º líneas de tratamiento. Como verán el campo de actuación en la Oncología es muy amplio. Los oncólogos médicos nos hemos formado en las Escuelas de Medicina que fundamente han analizado la eficacia y seguridad. Beneficiar al paciente y no dañar al paciente. Indudablemente en los últimos 20-30 años y sobre todo con la entrada de este siglo acompañado de una crisis económica, indudablemente tenemos que hablar también de costes y de eficiencia. Los oncólogos trabajadores del sector público o privado tienen que tener un comportamiento ético-social ya que manejamos dineros que nos dan para hacer una medicina eficiente, pero todo esto es indudablemente complejo. 65 De la misma manera que las personas que se dedican a la gestión han tenido que aproximarse a los clínicos para comprender la problemática de los pacientes y nos ayuden entre todos a tomas decisiones. Este tercer actor de los costes y la eficiencia contaminan las decisiones del día a día, afectando a otros actores como los pacientes , familia del paciente, los propios oncólogos cuando tomas decisiones, la gerencia del hospital, la farmacia del hospital , las CC.AA., a la propia sociedad, a la industria farmacéutica y al final a la misma innovación. Esto nos lleva a algo que nos debe hacer meditar a todos, el hecho de generar una variabilidad en la práctica clínica, lo que está perfectamente constatado. El paciente tendrá acceso a una medicina u otra dependiendo de la CC.AA, del hospital, dentro del propio hospital según por la puerta que entra. Este circuito del que tanto hemos hablado en el Plan del Cáncer en el paciente oncológico, ha sido una quimera, no se ha producido y esto es muy grave por la falta de equidad, comprometiendo la ley de calidad del Sistema Nacional de Salud, y en esto todos estamos de acuerdo. Volviendo al tema de esta reunión, podríamos decir que no sabemos definir que es el beneficio clínico, ni cómo medirlo y en un análisis de datos de un ensayo clínico lo interpretamos de forma diferente y esto crea un dilema importante, beneficio clínico vs. beneficio estadístico. Las agencias han podido aprobar un fármaco por unos resultados positivos en un estudio, pero luego dudamos del beneficio real para el paciente. Hay un extremo donde todo el mundo está de acuerdo, el fármaco muy potente que ha cambiado la historia natural de un tumor, este se aprueba si o si, después se discutirá si la sociedad puede pagarlo o no o la forma de cómo pagarlo, pero los pacientes tienen que beneficiarse de ese fármaco. El otro extremo, hay fármacos como por ejemplo el Erlotinib en cáncer de páncreas que solo daba un beneficio de 10 días de supervivencia, por lo que todos también estaríamos de acuerdo en no aprobarlo. El problema es definir la magnitud del beneficio clínico mínimo para incorporar un fármaco a la clínica y aquí vienen los graves problemas de interpretación. Los ensayos clínicos están diseñados en función para su aprobación por las agencias reguladoras. Esta mañana se hablaba del valor “delta” que es el beneficio que esperamos de un determinado fármaco o tratamiento, pero muchas veces esto no se cumple. Si una “delta” de una HR de 0.75 como reto del estudio no se cumple, pero sale una p<0.005, finalmente las agencias de regulación lo aprueban y de ahí vienen la concatenación de problemas en cada país y como se financian esos fármacos. Sobre estos problemas hay que trabajar en profundidad como cuales son los parámetros de medida de estos estudios que debemos utilizar. Para muchos la supervivencia global parece lo más adecuado; pero otros valoran la supervivencia libre de progresión, la supervivencia libre de enfermedad o el tipo de respuesta y ya sabemos que los criterios RECITS con los nuevos fármacos no identifican bien a todos los que se estén beneficiando. Y esto es importante si hablamos de “riesgos compartidos”. Podemos ver un paciente con mejoría clínica pero la exploración por imagen a los tres meses está igual y es porque no sabemos qué está pasando dentro del tumor, cuando utilizamos estos fármacos nuevos dirigidos a las dianas moleculares. Tendremos que aplicar nuevas tecnologías que nos permitan conocer si el paciente se va a beneficiar o no del tratamiento. 66 Recientemente nos encontramos con un problema sobreañadido, cuando observamos dos curvas de supervivencia, la experimental y el control, que se separan en favor de la experimental, podemos discutir si mucho o poco, pero parece claro que hay un beneficio en relación al tratamiento experimental, incluso con una “p” y HR potentes. Muchos pacientes ya viven más 6 meses porque se ha cambiado la historia natural, hay pacientes que viven más de 29 meses con enfermedad metastásica y explicar esto es más complejo, las curvas inicialmente pueden no separarse, con una media de supervivencias similar, pero después si lo hacen y esto es lo difícil de explicar, y probablemente el beneficio es poco, pero nos señala que un cierto número de pacientes se benefician del fármaco experimental, con una HR incluso de 0.35 y una “p” de varios ceros, aunque inicialmente no sepamos cuales se benefician , lo cual sería muy importante, siendo un criterio difícil de aplicar, más aún si intentamos cuantificar el valor de un AVAC. Se ha discutido de las ventajas del sistema NICE y establecer un coste por AVAC, pero en España no ha habido un consenso para ello y no se han puesto todos los medios para hacerlo. Se necesita una infraestructura e inversiones para poder realizarlo., y por ahora no parece que pueda ocurrir. Se ha intentado establecer un límite al beneficio ya que en ciertos estudios no han sido los adecuados, indicándose que se debe ser más exigentes y seleccionar mejor a los pacientes. De esto se ha hablado en ASCO y ESMO incluso se ha propuesto poner un HR de 0.4-0.5, para que eso realmente sea válido, y si el fármaco no cumple no sería aprobado. Pero eso excluye a los pequeños avances. En cáncer colorrectal metastásico la supervivencia antiguamente era de 6 meses, en la actual está en 29 meses de media y un 10% viven a los 5 años con metástasis. A esto se ha llegado poco a poco, si hubieran aplicado esos criterios tan estrictos, seguiríamos solo con el 5FU y los pacientes seguirían viviendo 6-8 meses y no se habría dado ese gran paso y esa es la critica a establecer un techo a los limites. Una cuestión importante es si realmente los estudios están bien diseñados en la actualidad. Las fases III son débiles, porque las fases II no han sido potentes. Si se hubiera hecho así muchos fármacos no habrían sido aprobados y no pasarían a fase III, lo que supondría un ahorro. En Hematología ha ocurrido que las fases II han sido potentes y han llevado a la aprobación del fármaco directamente con lo que los pacientes se benefician antes y además se ahorra en inversión. Esto podría ser conseguido el futuro con la medicina personalizada y los bancos de tumores para estudios genómicos y entonces no haremos un estudio p.e. para cáncer colorrectal metastásico, sino estudios de cáncer colorrectal con mutaciones K-RAS, B-RAS, HER2, XG etc. con lo que iremos a un tratamiento orientado y será más rápido pudiendo impactar en la eficiencia. Otra cuestión es la incorporación de fármacos orientados a las dianas moleculares, pero en donde no tenemos biomarcadores plantea un problema. Si se aceptan solo los fármacos que tienen sus biomarcadores y no a los otros que no los tienen, a no ser que muestren una gran potencia en los estudios en fase temprana. Otro aspecto es pedir que la “delta” tenga una magnitud mayor a la actual. Se habla en ciertos foros de una supervivencia global de 3 meses o una supervivencia libre de progresión de 4-6 meses, pero es algo que no podemos solucionar ahora y tampoco sabemos que piensa la industria farmacéutica y las agencias reguladoras. Otro aspecto es como trasladar los datos de los ensayos clínicos a la práctica clínica diaria. 67 En los ensayos clínicos hay selección de pacientes, selección de centros, seguimiento estrecho, compromiso del paciente etc. Por ello el trasladar estos datos a la práctica diaria es complejo y hace que la Medicina siga siendo un arte a pesar de los progresos científicos logrados. Esta segunda parte del seminario es muy interesante por lo que puedan aportar los grupos cooperativos, las sociedades científicas, las gerencias, los servicio de farmacia, la industria farmacéutica etc. Me gusta decir que en el campo de la Ontología Médica, los oncólogos son el resultado de la evolución por una selección natural a través de mutaciones que se han ido generando gracias a la incorporación de la innovación. El oncólogo cuando nace en España es un quimioterapeuta que mutó a oncología médica y el que no mutó quedó en vía muerta. Nuevamente tuvieron que mutar para lo que no estaban preparados, el conocimiento de la biología molecular para incorporar todas las dianas terapéutica y transformarse en el oncólogo actual. Pero otra nueva mutación se prepara y se transformaran en oncólogos clínicos moleculares e inmunólogos, por la llegada de los nuevos fármacos que cambiaran la historia natural del cáncer. Todo aquello que añada valor es importante, los gerentes tendrán que mutar y hacerse más clínico, el oncólogo también deben mutar y participar en la gestión y estamos en esa labor y todos juntos para hacer una medicina más eficiente que añada beneficio al paciente. Para terminar, decir que tenemos el reto de trabajar juntos, en equipo, comprendernos todos y finalmente hacer un análisis de lo que cuestan los fármacos, pero sobre todo cuanto cuesta el proceso, que no lo sabemos. Si me preguntan cuánto cuesta el proceso cáncer de colon, cáncer de ovario, cáncer de mama etc., diré que no se cuánto cuesta en mi Servicio, por lo que no dispongo de argumentos a donde deben ir dirigidos los recursos. Muy agradecidos a todos por su participación. LECTURA DE COMUNICADO DE LA RANM-FUNDACION ECO. Presidente: Dr. Carlos Camps. Lectura: Dr. Eduardo Díaz Rubio. Se ha celebrado en el día de hoy el “V Seminario Fundación ECO en la RANM, titulado “Beneficio clínico del tratamiento médico: objetivos y resultados en cáncer”. La oportunidad del contenido de este Seminario es indudable en los momentos actuales donde la Oncología Médica avanza ineludiblemente hacia la medicina de precisión con la utilización de los mejores tratamientos médicos, menos tóxicos y de mayor individualización, con el objetivo de poder curar el mayor porcentaje posible de cáncer 68 y si esto falla poder cronificarlos, haciendo que la vida del paciente continúe en la mejor situación clínica posible. Los criterios RECIST, de actual vigencia, categorizan los cambios cuantitativos del tamaño del tumor, en respuesta completa (RC), respuesta parcial (RP), enfermedad estable (SD), o enfermedad progresiva (EE) y proporcionan mediciones estandarizadas y objetivas de la respuesta de las lesiones diana del tumor a la terapia. Criterios que se han utilizado ampliamente en la última década para la valoración de quimioterapia citotóxica, así como para la toma decisiones de terapéuticas en la atención al paciente individual y a su respuesta. Sus limitaciones para la evaluación de agentes dirigidos molecularmente han sido cada vez más reconocidas, dado que estos nuevos agentes ejercen su efecto a través de un mecanismo citostático y no por actividad citotóxica, por lo que suelen inducir en general una limitada reducción del tumor. En particular el punto de corte de cambio del 30% se tiene como criterio de respuesta que diferencia la respuesta parcial de la enfermedad estable o de la enfermedad progresiva, lo cual ha sido criticado por no capturar adecuadamente tratamientos potencialmente eficaces desde el punto de vista clínico. Un ejemplo es la evaluación de respuesta en los pacientes con carcinoma metastásico de células renales tratados con agentes dirigidos, a pesar de que mejoran significativamente la supervivencia libre de progresión (SLP). En estos casos el umbral óptimo para determinar una respuesta puede ser del -5%. Por tanto un análisis de respuesta modificado puede ser clínicamente más significativo que RECIST para la identificación de pacientes en los que pudiera derivarse un beneficio de la SLP con la terapia dirigida. La exploración y validación de los criterios óptimos de los cambios de la carga tumoral o parámetros de imagen funcional como marcadores del efecto del fármaco y / o beneficio clínico, tienen la posibilidad de mejorar la eficiencia del desarrollo de nuevas terapias y del manejo terapéutico de los pacientes individualmente. Recientes estudios han analizado la relación entre los cambios en el tamaño del tumor y los resultados clínicos en pacientes tratados con agentes anti-angiogénicos. Estos análisis concluyeron que la reducción ≥ 10% del tamaño de la lesión diana según criterios RECIST (respondedores) en la primera exploración tempana se asoció con resultados significativamente mejores, en comparación con la de los no respondedores que eran aquellos que no logran la reducción del 10%. El tiempo hasta fracaso del tratamiento (TFT) y la supervivencia global fueron mayores. Por el contrario, el umbral de RECIST -30% en la primera exploración no predijo el resultado del paciente. Estos datos establecieron que una reducción >10% en primera exploración podrían ser utilizado para las decisiones de tratamiento en cuanto a si se deben continuar las terapias anti-angiogénicas. En definitiva, diferentes estudios sugieren que la modificación de los criterios de respuesta para capturar y clasificar las respuestas menores puede proporcionar una lectura más sensible del efecto terapéutico y potencialmente mejorar la precisión de la evaluación precoz de las drogas. La búsqueda del punto de corte óptimo puede ser un reto, ya que el umbral puede no ser igual para los mismos agentes en diferentes indicaciones o para distintos agentes en la misma indicación. Las limitaciones técnicas, como la variabilidad de medida, también pueden cambiar la elección de los umbrales que se pueden adoptar. 69 Se están realizando esfuerzos por el comité RECIST para expandir la base de datos para incluir los grandes ensayos clínicos aleatorios de agentes dirigidos, así como los estudios que utilizan la imagen molecular con la tomografía por emisión de positrones con fluorodeoxiglucosa (FDG-PET). El objetivo del plan es evaluar y actualizar las directrices y criterios para cumplir con las necesidades de desarrollo de fármacos y atención de los pacientes en la era de las nuevas terapias. Estos hechos ponen de manifiesto que la observación de la reducción del tumor por debajo del umbral de los criterios RECIST puede estar asociada con un beneficio clínico significativo, y que la flexibilidad en el cambio de tamaño tumoral debe ser considerada en la modificación futura de los criterios de respuesta. Otro hecho importante es clarificar a qué se denomina beneficio clínico en la era de las terapias de precisión. Hasta ahora en la práctica clínica con la quimioterapia, el beneficio clínico correspondía a la suma de las respuestas objetivas (completas y parciales) y las estabilizaciones cuando éstas duran al menos seis meses (24 semanas). Pero esto no es aplicable a las nuevas terapias donde una pequeña reducción puede acompañarse de una mejoría del paciente durante bastante tiempo. Por ello el beneficio clínico y su relación con la duración del mismo, se refiere a los síntomas del paciente, a su estado general, a la mejoría en el peso y en suma a la calidad de vida. En definitiva se trata de contestar a las preguntas que le hacemos al paciente cuando entra en la consulta ¿Cómo está? ¿Cómo se encuentra? ¿Cuáles son sus problemas? Todo ello debe relacionarse igualmente con parámetros como la supervivencia libre de progresión, el tiempo al fallo del tratamiento y a la supervivencia global. La primera mesa del Seminario ha analizado en detalle estos hechos con el objetivo de lograr los mayores beneficios de las terapias dirigidas a dianas moleculares en las neoplasias de mayor incidencia en nuestro medio. La segunda parte del Seminario se ha centrado en el papel que juegan los diferentes actores que intervienen desde puntos de vista dispares en todo el proceso neoplásico, pero que tienen como objetivo el beneficio clínico del paciente, para lo que deben promover una actitud de cooperación continua a favor de una mejor asistencia al paciente con cáncer. Todo lo anterior demuestra el hecho de que la evolución de la oncología con la entrada de los nuevos fármacos dirigidos a dianas moleculares, precisa a su vez una revolución en los criterios clásicos utilizados en la evaluación del beneficio, por lo que se debe trabajar en su modificación, hecho que respaldan y apoyan tanto la RANM como la Fundación ECO.