Unidad6
Anuncio

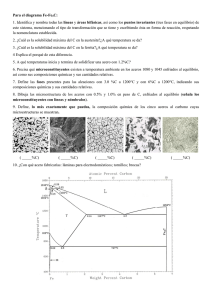
Unidad 6 ENDURECIMIENTO POR ALEACION. ALEACIONES CON SOLUBILIDAD PARCIAL EN ESTADO SOLIDO 1 PRESENTACION En esta Unidad se analiza la casuística que aparece cuando en el estado sólido existen componentes o aleaciones que cambian su estructura cristalina, alotropía. En concreto analizamos la transformación eutectoide; que describe el cambio de estructura cristalina a velocidades de enfriamiento calificadas de reversibles termodinámicamente. Igualmente, se analiza la transformación que sucede en las zonas de solubilidad variable con la temperatura, total a altas temperaturas y limitada a bajas temperaturas. Esto permite la precipitación de segundas fases en estado sólido, tras aplicaciones de enfriamiento irreversible, lo que permite el endurecimiento por envejecimiento. El objetivo de esta Unidad es, por tanto: • Definir los procesos que justifican cada una de las transformaciones. • Determinar sus variables de control e influencia sobre el proceso. • Correlacionarlas con las características resistentes. El ámbito de aplicación es amplio, aún no existiendo muchos metales que apunten este comportamiento, cambio de fase en estado sólido. En efecto, sólo la existencia del hierro y sus aleaciones, aceros, justifica un detenimiento en este tema por su gran importancia de aplicación industrial. FCM 6 / 75 Cuaderno de Laboratorio - Fundamentos de Ciencia de Materiales 2 ENDURECIMIENTO POR PRECIPITACIÓN El endurecimiento por precipitación de segundas fases en el cristal matriz se denomina envejecimiento. En el envejecimiento el campo de aplicación está limitado a aquellas aleaciones que muestran curvas de insolubilidad parcial, directas con la temperatura, delimitando una zona monofásica y otra bifásica. Las características de las composiciones de estas aleaciones en procesos reversibles conducen a estructuras fragilizadas, figura 6.1, pero bien conducidas, mediante procesos irreversibles, pueden alcanzar interesantes variaciones de características resistentes. El endurecimiento por precipitación entra en el rango de procesos de endurecimiento por tratamientos térmicos. Para su identificación se adoptan comúnmente denominaciones sinónimas: endurecimiento por precipitación, envejecimiento, bonificado, etc. 2.1 θ L L+α α A %B Figura 6.1. Diagrama típico para poder aplicar el endurecimiento por precipitación. EXPERIENCIA SOBRE EL PROCESO PRECIPITACION (ENVEJECIMIENTO) DE ENDURECIMIENTO POR 2.1.1 Objetivo de la experiencia Investigar el proceso de endurecimiento por envejecimiento y las teorías que lo justifican. 2.1.2 Material empleado Probetas de aluminio en estado de recocido, temple fresco, envejecidas y sobrenvejecidas. Probetas de aleación cobre-berilio recocidas, templadas y envejecidas. Probetas de acero ICO, endurecible por precipitación. 2.1.3 Descripción del proceso y equipos FCM 6 / 76 Unidad 6 - Endurecimiento por aleación. Aleaciones con solubilidad parcial en estado sólido 2.1.4 Dibuja el aspecto de las microestructuras de las diferentes muestras observadas. 2.1.5 Resultados de dureza obtenidos 3 ALEACIONES CON TRANSFORMACION EUTECTOIDE En los diagramas de fase binarios, pueden ocurrir transformaciones entre fases, componentes y productos, todas ellas en estado sólido, por cambio del sistema de cristalización, que son excepcionalmente importantes a causa del enorme valor industrial de estas aleaciones, nos referimos a los aceros. FCM 6 / 77 Cuaderno de Laboratorio - Fundamentos de Ciencia de Materiales 3.1 SOBRE LAS TRANSFORMACIONES EN ESTADO SOLIDO. Líquido Punto de fusión de A L+α Temperatura Durante el estudio de metales y estructura cristalina, se destaca que diversos metales pueden existir en más de un tipo de estructura cristalina, dependiendo α Cambio γ + de la temperatura. El hierro, el estaño, el manganeso y el alotrópico γ cobalto son ejemplos de metales que tienen esta propiedad, conocida como alotropía. En un diagrama de α equilibrio, este cambio alotrópico se indica por un punto o puntos en la línea vertical que representa el metal puro, tal como se muestra en la figura 6.2. En este diagrama, el campo de solución sólida gamma está anillado. El metal A B Composición puro A y las aleaciones ricas en A sufren dos Figura 6.2. Diagrama de equilibrio con un transformaciones. Muchos de los diagramas de equilibrio metal A alotrópico. que incluyen hierro, como Fe-Si, Fe-Mo y Fe-Cr, muestran este campo de solución sólida anillado. Como el tipo de hierro que existe en este intervalo de temperatura es hierro gamma, el campo generalmente se llama anillo gamma. En un enfriamiento lento, las estructuras que se obtienen son las indicadas en el diagrama, habitualmente monofásicas α o γ, según las temperaturas de estabilidad del metal. La transformación eutectoide es la transformación que sucede en estado sólido cuando en las fases producidas no existe solubilidad total entre los metales. Se asemeja en cierto modo con la transformación eutéctica por cuanto su diagrama mostraba insolubilidad total o parcial en la zona de fases producto. 3.2 SOBRE LA ALEACION HIERRO-CARBONO, ACEROS El hierro es un metal alotrópico, lo que significa, tal como se ha comentado anteriormente, que puede presentarse en diversas variedades de estructuras cristalinas, dependiendo de la temperatura a la que se encuentre. Al solidificar, a 1536°C, lo hace en la forma δ (delta), que pertenece a la red cúbica de cuerpo centrado. Cuando desciende la temperatura, a 1392°C, tiene lugar un cambio de fase reagrupándose los átomos y dando origen a la variedad γ (gamma), la cual cristaliza en el sistema de red cúbica de caras centradas y es no magnética. Al proseguir el enfriamiento del metal, se presenta un nuevo cambio alotrópico a 911°C, pasando la estructura del hierro de la variedad γ, a la α (alfa), que pertenece a la red cúbica de cuerpo centrado y también es no magnética. Finalmente, a 769°C, aparece un cambio en las propiedades magnéticas del hierro α, el cual pasa de no magnético a magnético, sin que la estructura cristalina sufra variación alguna. La adición de elementos de aleación al hierro, influye en las temperaturas a que se producen las transformaciones alotrópicas. Entre estos elementos, el más importante es el carbono, el cual al alearse con el hierro lo hace según el diagrama de equilibrio representado en la figura 6.3, cuyas transformaciones en estado sólido, hasta un 2% de carbono, aceros, investigaremos en la experiencia. En el diagrama aparecen tres líneas horizontales, las cuales indican reacciones isotérmicas. La horizontal que corresponde a la temperatura de 1493°C es la típica línea de una reacción FCM 6 / 78 Unidad 6 - Endurecimiento por aleación. Aleaciones con solubilidad parcial en estado sólido peritéctica, cuyo resultado es la aparición del hierro γ, que muestra una máxima solubilidad del carbono a los 1146°C, con un 2% aproximadamente, temperatura a la que tiene lugar la reacción eutéctica. 1600 Líquido + Fe δ 1493°C 1536 1500 Fe δ Líquido Temperatura, °C Ferromagnétic Paramagnétic o o 1400 1392 Austenita + Fe δ Líquido + Austenita 1300 Fe γ (Austenita) 1200 Recocido de homogeneización 1100 1000 Austenización Tem completa ple y norm aliza 769°C do 900 Austenita + ferrita 8 0 0 de n ió luc o S 723°C 700 ros u b car Esferoidización Alivio de tensiones 600 Fe α (Ferrita) Recocido de recristalización 300 200 100 Aceros eutectoides 400 Perlita Revenido 500 Aceros hipoeutectoides Aceros hipereutectoides 0 0 0 0,2 0,4 5 0,6 0,8 1 1,2 1,4 % en peso de carbono 10 15 1,6 20 % en peso de cementita 25 1,8 2 30 Figura 6.3 Diagrama de equilibrio Hierro - Carbono, en la parte de Aceros. La línea horizontal representada a los 723°C, corresponde a la transformación eutectoide del acero. FCM 6 / 79 Cuaderno de Laboratorio - Fundamentos de Ciencia de Materiales 3.3 EXPERIENCIA SOBRE LA TRANSFORMACION EUTECTOIDE. 3.3.1 Objetivo de la experiencia Investigar la transformación eutectoide, su conformación, microestructura y características resistentes. 3.3.2 Material empleado Aceros con diferente contenido en carbono, en concreto se observarán aceros con un 0.08, 0.15, 0.20, 0.30, 0.40, 0.60, 0.8 y 1.10 % de carbono. 3.3.3 Descripción del proceso y equipos utilizados 3.3.4 Resultados obtenidos FCM 6 / 80 Unidad 6 - Endurecimiento por aleación. Aleaciones con solubilidad parcial en estado sólido 3.3.5 Dibuja el aspecto de la microestructura del material tras el ataque, indicando la forma, coloración y distribución de los granos. 0.08% C 0.15% C 0.20% C 0.30% C 0.40% C 0.60% C 0.80% C 1.10% C FCM 6 / 81 Cuaderno de Laboratorio - Fundamentos de Ciencia de Materiales 4 CUESTIONES PROPUESTAS POR LAS EXPERIENCIAS 1 - Dibuja esquemáticamente el aspecto microscópico de una aleación de aluminio envejecible en los siguientes estados: en estado de equilibrio a temperatura ambiente, recién templada y tras el envejecimiento. 2 - Define las cuatro etapas más importantes en un proceso de endurecimiento por precipitación. 3 - ¿Qué tipos de granos se observan en los aceros hipoeutectoides? 4 - ¿Qué tipos de granos se observan en los aceros hipereutectoides? 5 - ¿Donde se encuentra la cementita, Fe3C, en los aceros hipoeutectoides? 6 - ¿Donde se encuentra la cementita, Fe3C, en los aceros hipereutectoides? 7 - Representa la evolución de las características mecánicas de los aceros al carbono en función del contenido en carbono y del contenido en perlita. 8 - Las características de los aceros con un 0.10% de C y 0.80% de C, son las siguientes: %C 0.10 0.80 R (MPa) 400 950 LE (MPa) 200 700 %A 35 10 a) ¿Pueden determinarse las características mecánicas mediante observación metalográfica? Establece un modelo matemático para R = f (% ferrita, % perlita) b) ¿Qué contenido en C presentan los aceros de construcción soldables (tipo AE420) empleados en perfiles estructurales? c) ¿Por qué no se emplean para dicha aplicación aceros con mayor contenido en carbono, por ejemplo, 0.8% C, que permitirían reducir el tamaño de las secciones? 9 - Indique los contenidos máximos admitidos en los aceros sin alear de los siguientes elementos: S, P, Si y Mn. 10 - Indica algunos de los aleantes y sus porcentajes de adición más habitualmente empleados en los aceros aleados. FCM 6 / 82 Unidad 6 - Endurecimiento por aleación. Aleaciones con solubilidad parcial en estado sólido ALUMNO APELLIDOS: GRUPO DE PRÁCTICAS: NOMBRE: FECHA DE ENTREGA: RESPUESTAS DE LAS CUESTIONES A RESOLVER FCM 6 / 83