LAS PROTEINAS: ESTRUCTURA Y PLEGAMIENTO
Anuncio

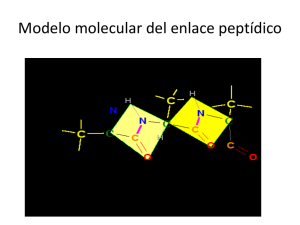
LAS PROTEINAS: ESTRUCTURA Y PLEGAMIENTO ESTRUCTURA Y FUNCION DE LAS PROTEINAS. Las proteínas son polímeros de aminoácidos unidos por uniones amida, llamadas uniones peptídicas. La cadena polipéptídica constituye la estructura primaria de la proteína, dada por la secuencia de los residuos de aminoácidos. Para ser funcional, la proteína requiere niveles superiores de estructura, que la llevan a su forma tridimensional, esencial para su función. Esos niveles estructurales son las estructuras secundaria, terciaria y, eventualmente, cuaternaria (si se trata de un oligómero con subunidades iguales o diferentes). NIVELES ESTRUCTURALES EN LAS PROTEÍNAS. 1) Estructura primaria: Secuencia de aminoácidos. Unión peptídica exclusivamente. Angulos de rotacion del carbono alfa. 2) Estructura secundaria: Disposición espacial de residuos de aminoácidos cercanos en la secuencia. Unión hidrógeno involucrando el N y el O de las uniones peptídicas exclusivamente. Tres elementos principales de estructura secundaria: αhélice, estructura β (hoja plegada) y giros β. 3) Estructuras supersecundarias: motivos y dominios. 4) Estructura terciaria: Disposición espacial de residuos de aminoácidos lejanos en la secuencia. Interacciones hidrofóbicas, puentes de hidrógeno entre restos laterales o entre ellos y la cadena peptídica, uniones salinas, puentes disulfuro. 5) Estructura cuaternaria: Disposición espacial de las subunidades en proteínas oligoméricas. Interacciones hidrofóbicas, uniones puente hidrógeno y salinas. PUENTE DISULFURO: SOLO EN ESTRUCTURA TERCIARIA DISTRIBUCION DE LOS RESIDUOS DE AMINOACIDOS EN LA MIOGLOBINA. Residuos hidrofobicos en amarillo, cargados en azul y el resto en blanco. (B): corte de la molecula, mostrando que los residuos hidrofobicos se encuentran en buen parte en su interior PROTEINAS DE MEMBRANA. Proteínas integrales y Proteínas periféricas PLEGAMIENTO DE LAS PROTEINAS. LA RIBONUCLEASA: EL EXPERIMENTO DE ANFINSEN. REDUCCION DE LOS PUENTES DISULFURO La urea desnaturaliza a la ribonucleasa (es decir, deja solo su estructura primaria) y el β-mercaptoetanol reduce los puentes disulfuro. Si se elimina la urea y luego se deja que los puentes disulfuro vuelvan a formarse por oxidacion con el aire, se recupera la estructura nativa. Si se oxida en presencia de urea, se obtiene una “ribonucleasa revuelta”, inactiva, pero esta recupera su actividad en presencia de trazas de β-mercaptoetanol. LA PARADOJA DE LEVINTHAL. Para una proteína pequeña, de 100 residuos de amino ácidos: Si cada residuo puede asumir 3 posiciones, el número total de estructuras posibles será igual a 3100, lo que es igual a 5 x 1047 Si toma 10-13 seg para convertir una estructura en otra el tiempo total requerido para el plegamiento correcto será 5 x 1047 x 10-13 seg = 5 x 1034 seg = 1.6 x 1027 años. (Paradoja de Levinthal) El plegamiento puede pasar a traves de un intermediario que ya tiene practicamente completa la estructura secundaria (el globulo fundido). Puede tener un camino unico o tener caminos alternativos. AGENTES DESNATURALIZANTES. 1) Extremos de pH. Muchas proteínas se desnaturalizan a valores de pH < 5 o > 10. Esto puede deberse a la ionización de grupos en el interior de la proteína (His a pH ácido, Tyr a pH alcalino); a repulsión electrostática entre grupos de la superficie de la proteína; a la destrucción de puentes salinos importantes en la estabilización de la estructura nativa. 2) Agentes desnaturalizantes. Los más usados son la urea y el clorhidrato de guanidina: DESNATURALIZACION DE UNA PROTEINA. PLEGAMIENTO DE LAS PROTEÍNAS IN VITRO E IN VIVO. In vitro: Plegamiento espontáneo, a muy bajas concentraciones de proteína para evitar agregados. Buffer redox (GSH/GSSG) para inducir la formación correcta de puentes disulfuro. In vivo: Plegamiento a altas concentraciones proteicas, asistido por otras proteínas. 1) Puentes disulfuro: proteína disulfuro isomerasa. Contiene secuencias –Cys-Gly-His-Cys- y acelera unas 6000 veces el intercambio de puentes disulfuro. 2) Uniones peptídicas X-Pro: Peptidil prolil isomerasa. En vez de ser todas uniones en trans, como para los demás aminoácidos, un 6 % de las con Pro es cis. La PPI acelera 300 veces la isomerización cis-trans. 3)Prevención de la formación de agregados moleculares: chaperonas moleculares. Se unen reversiblemente a zonas desplegadas del polipéptido naciente, evitan su agregación y facilitan su plegamiento correcto, con consumo de ATP.