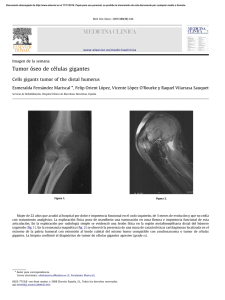
utilizacion de licopeno para reducir la actividad de las celulas, en
Anuncio

k OFICINA ESPAÑOLA DE PATENTES Y MARCAS 19 k kInt. Cl. : A61K 31/07 11 Número de publicación: 7 51 ESPAÑA k 2 181 682 A61P 35/00 TRADUCCION DE PATENTE EUROPEA 12 kNúmero de solicitud europea: 93203295.6 kFecha de presentación: 25.11.1993 kNúmero de publicación de la solicitud: 0 600 544 kFecha de publicación de la solicitud: 08.06.1994 T3 86 86 87 87 k 54 Tı́tulo: Utilización de licopeno para reducir la actividad de las células, en particular células cance- rosas y preparaciones farmacéuticas. k 73 Titular/es: k 72 Inventor/es: Levy, Joseph y 30 Prioridad: 30.11.1992 IL 103920 Lycored Natural Products Industries Ltd P.O. Box 320 84102 Beer Sheva, IL 45 Fecha de la publicación de la mención BOPI: 01.03.2003 k 45 Fecha de la publicación del folleto de patente: ES 2 181 682 T3 01.03.2003 Aviso: k k Sharoni, Yoav k 74 Agente: Curell Suñol, Marcelino En el plazo de nueve meses a contar desde la fecha de publicación en el Boletı́n europeo de patentes, de la mención de concesión de la patente europea, cualquier persona podrá oponerse ante la Oficina Europea de Patentes a la patente concedida. La oposición deberá formularse por escrito y estar motivada; sólo se considerará como formulada una vez que se haya realizado el pago de la tasa de oposición (art. 99.1 del Convenio sobre concesión de Patentes Europeas). Venta de fascı́culos: Oficina Española de Patentes y Marcas. C/Panamá, 1 – 28036 Madrid ES 2 181 682 T3 DESCRIPCION Utilización de licopeno para reducir la actividad de las células, en particular células cancerosas y preparaciones farmacéuticas. 5 10 Campo de la invención La presente invención se refiere a un procedimiento para reducir la actividad de las células y a la utilización de preparaciones farmacéuticas que comprenden licopeno. La invención se refiere además a la inhibición del crecimiento de las células cancerosas utilizando licopeno como agente activo contra el cáncer. Antecedentes de la invención 15 20 25 Se ha sugerido que los carotenoides tienen actividad para la prevención del cáncer y se ha mostrado que son efectivos en la inhibición del crecimiento de las células cancerosas. Se conoce desde hace tiempo que el β-caroteno tiene propiedades anticancerosas, tanto por estudios epidemiológicos como por experimentos que demuestran su efecto como depurador de radicales libres. Recientemente [patente US n◦ 5.008.295; Murakoshi et al., J. Natl. Cancer Inst., vol. 81; n◦ 21, nov.1 (1989)] se ha mostrado que el α-caroteno es un inhibidor del crecimiento de las células cancerosas mucho más potente que el β-caroteno. En otros estudios recientes se han comparado las actividades anticancerosas de varios retinoides y carotenoides in vitro [Wang, C. J. And Lin, J. K., Proc. Natl. Sci. Counc. B. ROC, vol. 13, n◦ 3:176-183, (1989)] e in vivo [Wang, C. J. et al., Cancer Letters, 48:135-142 (1989)]. Dichos trabajos mostraron que el licopeno tiene una actividad anticancerosa comparable, pero frecuentemente inferior, a la del β-caroteno. El licopeno tiene la fórmula: 30 35 40 45 Según la técnica, generalmente se considera que el licopeno no es activo por sı́ mismo, ya que se cree que la actividad anticancerosa de ciertos carotenoides está frecuentemente asociada con la actividad de la provitamina A [VanEenwyk, J. et al., Int. J. Cancer: 48;34-38 (1991)]. El β-caroteno es un precursor de la Vitamina A, mientras que el licopeno no lo es. Sumario de la invención Sorprendentemente se ha descubierto, lo cual constituye uno de los objetivos de la presente invención, que el licopeno tiene actividad en reducir la actividad general de las células, tanto in vitro como in vivo. 50 55 60 Se ha encontrado además, y este es otro de los objetivos de la invención, que contrariamente a las enseñanzas de la técnica anterior el licopeno puede ser utilizado como un agente activo para inhibir el crecimiento de las células cancerosas y que la concentración de licopeno necesaria para inhibir es muy inferior a la necesaria, p. ej., de α-caroteno. Se ha encontrado además, y este es otro objetivo de la presente invención, que el licopeno puede ser utilizado efectivamente para inhibir el crecimiento de ciertas células cancerosas particularmente agresivas, que en el mejor de los casos, han sido inhibidas solo ligeramente por una variedad de fármacos anticancerosos convencionales. Se ha encontrado además, y este es todavı́a otro de los objetivos de la presente invención, que el licopeno puede ser utilizado efectivamente para reducir el número de las células cancerosas y el tamaño de los tumores. 2 ES 2 181 682 T3 Es un objetivo de la presente invención proporcionar un procedimiento para reducir la actividad de una célula, procedimiento que comprende la utilización de licopeno como ingrediente activo. 5 Otro objetivo de la presente invención es proporcionar composiciones inhibidoras del crecimiento canceroso, que comprenden licopeno como ingrediente activo. Otro objetivo adicional de la presente invención es proporcionar composiciones anticancerosas basadas en el licopeno, que pueden ser toleradas relativamente bien por un paciente que las necesite. 10 Todavı́a otro objetivo de la presente invención es proporcionar un procedimiento útil para el tratamiento de una multiplicidad de pacientes de cáncer, basado en la utilización de licopeno como material activo. Otros objetivos y ventajas de la presente invención se harán evidentes con la lectura de la descripción. 15 En un aspecto, por consiguiente, la invención se refiere a un procedimiento para reducir la actividad de una célula, que comprende administrar a la célula de un sujeto que lo necesita, de forma directa o sistémica, una cantidad de licopeno efectiva para reducir la actividad de la célula. 20 25 30 Según una forma de realización preferida de la presente invención, las células cuya actividad se desea inhibir son células cancerosas. En consecuencia, en otro aspecto, la invención se refiere a un procedimiento para inhibir el crecimiento de las células cancerosas según la invención, comprende administrar a un sujeto en necesidad de ello una cantidad de licopeno efectiva para la inhibición del crecimiento. Es notorio que los resultados obtenidos en la técnica, cuando se ensayó el licopeno [Wang, et al., ibid], discrepan con la presente invención al calificar la actividad del licopeno como próxima o por debajo de la del β-caroteno. Los desalentadores resultados obtenidos por los investigadores anteriores son probablemente imputables a condiciones experimentales especı́ficas que ellos utilizaron, aunque los inventores no desean quedar sujetos a ninguna teorı́a en particular. Breve descripción de los dibujos La Figura 1 muestra una comparación de la inhibición de la actividad celular por medio de diferentes dosis de carotenoides en células Ishikawa de cáncer de endometrio; 35 40 La Figura 2 compara la actividad inhibidora de algunos carotenoides obtenidos de diversos orı́genes sobre el crecimiento de las células MCF-7 de tumor de mama; La Figura 3 es una comparación de la actividad inhibidora de diversos carotenoides originalmente disueltos en THF o en disolución acuosa, sobre el crecimiento de las células HEC-IA de cáncer de endometrio; La Figura 4 muestra el efecto inhibidor mejorado de una aplicación diaria de licopeno, en comparación con una única aplicación, sobre el crecimiento de las células MCF-7 de cáncer de mama; 45 La Figura 5 ilustra la inhibición por el licopeno del crecimiento inducido por IGF-1 en las células MCF-7 de cáncer de mama; La Figura 6 muestra el espectro de absorción amplificado del licopeno de dos orı́genes diferentes: extracto de tomate purificado, ex Sigma (Fig. 6(a)) y extracto de tomate recién preparado (Fig. 6(b)); 50 La Figura 7 muestra la correlación entre la incorporación de timidina y el número de células en células Ishikawa de cáncer de endometrio, a diferentes concentraciones de licopeno; La Figura 8 ilustra el efecto de los carotenoides disueltos sobre el crecimiento de células Ishikawa de cáncer de endometrio; 55 60 La Figura 9 ilustra el efecto de los carotenoides disueltos en el crecimiento de células H226 de cáncer de pulmón; La Figura 10 ilustra el efecto de licopeno de diferentes fuentes en disolución sobre el crecimiento de las células H226 de cáncer de pulmón; La Figura 11 muestra el nivel de carotenoides en plasma en ratas inoculadas dos veces por semana con 10 mg/kg β-caroteno o licopeno con un contenido de aprox. 20 % en β-caroteno; 3 ES 2 181 682 T3 La Figura 12 ilustra el número acumulativo de tumores /10 ratas en el experimento in vivo del Ejemplo 8; 5 La Figura 13 muestra la reducción obtenida con licopeno en el área media de los tumores mamarios inducidos por DMBA en el experimento in vivo del Ejemplo 8; La Figura 14 muestra los resultados de los experimentos de sobrevivencia en ratones desnudos. Descripción detallada de la invención 10 15 20 25 30 35 El licopeno es un material de origen natural, abundante en los tomates ası́ como también en otras frutas y verduras. También se puede producir sintéticamente o biosintéticamente, es decir, por procedimientos de ingenierı́a genética tales como los descritos en la patente EP 393.690. Cuando se prepara licopeno de fuentes naturales, es decir, de tomates, se machacan los tomates, se concentran y la fracción lipı́dica que contiene el licopeno se extrae del puré utilizando un disolvente adecuado, p.ej. acetona o un aceite, del cual se separa a continuación. El licopeno es esencialmente insoluble en agua y por consiguiente su posterior purificación es relativamente sencilla. Tal como será evidente para un quı́mico con experiencia, la extracción del licopeno de los tomates o de otras fuentes naturales, tales como las algas, no constituye problemas técnicos significativos. Se ha encontrado que el licopeno es un potente inhibidor de la actividad mitocondrial. La actividad celular se mide por el procedimiento MTT, que se basa en la actividad de las deshidrogenasas mitocondriales. Sorprendentemente, la actividad celular no es una medida directa del crecimiento de las células cancerosas y estos dos valores solamente se correlacionan bien a concentraciones de licopeno elevadas. En otras palabras, la actividad celular, tal como se mide por la actividad de las deshidrogenasas mitocondriales, no es directamente proporcional a la reducción del crecimiento de las células cancerosas a contenidos bajos de licopeno. En consecuencia, en el contexto de la presente invención, la reducción de la actividad celular se debe interpretar en un sentido más amplio que el de la inhibición del crecimiento de las células cancerosas. La naturaleza exacta y las consecuencias de la reducción de la actividad celular, tal como se mide por el procedimiento MTT, no han sido averiguadas totalmente. Sin embargo, parte de la reducción en la actividad mitocondrial parece tener un claro efecto inhibitorio en el crecimiento de las células cancerosas, tal como se describe en más detalle a continuación. Según una forma de realización preferida de la presente invención, el licopeno utilizado en el procedimiento de la invención es un extracto natural, en particular un extracto de tomate. En otra forma de realización de la presente invención, el licopeno utilizado es un producto biosintético o sintético. 40 45 50 55 60 Dependiendo del tipo de enfermedad implicada y del área afectada, se puede administrar el licopeno de formas diferentes. En los tumores superficiales localizados el licopeno se administra de forma tópica o por inyección in situ. Cuando se necesita una actividad sistémica, el licopeno se puede inyectar o administrar oralmente o por vı́a rectal. Debido a su naturaleza lipı́dica, el licopeno también se puede administrar tópicamente cuando se necesita una actividad sistémica. El licopeno, tal como se ha indicado, es esencialmente insoluble en agua y, por consiguiente, algunas aplicaciones necesitan de su disolución, p. ej. por una suspensión fina, utilizando agentes surfactantes, por combinación con dos o más medios de disolución, etc. Desde luego se pueden utilizar también otros vehı́culos farmacéuticos convencionales y sistemas de distribución, bien conocidos en la técnica y por consiguiente, por brevedad, no ser discuten con detalle en la presente memoria. El licopeno se puede administrar solo, o junto con otros materiales farmacológicamente activos, vehı́culos, adyuvantes y aditivos y además se puede administrar por muchas vı́as diferentes. Dichos materiales convencionales y rutas de administración pueden ser, por ejemplo, pero sin quedar limitado a ellas, las descritas en la patente US n◦ 5.008.295 mencionada anteriormente. Se ha encontrado que el licopeno es sorprendentemente activo en la inhibición del crecimiento de una multiplicidad de células cancerosas y no se debe interpretar la invención como quedando limitada a cualquier tipo de célula cancerosa en particular. Los ejemplos ilustrativos y no limitantes de dichos tipos de células cancerosas, cuyo crecimiento se puede inhibir según el procedimiento de la presente invención son: cáncer de mama, cáncer de endometrio, cáncer de próstata, cáncer de ovario, cáncer de pulmón (los tipos de célula pequeña y no pequeña), melanomas, cáncer de vejiga, cáncer de páncreas, cáncer gástrico, cáncer de hı́gado, leucemias, glioblastoma, neuroblastoma y otros tipos de tumores cerebrales y cáncer 4 ES 2 181 682 T3 de cervix. 5 La invención también se refiere a la utilización de composiciones para reducir la actividad de las células de los mamı́feros, en particular, pero no de forma limitante, para inhibir el crecimiento de las células cancerosas, composiciones que comprenden como ingrediente activo una cantidad de licopeno efectiva para inhibir el crecimiento de las células cancerosas, solo o en combinación con vehı́culos farmacéuticamente aceptables, adyuvantes o aditivos. Descripción detallada de las formas de realización preferidas 10 La presente invención se ilustra a continuación con más detalle a través de los siguientes ejemplos ilustrativos y no limitativos. Procesos Generales 15 Fuentes de carotenoides El licopeno se obtuvo de diferentes orı́genes: 20 1) material comercial de Sigma; 2) un extracto preparado especı́ficamente para los experimentos descritos más adelante, por extracción de tomates, tal como se explicó anteriormente (5 % oleoresina de tomate); 25 30 3) licopenos sintéticos totalmente trans (Hoffman La-Roche). El licopeno comercialmente disponible (ex Sigma), mostrado en la Fig. 6(a), fue comparado expectroscópicamente con el extracto recientemente preparado para los experimentos descritos más adelante (Fig. 6(b)), y se puede observar que no se encuentran diferencias significativas. Los carotenos α y β se adquirieron de Sigma. Lı́neas celulares y cultivos 35 40 La lı́nea de endometrio humano HEC-IA se obtuvo de la American Type Culture Collection (Rockville, MD). Representa un clon que se originó a partir de un adenocarcinoma papilar de endometrio de un paciente de 71 años de edad y es hormonoindependiente. La lı́nea celular Ishikawa hormonodependiente de endometrio humano que se originó de un tumor bien diferenciado fue generosamente suministrada por H. Rochefort (Instute National de la Sante et de la Recherche Medicale, Montpellier, Francia). Las células MCF-7 de cáncer de mama humano originadas a partir de un tumor bien diferenciado fueron generosamente suministradas por H. Rochefort (Institute National de la Sante et de la Recherche Medicale, Montpellier, Francia). 45 Cultivo celular 50 Las células cancerosas humanas MCF-7 (mamarias) Ishikawa y HEC-IA (endometriales) se cultivaron en frascos de 75 cm2 en medio Eagle modificación por Dulbecco (Biological Industries, Beth Haemek, Israel) con penicilina (100 U/ml), estreptomicina (0,1 mg/ml), nystatin (12,5 µg/ml), insulina (0,6 µg/ml) y 10 % suero bovino fetal. Crecimiento celular 55 60 Se despojó a las células de los esteroides endógenos de acuerdo con el procedimiento Vignon et al. (Biochem. Biophys. Res. Comm., vol. 146, n◦ 3 (1987)) por pasadas sucesivas en medio carente de rojo de fenol conteniendo primero 10 % y después 3 % de suero fetal lavado con carbón (FCS/DCC), sembrando en placas de 96 pocillos (12.000 - 20.000 células por pocillo) en medio conteniendo 3 % FCS/DCC carente de insulina. Un dı́a más tarde se cambió el medio por FCS/DCC al 3 % suplementado con adiciones tal como se indica en los pies de figura durante diversos perı́odos de tiempo. 5 ES 2 181 682 T3 Actividad celular por el procedimiento MTT 5 Una vez terminada la incubación, la actividad mitrocondrial se determinó por la reducción celular de MTT a un producto azul de formazano (Sigma) por las deshidrogenasas mitocondriales de las células viables. Cuando dicho producto se disuelve en DMSO, su absorbancia se mide espectrofotométricamente por ELISA. Determinación del número de células por incorporación de timidina 10 15 Una vez terminada la incubación, el número de células y la velocidad de proliferación celular se determinaron por incorporación de [3 H] timidina en el ADN celular. Se añadieron 10 µC de timidina marcada a cada pocillo y se continuó la incubación por cuatro horas adicionales. Para detener la incorporación, se descartó el medio, se lavaron los pocillos una vez con PBS y se despegaron las células con 50 µl de tripsina (0,25 %), se cosecharon por filtración al vacı́o en un filtro de fibra de vidrio y se contaron en un contador de centelleo. Para validar el procedimiento y correlacionar la radioactividad contada con el número de células, se contaron pocillos paralelos con un hemocitómetro. Existe una buena correlación entre ambos procedimientos (Fig. 7). Solubilización de los carotenoides 20 Los carotenoides se aplicaron a las células por dos procedimientos diferentes: 25 30 35 1) como un material disuelto (ver más adelante) y como una disolución en tetrahidrofurano (THF). Ningún efecto significativo es evidente en el crecimiento celular empleando una dilución final del 0,1 % ó 0,5 % de THF, que es suficiente para disolver la máxima concentración de carotenoides necesaria para los experimentos. Los carotenoides se disolvieron en THF conteniendo 0,05 % BHT como antioxidante a una concentración máxima de 2 mM. Dichas disoluciones se utilizaron en el mismo dı́a del experimento o se guardaron a -70◦ C para futura utilización. Dicha disolución se diluyó con THF y se añadió al medio que se agitó vigorosamente. La concentración final de THF fue de 0,5 %. Para verificar la concentración final de carotenoide, el medio de incubación se extrajo con isopropanol y con una mezcla de hexano/diclorometano (5:1) y se midió la absorbancia en un espectrofotómetro. Todos los procesos se realizaron en la penumbra. 2) Los carotenoides se disolvieron mezclándolos con agentes surfactantes. Una preparación tı́pica de licopeno implica añadir a una parte de un extracto de tomate con 5 % licopeno 1 parte de Tween 40 (monopalmitato sorbitano, Atlas Corp., U.S.A.) y una parte de Croduret 50-S (aceite de ricino hidrogenado, ex Croda Chem. Ltd., England), filtrando en caliente añadiendo a la disolución resultante, una vez enfriada de enfriar, una solución de ácido ascórbico en agua bidestilada y filtrando si fuese necesario. Se aplicaron las correspondientes preparaciones a los α y β-carotenos. 40 Los resultados presentados en las Figuras 1 a 5 son representativos. Se obtuvieron resultados similares con todas las lı́neas celulares, excepto cuando se indique lo contrario. Ejemplo 1 45 Actividad de las células Ishikawa de cáncer de endometrio 50 El efecto dosis dependiente del licopeno, α-caroteno (ex Sigma Chemical Co.) y β-caroteno (ex Sigma) en la actividad celular se ensayó sobre el crecimiento de las células Ishikawa. Se crecieron las células durante 3 dı́as en presencia de carotenoides a las concentraciones indicadas. Se midió la actividad celular tal como se ha descrito. Los resultados son la media de tres experimentos diferentes, cada uno realizado con diez réplicas. 55 En la Fig. 1 se muestran los resultados de dicho experimento. La ED50 para la inhibición de la actividad celular por el licopeno es de aprox. 3x10−10 M, (reducción de la actividad celular desde 53x103 hasta 33x103 ) comparado con aprox. 3x10−7 M para el α-caroteno. El β-caroteno, por otra parte, no mostró efecto en esta lı́nea celular (el efecto mostrado no es estadı́sticamente significativo). 60 6 ES 2 181 682 T3 Ejemplo 2 Efecto de los carotenoides de orı́genes diversos en la actividad de la lı́nea cancerosa MCF-7 5 El efecto del licopeno de diferentes orı́genes fue comparado con el de otros carotenoides, en las células cancerosas MCF-7. Se hicieron crecer las células durante tres dı́as en presencia de carotenoides a las concentraciones indicadas. Los resultados se muestran en la Fig. 2, en la que “Tomates” identifica licopeno disuelto extraı́do de tomates, disuelto en THF y llevado a un contenido de 2x10−8 M licopeno. También se ensayó el control (sin adición) y una solución acuosa de THF al 0,1 % en peso. 10 “Alga” identifica al material extraı́do de algas y suministrado por The Institute for Applied Research de la Ben-Gurion University de Negev, Beer-Sheva, Israel, en el que “beta” identifica β-caroteno y “canta” identifica cantaxantina, suministrada a las células una vez disuelta inicialmente en THF. 15 20 “Sigma” identifica material comprado a Sigma Chemical Co., St. Louis, Mo., USA., donde “beta” identifica β-caroteno, suministrado a las células tal como se describió anteriormente. “Hoffman La-Roche” identifica material obtenido de Hoffman La-Roche, Inc. Nutely, NJ, U.S.A., en forma de cuentas solubles en agua, en el que “beta” identifica β-caroteno y “canta” identifica cantaxantina. Se aprecia fácilmente en la Fig. 2 que el licopeno, independientemente de su origen, fue sustancialmente más efectivo en reducir la actividad celular. 25 Ejemplo 3 Efecto en la actividad de la lı́nea celular endometrial HEC-IA 30 35 40 Se ensayaron en el curso del tiempo los efectos del licopeno, el α-caroteno y el β-caroteno (3x10−7 M) en la actividad celular de las células de cáncer endometrial HEC-IA. Se incubaron las células durante dos dı́as con los carotenoides indicados en placas de 96 pocillos. La actividad de las células se midió por el procedimiento de MTT. Se compararon los efectos del α-caroteno, β-caroteno y licopeno de dos orı́genes (Sigma y extracto reciente de tomate) y de dos disoluciones obtenidas por dos procedimientos de preparación diferentes (disuelto en 0,1 % THF y en agua). Los resultados se muestran en la Fig. 3. La Fig. 3(a) compara los efectos del β-caroteno con un licopeno disuelto derivado de en un extracto de tomate, en disolución acuosa preparada tal como se describió anteriormente. Los dramáticos efectos del licopeno en la reducción de la actividad celular son auto evidentes, mientras que el β-caroteno es esencialmente inactivo, siendo su comportamiento esencialmente igual al del control. La Fig. 3(b) compara la actividad del α-caroteno con la del licopeno (el licopeno de Sigma y disuelto en 0,1 % THF). Se obtuvo el mismo resultado que en la Fig. 3(a), donde el α-caroteno también se comporta esencialmente como el control. Ejemplo 4 45 Efecto de las aplicaciones repetidas diarias (múltiple) versus una aplicación única de licopeno sobre la actividad de las células de tumor de mama MCF-7 50 55 Se aplicó diariamente 3x10−7 M licopeno (en los dı́as 0, 1 y 2), o una vez (solamente en el dı́a 0). El control contuvo 0,1 % THF. Los resultados se muestran en la Fig. 4. El medio se reemplazó a diario. Los resultados sugieren que las aplicaciones diarias mejoran dramáticamente el efecto reductor de la actividad del licopeno sobre las células MCF-7. Esto es probablemente debido a la corta vida media del caroteno en el medio de incubación. Dicha conclusión está apoyada por el hecho de que el licopeno ya no parece ser efectivo en el dı́a 2 cuando se añade solamente una vez (siendo paralelas la lı́nea control y la experimental). Ejemplo 5 60 Efecto del licopeno sobre la actividad de las células MCF-7 inducidas por IGF-I Para contestar a la pregunta de si la proliferación inducida por el Factor de Crecimiento Similar a 7 ES 2 181 682 T3 la Insulina-I (IGF-I) era afectada por el licopeno, las células MCF-7 fueron incubadas con IGF (3x10−8 M). El licopeno redujo la actividad mitrocondrial tanto de las células tumorales en ausencia de IGF-I ası́ como la de las estimuladas por IGF-I. En la Fig. 5 la actividad en presencia de 3x10−7 M licopeno es inferior que con IGF-I solamente. 5 En los siguientes ejemplos se demuestra la inhibición del crecimiento de las células tumorales in vitro e in vivo. La reducción general de la actividad celular no se examina y solamente se ensaya el efecto inhibidor directamente pertinente al crecimiento de las células cancerosas. 10 Ejemplo 6 Inhibición del crecimiento de las células Ishikawa de cáncer de endometrio 15 Los resultados de este experimento se muestran en la Fig. 8. En estos resultados se observa que el licopeno necesita solamente 0,8 µM, en comparación con los 3 µM del β-caroteno, para alcanzar una reducción del 50 % en el número de células de 18x103 a 9x103 . Ejemplo 7 20 Inhibición del crecimiento de las células H226 de cáncer de pulmón 25 Los resultados de este experimento se muestran en la Fig.9. De estos resultados se observa que el licopeno requiere solamente 1,8 µM, en comparación con 3,5 µM del β-caroteno, para alcanzar una reducción del 50 % en el número de células desde 17x103 hasta 8,5x103. Se necesitan concentraciones superiores de α-caroteno para obtener tales efectos. Estos resultados se confirmaron con diferentes preparaciones de licopeno (Fig.10), incluyendo aquellas obtenidas de Sigma, Hoffman- La Roche y de oleoresina de tomate. Se observa por consiguiente que el origen preciso del licopeno empleado no es esencial. 30 Ejemplo 8 Efecto de los carotenoides sobre la inducción y el crecimiento de tumores mamarios de rata inducidos in vivo por DMBA 35 El objetivo de estos experimentos fue estudiar el efecto del licopeno sobre el número y tamaño de los tumores mamarios de rata inducidos por DMBA y compararlo con el del β-caroteno. 40 El tumor mamario de rata es un modelo excelente para el cáncer de mama hormonodependiente humano, ya que la velocidad de crecimiento de los tumores se puede manipular fácilmente por estrógenos y otras hormonas [Levy, J. et al., Eur. J. Cancer Clin. Oncol., 17:1023-1026, (1981); Sharoni, Y et al., FEBS Lett., 189:133-136, (1985); Johnson, M. L., et al., Cancer Res., 43:2199-2209, (1983)]. En cada uno de los cuatro siguientes grupos experimentales hubo entre ocho y dieciséis ratas: 45 a. control, ningún tratamiento. b. placebo, inyectado intraperitonealmente con el vehı́culo utilizado para disolver los carotenoides. c. Licopeno, inyectado i.p. con oleoresina de licopeno 5 % disuelta. 50 d. β-caroteno, inyectado i.p. con un material sintético fabricado por Hoffman-La Roche. Este experimento se repitió 3 veces. 55 60 El placebo y los dos carotenoides (disueltos en agua) se administraron i.p. dos veces por semana (10 mg/kg). El tratamiento se inició dos semanas antes de la inducción de tumores por DMBA y se continuó durante veinte semanas. La dieta normal de las ratas consistió en 50 % maı́z y 50 % ingredientes sintéticos. Esta dieta proporciona un contenido muy bajo en carotenoides. Los tumores mamarios se indujeron en las ratas con 20 mg DMBA (7,12-dimetilbenz[a]antraceno), tal como describe [Sharoni, Y. et al., Eur. J. Cancer Clin. Oncol., 20:277-281, (1984)]. Dos veces por semana se inspeccionaron las ratas y una vez por semana se determinó el tamaño de los tumores por medición con un calibre del diámetro en dos dimensiones perpendiculares entre sı́. Los dos diámetros producen el 8 ES 2 181 682 T3 área del tumor. Veinte semanas después de iniciar la administración de carotenoide, se sacrificaron todos los animales y se extrajeron y congelaron (-70◦C) los tumores. Se recogió sangre, se separó el plasma y se guardó congelado bajo nitrógeno para medir los niveles de carotenoides. El análisis patológico de los animales no reveló ningún daño a los tejidos debido al tratamiento con el placebo o los carotenoides. 5 Para evaluar la eficiencia de la administración de los carotenoides, se midieron los niveles en sangre de grupos separados de ratas que fueron tratadas con carotenoides tal como se describió anteriormente. 10 Las ratas se sacrificaron cada dos semanas, 48 horas de la última inyección y la sangre se guardó para el análisis por HPLC. Dicho análisis mide los niveles de los diferentes carotenoides y sus isómeros [Elinder, L. S. y Walldius, G., Journal of Lipid Research, 33:131-137, (1992); Stahl, W. et al., Archives Biochem. Biophys., 294:173-177, (1992)]. Niveles de carotenoides en plasma 15 20 En el plasma de las ratas control y en las tratadas con el placebo no se detectó licopeno ni β-caroteno. Se detectaron carotenoides en los grupos tratados con licopeno o β-caroteno (Fig. 11). El nivel de βcaroteno fue significativamente más elevado que el nivel de licopeno aunque las ratas fueron inyectadas con cantidades iguales de los dos carotenoides. En el plasma de los animales tratados con licopeno se detectó un pico no identificado. Este puede representar una forma oxidada del licopeno. Tamaño y número de los tumores 25 El número de tumores por cada 10 ratas fue el inferior en el grupo tratado con licopeno (Fig.12). Este resultado fue reproducible en los tres experimentos. Durante la mayor parte del experimento el tamaño medio de los tumores fue inferior en el grupo tratado con licopeno (Fig.13). Ejemplo 9 30 Supervivencia en ratones desnudos Los experimentos de supervivencia se realizaron en ratones desnudos (embras, C. Rivers, 25g, d. fix) implantadas i.p. con tumores humanos de carcinoma de ovario Ovcar-3. 35 40 45 50 55 60 Se diluyó (1,2 g de licopeno en el vial con cuentas de vidrio estériles) una suspensión de 5 % licopeno (ex Makhteshim) con Emulphor/solución salina, para proporcionar una dilución de 1:10 (peso/vol.). En el experimento se utilizaron 60 ratones desnudos, en 6 grupos de 10 animales cada uno. Los tumores se implantaron en el dı́a 0 y licopeno se inyectó diariamente i.p. durante los dı́as 1 a 10. Los grupos se trataron como sigue a continuación: Grupo Grupo Grupo Grupo Grupo Grupo 1 (control): 2: 3: 4: 5: 6: Emulphor 100 mg/kg licopeno 50 mg/kg licopeno 25 mg/kg licopeno 12,5 mg/kg licopeno 6,25 mg/kg licopeno Se examinaron los ratones diariamente para determinar supervivencia. Los resultados se muestran en la Fig. 14, que ilustra el efecto hasta los 50 post implantación. En este experimento se encontró una actividad supresora de los tumores significativa, hasta una dosis mı́nima de 12,5 mg/kg. Tal como será apreciado por un experto en la materia, la dosis de licopeno que debe utilizarse en cada caso varı́a dependiendo del tipo de tumor, la ruta de administración y la severidad de los sı́ntomas. Son dosis ilustrativas de licopeno, p.ej., 7 mg/kg hasta 200 mg/kg. Sin embargo, como se entenderá, el licopeno no sufre de los graves problemas de toxicidad asociados con muchos fármacos para el cáncer y por consiguiente, se pueden dar al paciente dosis de licopeno relativamente elevadas. Además, debido a sus efectos sobre la actividad celular, el licopeno puede administrarse convenientemente como un componente en las composiciones farmacéuticas anticancerosas que contienen otros y/o agentes anticancerosos convencionales u otros agentes farmacéuticos, ası́ como en mezclas con otros ca9 ES 2 181 682 T3 rotenoides y aditivos farmacéuticamente efectivos. El licopeno se puede administrar por diferentes rutas, p.ej., por inyección intravenosa, subcutánea o intramuscular, tópica u oralmente, o por supositorios rectales. 5 10 15 20 Las preparaciones farmacéuticas par la utilización según la presente invención, que contienen una cantidad terapéuticamente efectiva de licopeno, se pueden preparar por procedimientos conocidos, en combinación con vehı́culos farmacéuticamente aceptables. Los ejemplos de vehı́culos y adyuvantes aceptables son: agentes con acción superficial, p.ej., éster de ácido graso y sacarosa, éster de propilenglicol y ácido graso, lecitina, etc.; sacarosa, lactosa, almidón, manitol, carbonato cálcico, bicarbonato sódico, y otros vehı́culos útiles; agregantes, p.ej., goma arábiga, gelatina, etc.; lubricantes, tales como el talco o el estearato magnésico; sabores y agentes preservantes; aceites, tales como el aceite de coco, el aceite de oliva, el aceite de soja; rellenos, recubrimientos, emulgentes y aditivos comerciales similares. Las preparaciones se pueden fabricar para la administración oral, p.ej., en forma de cápsulas blandas y duras, pastillas, gránulos, granos, polvos y pueden estar en formas de liberación retardada, o en forma lı́quida p.ej., como suspensiones. Para la administración parenteral se pueden utilizar otras formas comúnmente empleadas, p.ej., inyecciones, gotas, supositorios, etc. Son ejemplos ilustrativos de las preparaciones: Preparación A 25 Se suspenden en 1 kg de aceite de soja 10g de licopeno. Con la suspensión se rellenan cápsulas de gelatina (aproximadamente 1000 cápsulas). Preparación B 30 Se diluyen 12 g de licopeno con Emulphor/solución salina, para dar una dilución 1:10 (peso/vol.). La solución resultante se utiliza como solución inyectable. Preparación C 35 Se mezclan con calentamiento suave 1 g de licopeno y 3 kg de una mezcla que incluye 1,7 kg de cera de jojoba hidrogenada y 1,3 kg de monoestearato de glicerina en cera de jojoba lı́quida. Se obtiene un ungüento adecuado para aplicaciones tópicas. 40 45 50 55 60 10 ES 2 181 682 T3 REIVINDICACIONES 5 10 1. Utilización del licopeno para la preparación de un medicamento para reducir la actividad o inhibir el crecimiento de una célula cancerosa tal como se mide por el procedimiento MTT por administración a un sujeto que lo necesita, tópicamente o por inyección in situ o sistémicamente, de una cantidad de licopeno efectiva para reducir la actividad o inhibir el crecimiento, en la que las células cancerosas cuya actividad se ha de inhibir están seleccionadas de entre el grupo que consiste en células de: cáncer de mama, cáncer de endometrio, cáncer de próstata, cáncer de ovario, cáncer de pulmón los tipos de célula pequeña y no pequeña, cáncer de vejiga, cáncer de páncreas, cáncer gástrico, cáncer hepático y cáncer de cervix. 2. Utilización según la reivindicación 1, en la que el licopeno es un extracto natural. 3. Utilización según la reivindicación 2, en la que el extracto es un extracto de tomate. 15 4. Utilización según la reivindicación 1, en la que el licopeno es un producto sintético. 5. Utilización según cualquiera de las reivindicaciones 1 a 4, en la que el licopeno se administra de forma tópica. 20 25 30 35 6. Utilización según cualquiera de las reivindicaciones 1 a 4, en la que el licopeno se administra por inyección. 7. Utilización según cualquiera de las reivindicaciones 1 a 4, en la que el licopeno se administra de forma oral. 8. Procedimiento para reducir la actividad o inhibir el crecimiento de una célula cancerosa tal como se mide por el procedimiento MTT, que comprende la etapa de administrar in vitro a dicha célula una cantidad de licopeno efectiva para reducir la actividad o inhibir el crecimiento, en el que dicha célula cancerosa está seleccionada de entre el grupo que comprende células de: cáncer de mama, cáncer de endometrio, cáncer de próstata, cáncer de ovario, cáncer de pulmón con tipos de célula pequeña y no pequeña, cáncer de vejiga, cáncer de páncreas, cáncer gástrico, cáncer hepático y cáncer de cervix. 9. Procedimiento según la reivindicación 8, en el que el licopeno es un extracto natural, preferiblemente un extracto de tomate. 10. Procedimiento según la reivindicación 8, en el que el licopeno es un producto sintético. 40 45 50 55 60 NOTA INFORMATIVA: Conforme a la reserva del art. 167.2 del Convenio de Patentes Europeas (CPE) y a la Disposición Transitoria del RD 2424/1986, de 10 de octubre, relativo a la aplicación del Convenio de Patente Europea, las patentes europeas que designen a España y solicitadas antes del 7-10-1992, no producirán ningún efecto en España en la medida en que confieran protección a productos quı́micos y farmacéuticos como tales. Esta información no prejuzga que la patente esté o no incluı́da en la mencionada reserva. 11 ES 2 181 682 T3 12 ES 2 181 682 T3 13 ES 2 181 682 T3 14 ES 2 181 682 T3 15 ES 2 181 682 T3 16 ES 2 181 682 T3 17 ES 2 181 682 T3 18 ES 2 181 682 T3 19 ES 2 181 682 T3 20 ES 2 181 682 T3 21 ES 2 181 682 T3 22 ES 2 181 682 T3 23 ES 2 181 682 T3 24