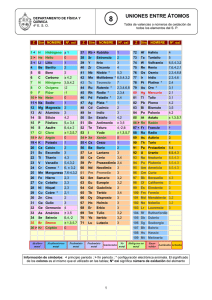
I. FORMULACIÓN DE QUÍMICA INORGÁNICA
Anuncio
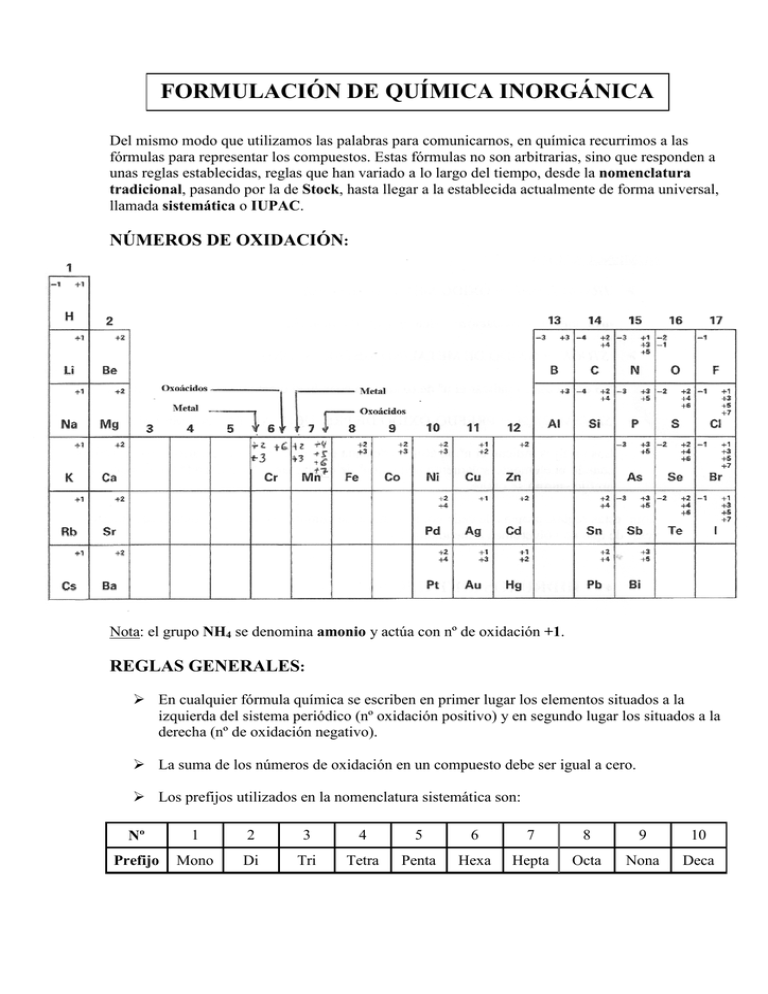
FORMULACIÓN DE QUÍMICA INORGÁNICA Del mismo modo que utilizamos las palabras para comunicarnos, en química recurrimos a las fórmulas para representar los compuestos. Estas fórmulas no son arbitrarias, sino que responden a unas reglas establecidas, reglas que han variado a lo largo del tiempo, desde la nomenclatura tradicional, pasando por la de Stock, hasta llegar a la establecida actualmente de forma universal, llamada sistemática o IUPAC. NÚMEROS DE OXIDACIÓN: Nota: el grupo NH4 se denomina amonio y actúa con nº de oxidación +1. REGLAS GENERALES: En cualquier fórmula química se escriben en primer lugar los elementos situados a la izquierda del sistema periódico (nº oxidación positivo) y en segundo lugar los situados a la derecha (nº de oxidación negativo). La suma de los números de oxidación en un compuesto debe ser igual a cero. Los prefijos utilizados en la nomenclatura sistemática son: Nº 1 2 3 4 5 6 7 8 9 10 Prefijo Mono Di Tri Tetra Penta Hexa Hepta Octa Nona Deca • ÓXIDOS Los óxidos son combinaciones del oxígeno con otro elemento (metal / no metal). En estos compuestos el oxígeno actúa con el nº de oxidación -2. FORMULACIÓN Se escriben los símbolos de los elementos (regla general) se intercambian los nº de oxidación sin signo y se simplifican (Tradicional / Stock). NOMENCLATURA TRADICIONAL ÓXIDO METAL (-oso / - ico) -oso: menor nº oxidación -ico: mayor nº oxidación STOCK ÓXIDO DE METAL/NO METAL (Nº OXI) No es necesario indicar el nº de oxidación cuando el elemento solamente tiene uno. SISTEMÁTICA PREFIJO-ÓXIDO DE PREFIJO(*)-METAL/NO METAL Los prefijos indican el nº de átomos de cada elemento. No es necesario utilizar prefijos cuando el elemento solamente tiene un nº de oxidación. El asterisco (*) indica que el prefijo -mono se omite. Nota: estas reglas, propias de cada nomenclatura, se cumplen en todos los demás compuestos a pesar de que no volveremos a mencionarlas. • HIDRUROS METÁLICOS Los hidruros metálicos son combinaciones de hidrógeno con un metal. En estos compuestos el hidrógeno actúa con nº de oxidación -1. FORMULACIÓN Se escriben los símbolos de los elementos (regla general) se intercambian los nº de oxidación sin signo y se simplifican (Tradicional / Stock). NOMENCLATURA TRADICIONAL HIDRURO METAL (-oso / - ico) STOCK HIDRURO DE METAL (Nº OXI) SISTEMÁTICA PREFIJO-HIDRURO DE PREFIJO(*)-METAL • HIDRUROS NO METÁLICOS Los hidruros no metálicos son las combinaciones del hidrógeno con un no metal. En estos compuestos el hidrógeno actúa con nº de oxidación +1. Dentro de los hidruros no metálicos podemos distinguir dos grupos: 1. HIDRUROS NO METÁLICOS DE LOS GRUPOS 13-14-15 NOMENCLATURA TRADICIONAL NOMBRES PROPIOS BH3: Borano CH4: Metano SiH4: Silano NH3: Amoníaco PH3: Fosfina AsH3: Arsina SbH3: Estibina SISTEMÁTICA PREFIJO-HIDRURO DE PREFIJO(*)-NO METAL 2. HIDRUROS NO METÁLICOS DE LOS GRUPOS 16-17 FORMULACIÓN Se escriben los símbolos de los elementos (regla general) se intercambian los nº de oxidación sin signo y se simplifican (Tradicional / Sistemática). NOMENCLATURA TRADICIONAL ÁCIDO NO METAL-HÍDRICO SISTEMÁTICA NO METAL-URO DE HIDRÓGENO • SALES BINARIAS Las sales binarias son la combinación de metal y no metal, o bien, de dos no metales. FORMULACIÓN Se escriben los símbolos de los elementos (regla general) se intercambian los nº de oxidación sin signo y se simplifican (Tradicional / Stock). NOMENCLATURA TRADICIONAL NO METAL-URO METAL (-oso / - ico) STOCK NO METAL-URO DE METAL/NO METAL (Nº OXI) SISTEMÁTICA PREFIJO-NO METAL-URO DE PREFIJO(*)-METAL/NO METAL • HIDRÓXIDOS Los hidróxidos son compuestos que resultan de la combinación de metal con el grupo hidroxilo (OH). El grupo hidroxilo actúa con nº de oxidación -1. FORMULACIÓN Se escriben los símbolos de los elementos (regla general) se intercambian los nº de oxidación sin signo y se simplifican (Tradicional / Stock). NOMENCLATURA TRADICIONAL HIDRÓXIDO METAL (-oso / - ico) STOCK HIDRÓXIDO DE METAL (Nº OXI) SISTEMÁTICA PREFIJO-HIDRÓXIDO DE PREFIJO(*)-METAL • OXOÁCIDOS Los oxoácidos son compuestos ternarios formados por hidrógeno, no metal y oxígeno. La fórmula general de un oxoácido es HaXbOc FORMULACIÓN En primer lugar se calcula el coeficiente (c) del oxígeno y luego el coeficiente (a) del hidrógeno de tal forma que, la suma de nº de oxidación en el oxoácido sea cero (regla general). Notas: en la nomenclatura tradicional: - El nº de átomos del no metal (b) se indica mediante un prefijo (el prefijo mono- se omite). Si el no metal lleva el prefijo di- el subíndice del oxígeno (c) debe ser un nº impar. El nº de átomos de hidrógeno se indica mediante un prefijo Meta- 1 o 2 átomos de hidrógeno (suele omitirse excepto en el P, As y Sb) Orto- más de 2 átomos de hidrógeno (suele omitirse en el P, As y Sb) NOMENCLATURA Hipo TRADICIONAL ÁCIDO NO METAL Per- -oso (menor nº oxidación) -oso -ico -ico (mayor nº oxidación) SISTEMÁTICA PREFIJO-OXO NO METAL-ATO (Nº OXI) DE HIDRÓGENO • OXISALES Las sales ternarias u oxisales son los compuestos que resultan de cambiar los hidrógenos de los oxoácidos por metales. FORMULACIÓN En primer lugar se formula el oxoácido correspondiente (-ito -oso // -ato -ico) y luego se sustituyen todos los hidrógenos por átomos del metal intercambiando su nº de oxidación con el resto de la molécula. NOMENCLATURA Hipo TRADICIONAL NO METAL Per- Hipo STOCK NO METAL Per- -ito -ito METAL (-oso / -ico) -ato -ato -ito -ito DE METAL (Nº OXI) -ato -ato SISTEMÁTICA PREFIJO-OXO NO METAL-ATO (Nº OXI) DE METAL (Nº OXI) +2 +3 -2 Ejemplo: Cu(NO2)2 Bis[dioxonitrato (III)] de cobre (II) Prefijo del paréntesis BisTrisTetraquisPentaquisNota: para facilitar la formulación/nomenclatura de oxoácidos y oxisales utilizar la tabla: Nº OXI Impares 1 3 5 7 Pares 2 4 6 PRE / SUF OXOÁCIDO PRE / SUF OXISAL Hipo- -oso -oso -ico Per- -ico HXO HXO2 HXO3 HXO4 Hipo- -ito -ito -ato Per- -ato M(XO)n M(XO2)n M(XO3)n M(XO4)n Hipo- -oso -oso -ico H2XO2 H2XO3 H2XO4 Hipo- -ito -ito -ato M2(XO2)n M2(XO3)n M2(XO4)n Esta tabla no tiene validez en el caso de que el oxoácido tenga más de dos hidrógenos (orto-) o más de un átomo de metal (X). EJERCICIOS: FORMULACIÓN DE QUÍMICA INORGÁNICA ÓXIDOS - Óxido de cobre (II) - Fe2O3 - Heptaóxido de dicloro - CaO - Óxido de estroncio - PtO2 - Óxido de hierro (II) - Al2O3 - Óxido de plata - HgO - Dióxido de plomo HIDRUROS METÁLICOS - Hidruro de aluminio - CoH3 - Tetrahidruro de plomo - NaH - Hidruro de oro (III) - ZnH2 - Dihidruro de cromo - PtH2 - Hidruro de calcio - LiH - Hidruro de estaño (IV) HIDRUROS NO METÁLICOS - Amoníaco - HCl - Ácido sulfhídrico - PH3 - Bromuro de hidrógeno - HI - Metano - HF - Seleniuro de hidrógeno - AsH3 - Ácido iodhídrico - SbH3 SALES BINARIAS - Cloruro de sodio - NH4Cl - Sulfuro de plata - FeBr2 - Fosfuro de aluminio - CoCl3 - Ioduro de hierro (II) - KBr - Fluoruro de sodio - AlP - Bromuro de amonio - CrSe HIDRÓXIDOS - Hidróxido de cinc - Pb(OH)4 - Trihidróxido de oro - Cd(OH)2 - Hidróxido de mercurio (I) - NH4OH - Hidróxido de mercurio (II) - Pt(OH)2 - Hidróxido de estroncio OXOÁCIDOS - Tetraoxosulfato (VI) de hidrógeno - HClO3 - Ácido fosfórico - H2CO3 - Ácido nítrico - HNO2 - Monoxoclorato (I) de hidrógeno - HIO2 - Ácido dicrómico - HBrO2 - Ácido perclórico - H3PO3 - Ácido permangánico - H2SO3 - Ácido hipoiodoso OXISALES - Sulfato de sodio - CaSO3 - Nitrato de magnesio - AgClO4 - Carbonato de magnesio - NaClO - Dicromato de potasio - KMnO4 - Carbonato de sodio - Pb(NO3)2 - Fosfato de aluminio - NaClO3 - Nitrito de litio - KNO3 - Sulfito de plomo (II) EJERCICIOS: FORMULACIÓN DE QUÍMICA INORGÁNICA II • FORMULACIÓN - Monóxido de carbono - Cloruro de hidrógeno - Óxido de hierro (III) - Ácido sulfhídrico - Dióxido de plomo - Metano - Tetracloruro de selenio - Hidruro de cesio - Amoníaco - Hidruro de cobre (I) - Ácido clorhídrico - Óxido de aluminio - Óxido de estaño (II) - Hidróxido de níquel (III) - Sulfuro de manganeso (II) - Ioduro de magnesio - Bromuro de mercurio (I) - Hidróxido de cesio - Cloruro de hierro (II) - Hidróxido de plomo (IV) - Ácido periódico - Ácido sulfúrico - Ácido selenioso - Ácido bromoso - Ácido carbónico - Ácido hipoiodoso - Ácido fosfórico - Ácido dicrómico - Ácido fosforoso - Nitrato de hierro (III) - Sulfato de potasio - Iodato de níquel (II) - Clorato de mercurio (I) - Carbonato de aluminio - Hipoclorito de sodio - Permanganato de potasio • NOMENCLATURA - H2Te - Au2O3 - CO - H2S - CuO - SO3 - PbO2 - MgO - HCl - Cl2O7 - NaH - SbH3 - IF3 - SiH4 - AsH3 - FeH2 - BH3 - CuI - KOH - AuCl - Ni2S3 - CoS - Pb(OH)2 - Cd(OH)2 - PCl5 - FeF3 - HgOH - HBrO - HNO3 - H3PO4 - HIO3 - H2SO4 - H2Cr2O7 - HBrO4 - Na2SO3 - Cu2SO4 - KMnO4 - CaCrO4 - K2Cr2O7