MANEJO DEL DOLOR AGUDO Y CRÓNICO EN PEQUEÑOS
Anuncio

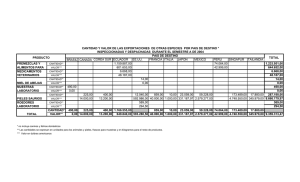
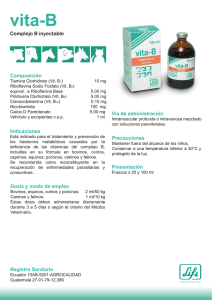
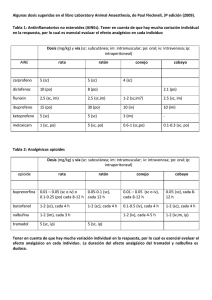
MANEJO DEL DOLOR AGUDO Y CRÓNICO EN PEQUEÑOS ANIMALES Prof. Pablo E. Otero DVM Profesor Regular Adjunto. Área Anestesiología y Algiología. Facultad de Ciencias Veterinarias Universidad de Buenos Aires. Vicepresidente de la Sociedad Latinoamericana de Emergencia y Cuidados Críticos (LAVECCS) Especialista en Anestesiología Veterinaria (AAVRA) Doctorando de la Universidad de Buenos Aires Docente de la Carrera de Médicos Especialistas en Anestesiología. Facultad de Medicina. UBA Investigador de la Universidad de Buenos Aires Introducción Las estadísticas demuestran que el abordaje terapéutico del dolor en los animales domésticos es una práctica postergada. Es importante tomar conciencia de que más allá del compromiso ético que existe con nuestro paciente, implementar un tratamiento analgésico arrojará un beneficio indiscutible. El tratamiento del dolor deberá instaurase toda vez que exista un proceso mórbido en curso que así lo exija. Una buena manera de decidir si la lesión cursa o no con dolor es tomar el lugar del paciente y pensar que todo aquello que produce dolor en el ser humano también lo produce en el animal. Además, aun sin estar indicado, la implementación precoz del tratamiento analgésico arrojará más beneficios que eventuales efectos adversos. Un conocimiento adecuado del comportamiento farmacológico de los compuestos utilizados evitará planear esquemas posológicos ineficaces, al tiempo que facilitará diseñar interacciones sinérgicas y mantener los niveles terapéuticos dentro de sus rangos de eficacia, asegurando el bienestar y la comodidad del paciente. Una vieja frase que dice “ el único dolor fácil de soportar es el ajeno”, nos invita a reflexionar y a no subestimar este magno signo clínico. El dolor es considerado actualmente como el quinto signo vital. Para poder tratarlo hay que mensurarlo por que sólo de esta manera tendremos la posibilidad de evaluar el resultado de nuestro tratamiento. Como se discutiera en el capítulo VI, se deberá apelar a las diversas manifestaciones que acompañan al proceso doloroso y evaluar el resultado del tratamiento sobre cada una de ellas. Tanto el manejo del dolor agudo como el producido por las diferentes maniobras quirúrgicas, exige protocolos que aporten niveles de analgesia eficaces y predecibles. El uso de protocolos que deleguen su eficacia en la combinación de agentes analgésicos es la base de la terapia multimodal. Esta se apoya en el principio farmacodinámico que sostiene que dos drogas con mecanismos de acción diferentes pero con un mismo efecto (analgesia), se potencian al interactuar en el organismo promoviendo un efecto terapéutico superador. Por otra parte, y más allá del beneficio intrínseco que esto ocasiona, la potenciación permite reducir la dosis de los diferentes actores de la interacción farmacodinámica, disminuyendo a su vez la posibilidad de ocasionar los efectos adversos que acompañan a las altas dosis. A la hora de diseñar el protocolo analgésico es importante responder una serie de cuestiones relacionadas con los datos del paciente, los antecedentes terapéuticos si los hubiese, las condiciones en las que se implementará el tratamiento, así como también la infraestructura de la que dispongamos y el entrenamiento tanto del personal médico como del afectado al cuidado del animal. El grado de dolor, las alternativas terapéuticas a disposición así como el costo de éstas, también deberán ser puestos en la balanza a la hora de la elección. Analgesia y anestesia La elección del protocolo anestésico se deberá ajustar a cada paciente evitando caer en la tentación de repetir recetas sin contemplar las necesidades de cada caso en particular. Como vimos, la posibilidad de aportar analgesia preventiva en pacientes quirúrgicos es una alternativa a explotar. Lo primero que se deberá decidir es el grado de depresión del SNC que se proporcionará. Cuanto menor sea la depresión central, mayor deberá ser la eficacia analgésica del protocolo. Este último principio también se aplica a la intensidad del estímulo a realizar, debiendo promover una analgesia mayor en los procedimientos más dolorosos. Cuando la depresión central es ligera como el caso de una sedación o una anestesia superficial, los anestésicos locales suelen ser una excelente opción. Otra posibilidad es incorporar analgésicos centrales antes, durante y después del acto quirúrgico. En este sentido, los hipnoanalgésicos y los agonistas α2 son los compuestos más utilizados. El uso de depresores centrales, tanto anestésicos inhalatorios como inductores del tipo del tiopental sódico, propofol y etomidato a altas dosis, tratando de apelar a su efecto analgésico, es una práctica insegura y de eficacia dudosa. Por lo tanto, se propone suplementar la analgesia de los anestésicos generales, con el fin de equilibrar el protocolo. Los anestésicos disociativos como la ketamina y la tiletamina, muy ampliamente utilizados en medicina veterinaria, son muchas veces sobreestimados con relación a su eficacia analgésica. Al igual que los demás compuestos analizados, éstos mejoran la calidad de la analgesia cuando se los combina con drogas potenciadoras. Los AINES cumplen un papel fundamental en el manejo del dolor del paciente quirúrgico. La discusión se centra en el lugar que deben ocupar en el protocolo anestésico. El consenso general es que, en el posoperatorio, aportan la analgesia necesaria para controlar el dolor en la mayoría de los procedimientos. Si bien se ha propuesto que aportan analgesia preventiva cuando son administrados en el preoperatorio, algunos de ellos se asocian a trastornos renales, sobre todo en pacientes que sufren hipotensiones graves durante el acto operatorio ANTIINFLAMATORIOS NO ESTEROIDES Los AINES son de uso tradicional para el tratamiento del dolor agudo tanto de origen traumático como quirúrgico. Su capacidad para reducir la concentración tisular de autacoides contribuye a evitar tanto la sensibilización de los receptores periféricos como la hipersensibilización central al disminuir la activación antidrómica de las fibras nerviosas y la consecuente liberación de sustancias algésicas en el asta dorsal de la médula espinal. La administración de estos fármacos reduce la intensidad del dolor y la dosis de opiáceos, pero rara vez promueven analgesia completa y satisfactoria después de intervenciones quirúrgicas, a menos que se traten de procedimientos menores. La principal desventaja de sumar estos compuestos al protocolo anestésico durante la premedicación es, exponer al riñón a un daño potencial, en caso de que se produzca una hipotensión intraoperatoria. La mayoría de los trabajos sugieren, al discutir sobre este punto, que los efectos secundarios están más asociados al desarrollo del evento quirúrgico que al uso de los AINES, sobre todo porque el resto de las drogas utilizadas también pueden traer aparejados, como efecto colateral a la hipotensión, trastornos renales de igual magnitud. Es sabido que los AINES disminuyen la síntesis de prostaglandinas y que éstas desempeñan un papal preponderante en la autorregulación del flujo renal. Ante la disminución de estos prostanoides, la capacidad del riñón para evitar la hipoperfusión y la consecuente hipoxia es menor. Se debe tener en cuenta que los desequilibrios hemodinámicos se pueden evitar conservando un correcto equilibrio hídrico en el paciente. Los AINES también disminuyen la agregación plaquetaria y pueden aumentar el sangrado perioperatorio. Por esta razón, no se deben utilizar en pacientes con trastornos de la coagulación. Los trastornos gastrointestinales (gastritis, úlceras y sangrado) son poco frecuentes en tratamientos de corta duración. Los AINES más utilizados en el tratamiento del dolor agudo son: megluminato de flunixin, ketoprofeno, meloxicam, etodolac y carprofeno. Además de los efectos antiinflamatorios, antipiréticos y analgésicos el flunixin (0,5-1 mg/kg IM o IV cada 24 horas en caninos), tiene probada acción antitóxica. Con sólo un 25% de la dosis terapéutica se ha demostrado beneficioso para contrarrestar el efecto de endotoxinas bacterianas en caninos. Por la alta incidencia de efectos colaterales, su uso está contraindicado en felinos mientras que en caninos se restringe al tratamiento del dolor agudo por un corto tiempo (tres días máximo). El piroxicam, otro inhibidor no selectivo de las isoenzimas ciclooxigenasa (COX), se caracteriza por su eficacia antiinflamatoria, además de sus efectos analgésicos y antipiréticos. En caninos su principal indicación (0,3 mg/kg cada 24-48 horas) es como coadyuvante del tratamiento de tumores con importante componente inflamatorio como el carcinoma maligno de vejiga o el carcinoma mamario inflamatorio. Debido a la alta incidencia de efectos colaterales a nivel gastrointestinal, se sugiere la administración conjunta con protectores de la mucosa gástrica como el omeprazol (0,5-1 mg/kg cada 24 horas), un inhibidor de la bomba de protones o la ranitidina, un antihistamínico anti-H2, tanto por vía oral como IV a razón de 0,5-2 mg/kg cada 12 horas. El piroxicam no se recomienda en felinos. El ketoprofeno es un potente inhibidor no selectivo de las isoenzimas COX1 y COX2 con un excelente efecto analgésico, antiinflamatorio y antipirético. Numerosos reportes implican al ketoprofeno en un mecanismo analgésico a nivel del SNC, el cual potenciaría su eficacia en el tratamiento del dolor. En el postoperatorio ha demostrado ser un compuesto eficaz y seguro tanto en caninos como en felinos. El autor lo emplea a 0,25 mg/kg IV durante la fase de eliminación del anestésico volátil pero antes de la extubación, reduciendo de manera significativa el dolor y la incomodidad desde los primeros instantes del período de recuperación. El tratamiento se continúa por vía oral o parenteral a razón de 0,5-1 mg/kg tanto en caninos como en felinos. La dipirona, también conocida como metamizol, (20-30 mg/kg IV, SC, IM cada 8 horas) es efectiva como analgésico en el tratamiento del dolor agudo en los pequeños animales. Se la indica también por su eficaz su acción antipirética, cuando otros AINES no son efectivos. Recientes estudios sindican a la dipirona como efectiva en el manejo del dolor posoperatorio en caninos, administrada por infusión continua en pacientes hospitalizados. Los estudios realizados mantuvieron la infusión por un promedio de 20 horas a la dosis de 10 mg/kg/hora, registrando una disminución en las escalas de dolor sin que se registren efectos adversos relevantes. El carprofeno (2-4 mg/kg PO cada 24 horas en caninos y 4 mg/kg PO en toma única en felinos) es un potente analgésico y antiinflamatorio con escasa actividad diferencial sobre las isoenzimas COX. Esto se refleja en una menor toxicidad asociada a la anestesia general. Informes recientes sostienen que su uso en el período preoperatorio tiene una mayor efectividad que en el posoperatorio. La falta de una presentación inyectable (en Latinoamérica), limita su aplicación durante el perioperatorio. El meloxicam (0,2 mg/kg IV o IM como dosis de carga seguido por una dosis de mantenimiento de 0,1 mg/kg cada 24 horas en caninos y felinos), es un inhibidor selectivo de la COX2. Esto se ve reflejado en una menor presentación de efectos adversos en tratamientos prolongados. Estudios recientes lo indican como efectivo cuando se emplea en la premedicación anestésica. A diferencia del carprofeno, para el meloxicam existe la presentación en solución inyectable. El etodolac (10-15 mg/kg cada 24 horas en caninos), al igual que el meloxicam, inhibe predominantemente a la COX2. Como sucede con el carprofeno sólo se puede prescribir por vía oral. El vedaprofeno es un AINE de excelente tolerancia gástrica, con una alta unión a proteínas lo cual le permite acumularse en el exudado inflamatorio. Este compuesto ha sido aprobado recientemente para ser usado en caninos. Su uso no se encuentra aprobado aun en felinos. Se recomienda a la dosis de 0,5 mg/kg PO cada 24 horas. La tepoxalina es un inhibidor dual ciclooxigenasa/lipoxigenasa recientemente aprobado en algunos países de la Comunidad Europea para ser utilizado en caninos. Los reportes preliminares lo indican como un analgésico efectivo en procesos dolorosos de origen osteoarticular. La forma de administración, mediante tabletas efervescentes de fácil y rápida disolución, la convierten en una alternativa en pacientes resistentes a la ingesta de comprimidos. La dosis sugerida es de 10 mg/kg y la duración del tratamiento no debe exceder las 4 semanas. Al igual que sus congéneres, aumenta la toxicidad en combinación con otros AINES y glucocorticoides. Un significativo avance en el manejo del dolor agudo y crónico ha sido la incorporación de los agentes COX2 selectivos. El deracoxib (aprobado para ser empleado en caninos) celecoxib, valdecoxib, parecoxib (prodroga del valdecoxib) y etoricoxib, todo empleados en medicina humana, estan disponibles para el tratamiento del dolor. La literatura muestra sin embargo, que estos agentes son tan buenos como sus congéneres, los AINES mixtos, pero no mejores. Sin embargo, poseen a favor menores efectos secundarios asociados con desordenes gastrointestinales o aquellos relacionados con la inhibición de la función plaquetaria. Desafortunadamente, la COX2 está presente en el riñón y desempeña un importante papel en la prevención la falla renal durante la deshidratación o la hipotensión. Por esta razón los COX2 selectivos deben ser utilizados con suma precaución en pacientes con afecciones renales previas y en individuos que reporten intensos dolores agudos como por ejemplo los traumatizados. En el paciente traumatizado, los AINES aportan analgesia, aunque su efectividad no es tan marcada como la de los opiáceos durante las primeras horas. Antes de instaurar el tratamiento se debe constatar la ausencia de hemorragias y una perfusión renal adecuada. En caso de encontrar un paciente hipotenso, el procedimiento exige garantizar una efectiva circulación tisular antes de iniciar la terapia con estos agentes. El uso concomitante de AINES y glucocorticoides potencia los efectos tóxicos de ambos tanto a nivel digestivo como renal. La potencial toxicidad de estos fármacos en felinos nos invita a proponerlos como una segunda opción en el paciente traumatizado. Cuando el paciente está siendo tratado con AINES y debe ser anestesiado, la norma es promover una expansión del volumen plasmático mediante la infusión de soluciones electrolíticas a razón de 20 ml/kg antes de la inducción anestésica y chequear, mediante análisis complementarios, el tiempo de coagulación. Si la intervención es electiva, se suspende el tratamiento entre 24 y 48 horas antes de la anestesia pero se mantienen las recomendaciones antes mencionadas. Dolor posoperatorio El tratamiento del dolor posoperatorio se verá ampliamente facilitado por la implementación de protocolos que eviten la sensibilización del tejido nervioso (analgesia preventiva), así como también por el uso de protocolos anestésicos que prioricen la analgesia. Se deberá tener en cuenta que es más sencillo evitar que el dolor se presente que tratarlo una vez instaurado. La terapéutica estará en relación con el procedimiento ejecutado. En la tabla 1 se muestra el esquema propuesto. Tabla 1: Criterio terapéutico a seguir según el grado de dolor presente Condición Criterio Con dolor leve a moderado • AINES (ketoprofeno, meloxicam, carprofeno), u • Opioides agonistas-antagonistas (butorfanol, buprenorfina, nalbufina, dextropropoxifeno, tramadol) Dolor grave • Opioides agonistas puros (morfina, metadona, fentanilo, codeína) + Si el dolor no cede • AINES (ketoprofeno, meloxicam, carprofeno) • Bloqueos regionales centrales o periféricos con anestésicos locales + opioides El uso de hipnoanalgésicos por vía epidural se presenta como una alternativa eficaz en casos refractarios. Para realizar un bloqueo nervioso central efectivo es necesario que el analgésico acceda a las metámeras que reciben los impulsos originados en la zona lesionada. El conocimiento de la anatomía de la especie a tratar garantiza una maniobra efectiva. Recalcamos el concepto de que la analgesia del procedimiento se logra como resultado tanto de las drogas utilizadas como de las maniobras realizadas; un manejo imprudente y agresivo de los tejidos, se traduce invariablemente en un posquirúrgico doloroso y de difícil tratamiento. La valoración correcta del dolor durante el período de recuperación posquirúrgico ayuda a tomar decisiones y evaluar la eficacia terapéutica del protocolo en ejecución. Se recomienda el uso de escalas de valoración a fin de disminuir al máximo la subjetividad del operador. El registro escrito evita desinteligencias entre el personal y permite realizar análisis retrospectivos. La duración del tratamiento se encuentra estrechamente relacionada al procedimiento ejecutado. Como norma los pacientes reciben siempre una administración de analgésicos en el posoperatorio inmediato y se evalúa la continuación del tratamiento en función de las necesidades y la respuesta del sujeto. Las primeras horas del posoperatorio coinciden con el período de mayor dolor. Los efectos analgésicos residuales de las drogas utilizadas durante el acto anestésico junto a dosis de rescate con hipnoanalgésicos, suelen ser la elección en estos períodos iniciales. Los AINEs han demostrado ser efectivos para tratar el dolor en el período posterior que va de las 4 a las 24 horas de finalizada la intervención. Valoración del dolor en el paciente posquirúrgico La imposibilidad de contar con el relato verbal del paciente complica la evaluación del dolor. Lo importante es habituarse a una determinación sistemática y tratar de despojarla al máximo de la subjetividad. Existen diferentes métodos, los más utilizados son la escala visual análoga, numérica y descriptiva. La escala visual análoga consiste en una línea de 100 mm de largo. En el extremo izquierdo se coloca la ausencia de dolor y en el extremo derecho el máximo dolor soportable. El evaluador marca en la línea el dolor que supone está sufriendo el paciente. Con la escala numérica el evaluador asigna un valor de 0 a 10 al dolor que supone está padeciendo el animal. Por último, la escala descriptiva utiliza cuatro categorías para evaluar la intensidad del dolor: 0) Ausencia de dolor 1) Dolor leve 2) Dolor moderado 3) Dolor grave Otra forma sería: 0) Ausencia de dolor 1) Dolor mínimo (fácilmente tolerable sin analgésicos) 2) Dolor moderado (solamente tolerable con analgésicos) 3) Dolor grave (difícil de tolerar aun con analgésicos) Los puntajes de recuperación anestésica utilizan también estos esquemas y le asignan un valor a cada condición. Se emplean: los siguientes parámetros, nivel de actividad, nivel de conciencia, analgesia, estado hemodinámico y respiratorio, los cuales se suman y el resultado refleja la condición del paciente. Opiáceos (hipnoanalgésicos) Los hipnoanalgésicos han demostrado ser una excelente alternativa; a la hora de aportar analgesia preventiva ya que reducen el estado de hiperexcitabilidad causado por la andanada de estímulos aferentes provenientes de diversas maniobras quirúrgicas. Esta salva de estímulos y la consecuente hiperexcitabilidad se conoce como “wind-up”. La eficacia analgésica de los opiáceos es útil en el tratamiento del dolor agudo en los pequeños animales. Como parte del protocolo anestésico, permiten reducir sustancialmente la dosis de anestésicos generales. La morfina (0,4-1 mg/kg en caninos y 0,05-0,2 mg/kg en felinos) y la meperidina (2-6 mg/kg en caninos y 4-10 mg/kg en felinos) por vía IM 20-30 minutos antes de la inducción anestésica potencian a los anestésicos inhalatorios y llegan a reducir su CAD en un 60-70%. La incorporación de fentanilo o cualquiera de sus análogos a las dosis apropiadas, llega a reducir la CAM de los anestésicos inhalatorios hasta un 90%. Como parte del protocolo anestésico y a las dosis recomendadas estos compuestos permiten mantener un equilibrio hemodinámico adecuado. La solidez de su efecto analgésico evita la sensibilización central mejorando el despertar y favoreciendo el manejo del dolor durante el período de recuperación. Estos fármacos pueden combinarse entre sí aunque se deben tener en cuenta sus interacciones farmacodinámicas. La meperidina, cuando se utiliza sin el agregado de tranquilizantes mayores, puede emplearse a altas dosis (5-10 mg/kg IM dosis única) para promover analgesia y sedación. De esta manera se logra una analgesia adecuada durante el acto quirúrgico, aunque su corta duración (90-120 minutos), exige reforzar el tratamiento del dolor durante el período de recuperación. Los agonistas-antagonistas como la buprenorfina (0,02 mg/kg IM), el butorfanol (0,4 mg/kg IM) y la nalbufina (1 mg/kg IM), si bien poseen una eficacia analgésica menor en comparación con los agonistas puros, permiten afianzar la analgesia y potenciar, aunque en menor medida, a los anestésicos generales. El dextropropoxifeno (2 - 4 mg/kg IV, IM) afianza la analgesia y permite reducir el aporte de anestésicos generales. Este compuesto se presenta como una excelente alternativa para sumar analgesia al protocolo anestésico tanto en cirugías tegumentarias como aquellas de tejidos blandos. A la dosis recomendada en combinación con acepromacina (neuroleptoanalgesia) se incrementa el efecto sedante. La duración del efecto analgésico oscila entre 4 y 6 horas. Bajo la acción de este fármaco el perfil hemodinámico del paciente se mantiene estable, aunque se registra una tendencia a la bradicardia. La atropina y el glicopirrolato contrarrestan este efecto. La combinación de dextropropoxifeno (2 mg/kg IV) con agonistas alfa 2 adrenérgicos (xilacina 0,1 – 0,2 mg/kg IV; dexmedetomidina 2 µg/kg IV), incrementa tanto el efecto sedante como la eficacia analgésica, convirtiendo a la asociación en una excelente opción para el manejo del dolor agudo. El compromiso hemodinámico en éste último caso es mayor al observado en la asociación con tranquilizantes mayores pero sin llegar a promover alteraciones de significación clínica. La eficacia y seguridad de los derivados opiáceos se extienden al paciente traumatizado. En éstos, se deberá titular la dosis y plantear, en caso de estar indicado, una terapia multimodal. La combinación con AINES y anestésicos locales suele paliar las necesidades más exigentes. Si el paciente presenta un dolor intenso, la morfina (0,25 mg/kg IM, SC, IV cada 4-6 horas), la oximorfona (0,05-0,2 mg/kg IV o IM cada 2-4 horas) o la buprenorfina (0,005-0,02 mg/kg IM cada 6-8 horas) son los compuestos de elección. Si el dolor es moderado, el butorfanol (0,2-0,4 mg/kg IM, IV cada 1-4 horas), la meperidina (0,4-1 mg/kg IM, IV en caninos y 0,2-0,4 mg/kg en felinos, cada 2 horas), la nalbufina (1 mg/kg IM, SC cada 6-8 horas), el dextropropoxifeno (2-4 mg/kg IV, IM cada 46 horas en caninos) o el tramadol, aportan analgesia en un plazo adecuado. La vía de elección se relacionará con la gravedad del caso. Como por vía IM y SC el período de latencia suele ser prolongado, entre 20 y 30 minutos, en casos de dolor muy intenso se sugiere una dosis de carga por vía IV. Se recuerda que tanto la morfina como la meperidina se deberán administrar diluidas y lentamente cuando se utiliza esta última ruta. Por vía epidural, los opiáceos resultaron referidos como provechosos en el control de numerosas afecciones dolorosas. Antes de medicar al paciente siempre se deberá realizar un exhaustivo chequeo clínico. Se recuerda que los efectos colaterales de los hipnoanalgésicos se concentran sobre el aparato cardiovascular y respiratorio. Si bien cuando se utilizan estas drogas la incidencia de depresión respiratoria en los animales domésticos es baja, se deberá monitorizar al paciente sobretodo cuando recibe altas dosis. En los animales traumatizados descompensados, un eventual compromiso hemodinámico puede alterar la farmacocinética de los agentes utilizados potenciando sus efectos adversos. La centralización del volumen minuto se acompaña de una mayor biodisponibilidad central de los agentes analgésicos empleados. Por esta razón, se recomienda no utilizar “recetas” y planear el esquema posológico en función de la respuesta del enfermo. Se deberá descartar el trauma craneano en los pacientes en los que se utilizarán agentes que comprometan la ventilación, como el caso de los opiáceos, ya que un aumento de la PaCO2 promoverá una elevación de la presión intracraneana agravando el cuadro. Cuando estos compuestos se emplean para manejar animales con dolor grave, como el que resulta de un traumatismo, se aconseja administrarlos con lentitud por vía IV. La dosis de carga para la morfina en el canino se logra con dosis sucesivas de 0,1 mg/kg IV (lenta y diluida) cada 3-5 minutos hasta alcanzar la reducción del dolor hasta el nivel deseado. Una vez calculada la dosis de carga, luego se repite la misma cantidad por infusión continua durante las próximas 4 horas. En caninos con manifestaciones de dolor grave el fentanilo se administra a razón de 2 µg/kg a modo de dosis de carga, seguida por una infusión de 1-6 µg/kg/min siempre por vía IV. En felinos la dosis de carga es de 1-2 µg/kg y la tasa de infusión es de 1-4 µg/kg/min (se recuerda que 1 mg es equivalente a 1000 µg). La duración de la analgesia para el fentanilo es, tanto en caninos como en felinos, semejante al tiempo de infusión más 20-30 minutos. Para aplicar este esquema a los análogos del fentanilo se ajusta la dosis en función de la potencia relativa del compuesto elegido, teniendo en cuenta que el sufentanilo es 10 veces más potente, con una duración de 10-15 minutos y el alfentanilo posee sólo el 25% de la potencia del fentanilo y su duración es similar a la del sufentanilo. El remifentanilo se infunde a razón de 0,025 a 0,1 µg/kg/min y su efecto expira al suspender la administración. El alfentanilo, sufentanilo y remifentanilo se utilizan más durante la anestesia que en el manejo del dolor en pacientes conscientes. Además del efecto analgésico estos compuestos permiten reducir la ansiedad del animal, mejorando su manipulación. La combinación con tranquilizantes (neuroleptoanalgesia), siempre y cuando no esté contraindicado, mejora la acción sedante y analgésica contribuyendo a la estabilidad del paciente. Parches de liberación sostenida de fentanilo En época reciente se han incorporado al mercado parches de liberación sostenida que contienen como principio activo al fentanilo. Su aplicación sobre la piel depilada del animal genera niveles plasmáticos adecuados del agente durante un largo período de tiempo, promoviendo un efecto analgésico sostenido, hasta que se agota el compuesto. Las presentaciones para esta forma farmacéutica son: parches que liberan 25, 50, 75 y 100 µg/hora. En caninos, los niveles terapéuticos se logran luego de pasadas las primeras 24 horas de colocado el parche; el período de latencia en los felinos es menor. En pacientes con dolor agudo, se recomienda comenzar con una dosis de carga por vía parenteral continuando hasta lograr la acción del parche. La duración del parche oscila alrededor de 72 horas. Las dosis recomendadas (por kg de peso) son: Caninos: Felinos: 10 kg: parche de 25 µg/hora parche de 25 µg/hora * 10 a 20 kg: parche de 50 µg/hora 20 a 30 kg: parche de 75 µg/hora Más de 30 kg: parche de 100 µg/hora * En pacientes de menos de 10 kg o gatos pequeños, esta presentación puede promover altos niveles sanguíneos y los consecuentes efectos adversos. En estos casos, algunos autores sugieren exponer sólo una porción del parche al contacto de la piel aislando el resto con bandas adhesivas. Es importante que el operador use guantes para evitar el contacto con la superficie del parche durante su colocación. La zona sobre la que se aplicará el parche se depila y se debe evitar erosionar la piel que contactará con el parche ya que puede alterar la absorción del principio activo. Los lugares más utilizados para la colocación son la pared costal y la región cervical dorsal. En felinos también se puede utilizar la región axilar. El parche debe ser desechado atendiendo las normas previstas por la legislación local del país en el que se utilice. Si bien el uso de esta forma farmacéutica puede proporciona una alternativa más en el diseño del protocolo analgésico, se necesita más experiencia para evaluar al máximo sus ventajas. Los efectos colaterales, así como su tratamiento, no difieren de los mencionados anteriormente para los hipnoanalgésicos empleados por otras vías. Los lineamientos generales recomiendan tener siempre un antagonista selectivo como la naloxona cerca del paciente que recibe un agonista puro para poder tratar eventuales complicaciones. Otra alternativa consiste en administrar un agonista-antagonista como la nalbufina a razón de 0,03 mg/kg IV, en bolos cada 10 minutos hasta lograr la reversión deseada. Una dosis total final de 0,1 mg/kg IV suele ser suficiente para recuperar una apropiada ventilación (PaCO2 ≥ 50 mmHg) y conservar efectos analgésicos. La prescripción de hipnoanalgésicos está legislada en la mayoría de los países del mundo. El manejo de estos compuestos exige autorizaciones y controles especiales. Esta situación suele conspirar contra su utilización pero, como hemos repasado en el presente capítulo, su empleo es la mayoría de las veces ineludible y su exclusión de los protocolos analgésicos aumentará significativamente la probabilidad de un fracaso terapéutico. Por esta razón, invitamos a los colegas no habituados a contar con estos compuestos dentro de su arsenal terapéutico a sumarlos tanto en el manejo del paciente traumatizado como quirúrgico. Administración oral de hipnoanalgésicos La administración oral de analgésicos se restringe más al paciente con dolor crónico. No obstante, existe una importante lista de compuestos, como gran parte de los AINES, que sólo admiten esta ruta. Por otro lado, la vía oral permite prescindir de material descartable y de personal entrenado, facilitando el manejo domiciliario del paciente por parte del propietario y reduciendo los costos. Los siguientes integran el grupo de hipnoanalgésicos que admiten la vía oral: Morfina: Comprimidos, 0,3-1 mg/kg PO cada 6-8 horas en caninos. Butorfanol: Comprimidos, 0,2-1 mg/kg PO cada 1-4 horas en caninos y cada 4 horas en felinos. Codeína: Comprimidos, 1-2 mg/kg PO cada 2-8 horas en caninos y 0,1-1 mg/kg cada 4-8 horas en felinos. Clorhidrato de tramadol: uso en caninos y felinos Tramadol en caninos. El tramadol puede administrarse durante la premedicación anestésica con el fin de mejorar la analgesia intraoperatoria de los anestésicos inhalados y proporcionar al paciente una recuperación confortable. Su duración de acción, entre 6 y 8 horas, aporta un efecto analgésico residual durante las primeras horas del período de recuperación. En cirugías de abdomen, traumatológicas y de columna lumbar, el tramadol a razón de 1-2 mg/kg IM o IV en caninos, se presenta como un buen complemento de los anestésicos inhalatorios aunque no modifica de modo significativo la CAM. En rinotomías, cirugías de tórax y de columna, tanto torácica como cervical, la analgesia suele ser insuficiente. La estabilidad cardiovascular a la dosis recomendada la sindica como alternativa segura en pacientes con cardiopatías. La alteración del patrón respiratorio, en animales comprometidos, puede promover cuadros de hipoventilación. En estos casos se recomienda no superar la dosis de 1 mg/kg. El tramadol puede combinarse en la misma jeringa tanto con tranquilizantes como anticolinérgicos. La combinación con tranquilizantes mayores incrementa la acción sedante y justifica una reducción de la dosis. Cuando se lo combina con agonistas α2, como la xilacina o la medetomidina, puede observarse depresión respiratoria. En estos casos, se recomienda utilizar la vía IM, reducir la dosis final de los agonistas α2 y contemplar la necesidad de atropinizar al paciente. En el posquirúrgico de pacientes ambulatorios y hospitalizados, el tramadol a las dosis sugeridas cada 6-8 horas, se presenta como una alternativa eficaz para la mayoría de las cirugías de abdomen, mastectomías, traumatologías y columnas. En estos casos, la vía se ajusta a las necesidades. El tramadol admite las vías oral, SC, IM e IV. Cuando el tratamiento del dolor debe prolongarse durante el posoperatorio el esquema sugerido es el siguiente: 2 mg/kg cada 6 horas durante las primeras 24-48 horas y reducir luego a 1 mg/kg o espaciar el intervalo cada 8 horas, según lo requiera el caso. Como para los demás opioides la combinación del tramadol con AINES produce un efecto analgésico de gran eficacia. Los efectos colaterales son de escasa ocurrencia. Los trastornos digestivos, frecuentes en seres humanos, no se observan en los pequeños animales. En algunos casos puede detectarse somnolencia. Las diferentes formas de presentación: gotas, comprimidos, cápsulas e inyectable, permiten diseñar el protocolo en función de las necesidades de cada caso. Tramadol en felinos El uso del tramadol en felinos merece algunas consideraciones. Combinado con acepromacina puede producir depresión cardiovascular y respiratoria. Por esta razón, la dosis de acepromacina no debe superar los 0,1 mg/kg IM y el tramadol no se debe administrar a una dosis mayor a 1 mg/kg IM. En tratamientos prolongados se propone comenzar cada 6 horas durante las primeras 24-48 horas y espaciar luego el intervalo cada 8 horas, según lo requiera el caso. La administración del tramadol solo, por vía IV y a la dosis indicada, puede emplearse en pacientes deprimidos y descompensados, siendo una objeción los compromisos de origen respiratorio. La recuperación suele ser tranquila, rápida y con manifestaciones de dolor infrecuentes. A diferencia de lo que puede observarse con los demás hipnoanalgésicos en esta especie, no se advirtió excitación aun cuando fue administrado sin el agregado de tranquilizantes mayores. Esto último puede deberse al complejo mecanismo de acción del fármaco. Agonistas α2 presinápticos Los agonistas α2 encuentran una excelente indicación en el manejo del paciente quirúrgico. En combinación con anestésicos disociativos se muestran útiles para realizar intervenciones de corta duración y dolor moderado. La corta duración de su efecto analgésico exigirá suplementar la analgesia durante el posoperatorio. El uso de estos fármacos para el manejo del dolor agudo, tanto en el posoperatorio como en el paciente traumatizado no ha sido extensamente reseñado, aunque se debe tener en cuenta que los potenciales efectos colaterales, como la depresión cardiovascular y la alteración del patrón respiratorio, pueden complicar el cuadro en pacientes críticos o debilitados. El uso de estos compuestos ha logrado gran aceptación como parte del protocolo anestésico de pacientes sanos (ASA I o II). La xilacina a 0,1-1,0 mg/kg y la demetomidina a 0,001-0,01 mg/kg por vías IV, IM o SC, han sido utilizadas en caninos y felinos para aportar analgesia tanto en el posoperatorio como en procesos de dolor agudo durante 0,5-2 horas. La infusión continua es una alternativa para prolongar la duración de acción de estos compuestos. La dexmedetomidina a razón de 1 µg/kg/hora, durante la primera hora del procedimiento continuando con 0,5 µg/kg/hora, es un excelente recurso terapéutico en pacientes con dolor de moderado a grave. Este mismo esquema permite disminuir la CAD del isoflurano y del sevoflurano a valores ligeramente por debajo de la CAM en los pacientes quirúrgicos (datos no publicados). En procedimientos muy traumáticos se administra una dosis de carga de 1 µg/kg IV en no menos de 15 minutos a manera de premedicación, seguido por la tasa de infusión propuesta anteriormente. En los pacientes en los que se administra la dosis de carga, es frecuente observar bradicardias que revierten rápidamente con el agregado de anticolinesterásicos como la atropina o el glicopirrolato. En los animales de escasa talla (menos de 8 kg), más propensos a la bradicardia inducida por el compuesto, se recomienda la atropinización previa (10 minutos antes). La xilacina es el compuesto de menor duración del grupo. Cuando se la utiliza por vía IM en la premedicación anestésica, el tiempo durante el cual ejerce su mayor efecto analgésico se “consume” en el preparado del campo operatorio que, como quedara expresado en el capítulo de Drogas analgésicas, es de tan sólo 15-20 minutos. Para explotar al máximo la acción analgésica de esta droga el autor sugiere administrar la dosis total calculada repartida durante la anestesia mediante una infusión continua. ANESTÉSICOS LOCALES. BLOQUEOS REGIONALES CENTRALES Y PERIFÉRICOS. La predecible eficacia para interrumpir la conducción nerviosa de los anestésicos locales ha sido explotada en todo tipo de tratamiento doloroso. El empleo de los anestésicos locales como parte del protocolo anestésico es una maniobra muy difundida en medicina veterinaria. El escaso impacto sobre la economía corporal que produce la utilización de éstos compuestos, sumado a la posibilidad de combinarlos con anestésicos generales a bajas dosis, hace de ésta opción una alternativa a ponderar en pacientes con diversas patologías preexistentes. Las drogas más utilizadas son la lidocaína, bupivacaína y ropivacaína. La principal diferencia entre estas radica en el período de latencia, la duración, la intensidad del bloqueo nervioso y finalmente en la toxicidad. Existen diferentes modalidades para el uso de estos compuestos. Para los bloqueos regionales periféricos, un acabado conocimiento anatómico del recorrido de los diversos nervios, asegura el éxito de la técnica. Los bloqueos más utilizados incluyen el plexo braquial, las ramas ocular, maxilar y mandibular del nervio trigémino, la infiltración de los nervios intercostales, la infusión interpleural de solución anestésica y la infiltración intraarticular. El plexo braquial se aborda desde la articulación del encuentro. La aguja se inserta paralela al eje de la columna cervical entre la escápula y la pared del tórax. La solución se instila a la altura del borde caudal de la primera costilla. Se utilizan agujas 22-24G de 5 a 7 centímetros de longitud. La dosis para bupivacaína al 0,5% y lidocaína al 2% es de 1ml cada 4,5 kg de peso. Tanto la rama maxilar como la ocular del nervio trigémino se abordan por punción percutánea. Los puntos de referencia son el arco zigomático y el canto lateral del ojo. Para bloquear la rama maxilar, la aguja se inserta perpendicular al eje de la cara y se dirige hacia craneal hasta llegar a la fosa pterigopalatina, donde se deposita la solución anestésica a razón de 2 a 5 ml, dependiendo de la talla del paciente y la concentración utilizada del anestésico local. Para bloquear la rama oftálmica la aguja se inserta como en el caso anterior, por debajo del arco zigomático uno a dos dedos por detrás del canto lateral del ojo. En éste caso la aguja se dirige hacia caudal en dirección al foramen infraorbital. La instilación de grandes volúmenes (2 a 5 ml) se acompaña de una protrución del globo ocular. Esta que remite rápidamente al absorberse el preparado. La punción vascular accidental se acompaña de hemorragias que producen exoftamias de mayor envergadura y duración. Estas últimas en general evolucionan, sin complicaciones. El coagulo suele reabsorberse en aproximadamente 24 horas. La rama mandibular del nervio trigémino, que proporciona inervación sensitiva a los dientes mandibulares, se bloquea interceptando el recorrido del mismo a la altura del foramen mandibular, ubicado cranealmente al ángulo de la mandíbula. Este se palpa fácilmente desde el interior de la boca del paciente, hacia caudal del último molar. El bloqueo puede realizarse desde el interior de la cavidad bucal o en forma percutánea introduciendo la aguja por ventral de la mandíbula hasta hacer coincidir la punta de la misma con el dedo que palpa el foramen. En ese mismo lugar se inyecta la solución anestésica. En general la resistencia a la instilación es mayor que en otros sitios debido a las características de los tejidos en esa zona. El bloqueo de los nervios intercostales se realiza introduciendo la aguja en forma percutanea. La punción se realiza lo más próxima a la unión costo-vertebral, sobre el borde caudal de la costilla. La solución anestésica se instila luego de haber atravesado los músculos intercostales sin ingresar al espacio pleural. Se suele bloque el espacio intercostal afectado más hacia caudal y dos hacia craneal del mismo. Se depositan entre 0,25 y 1 ml de solución por espacio de bupivacaína 0,5% o lidocaína 2%. La inyección intraarticular de anestésico es una maniobra práctica y de fácil ejecución. Los puntos de referencia para el abordaje articular dependerán de la articulación afectada. El volumen de anestésico a instilar se relaciona con la capacidad articular. Se deberá evitar una excesiva distensión de la cápsula articular. El autor utiliza lidocaína al 2% presentada como gel estéril. Este preparado suele aportar, merced a su lenta eliminación, un prolongado efecto analgésico (más de 24 horas). El uso de la anestesia epidural se ha difundido enormemente en los últimos años tanto en pequeños como en grandes animales. La instilación de anestésicos locales y analgésicos con diferentes mecanismos de acción, ha sido utilizada tanto para el tratamiento del dolor intra como postoperatorio. En caninos y felinos la punción se realiza generalmente en el espacio lumbosacro, bajo estrictas condiciones de asepsia. El paciente se coloca en decúbito esternal, con los miembros posteriores recogidos y la cabeza apoyada sobre la camilla, para no influir en la migración cefálica de la solución anestésica. La aguja se introduce entre 1,25 y 4 cm, según el tamaño del animal. Se recomiendan agujas para punción espinal de 2,5 a 7,5 cm, 20 a 22G. Se deberá infundir al menos 20 mL/kg de peso de la solución electrolítica elegida, antes de instilar el anestésico, para expandir el volumen plasmático y contrarrestar eventuales hipotensiones. Con la aguja en la posición correcta la solución es impulsada hacia el espacio epidural sin que se registre resistencia. Se puede hacer una inyección de aire o solución salina para constatar la permanencia de la aguja en el canal. En todos los casos es factible colocar un catéter, para la infusión continua o seriada de las diversos agentes analgésicos utilizados. Para colocar el catéter es indispensable utilizar agujas de punción con bisel curvo (Tuhoy). El catéter se introduce sólo 1-1,5 cm. En animales de gran talla el catéter puede desplazarse hacia craneal para instilar la solución en la proximidad de la metámera deseada. Esta última maniobra se complica en pacientes de menos de 10-15 kg de peso. La extensión del bloqueo metamérico, en la anestesia epidural, depende del volumen instilado y de la concentración del fármaco utilizado y del sitio por el cual se aborda el espacio epidural. Existen diferentes modalidades para calcular la dosis a administrar. En pequeños animales se puede hacer sobre la base del peso corporal o la longitud de la columna vertebral. La dosis promedio es de 1 mL cada 3,5 a 4,5 kg de peso o 0,8 a 1 mL cada 10 cm de longitud occipito-coccígea. La anestesia epidural permite realizar un sinnúmero de intervenciones quirúrgicas. Es principalmente utilizada en cirugías del miembro posterior, perineales y abdominales. El abordaje quirúrgico del abdomen exige bloqueos extensos (hasta T5) ya que tanto las vísceras como el peritoneo parietal son y se comportan como estructuras continuas. Se recomiendo atropinizar a los pacientes que serán sometidos cirugías abdominales. La anestesia epidural está contraindicada en pacientes con cuagulopatías, hipotensos y en aquellos que presentan infección en los tejidos por los que debe transcurrir la aguja. La abundante presencia de numerosos receptores opiáceos en la sustancia gelatinosa del asta dorsal de la médula espinal permite que pequeñas dosis de hipnoanalgésicos, aproximadamente una décima parte de una dosis por vía sistémica, instiladas en el espacio epidural promuevan un prolongado efecto analgésico. Este se expresa a nivel somático y visceral sin interferir con las funciones sensitivas y motoras. Otros compuestos como los agonistas alfa2 y la ketamina son también, utilizados en medicina veterinaria por ésta vía. La droga elegida es diluida en solución fisiológica y el volumen final se ajusta al tamaño del paciente (ver tabla). Tabla: DROGAS ADMINISTRADAS EN EL ESPACIO PERIDURAL EN PEQUEÑOS ANIMALES. DROGA DOSIS (mg/kg) DURACION (horas) 10-24 10-15 4-5 10-13 3-5 1-1.5 s/epinefrina 1.5-2 c/epinefrina 2.5-3.0 Bloqueo hasta D5 5-15 1-1.5 s/epinefrina Lidocaína 2% 1.5-2 c/epinefrina Bloqueo hasta L2 10-20 4-6 Bupivacaina 0.5% 0.25 Bloqueo hasta D2 10-20 4-6 Bupivacaina 0.5% 1.35 b Bloqueo hasta L2 10-20 1-1.5 Ropivacaina 0.2% 1 ml/10 cm 10-20 1-1.5 Ropivacaina 0.2% 1.5 ml/10 cm b Bloqueo hasta D5 10-20 2-4 Ropivacaina 0.5% 0.8 ml/10 cm b Bloqueo hasta L2 b 10-20 2-4 Ropivacaina 0.5% 1.2 ml/10 cm Bloqueo hasta D2 a Las drogas se diluyen en solución fisiológica estéril , bajo estructas condiciones de asépsia. b Mililitros instilados en el espacio epidural, calculados a partir de la longitud occípito-coccigea. Morfina Oximorfona Xilacina Medetomidina Fentanilo Lidocaína 2% 0.1 0.05-0.1 0.02 0.002-0.005 0.001-0.01 1.0 VOLUMEN A INSTILAR LATENCIA a (minutos) (ml/kg) 0.13-0.26 30-60 0.26 20-40 0.26 20-30 0.26 20-30 0.26 15-20 Bloqueo hasta L2 5-15 DOSIS DE ALNALGESICOS EN CANINOS AINES en Caninos. Dosis e intervalo posológico Droga Acetaminofeno (Paracetamol) Acido Acetilsalisílico (Aspirina) Acido Tolfenámico Carprofeno Dipirona Etodolac Fenilbutazona Flunixin Ibuprofeno Ketoprofeno Canino 15 mg/kg Vía PO Intervalo 6 a 8 horas 10 – 25 mg/kg Hasta 4 mg/kg 2 – 4 mg/kg 20 – 30 mg/kg 10 –15 mg/kg 10 – 25 mg/kg 0,5 - 1 mg/kg 5 – 10 mg/kg 1- 2 mg/kg PO SC, PO PO IV, SC, IM PO PO IV, SC, IM PO IV, SC, IM, PO 8 a 12 horas 24 horas 12 a 24 horas 8 horas 24 horas 8 a 12 horas 24 horas 24 a 48 horas 24 horas 0,3 – 0,5 mg/kg 0,1 - 0,2 mg/kg 1 – 2 mg/kg 0,3 mg/kg 10 mg/kg 0,5 mg/kg Ketorolac Meloxicam Naproxeno Piroxicam Tepoxalin Vedaprofeno IV, IM IV, SC, PO PO PO PO PO 8 a 12 horas 24 horas 24 horas 24 horas 24 horas 24 horas Opioides en Caninos. Dosis e intervalo posológico Droga Morfina Canino 0,1 - 1 mg/kg Meperidina (Petidina) Codeína Metadona Oximorfona Fentanilo Sufentanilo Alfentanilo Remifentanilo 3,5 - 10 mg/kg Buprenorfina Butorfanol 1 – 2 mg/kg 0,1-0,25 mg/kg 0,05-0,2 mg/kg 2 - 10 µg/kg 0,75 - 2 µg/kg 15 - 30 µg/kg 0.025 – 0.1 µg/kg/min 5 - 20 µg/kg 0,2 – 0,6 mg/kg Nalbufina Pentazocina Tramadol D-propoxifeno 05 a 1 mg/kg 1 – 4 mg/kg 1 – 2 mg/kg 2 a 5 mg/kg Naloxona Vía Duración SC, IM, PO, 4 a 6 horas (IV) IM 2,5 a 3,5 horas 0,04 – 1 mg/kg PO IM, SC, IV IM, SC, IV IV IV IV IV 6 a 8 horas 4 a 6 horas 2 a 4 horas 20 a 30 minutos 10 a 15 minutos 10 a 15 minutos Infusión continua IM, SC, IV IM, SC, IV, PO IM, SC, IV IM, IV IM, IV, PO IV, IM, (PO) 6 a 12 horas 2 a 4 horas IM, SC, IV 4 a 6 horas 2 a 4 horas 6 a 8 horas 4 a 6 horas 8 a 12 horas Según signos clínicos. DOSIS DE ANALGÉSICOS EN FELINOS AINES en Felinos. Dosis e intervalo posológico Droga Acetaminofeno (Paracetamol) Acido Acetilsalisílico (Aspirina) Felino ------------10– mg/kg Vía ------------- 15 PO Intervalo ------------48 horas Acido Tolfenámico Carprofeno Dipirona Etodolac Fenilbutazona Flunixin Ibuprofeno Ketoprofeno Ketorolac Meloxicam Naproxeno Piroxicam Hasta 4 mg/kg 4 mg/kg 20 – 30 mg/kg ------------10 – 25 mg/kg 0,5 1 mg/kg ------------1- 2 mg/kg 0,25 mg/kg 0,1-0,2 mg/kg ------------------------- SC, PO 24 horas PO IV, SC, IM 24 horas 8 horas ------------PO ------------8 a 12 horas IV, SC, IM Toma única ------------------------IV, SC, IM, 24 horas PO IM 12 horas IV, SC, PO 24 horas ------------------------- ------------------------- Opioides en Felinos. Dosis e intervalo posológico Droga Morfina Meperidina (Petidina) Codeína Metadona Oximorfona Fentanilo Sufentanilo Buprenorfina Butorfanol Nalbufina Pentazocina Tramadol D-propoxifeno Naloxona Felino 0,1 – 0,2 mg/kg 3,5 - 10 mg/kg Vía SC, IM IM Duración 6 a 8 horas 2 a 3 horas 1 – 2 mg/kg 0,1-0,2 mg/kg 0,01-0,1 mg/kg 1 – 5 µg/kg 0,1 – 0,5 µg/kg 5 - 20 µg/kg 0,2 – 0,8 mg/kg 05 a 3 mg/kg 1 – 4 mg/kg 1 – 2 mg/kg 2 mg/kg 0,04 – 1 mg/kg PO SC, IV IM, SC, IV IV IV IM, SC, IV IM, SC, IV IM, SC, IV IM, IV IM, IV, PO IV, IM, PO IM, SC, IV 6 a 8 horas 2 a 3 horas 2 a 4 horas 20 a 30 minutos 10 a 15 minutos 3 a 8 horas 2 a 4 horas 2 a 4 horas 4 a 6 horas 6 a 8 horas 4 a 6 horas Según signos clínicos.