Resolución espacial de un sistema para dosimetría por fibra óptica
Anuncio

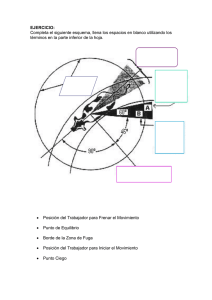
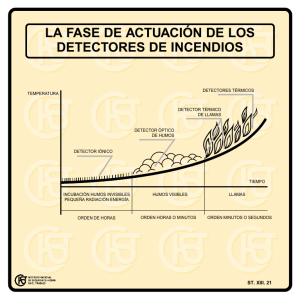
1 Resolución espacial de un sistema para dosimetría por fibra óptica basado en ZnSe(Te) Marcela Ramírez, Martín Santiago y Julián Marcazzó Instituto de Física Arroyo Seco-UNICEN, msantiag@exa.unicen.edu.ar, 0249-4439660, Pinto 399, Tandil 7000, Argentina Adrián Faigón, José Lipovetsky y Mariano García Inza Facultad de Ingeniería-UBA, afaigon@fi.uba., Av. Paseo Colón 850, Buenos Aires 1063, Argentina Resumen—La dosimetría por fibra óptica se basa en el uso de un centellador de pequeñas dimensiones (1 mm3 aprox.) adherido al extremo de una fibra óptica. La intensidad de la luz emitida por el centellador mientras es irradiado, o radioluminiscencia, se mide en el otro extremo de la fibra y se utiliza para determinar la tasa de dosis absorbida por el centellador. La robustez del sistema, el escaso tamaño del detector y la posibilidad de realizar mediciones en tiempo real convierten a esta técnica en una alternativa interesante para su aplicación a nivel clínico en dosimetría de radioterapia. En este trabajo se presentan resultados preliminares acerca de la resolución espacial de un sistema de dosimetría por fibra óptica que utiliza un cristal comercial de ZnSe(Te) como centellador. Se comparó la respuesta del sistema con respecto a la de una cámara de ionización tipo PinPoint al ser irradiada en una cámara de cobalto en distintas condiciones geométricas, haciendo hincapié en su capacidad para resolver altos gradientes de dosis (borde de campo, borde de objeto dentro del campo, etc.). De manera general, el sistema dosimétrico por fibra óptica demostró una mayor resolución espacial que la cámara de ionización. Palabras clave— radioterapia, dosimetría in-vivo, radioluminiscencia I. INTRODUCCIÓN L AS técnicas de teleterapia más recientes, tales como la radioterapia 3D conformada, la radioterapia de intensidad modulada, la radiocirugía y la radioterapia estereotáxica, dan lugar muchas veces a tratamientos que se caracterizan por la deposición de altas dosis de radiación en campos pequeños y, por lo tanto, a la presencia de altos gradientes de dosis [1]. En el caso de la radiocirugía esterotáxica, por ejemplo, la dosis se entrega en una única aplicación, lo cual vuelve crítica la exactitud del tratamiento y la necesidad de un preciso control dosimétrico [2]. De manera general, se reconoce la necesidad de realizar dosimetría in-vivo y en tiempo real para evitar accidentes, sub- o sobredosificación de la región de interés, como así también para identificar errores que impliquen sobreirradiación de tejido sano circundante [3][4][5][6]. La posibilidad de contar con sistemas dosimétricos que permitan realizar dosimetría en tiempo real con alta resolución espacial (<1 mm3) para mediciones in-vivo brindaría atractivas posibilidades [7]. De hecho, recientemente se ha sugerido la posibilidad de utilizar este tipo de sistemas dosimétricos como feedback para modificar on-line los parámetros del tratamiento radiante (dose- guided radiation therapy), en una manera similar a la utilizada en la radioterapia guiada por imágenes (image guided radiation therapy, IGRT) [8]. La dosimetría por fibra óptica (DFO) ha emergido como una tecnología posible para dosimetría in vivo en tiempo real con alta resolución espacial a partir de trabajos iniciales de S. Beddar [9][10]. Desde entonces ha dado lugar a una permanente y creciente investigación por parte de varios laboratorios en diversos países. La DFO consiste en el uso de un centellador de muy pequeño tamaño (<1 mm3) adherido al extremo de una fibra óptica (FO). Durante la irradiación, la emisión del centellador es transportada por la FO hasta su otro extremo, donde un detector de luz adecuado mide su intensidad. A partir de esta última es posible determinar la tasa de dosis absorbida por el centellador en tiempo real, a partir de una adecuada calibración [10]. De manera general, la DFO provee alta resolución espacial, no requiere conexiones eléctricas en la proximidad del paciente, es reusable, mecánicamente robusta y de bajo costo. Los materiales más investigados hasta la fecha como centelladores para DFO han sido los centelladores plásticos y el óxido de aluminio dopado con carbono o alúmina (Al2O3:C). Los centelladores plásticos se utilizan como detectores de radiación para detección y conteo de partículas en física nuclear. La alúmina fue desarrollada inicialmente como un eficiente dosímetro termoluminiscente. Ambos materiales poseen la ventaja de estar disponibles comercialmente (Saint Gobain Crystals y Landauer Inc., respectivamente). Los centelladores plásticos poseen la ventaja de ser tejido equivalentes, es decir, de absorber radiación de manera similar al tejido blando o agua [11]. Sin embargo, no son muy eficientes y pueden presentar degradación de sus propiedades a altas dosis [12][13]. En el mercado existen centelladores que emiten en diversas regiones del espectro visible. Todos ellos presentan un tiempo de decaimiento del orden de las decenas de nanosegundos [14]. La información acerca del tiempo de decaimiento de la señal RL de un centellador es relevante al considerar la posibilidad de aplicarlo para dosimetría DFO en el caso particular de que la fuente de radiación es un LINAC. La alúmina (Al2O3:C) se presenta en forma de polvo, pellets o cilindros monocristalinos (Landauer Inc.) fabricados en atmósfera reductora. Es un material costoso 2 que presenta una importante eficiencia comparado con otros estudiados en el marco de DFO. Por tal motivo, se ha convertido en un punto de referencia en estudios de nuevos materiales. Su tejido-equivalencia es moderada y parece comprometer la validez de una determinación dosimétrica sólo en el caso de haces de fotones con energías menores a 100 KeV. El tiempo de decaimiento característico de la señal de la Al2O3:C es de 35 ms. Sin embargo, presenta componentes de mayor tiempo de decaimiento que comprometen el uso de este material en ciertas situaciones. De todas maneras, ha sido posible encontrar caminos alternativos para compensar este problema, basados en la corrección de los datos experimentales (RL en función del tiempo) a partir de modelos teóricos del proceso de centelleo [16]. En menor proporción, se han investigado otros materiales desde el punto de vista de su aplicación en DFO. Entre ellos podemos mencionar: Li2B4O7:Mn, LiF:W, Mg2SiO4:Tb, Al2O3:Cr2O3, SiO2:Ce , SiO2:Cu , KBr:Eu , SrS:Ce,Sm, (Zn,Cd)S:Ag, Gd2O2S:Tb, GaNi, etc. [15][17]. La mayor parte de ellos han dado lugar a implementaciones exitosas de la técnica de DFO en mediciones de laboratorio o en fantomas. Sin embargo, no se han reportado avances posteriores en clínica o caracterizaciones más detalladas o, menos aún, realizaciones comerciales. El principal problema radica en que dichos materiales no han sido fabricados expresamente para ser aplicados en la técnica y, por lo tanto, no es posible proceder a su optimización luego de las investigaciones iniciales de factibilidad. El principal inconveniente encontrado al implementar la técnica de DFO es la luz generada por la radiación en la propia FO. Esta luz espuria, o efecto stem, se suma a la luz de centelleo del detector y genera un error sistemático que perturba el resultado de la medición. La intensidad del efecto stem depende de la longitud de FO efectivamente irradiada por la radiación primaria o secundaria, como así también de la orientación relativa entre el haz y la FO. Estos parámetros de la medición no son gobernables en la rutina clínica. Por este motivo el efecto stem debe ser eliminado o reducido a valores clínicamente aceptables. La principal contribución del efecto stem es la radiación Cherenkov generada en la FO por los electrones que penetran en ella con velocidades superiores a la velocidad de la luz en la FO. La intensidad de la radiación Cherenkov es proporcional a la inversa del cubo de la longitud de onda. Por dicho motivo, es más intensa en la región azul del espectro. Los métodos propuestos para remover el efecto Cherenkov son varios: a) Uso de otra FO sin detector en su extremo: su lectura se usa como estimación del efecto stem en la FO principal. b) Uso de detectores que emitan en rojo: mediante el uso de filtros pasa alto se remueve la contribución azul del efecto stem. c) Método cromático: se utiliza un detector que emite en verde y se mide la intensidad de luz saliente de la FO en dos canales (azul y verde). Mediante una adecuada calibración se recobra el valor de dosis sin la contribución del efecto stem. d) Método pulsado: esta técnica es válida para ser usada sólo en LINAC y con detectores cuyo centelleo tenga un tiempo de decaimiento del orden de 1 ms. Aprovecha el carácter pulsado de la radiación en dicho tipo de equipo (pulsos de 10 µs cada 10 ms) y la corta duración de la emisión Cherenkov (del orden de los ns). Mediante una adecuada sincronización, se mide la emisión RL durante el tiempo intermedio entre pulsos de radiación [18]. Si bien la DFO aún se encuentra en etapa experimental, se han reportado varias aplicaciones clínicas promisorias [19]-[22], desarrollos de DFO para mediciones intracavitarias [23] y dosimetría 2D [2], entre otras. En este trabajo se estudia de manera preliminar la resolución espacial de un sistema de DFO basado en el centellador comercial ZnSe(Te). La respuesta de sistema se compara con la de una cámara de ionización de alta resolución espacial (PinPoint). En particular, se estudia la respuesta de ambos tipos de detectores al resolver la penumbra del borde de campo de irradiación y del borde de un objeto opaco en una bomba de cobalto. II. EXPERIMENTAL La punta dosimétrica se fabricó utlizando un cilindro de ZnSe(Te) de 1 mm (diám.) × 2 mm (largo) provisto por Moltech GMBH [24], siendo entonces el volumen total del detector igual a 1.6 mm3. Este centellador emite en la región del rojo (640 nm) y posee un número atómico efectivo Zeff = 33. El centellador se adhirió al extremo de una FO plástica SuperEska (Mitsubishi) de 1 mm de diámetro y 10 m de longitud recubierta por una camisa de PVC negro mediante una capa de adhesivo Norland 65. El curado de la capa de adhesivo se completó exponiendo la juntura a la emisión de un LED UV Nichia de alta potencia (NCSU033A, emisión en 365 nm) durante 40 minutos. El centellador se recubrió con dos capas de pintura vinílica opaca para protección mecánica y aislación de la luz ambiente. Denominaremos extremo sensible al extremo que contiene al centellador. El otro extremo de la FO se terminó mediante un conector tipo SMA para su conexión al sistema de detección de luz. La intensidad de la luz de centelleo emitida por el detector de ZnSe(Te) se midió mediante un cabezal de conteo de fotones Hamamatsu H9319. La contribución del efecto stem se suprimió interponiendo entre la FO y el cabezal de conteo de fotones un filtro óptico pasa-alto de vidrio coloreado Schott RG610 con longitud de onda de corte a 610 nm. La respuesta del sistema DFO se comparó con la de una cámara de ionización PTW tipo PinPoint (modelo N31014, 15 mm3) polarizada con una tensión de 400 V. La corriente generada en la cámara por la radiación se midió mediante un electrómetro PTW UNIDOS E. Los experimentos se realizaron en una bomba de cobalto Theratron 60 (Htal. Prov. de Oncología L. Fortabat, Olavarría), utilizando un campo de tamaño 10 × 10 cm2 a una distancia fuente detector de 60 cm. Se utilizaron dos disposiciones experimentales. En la primera (Fig. 1-a) el extremo sensible del sistema FOD se trasladó a lo largo de un eje transversal al haz de radiación, de manera que atravesara el borde del campo. En cada posición a lo largo del recorrido del detector se midió la intensidad del centelleo. El eje de la FO se mantuvo perpendicular a la dirección de movimiento y paralelo al plano de campo. En la segunda disposición experimental (Fig. 1-b) se dispuso una planchuela de acero de 10 mm de espesor a 33 mm por encima del plano del campo, la cual actuó como un obstáculo opaco a la radiación. El borde de la planchuela se situó en el centro del campo. De manera 3 Plano del campo Extremo del detector (a) Obstáculo (b) Plano del campo Extremo del detector Fig. 1: Esquema de las disposiciones experimentales utilizadas. Utilizando las mismas disposiciones experimentales descritas se repitió el conjunto de mediciones utilizando la cámara de ionización PinPoint en lugar del sistema FOD. Con el fin de maximizar la resolución espacial de este detector no se utilizó la caperuza acrílica provista por el fabricante, es decir, se utilizó la cámara desnuda. En la Fig. 1 se muestra a modo ilustrativo una curva de medición típica del sistema FOD. En este caso se grafica la intensidad de centelleo en función del tiempo cuando el extremo sensible del sistema FOD se encuentra en el centro del campo de irradiación. La curva se caracteriza por un rápido crecimiento de la señal (a partir de t = 9 s), seguido por una etapa de estabilización (hasta t = 22 s) y una respuesta contante hasta la finalización de la irradiación (t = 68 s). 3 Intensidad [10 cps] 700 600 500 400 300 200 100 0 20 40 60 1,8 1,6 1,4 1,2 1,0 0,8 0,6 0,4 FOD PinPoint 0,2 0,0 -2 III. RESULTADOS Y DISCUSIÓN 0 (sistema FOD y cámara de ionización PinPoint) en función de la posición. La posición igual a cero se fijó situando visualmente el centro de cada detector en el borde del campo de irradiación determinado por el sistema de iluminación de la bomba de cobalto. Los valores mostrados en la figura han sido normalizados al valor obtenido en esta posición. Los valores negativos de la posición corresponden a puntos situados fuera del campo de irradiación. Puede observarse que los dos sistemas no presentan diferencias de resolución espacial al resolver la penumbra del borde del campo. Esto se debe probablemente a que el ancho efectivo de la penumbra de borde de campo observada en este caso se corresponde con el esperado en equipos de estas características [25][26]. Las diferencias observadas entre la respuesta normalizada del sistema FOD y la cámara PinPoint en los puntos extremos del recorrido son asignables a la diferente respuesta de cada detector en función de la energía de las partículas ionizantes [27]. Respuesta normaizada [1] similar a la de la disposición anterior, se desplazó el extremo del detector de manera que atravesara la penumbra del borde del obstáculo. Las mediciones se realizaron en aire y a temperatura ambiente. 80 Tiempo [s] Fig. 2: Curva de respuesta típica del sistema FOD. La exposición comienza en el instante t = 9 s. Luego de una rápida estabilización, la respuesta alcanza un punto estable a partir de los 22 s. En la Fig. 3 se muestran los resultados de las mediciones en la disposición experimental correspondientes a la Fig. 1a (borde de campo). Se grafica la respuesta de cada detector -1 0 1 2 Posición [cm] Fig. 3: Respuesta del sistema FOD y de la cámara de ionización PinPoint al atravesar el borde de penumbra del campo de irradiación. La respuesta de cada detector ha sido normalizada con respecto a su valor en el borde nominal del campo. Los valores negativos de la posición corresponden a puntos situados fuera del campo de irradiación. En la Fig. 4 se muestra la respuesta normalizada de ambos detectores al atravesar transversalmente el borde de penumbra generado por un obstáculo opaco a la radiación. El valor de la posición igual a cero se fijó posicionando visualmente el centro de cada detector debajo del borde del objeto opaco. La respuesta de cada detector ha sido normalizada con respecto a su valor en dicha posición. Los valores negativos de la posición corresponden a puntos ubicados debajo del objeto. En este caso es posible observar alguna diferencia en la capacidad de cada tipo de detector para resolver el borde de penumbra creado por el objeto opaco. Si definimos la resolución como la distancia entre el valor máximo y mínimo de la curva de respuesta de cada tipo de detector arribamos a la conclusión de que la resolución del sistema FOD es de 3 mm, mientras que la resolución de la cámara de ionización PinPoint es mayor a 4 mm. De manera similar a la disposición experimental previa, las diferencias observadas entre la respuesta normalizada del sistema FOD y la cámara PinPoint en los puntos extremos del recorrido son asignables a la diferente respuesta de cada detector en función de la energía de las partículas ionizantes [27]. 4 Respuesta normaizada [1] 1,15 [4] 1,10 [5] 1,05 1,00 [6] 0,95 0,90 FOD PinPoint 0,85 [7] 0,80 -1,0 -0,5 0,0 0,5 1,0 Posición [cm] Fig. 4: Respuesta del sistema FOD y de la cámara de ionización PinPoint al atravesar el borde de penumbra producido por un obstáculo opaco. La respuesta de cada detector ha sido normalizada con respecto a su valor en la posición nominal del borde del objeto. Los valores negativos de la posición corresponden a puntos ubicados debajo del objeto. Puede decirse que el sistema FOD presenta una resolución espacial mayor a la de la cámara de ionización PinPoint al resolver un borde de penumbra agudo creado por un obstáculo opaco a la radiación. Esta evidencia es alentadora para continuar con investigaciones más profundas en situaciones de interés clínico en las que la resolución espacial sea un parámetro crítico de la determinación dosimétrica. IV. CONCLUSIONES En este trabajo se analizó de manera preliminar la respuesta de un sistema FOD basado en el centellador ZnSe(Te) al resolver el borde de campo y la penumbra creada por el borde de un objeto opaco a la radiación en una bomba de cobalto. Dicha respuesta se comparó con la de una cámara de ionización PinPoint (PTW). Se encontró que la resolución de ambos sistemas es similar al resolver la penumbra del borde de campo. Sin embargo, el sistema FOD presenta una resolución espacial mayor que la de la cámara PinPoint al resolver el borde de penumbra agudo creado por el objeto opaco. Este resultado promueve el interés por llevar adelante investigaciones en las que la alta resolución espacial resulte crítica desde el punto de vista dosimétrico. [8] [9] [10] [11] [12] [13] [14] [15] [16] [17] [18] AGRADECIMIENTOS Este trabajo ha sido financiado con fondos del proyecto PICT Red 1907 (ANPCyT). Los autores agradecen al Dr. G. Zanelli, Dra. L. Bianchi y Srta. C. Pérez (Htal. Prov. de Oncología L. Fortabat, Olavarría) por su asistencia durante las mediciones en bomba de cobalto. REFERENCIAS [1] [2] [3] ] M. Taylor, T. Kron, R.D. Franich, A contemporary review of stereotactic radiotherapy: Inherent dosimetric complexities and the potential for detriment, Acta Oncologica 50 (2011) 483-508. J. Gagnon, D. Theriault, M. Guillot, L. Archambault, S. Beddar, L. Gingras, L. Beaulieu, Dosimetric performance and array assessment of plastic scintillation detectors for stereotactic radiosurgery quality assurance, Med. Phys. 39 (2012) 429. A. Noel, P. Aletti, P. Bey, L. Malissard, Detection of errors in individual patients in radiotherapy by systematic in vivo dosimetry, Radiotherapy and Oncology 34 (1995) 144-151. [19] [20] [21] [22] [23] M. Essers, B. Mijnheer, In Vivo Dosimetry During External Photon Beam Radiotherapy, Int. J. Radiation Oncology Biol. Phys. 43 (1999) 245-259. A. Ismail, J.-Y. Giraud, G.N. Lu, R. Sihanath, P. Pittet, J.M. Galvan, J. Balosso, Radiotherapy quality insurance by individualized in vivo dosimetry: State of the art (Review), Cancer/Radiothérapie 13 (2009) 182-189. Z. Qi, X. Deng, S. Huang, A. Shiu, M. Lerch, P. Metcalfe, A. Rosenfeld, T. Kron, Real-Time In Vivo Dosimetry With MOSFET Detectors in Serial Tomotherapy for Head and Neck Cancer Patients, International Journal of Radiation Oncology 80 (2011) 1581-1588. M.L.F. Lerch, M. Petasecca, A. Cullen, A. Hamad, H. Requardt, E. Bräuer-Krisch, A. Bravin, V.L. Perevertaylo, A.B. Rosenfeld, Dosimetry of intensive synchrotron microbeams, Radiation Measurements 46 (2011) 1560-1565. C.W. Scarantino, B. Prestidge, M. Anscher, C. Ferree, W. Kearns, R. Black, N. Bolick, G. Beyer, The observed variance between predicted and measured radiation dose in breast and prostate patients utilizing an in vivo dosimeter, International Journal of Radiation Oncology 72 (2008) 597-604. A.S. Beddar, Water-equivalent plastic scintillation detectors for high-energy photon and electron beams, PhD Thesis Department of Medical Physics, University of Wisconsin (Madison. WI: Medical Physics Publishing Corporation) 1990. A.S. Beddar, T.R. Mackie, F.H. Attix, Water-equivalent plastic scintillation detectors for high-energy dosimetry: I. Physical characteristics and theoretical considerations, Phys. Med. Biol. 37 (1992) 1883-900. A.S. Beddar, Plastic scintillation dosimetry and its application to radiotherapy, Radiation Measurements 41(2007) S124-S133. W. Busjan, K. Wick, T. Zoufal, On the behaviour of plastic scintillators during an experiment in a high dose rate environment, Nuclear Instruments and Methods in Physics Research B 151 (1999) 434-437. A. Beierholm, C. Andersen, L. Lindvold, F. Kjær-Kristoffersen, J. Medin, A comparison of BCF-12 organic scintillators and Al2O3:C crystals for real-time medical dosimetry, Radiation Measurements 43 (2008) 898-903. A.M. Frelin, J.M. Fontbonne, G. Ban, J. Colin, M. Labalme, Comparative Study of Plastic Scintillators for Dosimetric Applications, IEEE Transactions On Nuclear Science 55 (2008) 2749. C.E. Andersen, Fibercoupled Luminescence Dosimetry in Therapeutic and Diagnostic Radiology, AIP Conf. Proc. 1345, 100 (2011). C.E. Andersen, S.M.S. Damkjær, G. Kertzscher, S. Greilich, M.C. Aznar, Fiber-coupled radioluminescence dosimetry with saturated Al2O3:C crystals: Characterization in 6 and 18 MV photon beams, Radiation Measurements 46 (2011) 1090-1098. A. Ismail, P. Pittet, G.N. Lu, J.M. Galvan, J.Y. Giraud, J. Balosso, In vivo dosimetric system based on Gallium Nitride radioluminescence, Radiation Measurements 46 (2011) 1960-1962. P.Z.Y. Liu, N. Suchowerska, J. Lambert, P. Abolfathi, D.R. McKenzie, Plastic scintillation dosimetry: comparison of three solutions for the Cerenkov challenge, Phys. Med. Biol. 56 (2011) 5805-5821. M.C. Aznar, B. Hemdal, J. Medin, C.J. Marckmann, C.E. Andersen, L. Bøtter-Jensen, I. Andersson, S. Mattsson, In vivo absorbed dose measurements in mammography using a new real-time luminescence technique, British Journal of Radiology 78 (2005) 328-334. C.E. Andersen, S. Nielsen, K. Tanderup, J. Lindegaard, Timeresolved in vivo luminescence dosimetry for online error detection in pulsed dose-rate brachytherapy, Med. Phys. 36 (2009) 5033. N. Suchowerska, M. Jackson, J. Lambert, Y. Yin, G. Hruby, D.R. McKenzie, Clinical Trials of a Urethral Dose Measurement System in Brachytherapy Using Scintillation Detectors, International Journal of Radiation Oncology 79 (2011) 609-615. P. Gueye, C. Velasco, C. Keppel, B. Murphy, C. Sinesi, SU-FF-T390: In-Vivo Prostate Brachytherapy Absorbed Dose Measurements, Med. Phys. 36 (2009) 2611. E. Spasic, S. Magne, I. Aubineau-Laniece, L. de Carlan, C. Malet, C. Ginestet, P. Ferdinand, Intracavitary in vivo dosimetry based on multichannel fiber-coupled Radioluminescence and Optically Stimulated Luminescence of Al2O3:C, Advancements in Nuclear Instrumentation Measurement Methods and their Applications (ANIMMA) Proceedings (2011) 1-6. 5 [24] http://www.mt-berlin.com/ [25] G.H. Zeman, M.A. Dooley, Performance and dosimetry of Theratron 80 Cobalt 60 Unit at Armed Forces Radiobiology Research Institute, AFRRI Technical Report, 1984. [26] A.P. Warrington, E.J. Adams. Proceedings of IEE on Appropriate Medical Technology for Developing Countries. Cobalt-60 Teletherapy for Cancer - A Revived Treatment Modality for the 21st Century. London (2002) pp 21.1–21.19. [27] P. Molina, M. Prokic, J. Marcazzó, M. Santiago, Characterization of a fiberoptic radiotherapy dosimetry probe based on Mg2SiO4:Tb, Radiation Measurements 45 (2010) 78-82.