Descargar pdf - Foro Nuclear
Anuncio

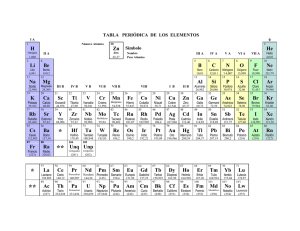
- s 1 TABLA PERIODICA DE LOS ELEMENTOS 1 1 1,008 H Hidrógeno 2 1s1 Li 6,94 Litio 4 Be Berilio [He]2s2 22,990 12 [Ne]3s2 39,098 K Potasio 20 Rb Rubidio 38 Cs Cesio Bario Fr Francio 1939 ––/–– 27 [Rn]7s1 88 Ra Radio [Rn]7s2 2 0,9 1737 23 Gas Sintético Líquido 6 50,942 V 24 7 51,996 Cr Vanadio 40 Cromo [Ar]3d34s2 91,224 Zr Circonio [Kr]4d15s2 t 41 25 8 54,938 Mn 26 9 55,845 Fe Manganeso Niobio [Kr]4d25s2 174,97 Lu Lutecio 72 ª Lr Lawrencio 1961 ––/–– 1627 27 10 58,933 Co Hierro 13 5 B 14 10,81 Boro 1808 85/82 2076 6 12,011 C Carbono 3 ––a 2,04 70/77 3927 3500 [He]2s22p1 13 He 14 28 11 58,693 Ni Cobalto 29 Cu Níquel 30 73 43 Tc Molibdeno Ta Tántalo [Xe]4f145d26s2 [Xe]4f145d36s2 74 44 W 75 76 Rh 46 [Ar]3d104s1 106,42 Pd Rodio 47 48 Galio 77 [Kr]4d10 192,22 Ir 78 Cadmio [Kr]4d105s1 195,08 Pt Osmio Iridio Platino [Xe]4f145d66s2 [Xe]4f145d76s2 [Xe]4f145d96s1 79 Au 80 Rutherfordio Db Dubnio 4 1967 –– ––/–– –– –– [Rn]5f146d27s2? [Xe]4f145d46s2 (268,13) f t Sg Seaborgio ¿? 1974 –– ––/–– –– –– [Rn]5f146d37s2 57 Bh 138,91 La Bohrio Lantano 58 140,12 Ce Cerio 2 [Xe]5d 6s (227,03) Ac Actinio 1899 195/–– 1050 1 [Rn]6d 7s 1 Th 2 Hassio [Rn]5f146d67s2 59 140,91 Pr 2 [Rn]6d 7s 3 2 60 144,24 Pa Neodimio 92 4 2 [Rn]5f146d107s1 [Rn]5f146d107s2 61 (144,91) Prometio 62 150,36 U 2 3 Samario 3 1879 –– 185/–– 3000 1072 5 2 [Xe]4f 6s 238,03 Uranio 3, 4, 5 1789 1,5 175/–– –– 1132,2 [Rn]5f 6d 7s [Rn]5f146d97s1 ¿? 1996 –– ––/–– –– –– 93 6 2 Np Neptunio 94 (244,06) 151,96 Europio 7 2 (243,06) 2 [Rn]5f 6d 7s 4 1 2 [Rn]5f 6d 7s Tl Americio 6 [Rn]5f 7s 2 7 2 [Rn]5f 7s [Ar]3d104s24p2 50 Sn [Kr]4d105s25p2 82 207,2 Pb Nh Nihonio 64 157,25 Gd Gadolinio 7 Flúor [He]2s22p4 30,974 P 16 1s2 20,180 Ne Neón S [He]2s22p5 32,06 17 Azufre [Ne]3s23p3 33 As Arsénico 34 Cl 18 39,948 Ar Argón [Ne]3s23p5 78,96 Se Selenio 35 [Ar]3d104s24p3 51 121,76 Sb 127,60 Br 36 83,798 Kr Kriptón Te Antimonio [Ar]3d104s24p5 53 126,90 I Telurio [Kr]4d105s25p3 83 208,98 Yodo Bi Bismuto [Kr]4d105s25p4 84 (209,98) Po Polonio (209,99) At Astato 4 [Ar]3d104s24p6 54 131,29 Xe Xenón [Kr]4d105s25p5 85 3 [Ne]3s23p6 79,904 Bromo [Ar]3d104s24p4 52 2 [He]2s22p6 35,45 Cloro [Ne]3s23p4 74,922 2 [Xe]4f 5d 6s 96 (247,07) Curio 7 1 5 [Kr]4d105s25p6 86 (222,02) Rn Radón 2, 4, 6 1940 –1, 1, 3, 5, 7 1900 2 2,0 ––/–– 2,2 ––/145 –– 962 302 –– –71–61,7 68 158,93 Terbio 9 2 [Rn]5f 7s 2 98 10 2 (251,08) Cf Californio 3, 4 1950 1,3 ––/–– –– 900 10 67 Holmio 6 [Rn]5f 7s 11 Es Einstenio 11 2 [Rn]5f 7s 12 69 (294) Og Oganessón –– 2002 –– ––/–– –– –– 168,93 Tm Tulio 3 1879 1,24 175/–– 2868 1545 [Xe]4f 6s (252,08) Ts Tennesso ¿? 2010 –– ––/–– –– –– 167,26 Er Erbio 2 (294) *118 ¿? –– –– 7 [Rn]5f146d107s27p4 [Rn]5f146d107s27p5 [Rn]5f146d107s27p6 3 1842 1,23 175/–– 2720 1529 [Xe]4f 6s 99 2, 3, 4 1952 1,3 ––/–– –– 860 2 164,93 Ho 2, 3 1878 1,22 175/–– 2567 1461 [Xe]4f 6s (247,07) 9 162,50 Dy Disprosio [Xe]4f 6s 97 66 1, 3, 4 1886 –– 175/–– 3230 1407 Berkelio [Rn]5f 6d 7s Lv 65 Tb (293) *117 Livermorio 2000 ––/–– –– 3, 4 1949 1,3 ––/–– 3110 986 2 Mc Moscovio ¿? 2004 ¿? –– ––/–– –– –– –– –– [Rn]5f146d107s27p1 [Rn]5f146d107s27p2 [Rn]5f146d107s27p3 1, 2, 3 1843 1,20 175/–– 3250 1356 1 Fl Flerovio ¿? 1999 –– ––/–– –– –– ISBN: 978-84-7360-576-2 Tabla periodica2016_FORO_4_B.indd 1 118,71 Plomo 2004 ––/–– –– 3, 4, 5, 6 1940 3, 4, 5, 6, 7 1940 3, 4, 5, 6, 7 1944 2, 3, 4, 5, 6 1944 1,38 175/–– 1,36 175/–– 1,28 175/–– 1,3 ––/–– 3927 637 4000 639,4 3230 1176 2607 1340 1 204,38 Pu Am Cm Bk Plutonio [He]2s22p3 15 113 (284,18) 114 (289,19) *115 (288,19) 116 2, 3 1880 –– 180/–– 1527 1312 [Xe]4f 6s 95 F 10 1 [Xe]4f145d106s26p1 [Xe]4f145d106s26p2 [Xe]4f145d106s26p3 [Xe]4f145d106s26p4 [Xe]4f145d106s26p5 [Xe]4f145d106s26p6 * ¿? –– –– Eu 2, 3 1901 1,17 185/–– 1803 826 [Xe]4f 6s (237,05) 63 Ge Talio Cn Copernicio 2, 3 1945 1,14 185/–– 3100 1100 Protactinio 2 Rg Roentgenio ¿? 1994 –– ––/–– –– –– 18,998 Oxígeno 1861 1, 3 ––a 2, 4 1753 3, 5 1898 190/1481,62 180/1472,33 160/1462,02 190/–– 304 1473 327,46 1749 271,3 1564 254 112 (285,17) Darmstadtio 72,63 Estaño [Kr]4d105s25p1 [Xe]4f145d106s2 (280,16) Nd Pm Sm [Xe]4f 6s 231,04 1 Ds 111 114,82 In 81 200,59 Mercurio [Xe]4f145d106s1 (281,16) ¿? 1994 –– ––/–– –– –– [Rn]5f146d77s2 2, 3, 4 1885 1,13 185/–– 3290 1024 [Xe]4f 6s 91 2, 3, 4 1913 1,3 180/–– 4820 1568 2 Mt Meitnerio ¿? 1982 –– ––/–– –– –– Praseodimio 232,04 Torio Hs 2, 3, 4 1885 1,12 185/–– 3360 935 [Xe]4f 5d 6s 90 3 1828 1,1 180/–– 3300 1842 2 1 108 (277,15) 109 (276,15) 110 ¿? 1984 –– ––/–– –– –– [Rn]5f146d57s2 1839 2, 3 1803 195/1691,10 185/–– 920 3470 795 89 (270) 1976 –– ––/–– –– –– [Rn]5f146d47s2 1 ª [Xe]4f145d56s2 106 (271,13) 107 32 Indio Hg Oro O 9 1863 3 ––a 2, 4 ––a –3, 3, 5 1782 –2, 2, 4, 6 1811 –1, 1, 3, 5, 7 1898 2, 4, 6, 8 155/1441,78 145/1411,96 145/1382,05 140/135 2,1 140/1332,66 ––/130 2,6 156,6 2072 231,93 2602 630,63 1587 449,51 988 113,7 184,3 –111,7–108 [Kr]4d105s2 196,97 Nitrógeno 17 15,999 Fósforo Germanio [Ar]3d104s24p1 49 112,41 Cd Plata N 8 1875 3 1886 2, 4 1250 –3, 3, 5 1817 –2, 2, 4, 6 1826 –1, 1, 3, 5, 7 1898 2 130/1261,81 125/1222,01 115/1192,18 115/1162,55 115/1142,96 ––/110 3,00 29,76 2204 938,3 2820 817 614 221 685 –7,3 59 –157,36–153,22 [Ar]3d104s2 107,87 Ag Paladio [Kr]4d85s1 190,23 Os Renio [Ar]3d84s2 102,91 Si [Ne]3s23p2 69,723 Ga Cinc 3, 4, 8 1803 2, 3, 4 1803 2, 4 ––a 1, 2 1817 2 2,2 135/1352,28 140/1312,20 160/1531,93 155/1481,69 4150 1964 3695 1554,9 2963 961,78 2162 321,07 767 [Kr]4d75s1 186,21 Re Wolframio 45 Rutenio 4, 6, 7 1844 1,9 130/126 4265 2334 [Kr]4d55s2 183,84 [Ar]3d74s2 101,07 Ru Tecnecio [Kr]4d55s1 180,95 [Ar]3d64s2 (97,91) 28,085 Silicio [Ne]3s23p1 31 65,38 Zn Cobre 16 14,007 –– –– –268,93 1825 3 1824 –4, 2, 4 1669 –3, 3, 5 ––a –2, 2, 4, 6 1774 –1, 1, 3, 5, 7 1894 –– 125/1181,61 110/1111,90 100/1062,19 100/1022,58 100/99 3,16 ––/97 –– 660,32 2519 1414 2900 44,2 277 115,21444,72 –101,5–34,04 –189,3–185,8 12 63,546 15 7 1895 ––/32 –272,2 –4, 2, 4 1772 –3, 2, 3, 4, 5 1774 –2, –1 1886 –1 1898 –– 2,55 65/75 3,04 60/73 3,44 50/71 3,98 ––/69 –– 4027 –210,1–195,79 –218,3–182,9 –219,62–188,12 –248,59–246,08 [He]2s22p2 26,982 Al 2, 3, 4 1802 2, 3, 4, 5 1783 2, 3, 4, 5, 6 1925 2, 4, 5, 6, 7 1803 2, 3, 4, 6, 8 1803 2, 3, 4, 5, 6 1735 2, 4 ––a 1, 3 ––a 1, 2 1,3 145/138 1,5 135/1462,36 135/159 1,9 130/128 2,2 135/1372,20 135/1282,28 135/1442,54 150/1492,00 4603 3017 5458 3422 5555 3186 5596 3033 5012 2466 4428 1768,3 3825 1064,182856 –38,83356,73 Rf [Rn]5f147s27p1? [Ar]3d54s2 95,96 3, 5 1781 2, 3, 4, 5, 6 1937 1,6 145/1452,16 135/156 4744 2623 4639 2157 Hafnio 3 1964 –– ––/–– –– –– 42 [Kr]4d45s1 178,49 Hf 1907 3 1923 175/1601,27 155/150 1652 3402 2233 [Xe]4f145d16s2 [Ar]3d54s1 92,906 Nb Mo 103 (262,11) 104 (265,12) 105 (226,03) 1 1898 0,7 215/–– –– 700 Y 71 [Xe]6s2 (223,02) Ti [Ar]3d24s2 88,906 Itrio 137,33 Ba 5 47,867 1794 3 1789 4 1801 180/1621,22 155/1481,33 145/137 1526 3336 1855 4409 2477 [Kr]5s2 1860 1 1808 2 260/2250,79 215/1980,89 28,44 671 727 1870 22 Titanio [Ar]3d14s2 Sr 56 4 44,956 39 87,62 Estroncio 132,91 3 21 Escandio [Ar]4s2 85,468 [Xe]6s1 7 –– Sin datos a Antigüedad ¿? Desconocidos * Los elementos 113, 115, 117 y 118 han recibido el visto bueno de la División de Química Inorgánica de la IUPAC, el 8 de junio de 2016, para ser nombrados como nihonio (Nh), moscovio (Mc), tennesso (Ts) y oganessón (Og), respectivamente, hasta su próxima aprobación formal por el Consejo de la IUPAC. 1879 3 1791 2, 3, 4 1801 2, 3, 4, 5 1797 2, 3, 4, 5, 6 1774 2, 3, 4, 6, 7 ––a 2, 3, 4, 6 1735 2, 3 1751 2, 3 ––a 1, 2 1746 2 160/1441,36 140/1361,54 135/1251,63 140/1271,66 140/1391,55 140/1251,83 135/1261,88 135/1211,91 135/1381,90 135/1311,65 1541 2830 1668 3287 1910 3407 1907 2671 1246 2061 1538 2861 1495 2927 1455 2913 1084,622927 419,53 907 1861 1 1790 2 235/2110,82 200/1920,95 39,31 688 777 1382 87 W Sc Calcio [Kr]5s1 6 d 40,078 Ca [Ar]4s1 55 p Sólido Aluminio 1807 1 1808 2 220/1960,82 180/1741,00 63,38 759 842 1484 37 2 Magnesio [Ne]3s1 5 24,305 1807 1 1808 2 180/1540,93 150/1301,31 97,72 883 650 1090 19 4 2 1,57 2469 Na Mg Sodio 74 3 183,84 1Número atómico 2Símbolo 3Peso atómico 4Nombre 5Año del descubrimiento 4 Wolframio 6 5 1783 6 2, 3, 4, 5, 6 7Estados de oxidación Radio (Atómico/Covalente, pm) 8 2,36 8Electronegatividad (Pauling) 7 135/146 10 5555 9Punto de fusión (ºC) 9 3422 10Punto de ebullición (ºC) 11 [Xe]4f145d46s2 11Configuración electrónica 9,0122 [He]2s1 3 1 1817 1 1828 145/1340,98 105/90 180,54 1342 1287 11 4,0026 Helio 1766 –1, 1 25/37 2,20 –259,14–252,87 3 2 18 2 2 13 70 173,05 Yb Iterbio 2, 3 1878 1,25 175/–– 1950 824 [Xe]4f 6s 2 14 2, 3 –– 1196 [Xe]4f 6s2 100 (257,10) 101 (258,10) 102 (259,10) Fm Md No Fermio 2, 3 1952 1,3 ––/–– –– 1527 12 Mendelevio 2 [Rn]5f 7s Revisión de Pascual Román Polo 2, 3 1955 1,3 ––/–– –– 827 13 2 [Rn]5f 7s Nobelio 2, 3 1958 1,3 ––/–– –– 827 14 2 2, 3 1,3 –– [Rn]5f 7s Diseño: Editorial Tébar Flores 29/08/2016 9:24:41 - s 1 3 –1, 1 2,20 –252,87 9,0122 4 6,94 Li Be Berilio Litio 1 2 1,57 1 1828 2469 0,98 105/90 2 1287 1342 [He]2s [He]2s 11 [Xe]4f 24,305 12 22,990 io Magnes Sodio 1 20 39,098 K Potasio 1807 220/196 63,38 1 40,078 Ca 38 85,468 Rb Rubidio 1861 235/211 39,31 1 39 87,62 1 (223,02) Fr Francio 1939 ––/–– 27 1 [Rn]7s 88 (226,03) Ra Y 40 2 0,9 1737 2 [Rn]7s Lu 103 ª Radio 1 1898 0,7 215/–– –– 700 Ti 23 50,942 V 24 8 7 51,996 Cr Mn 91,224 Zr 43 42 Nb Mo 41 92,906 27 Fe 28 58,933 Co eso 7 6, Mangan 2, 3, 4, 58,693 29 Ni Cu Tc 46 102,91 45 Rh Ru 47 Ag Pd 1 69,723 [Ar]3d 49 Cd P Ne F 17 S 114,82 33 50 a 204,38 Tl Hg 78,96 34 74,922 35 Se As Br Estaño 82 [Ar]3d 51 121,76 52 127,60 Te 53 I Plomo [Kr]4d 83 208,98 Bi 84 85 (209,98) Po Es una ordenación sistemática de los elementos químicos, que ofrece una valiosa información sobre su estructura electrónica. Muestra una periodicidad de las propiedades de los elementos cuando están dispuestos según su número atómico creciente. 4 Xe 5 86 Rn At Radón 2 –– Astato 5, 7 1900 –61,7 –1, 1, 3, 2,2 ––/145 Polonio2, 4, 6 1940 2 6 –– –71 14 5d10 6s 6p 2,0 ––/–– Bismuto 3, 5 1898 2 5 [Xe]4f 962 302 14 5d10 6s 6p 2,02 190/–– (294) 2, 4 1753 254 14 10 6s2 6p4 [Xe]4f * 1564 5d 2,33 160/146 (294) 271,3 14 10 6s2 6p3 [Xe]4f * 1749 5d 207,2 Pb Sb Lr 72 Hf 104 Rf 73 Ta 105 74 75 W 77 Os 108 Bh Sg Db 76 Re 107 106 Hs 78 Ir Au Pt Ds Mt 57 La 89 ª 58 Ce 90 Ac 59 Pr 91 Rg Th Pa 93 U Np Cn 63 61 Sm Nd Pm 60 92 Nh 112 111 94 Eu 64 Gd 65 Tb 97 96 95 Cm Bk Pu Am ISBN: Dy 117 Ts Lv Mc Fl 66 116 115 114 113 110 109 62 f t a 68 67 Ho Er 6 118 69 Og 70 Tm 7 Yb La tabla periódica consiste en disponer los elementos en períodos recurrentes en orden creciente de sus números atómicos. Los elementos que se hallan en una columna vertical, llamada grupo, tienen propiedades comunes. 102 98 99 Cf 76-2 978-84-7360-5 101 No Fm Md 100 Es Revisión de Pascual Román Polo Diseño: Tébar Flores Editorial - [Rn]6d - - 3 Kr 54 Xenón 8 2, 4, 6, 2,6 Yodo 7 1898 1, 3, 5, –108 2,66 ––/130 Telurio 6 1811 –1, –111,7 10 2 5p6 5s 184,3 io 1782 –2, 2, 4,2,1 140/133 [Kr]4d 5 Antimon –3, 3, 5 140/135 988 113,7 10 5s2 5p a 2,05 [Kr]4d (222,02) 2, 4 –– 449,51 10 2 5p4 1587 5s 1,96 145/138 [Kr]4d (209,99) 630,63 10 2 5p3 2602 5s 118,71 Sn Indio 3 –– 1,78 145/141 1863 231,93 10 2 5p2 2072 5s 155/144 [Kr]4d 156,6 10 2 5p1 5s [Kr]4d 2 Ar 36 io In 81 18 Cl - 20,180 Kriptón 2 3,00 Bromo 5, 7 1898 –1, 1, 3, 2,96 ––/110 –153,22 6 Selenio 6 1826 59 –157,36 10 4s2 4p –2, 2, 4, 2,55 115/114 1817 [Ar]3d 5 Arsénico –3, 3, 5 115/116 10 4s2 4p 685 –7,3 2,18 131,29 [Ar]3d 4 2, 4 1250 10 4s2 4p 614 221 2,01 115/119 126,90 [Ar]3d 3 817 10 4s2 4p 2820 72,63 Ge German Galio 3 1886 1,81 125/122 1875 938,3 10 2 4p2 2204 4s 130/126 [Ar]3d 29,76 10 2 4p1 4s 80 79 32 Ga Cadmio 2 101,07 1,69 Plata 1, 2 1817 767 a 1,93 155/148 Paladio 2, 4 –– 321,07 10 5s2 2162 [Kr]4d 2,20 160/153 Rodio 2, 3, 4 1803 961,78 10 5s1 2963 [Kr]4d 2,28 140/131 200,59 Rutenio3, 4, 8 1803 10 1554,9 3695 [Kr]4d 2,2 135/135 196,97 1844 1964 8 1 4150 1,9 130/126 [Kr]4d 5s 195,08 2334 7 1 4265 [Kr]4d 5s 44 Tecnecio4, 6, 7 3 1824 1,61 110/111 1414 2 2 2519 [Ne]3s 3p 2 [Ne]3s 3p Zn 48 O 16 30,974 15 Silicio–4, 2, 4 QUE ES LA TABLA PERIODICA? –– –– –268,93 1s2 10 Argón –– –– Cloro 5, 7 1894 –1, 1, 3, 3,16 ––/97 –185,8 Azufre 6 1774 –189,3 2 6 –2, 2, 4, a –34,04 [Ne]3s 3p 2,58 100/99 –– Fósforo –101,5 2 5 –3, 3, 5 100/102 444,72 [Ne]3s 3p 2,19 1669 83,798 2 4 277 115,21 [Ne]3s 3p 1,90 100/106 79,904 44,2 2 3 2900 [Ne]3s 3p 28,085 Si o Alumini 31 65,38 Cinc 2 55,845 1,65 Cobre 1, 2 1746 907 1,90 135/131 Níquel 2, 3 ––a 419,53 10 4s2 2927 [Ar]3d 1,91 135/138 Cobalto 2, 3 1751 1084,62 10 4s1 2913 [Ar]3d 1,88 135/121 112,41 Hierro 6 1735 1455 8 2 2, 3, 4, 2927 a [Ar]3d 4s 1,83 135/126 107,87 –– 1495 7 2 2861 [Ar]3d 4s 1,55 140/125 106,42 1538 6 2 2061 [Ar]3d 4s 26 54,938 25 30 63,546 C 14 26,982 Al 1825 125/118 660,32 12 11 10 9 N 1 Helio 9 15,999 8 14,007 7 4,0026 He 1895 ––/32 –272,2 18,998 Talio 1, 3 –– no 6 1937 Molibde 5, 1,62 180/147 (293) 2, 3, 4, 1861 2,16 135/156 327,4614 10 6s2 6p2 [Xe]4f 192,22 Niobio 3, 5 1781 o 1473 190/148 2157 5 2 5d 4639 Mercuri 1, 2 (288,19) 1,6 145/145 [Kr]4d 5s 304 14 10 6s2 6p1 [Xe]4f 190,23 * ón Circonio 4 1801 2623 5 1 5d 2,00 Oro 1, 3 ––a Oganess ¿? 4744 [Xe]4f (289,19) [Kr]4d 5s 1,33 145/137 186,21 Itrio o 3 1789 –– 356,73 2477 4 1 2,54 150/149 Tenness –– 2002 4409 Platino 2, 4 ––a (284,18) –– –38,83 14 10 6s2 [Kr]4d 5s 1,22 155/148 183,84 * rio 2856 –– ––/–– 5d 1855 2 2 2,28 135/144 2 6 Livermo ¿? 2010 [Xe]4f 3336 Iridio 5, 6 1735 –– –– 1064,18 14 10 6s1 [Kr]4d 5s 14 6d10 7s 7p 180,95 io 3825 –– ––/–– 2, 3, 4, 5d 1 2 2 5 [Rn]5f 2,20 135/128 [Xe]4f Moscov ¿? 2000 Osmio (285,17) –– –– 6, 8 1803 1768,3 14 9 6s1 14 6d10 7s 7p [Kr]4d 5s 178,49 2, 3, 4, 2,2 135/137 4428 5d –– ––/–– Flerovio ¿? 2004 2 4 [Rn]5f [Xe]4f Renio (280,16) 2 7 1803 2466 14 6d10 7s 7p –– –– 174,97 14 5d7 6s –– ––/–– 5012 io 6 1925 2, 4, 5, 6,1,9 130/128 2 7p3 [Rn]5f Nihonio ¿? 1999 [Xe]4f (281,16) 2 Wolfram –– –– 5, 14 6d10 7s 3033 14 5d6 6s 2, 3, 4, 5596 –– ––/–– 2004 2 2 [Rn]5f 2,36 135/159 [Xe]4f (276,15) 2 Tántalo 5 1783 –– –– 3186 14 6d10 7s 7p cio ––/–– 14 5d5 6s 2, 3, 4, 173,05 5555 1,5 135/146 Coperni ¿? 2 1 [Rn]5f [Xe]4f –– 2 Hafnio2, 3, 4 1802 (277,15) 3422 14 6d10 7s 7p nio 14 5d4 6s –– 168,93 5458 1,3 145/138 [Rn]5f Roentge ¿? 1996 (270) [Xe]4f 2 Lutecio 3 1923 –– 3017 dtio ¿? 1994 14 5d3 6s –– ––/–– 167,26 4603 2 1,27 155/150 Darmsta [Xe]4f 1907 2 (271,13) 14 6d10 7s –– –– 2233 io 14 5d2 6s –– ––/–– 164,93 3402 175/160 [Rn]5f 1 Meitner ¿? 1994 [Xe]4f (268,13) 2 14 6d10 7s –– –– 1652 Iterbio 2, 3 14 5d1 6s –– ––/–– 162,50 [Rn]5f 1 Hassio ¿? 1982 [Xe]4f –– (265,12) 14 6d9 7s –– –– Tulio 2, 3 1878 –– ––/–– 158,93 [Rn]5f 2 Bohrio ¿? 1984 1196 175/–– 7 –– (262,11) 1,25 14 6d 7s –– Erbio 3 1879 io 824 –– ––/–– 157,25 14 6s2 1976 [Rn]5f 2 1950 Seaborg [Xe]4f 1,24 175/–– 14 6d6 7s –– –– Holmio 3 1842 1545 –– ––/–– 151,96 13 6s2 [Rn]5f 2 Dubnio ¿? 1974 2868 o [Xe]4f 1,23 175/–– 14 6d5 7s –– –– Disprosi 2, 3 1878 (259,10) ordio 4 1967 1529 –– ––/–– 150,36 12 6s2 [Rn]5f 2 2720 Rutherf [Xe]4f 1,22 175/–– 14 6d4 7s –– –– Terbio1, 3, 4 1886 io (258,10) 1461 –– ––/–– 11 6s2 (144,91) [Rn]5f 2 2567 175/–– Lawrenc 3 1964 io –– [Xe]4f 14 6d3 7s –– –– Gadolin 1, 2, 3 1843 (257,10) 1407 –– ––/–– 144,24 10 6s2 [Rn]5f 1961 2 3230 [Xe]4f 1,20 175/–– 14 6d2 7s ? –– –– ––/–– Europio 2, 3 1880 (252,08) 1356 140,91 9 2 [Rn]5f 3250 1627 14 2 7p1 ? –– 180/–– [Xe]4f 6s 7s 2 Nobelio 2, 3 Samario 2, 3 1901 (251,08) 1312 140,12 7 1 6s [Rn]5f 1527 o vio 1,3 1,17 185/–– [Xe]4f 5d Prometi 3 1879 (247,07) Mendele 2, 3 1958 826 138,91 7 2 –– 1803 io –– 185/–– 1,3 ––/–– [Xe]4f 6s Fermio 2, 3 1955 Neodim 2, 3 1945 (247,07) 1072 14 7s2 6 2 –– 827 3000 o imio 1,3 ––/–– [Xe]4f 6s [Rn]5f 1,14 185/–– Einsteni 2, 3 1952 (243,06) Praseod 2, 3, 4 1885 1100 13 7s2 5 2 –– 827 3100 io 1,3 ––/–– [Xe]4f 6s [Rn]5f 1,13 185/–– Cerio 2, 3, 4 1885 Californ2, 3, 4 1952 (244,06) 1024 12 7s2 4 2 –– 1527 3290 1,3 ––/–– [Xe]4f 6s [Rn]5f 1,12 185/–– 1950 4 Berkelio Lantano 2, 3 1803 2 2 3, (237,05) 860 935 11 7s 3 –– 3360 1,3 ––/–– [Xe]4f 6s [Rn]5f 1,10 185/–– 1839 Curio 3, 4 1949 2 238,03 795 10 7s2 1 1 6s –– 900 3470 195/169 1,3 ––/–– [Rn]5f [Xe]4f 5d 231,04 Americio 5, 6 1944 986 920 9 2 1 2 2, 3, 4, 1,3 ––/–– 3110 [Rn]5f 7s [Xe]5d 6s 2 Plutonio 6, 7 1944 232,04 1340 7 1 7s 2607 175/–– o 7 1940 3, 4, 5, 1,28 [Rn]5f 6d Neptuni 6, (227,03) 1176 7 2 3, 4, 5, 3230 [Rn]5f 7s 1,36 175/–– Uranio 6 1940 639,4 6 2 3, 4, 5, 4000 nio [Rn]5f 7s 1,38 175/–– 2 Protacti 3, 4, 5 1789 637 4 1 7s 3927 1,5 175/–– [Rn]5f 6d Torio 2, 3, 4 1913 2 –– 1132,2 3 6d1 7s 180/–– 1,3 [Rn]5f 2 Actinio 3 1828 1568 2 1 7s 4820 1,1 180/–– [Rn]5f 6d 1899 1842 2 7s2 3300 195/–– [Rn]6d 1050 1 7s2 71 t 2 47,867 Cromo 5, 6 1774 2, 3, 4, 1,66 140/139 5 1797 Vanadio 1246 5 2 2, 3, 4, 2671 [Ar]3d 4s 1,63 140/127 Titanio2, 3, 4 1801 1907 5 1 3407 [Ar]3d 4s 1,54 135/125 (97,91) 3 1791 1910 3 2 3287 [Ar]3d 4s 95,96 1,36 140/136 1668 2 2 2830 [Ar]3d 4s 88,906 1794 180/162 1526 o 137,33 Ba 0,89 1 1808 1870 0,79 215/198 671 727 [Xe]6s2 [Xe]6s 87 7 22 1 2 [Ar]3d 4s Bario Cesio Sc Escandio Sr 56 132,91 Cs 1860 260/225 28,44 21 44,956 6 5 4 3 1879 160/144 1541 Estronci 2 0,95 1 1790 1382 0,82 200/192 688 777 [Kr]5s2 [Kr]5s 55 6 d Calcio 2 1,00 1 1808 1484 0,82 180/174 759 842 [Ar]4s2 [Ar]4s 37 5 2 1,31 1 1808 1090 0,93 150/130 883 650 [Ne]3s2 [Ne]3s 19 4 6s 15 14 6 1 2 [He]2s 2p 13 o 18 2 17 16 Neón –– 12,011 –– Flúor –1 1898 –246,08 3,98 ––/69 Oxígeno–2, –1 1886 –248,59 2 2p6 o 1774 –188,12 [He]2s 3,44 50/71 Nitrógen 4, 5 –219,62 2 2p5 –3, 2, 3, 3,04 60/73 –182,9 [He]2s 39,948 1772 Carbono –218,3 2 4 –4, 2, 4 65/75 a –195,79 35,45 [He]2s 2p 2,55 3 –– –210,1 2 3 4027 32,06 [He]2s 2p 2,04 70/77 3500 2 2 3927 [He]2s 2p 10,81 B 1808 85/82 2076 Gas W 14 5d Na Mg 1807 180/154 97,72 2 13 Boro 3 183,84 2 Símbolo 3 Peso atómico 4 Nombre imiento n 5 Año del descubr oxidació ente, pm) 6 Estados de o/Coval ) 4 Wolframio 7 Radio (Atómic ad (Pauling 6 3, 4, 5, 6 egativid 5 1783 2, 8 2,36 8 Electron fusión (ºC) 9 Punto de n (ºC) 7 135/146 10 ebullició ica 5555 10 Punto de electrón 9 3422 11 Configuración 4 2 2 1s1 11 1 74 5 datos bueno –– Sin el visto junio recibido a Antigüedad 8 de y 118 han la IUPAC, el ocidos io (Mc), 115, 117 ica de moscov ¿? Descon tos 113, a Inorgán nihonio (Nh), hasta su próxielemen te, dos como * Los la División de Químic ivamen nombra respect de Sintétic para ser són (Og), de la IUPAC. de 2016, (Ts) y oganes o por el Consejo tenness ción formal ma aproba Líquido 1 Número atómico no 1817 145/134 180,54 3 p Sólido 1,008 H Hidróge 1766 25/37 –259,14 2 PER TA B L A 1 1 ? NTOS ELEME DE LOS IO D IC A APUNTES DE HISTORIA D I M I T R I I VA N O V I C H M E N D E L E I E V (Weymouth, Reino Unido, 1887 - Galípoli, Turquía, 1915) Físico inglés que resolvió los problemas de organización de la tabla de Mendeléiev, en 1913, mediante la ley que lleva su nombre. Descubrió que el número atómico constituía el fundamento para ordenar los elementos en la tabla periódica. La tabla de Moseley constituye la base de la actual tabla periódica de los elementos químicos. Tabla periodica2016_FORO_4_B.indd 2 Gracias a los descubrimientos sobre la teoría de la materia del primer cuarto del siglo XIX, los científicos pudieron determinar las masas atómicas relativas de los elementos conocidos. Cada grupo contiene los elementos que poseen propiedades semejantes, debido a la estructura electrónica común de su nivel más externo. Por ejemplo, en la columna 18 se agrupan los gases nobles. noció la existencia de tríadas en ciertos elementos que tenían propiedades muy similares (“ley de las tríadas”). Además, la tabla periódica contiene siete filas horizontales, llamadas períodos. Los elementos de un período poseen el mismo número de niveles de electrones. La tabla también se divide en cuatro bloques con algunas propiedades químicas similares. ■ En 1829, el químico alemán Johann W. Döbereiner reco- ■ En 1860, el italiano Stanislao Cannizzaro enunció la famosa “ley de los átomos”, que permitía distinguir los átomos de las moléculas. ■ En 1862, Alexandre-Émile B. de Chancourtois fue el pri- mero en ordenar los elementos químicos según su peso atómico. ■ En 1864, el químico británico John A. R. Newlands clasifi- - HENRY GWYN JEFFREYS MOSELEY Existen distintos formatos de tablas periódicas. Sin embargo, todos coinciden en que los elementos están dispuestos en el orden creciente de sus números atómicos. La más común de las tablas es la que presenta 18 grupos. - Químico ruso conocido por haber elaborado la primera versión de la tabla periódica moderna de los elementos químicos, ordenándolos en orden creciente de su peso atómico. La clave de su éxito fue comprender que todavía quedaban cierto número de elementos por descubrir, y había que dejar huecos para esos elementos en la tabla. Entre sus investigaciones cabe destacar el estudio de la teoría química de la disolución, la expansión térmica de los líquidos y la naturaleza del petróleo. - (Tobolsk, actual Rusia, 1834 - San Petersburgo, 1907) LA TABLA PERIODICA ESTA SIEMPRE SUJETA A REVISION, EN ESPERA DE NUEVOS ELEMENTOS. có los elementos por orden creciente de sus pesos atómicos y observó que después de cada siete elementos, en el octavo, se repetían las propiedades del primero. ■ En 1868, Julius L. Meyer propuso una tabla de clasifica- ción similar a la de Mendeléiev, en la que mostraba las relaciones entre el volumen y el número atómico y las propiedades periódicas de sus pesos atómicos. ■ En 1869, Dimitri I. Mendeléiev publicó la primera versión de la tabla periódica moderna, basada en los pesos atómicos, y en 1871 una nueva. Esta tabla presentaba ciertas anomalías, que fueron subsanadas por el inglés Moseley. ■ En 1913, Henry G. J. Moseley demostró la relación entre el número atómico y la frecuencia de los espectros de rayos X de los elementos (“ley de Moseley”). 29/08/2016 9:24:42