taller de recuperación
Anuncio

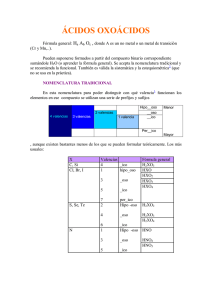
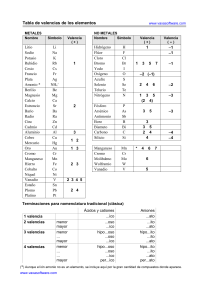
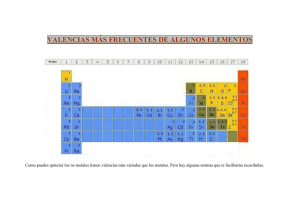
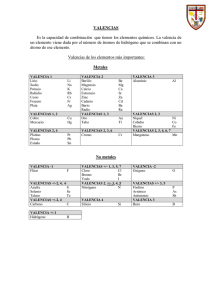
F -X C h a n ge F -X C h a n ge ko p u y c o m p u ti n COLEGIO INTEGRADO SIMÓN BOLIVAR CODIGO: MBP3S5 TALLER DE RECUPERACIÓN O NIVELACIÓN FORMATO N°1 20 AÑOS EDUCANDO A LOS JÓVENES DE LA FRONTERA VERSIÓN 1 ASIGNATURA: QUIMICA DOCENTE: Mg. JOSÉ A. CELÍN LUNA DESEMPEÑOS: PERIODO: 1 Valoración: ___ FECHA: SEDE: CENTRAL GRADO: JORNADA:TARDE * Identifica los compuestos inorgánicos sus propiedades físicas y químicas, numero de oxidación y los tipos de nomenclatura. ESTUDIANTE NOMBRES APELLIDOS 8°____ TALLER DE RECUPERACIÓN: EXAMEN ESCRITO DE RECUPERACIÓN: VALOR VALOR COLABORACIÓN PROYECTO RECICLAJE (LATAS DE ALUMINIO): 5 KILOS VALOR 40% 40% 20% 22 DE ABRIL DE 2014 23 DE ABRIL DE 2014 25 DE ABRIL DE 2014 O EVALUACIÓN ORAL SOBRE EL TALLER. TOTAL NOTAS 100% OBSERVACIÓN: EL ESTUDIANTE QUE NO DESEE COLABORAR CON EL PROYECTO DE RECICLAJE, DEBERÁ PRESENTAR EVALUACIÓN ORAL SOBRE LOS TEMAS DE RECUPERACIÓN VALOR 20% A) Según las valencias positivas de los siguientes METALES realice la Reacción y de el nombre al producto o compuesto finalmente obtenido para cada valencia, usando los tres tipos de Nomenclatura: Stock (I,II,III,IV), Tradicional (ico, oso), o sistemática ( Monóxido, dióxido, trióxido etc).las valencias dadas pertenecen al metal, pues la de Oxígeno siempre es (-2 ). 1) Ca + O2 + O2 (+2) (+1) 3) Ni + O2 (+2) 4) Ni + O2 (+3,) 5) Au + O2 ( + 3) 6) Zn + O2 (+2) B) Según las valencias positivas de los siguientes NO METALES realice la Reacción y de el nombre al producto o compuesto finalmente obtenido para cada valencia. Recuerde que si tiene solo 2 valencias formará óxidos terminados en oso (menor valencia) e Ico ( mayor valencia ) Si tiene 3 valencias el no metal formará óxidos así empezando por Hipo _NM__ y terminado en oso ( para la menor de las 3 valencias) terminando en _____ oso ( para la valencia del medio) y terminado en _______ Ico ( para la mayor de las 3 valencias). Si tiene 4 valencias el No metal, favor realizar la nomenclatura similarmente que en el cloro. 1) Mn + O2 2) P .e + O2 3) S + O2 (+4 + 6 + 7) (+3 + 4 + 5) (+2 + 4 + 6) 4) Br + O2 (+1 + 5) 5) At + O2 (+1 +3 + 5 + 7) C) Forme los Hidróxidos para cada reacción y de los nombres a cada compuesto según corresponda (observe la tabla de valencias para saber cuántas y cuales tiene cada metal). 1) MgO + H2O = ______________ 2) Na2O + H2O =_______________ 3) Li 2O + H2O=________________ 4) RaO + H2O =________________ 5) CaO + H2O=_________________ D) Forme los Hidróxidos para cada reacción y de los nombres a cada compuesto según corresponda (observe la tabla de valencias para saber cuántas y cuales tiene cada metal, y recuerde que la menor valencia forma hidróxidos del metal con terminación en oso, y la mayor valencia terminación ico). 1) Cu2O + H2O = ___________________ 2) CuO + H2O =___________________ 3) Hg2O + H2O =___________________ 4) HgO + H2O =___________________ 5) PbO2 + H2O =__________________ 6) PbO + H2O =__________________ as om .c g 2) Rb N om .c as w w .e ww ww N u ko p en ! PD en ! PD y c o m p u ti n g