observación de células parenquimáticas
Anuncio

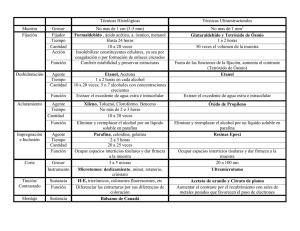
PRÁCTICAS BIOLOGÍA COLEGIO MARAVILLAS © Miguel Conesa 3ªed PRÁCTICA nº 16 OBSERVACIÓN DE TEJIDOS PARENQUIMÁTICOS y DE TEJIDOS DE SOSTÉN Materiales: Microscopio Materiales de disección. Porta y cubreobjetos Pocillos de porcelana para tinción Cuchillas Agua destilada Verde brillante o Carmín Sudán III Lugol Hematoxilina de Hansen Hojas de lirio, lechuga, adelfa, malva etc. Mesocarpio de pera, aceituna, cáscara de nuez antes de su maduración. Alcohol de 70° Método TEJIDO COLENQUIMATICO Realizar cortes transversales de tallos o peciolos de las plantas indicadas con anterioridad. o Recoged los cortes en agua o Fijar los cortes en portaobjetos con alcohol de 70° o Después de lavar con agua teñir con Verde brillante o Carmín alumínico durante 15 m. o Lavar en agua, escurrir la preparación. Añadir glicerina y observar al microscopio. o Observar las zonas externas del corte, correspondiente al tejido colenquimatoso. Observar los depósitos de celulosa en las membranas celulares. TEJIDO PARENQUIMATICO o Practicar cortes transversales muy finos en hojas de diferentes plantas: Lirios, hiedra, pino etc. o Recoger los cortes en agua y elegir los más finos o Colocar los cortes en el portaobjetos, añadir agua y observar al microscopio. o En el caso de que el estudio se realice sobre tubérculo de patata se procederá a teñir las preparaciones una vez fijada con alcohol de 96° ,con Verde brillante durante 1 m. PRÁCTICAS BIOLOGÍA COLEGIO MARAVILLAS © Miguel Conesa 3ªed o Lavar profundamente y volver a teñir con Lugol para colorear los depósitos de almidón. En el caso de la observación de esclerénquima de frutos se procede a rascar con la punta del escalpelo el mesocarpio, el producto obtenido se reparte en el portaobjetos con la ayuda de la aguja enmangada. Posteriormente se observa al microscopio. En el caso del estudio del mesocarpio de aceitunas se procederá de la forma siguiente: Una vez practicados los cortes se fijan con alcohol de 50°, posteriormente se tiñen con Sudan III y lavado con agua destilada. La coloración se hace con Hematoxilina de Hansen durante 5 minutos. Lavar con agua destilada abundantemente, montar y observar al microscopio. Resultados: Las grasas aparecen siempre teñidas de un color anaranjado, la cutícula anaranjado suave y las membranas de las células parenquimáticas de color violeta a veces poco intenso. Realizar dibujos de diversos campos microscópicos a diversos aumentos de distintos tipos de materiales • Indicar en cada caso las estructuras observadas. MERISTEMOS APICALES Los meristemos son conjuntos de células perennes de las que se producen nuevos tejidos y órganos. Existen dos clases de meristemos: primarios y secundarios. Los meristemos primarios se pueden considerar como "masas" celulares constituidas por células indiferenciadas de multiplicación continuada. La forma de estas células es generalmente cúbica de núcleos grandes y paredes delgadas. Los meristemos primarios son los que aparecen en primer lugar y se les denomina meristemales, ya que se localizan en el extremo de la raíz y del tallo , son los que producen el crecimiento en longitud. Además de estos meristemos, existen otros en el cuerpo vegetativo, que son los meristemos secundarios o laterales, responsables del crecimiento en grosor. Materiales Microscopio Porta y cubreobjetos Microtomo de mano Elementos de disección Frascos lavadores Pinza de precisión Alcoholes de 70°,80°,90° y 96° y absoluto. 1 Alcohol-xilol Parafina Hematoxilina de Hansen. Orceina acética al 2% PRÁCTICAS BIOLOGÍA COLEGIO MARAVILLAS © Miguel Conesa 3ªed Método : 1) Fijación. Fijar una célula consiste en conservarla en un estado lo más parecido posible al estado vivo. En la práctica se trata de protegerla de ataques bacterianos; evitar la auto lisis de los constituyentes fundamentales; insolubilizar los constituyentes celulares; evitar distorsiones y retracciones, pero sobre todo unas células fijadas correctamente debe permitir posteriores tratamientos. La fijación de los meristemos apicales se hace introduciendo éstos en alcohol de 70° durante un día o más. Si se trata de ápices de raíz de monocotiledóneas es suficiente con unas horas. 2) Deshidratación : La deshidratación tiene como misión eliminar completamente el agua contenida en los tejidos ya que la parafina no es soluble en agua • Si el tejido no estuviese deshidratado la parafina no podría penetrar y no sería posible la inbibición. Para la deshidratación pasamos los ápices por una serie de alcoholes, concretamente estarán 30 minutos en cada uno de los alcoholes y tres pasadas por el alcohol absoluto. 3) Clarificación. Como la parafina tampoco es soluble en alcohol es necesario sustituir éste por un disolvente de la parafina, los empleados más comunes son el xilol y el benceno. Para ello es necesario pasar los ápices a un frasco con una mezcla 1:1 de xilol - alcohol durante media hora y posteriormente al xilol puro durante otra media hora. Este tiempo de exposición al xilol debe ser exactamente medidos. 4) Inbibición. La impregnación por parafina y la eliminación del xilol debe ser gradual, por tanto pasaremos los ápices a una mezcla de xilol-parafina a partes iguales contenida en una cápsula de porcelana es una estufa a 58°C. durante media hora. Posteriormente se pasará a parafina pura también en estufa. Para que sea eliminado totalmente el xilol, habrá que hacer tres pases por parafina pura, como mínimo tres horas cada uno. Todos los pases en la estufa se harán con las pinzas calientes, tomando la precaución de dejarles dentro de la estufa media hora antes; de esta manera evitamos que solidifique la parafina en las puntas de las pinzas y se dificulte el pase de los ápices. 5) Inclusión. Una vez orientadas las piezas antes de que solidifique la parafina se sacan de la estufa para que solidifique la capa superior del molde, posteriormente se sumergen en un cristalizador con agua para que acabe la cristalización. 6) Cortes. Se utiliza el microtomo de mano, efectuando cortes de 0,1 mm, tanto longitudinalmente como transversalmente. Para la realización de los cortes utilizar una cuchilla de microtomo nueva o recién afilada. 7) Colocación de los cortes en el portaobjetos. Para facilitar la adherencia de la cinta de parafina de los cortes a los portaobjetos, se extenderá sobre ellos líquido de extensión. El más empleado de ellos es la albúmina-glicerada de Mayer. Posteriormente se coloca una PRÁCTICAS BIOLOGÍA COLEGIO MARAVILLAS © Miguel Conesa 3ªed gotita de ésta solución y la extenderemos sobre el portaobjetos con una varilla de vidrio, de forma que quede una película lo más fina posible. La albúmina glicerada de Mayer la emplearemos sin diluir, porque después hay que sumergir los portas en agua para recoger los cortes. Una vez recuperados se colocan los portaobjetos en estufas a 58°C., esta temperatura tiene dos funciones: en primer lugar hace que la parafina se estire más sobre el porta y se facilite el desparafinado posterior; y en segundo lugar hace que la pequeña película de albúmina del líquido de extensión coagula y pegue los cortes al portaobjetos. 9) Tinción. Se desparafina con dos pases de Xilol de 15 minutos cada uno. Posteriormente se hace una pasada de cinco minutos por la serie de alcoholes pero empezando por el absoluto y acabando por el de 70°. Después se lavan profusamente. La coloración se hará con Hematoxilina de Hansen durante 10 minutos. En este momento las preparaciones se montan con Bálsamo de Canadá hasta su cristalización. Observación : Observar los cortes al microscopio, primero con menor aumento para tener una visión de conjunto. Luego emplearemos los objetivos de mayor aumento, para estudiar con detalle la morfología de las células meristemáticas. Dibujar una vista de conjunto, en corte longitudinal y transversal, finalmente algunas células típicas aisladas con mayor aumento. Colénquima y floema Xilema y floema secundario