Diapositiva 1 - Departamento de Química Orgánica
Anuncio

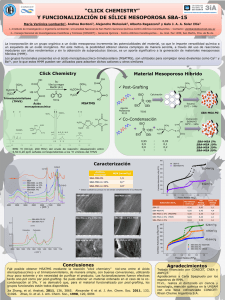
FACULTAD DE QUÍMICA DR. AGUSTÍN PALMA DE LA CRUZ O R 1 N H O N H Espilantol O -Sanshool Anestésico Insecticida Antiinflamatorio Amebicida Antihelmíntico N H MATERIA PRIMA RENOVABLE MEDIDAS VERDES DE PROCESOS QUÍMICOS QUÍMICA EN MICROESCALA DISOLVENTES POSTULADOS HERRAMIENTAS DE LA QV ¿ELECTROQUÍMICA? BIOCATÁLISIS CATALIZADORES FUENTES ALTERNAS DE ACTIVACIÓN CONTENIDO 1. Introducción: Principios;Descripción experimental; Ventajas y desventajas 2. Energía 3. Ejemplos de electrosíntesis orgánica verde: Apareadas; electrocatalíticas; en líquidos iónicos; reactivos electrogenerados; uso de materia prima renovable; en microemulsiones, evitar uso de derivados; Electrosíntesis de flujo 4. Preparación de moléculas complejas. 5. Iniciación con equipo sencillo y barato : BBB 6. Conclusiones 7. Bibliografía 1. Introducción 1. INTRODUCCIÓN EQUIPO CLÁSICO EN SINTESIS ORGANICA 4 5 6 7 4 3 8 3 2 9 2 1 11 5 6 7 8 9 1 10 1. INTRODUCCIÓN QUÍMICA ORGÁNICA CLÁSICA MATERIA PRIMA NO RENOVABLE NO BIODEGRABLE TÓXICO ENERGÍA (Calor) PELIGROSO TÓXICO ESTEQUIOMÉTRICO SEPARACIÓN Y TRATAMIENTO DE RESIDUOS 1. INTRODUCCIÓN ELECTRÓLISIS H2O H2O e-e- HO- + H2 H+ + O2 1. INTRODUCCIÓN ELECTROQUÍMICA MICHAEL FARADAY 1791-1867 DESCUBRE EL BENCENO LEYES QUE DESCRIBEN LA ELECTRÓLISIS -2e 2CH3COO-CO2 2CH3 Kolbe INVENTOR DEL GENERADOR ELÉCTRICO (Producción de electricidad a partir del movimiento mecánico) CH3CH3 1. INTRODUCCIÓN ¿PORQUÉ LA ELECTROQUÍMICA ES VERDE? Producción de energía sostenible Electrosíntesis de productos químicos Monitoreo electroquímico en tiempo-real Tratamiento de contaminantes 1. INTRODUCCIÓN PRINCIPIOS DE LA ELECTROSÍNTESIS FUENTE DE PODER (ENERGÍA ELÉCTRICA) v ÁNODO e +3V vs ECS F2 MnO4 -1 O2 Pb+2 Li + e F -1 R R Mn +2 CrO4Ag +1 CÁTODO Membrana Ag 0 R Zn 0 R NaBH4 L Anión NaH Catión M Electrolito Disolvente Li0 - 3V vs ECS OXIDACIÓN REDUCCIÓN 1. INTRODUCCIÓN 1. INTRODUCCIÓN CELDA NO DIVIDIDA Fuente de corriente directa V A Ánodo -e-e - Disolución para ser S electrolizada A -eS +eElectrolito soporte ClO4 A Li REACCIONES : A POTENCIAL CONTROLADO (V) A CORRIENTE CONTROLADA (I) Cátodo 1. INTRODUCCIÓN CELDA DIVIDIDA Eletrodo de referencia Electrodo Membrana Electrodo auxiliar de trabajo 1. INTRODUCCIÓN INTERMEDIARIOS FORMADOS ELECTROQUÍMICAMENTE Y REACCIONES QUÍMICAS ACOPLADAS RX Oxidación e Ánodo -e -e Reducción Cátodo e RX RX A red - X+ A ox - X- A ox A red R A red R -e -e e + A ox e R- R -H+ C=C Eliminación E+ Nu Nu-R R-R R-E Sustitución Dimerización Sustitución nucleofílica electrofílica H-A R-H + A Reacciones ácido-base 1. INTRODUCCIÓN RANGO DE POTENCIALES REDOX DE ALGUNOS ELECTROFILOS VS ECS 1. INTRODUCCIÓN VARIABLES EXPERIMENTALES COMÚNES EN PROCESOS Q y EQ CONVENCIONAL ELECTROQUÍMICO Concentración Concentración Disolvente Disolvente Temperatura Temperatura pH pH Tiempo Tiempo Potencial Densidad de corriente Electrodos Electrolito soporte Celda: dividida o no dividida Celda: estática o de flujo Tipo de membrana 2. ENERGÍA 2. ENERGÍA TECNOLOGÍA ACTUAL: COMBUSTIÓN CON COMPUESTOS DE CARBÓN ELECTRICIDAD ELECTRÓLISIS 2. ENERGÍA TECNOLOGÍA VERDE EÓLICA NUCLEAR SOLAR OCEÁNICA GEOTÉRMICA ELECTRICIDAD ELECTRÓLISIS 3 Ejemplos de electrosíntesis orgánica en la que están involucrados varios principios de la química verde 3.1 ESOV: REACCIONES APAREADAS 3.1. Reacciones apareadas Ánodo productos de interés Sustrato 1 e- Intermediario 1 Cátodo Sustrato 2 Intermediario 2 -APROVECHAMIENTO DE LA ENERGÍA -DISMINUCIÓN DE CONTAMINANTES - e 3.1 ESOV: REACCIONES APAREADAS 3.1.1 Electrosíntesis apareada paralela. BASF (1999) 4000 t/año ALTA ECONOMÍA ATÓMICA Chemosphere. 43, 63-73, 2001 3.1 ESOV: REACCIONES APAREADAS 3.1.2 Electrosíntesis apareada convergente J. Org. Chem., 69, 2423-2426 2004 USO DE REACTIVOS NO TÓXICOS SNA POR ELECTROSÍNTESIS APAREADA Tetrahedron Letters, Vol. 36, (39),7027-7030, 1995 3.1 ESOV: REACCIONES APAREADAS 3.1.3 Electrosíntesis apareada divergente J. Electrochem. Soc. 135, 1400 1988 USO DE MATERIA PRIMA RENOVABLE 3.1 ESOV: REACCIONES APAREADAS 3.1.4 Electrosíntesis apareada lineal Altas conc. es peligroso 3.1 ESOV: REACCIONES APAREADAS 3.1.4.1Obtención de nitronas EFICIENCIA TEORICA DE CORRIENTE: 200% 180% de eficiencia de corriente experimental Chemistry Letters. 1271-1272, 1997 3.1 ESOV: REACCIONES APAREADAS 3.1.4.2 Obtención de sulfonas Electrochemistry. 67, 4, 1999 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS 3.2 REACCIONES ELECTROCATALÍTICAS ES MEJOR PREVENIR RESIDUOS MAS QUE TRATARLOS 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS a) Reacción convencional b) Electrólisis directa 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS c) Electrólisis indirecta (Reacciones electrocatalíticas) ÁNODO Med ox S red Med red S ox Heterogénea Homogénea Reacción redox Menos energía Disminuye pasivación de electrodo Más selectividad Robert Francke , R. Daniel Little Chem. Soc. Rev., 2014, 43, 2492—2521 181 referencias P 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS Reacciones electrocatalíticas con multimediadores Med n (cantidad catalítica) ÁNODO e- Med red 1 Med ox 2 Med red 3 PRODUCTO Ox Med ox 1 Med red 2 Med ox 3 Reacción Heterogénea Reacción Homogénea SUSTRATO Red SOLO SEPARACIÓN Ejemplo: Oxidación de alcoholes a aldehídos Tradicional: 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS TRABAJAR Y GENERAR SUSTANCIAS CON BAJA TOXICIDAD PARA EL SER HUMANO Y EL MEDIO AMBIENTE K2CrO4 Cromatos de México tumba tóxica 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS Electrocatalítico: USO DE CATALIZADORES 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS CELDA ELECTROQUÍMICA NO DIVIDIDA 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS 3a 3b EQ:84-86% Q , PCC:66-67% 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS En una celda termostada: Disolver el alcohol y TEMPO en CH2Cl2 (30mL) Adicionar NaBr al 15% saturada con NaHCO3 (60 mL) Introducir electrodos Conectar electrodos al convertidor de corriente. electrolizar a 6.5 V (0.50-0.6 A ), a10°C, por 15 min. Agitar vigorosamente por 30 min. Realizar una ccf: hexano / AcOEt (4:1) Separar fases y lavar con:de HCl al 10% , tiosulfato de sodio al 10 % y por último con salmuera. Secar con Na2SO4 anhidro. Purificar producto 3.2 ESOV: REACCIONES ELECTROCATALÍTICAS OXIDACIÓN DE ALCOHOLES Q: PCC, CH2Cl2 anh. RCH2OH 66-67% RCHO E: Doble mediador TEMPO/Br-, sistema de dos fases, 0-10°C VENTAJAS DE E RESPECTO A Q 84-86% Disminución de contaminantes No se necesitan condiciones anhidras Mejores rendimientos Más fácil purificación Es auto indicador del término de la reacción Uso de catalizador Disminución de riesgos para la salud LIMITACIONES DE E: No funciona con alcoholes que tienen anillo aromático con grupos electro-donadores No funciona con alcoholes que contienen insaturaciones Chem. Soc. Rev., 2014, 43, 2492--2521 3.3. ESOV: REACCIONES EN LÍQUIDOS IÓNICOS 3.3 Reacciones en líquidos iónicos • Alta conductividad iónica • No volátiles • Baja flamabilidad • Reciclables • Amplia ventana de trabajo 3.3. ESOV: REACCIONES EN LÍQUIDOS IÓNICOS fluoración anódica selectiva con líquidos iónicos J. Electrochem. Soc., 153 ,D162-D166, 2006. 3.3. ESOV: REACCIONES EN LÍQUIDOS IÓNICOS Chem. Commun. 274 , 2002. J. Org. Chem. 72, 200-203, 2007 3.4. Reacciones con reactivos electrogenerados 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS MINIMIZAR LOS ACCIDENTES QUÍMICOS BHOPAL, INDIA 1984 H3C N C O 40 TON 3,500 muertes 150, 000 heridos Heyglin M. Chem. Eng. News. 3, 1994 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS 3.4.1 Electrogeneración de superóxidos (O2•–). Método tradicional parte de fósgeno: CCl2O J. Org. Chem. 62, 6754- 1997 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS 3.4.2 Electrogeneración de S-2 y de S+2 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS 3.4.3 Electrogeneración de halógenos(+) Nieto-Mendoza E. J. etal J. Org. Chem., 70, 4538-4541, 2005 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS 3.4.4 Ácidos electrogenerados Chemistry Letters. 529-530, 1984 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS Tradicional: endo / exo:3:3.9 Problemas de polimerización J. Org. Chem. 55, 3958-3961, 1990 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS 3.4.5 Bases electrogenerados PB BEG REACCIÓN Electrochem. Acta. 20, 33-36, 1975 J.Electroanal. Chem. 584,174–181, 2005 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS PB BEG REACCIÓN J. Org. Chem. 61, 5532-6, 1996 Electrochim. Acta. 50, 2029-2036, 2005 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS REACCIÓN DE HORNER-EMMON: SIN BASE O O (EtO)2P OEt 8 H H PROCESO C PROCESO E REDUCCIÓN CATÓDICA NaH CELDA NO DIVIDIDA CON Mg COMO ÁNODO DE SACRIFICIO CELDA DIVIDIDA O O (EtO)2P + H2 OEt 9 RCHO O O O P(OEt)2 + R OEt 10 Éster -insaturado Isómero (E) 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS Estudios de voltamperometría cíclica O O (EtO)2P OEt 8 O Cl 4a • a) Medio: Et4NBF4, 0.1M, DMF H • b) 8 (8mM) • c) 8 (8mM), MgSO4 sat. • d) Como (c) + 4-clorobutanal • e) Barrido lineal anódico. Mg como ánodo de sacrificio + 8 (8mM) 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS Palma A., etal. Electrochem. Commun. 5, 455–459 2003. 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS ELECTRÓLISIS PREPARATIVA CELDA NO DIVIDIDA CON MAGNESIO COMO ÁNODO DE SACRIFICIO 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS O O (EtO)2P OEt 8 H H PROCESO C PROCESO E REDUCCIÓN CATÓDICA Desventajas NaH 81% O CELDA DIVIDIDA CELDA NO DIVIDIDA CON Mg COMO ÁNODO DE SACRIFICIO 60% 84% Electrochem. comm.5, 455-9 (2004) O (EtO)2P + H2 OEt 9 RCHO O O O P(OEt)2 + ventajas R OEt 10 Éster -insaturado Isómero (E) O Cl 10a OEt No procede: ACN, Al, Benzaldehído, si el prod. es más electroactivo que 8 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS Síntesis convencional y electroquímica de amidas con el ión aciloxitrifenilfosfonio O Cl OH NBS, Ph3P CH2Cl2 11 SOCl2 O O Cl Cl OPPh3 Cl Ion aciloxitrifenilfosfonio Cloruro de ácido i i BuNH2 BuNH2 O 70% Cl N H 12 27% 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS MECANISMO PARA LA ELECTROSÍNTESIS DE AMIDAS VÍA EL IÓN ACILOXITRIFENILFOSFONIO Proceso anódico: O Ph3P -e Ph3P RCOOH, -e-H+ Ph3P Catión R aciloxitrifenilfosfonio O En disolución: O R1NH2 O Ph3P R O R N H O RCOOH o RCOO- R1 + Ph3PO + H O + Ph3PO + H R O R R1NH2 O R R1NH2 + RCOOH N H R1 + RCOOH R1NH3 RCOO R1NH2 + Lut ClO4 R1NH3 ClO4 + 2,6-lutidina Proceso catódico: 2H + 2e- H2 Ohmori H., etal. Tetrahedron. 47, (4/5) 767-776 (1991) 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS ESTUDIOS DE VOLTAMPEROMETRÍA CÍCLICA O Cl OH A a) LutClO4 (0.1M), CH2Cl2 b) Ph3P (I), (5 mM) c) Igual que b + A (5 mM) d) Igual que b + A (15 mM) Electrodos de Pt, V= 50 mVs -1 O Ph3P O (II) -eH O Ph3P O C A Ph3P -e- Ph3P I -H+ R C R 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS ELECTRÓLIS PREPARATIVA Celda no dividida para la electrosíntesis de N-isobutilamidas 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS O Cl OEt Proceso E 10a Ph3P O Cl Ph3P OH 11 SOCl2 67% Proceso C Proceso C Ph3P NBS 70% 27% O O Cl Cl OPPh3 Cl Cloruro de acilo i Ión aciloxitrifenilfosfonio i BuNH2 O Cl N H 12 BuNH2 3.4. ESOV: REACCIONES CON REACTIVOS ELECTROGENERADOS Características verdes de reactivos electrogenerados • Disminución de accidentes: nunca se manipula el reactivo, se genera in situ. • No hay problemas económicos por descomposición del reactivo ( su uso y almacenamiento) 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE 3.5. Reacciones electroquímicas con materia prima renovable BIOMASA: ALMIDÓN DE GRANOS ACEITES GRASAS CERAS 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE IMPORTANCIA EN EL USO DE MATERIA PRIMA RENOVABLE • Disminución gradual y alto costo de materia prima no renovable • La adición de oxígeno al petróleo es un paso muy contaminante 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE 3.5.1 Obtención de glucosa por hidrólisis electroquímica de carbohidratos H OH HO O HO H H H H OH H OH OH HO O HO H H HO n HO H HO OH H O n H J. Electrochem. Soc. 135, 83-87, 1988 H OH OH 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE 3.5.2 Hidrólisis electroquímica de la ligninia Lin S.Y. En Tillman D.A. y Jahn E.C. eds. Progress in biomass conversion. 4, 32-37, 1983 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE 3.5.2 Electrosíntesis apareada de ácido furóico y alcohol furfurílico 2H + 2e O CH2OH H2O O CHO 2H + 2e O CO2H Electrodos tridimensionales Electrochim. Acta 46, 2757-2760, 2001 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE 3.5.4 Obtención de acido L-cistéico y L-cisteina a partir de la electrólisis apareada de la L-cistina NH2 NH2 NH2 NH2 10Br 5Br2 10H, 10e 10 HO CCHCH SH 2 HO2CCHCH2SO3H 6 HO2CCHCH2SSCH2CHCO2H 2 2 6H2O Chemistry Letters Vol.33, No.3 (2004) 3.5. ESOV: REACCIONES EQ DE MATERIA PRIMA RENOVABLE Obtención de ácidos carboxílicos a partir de ceras 3 R(CH2)nCOO(CH2)nR1 Cera 12e 4Cr(VI) H3O 3 R(CH2)nCOOH + 3 R1(CH2)nOH 4Cr(III) 3 R1(CH2)n-1COOH 3.6. ESOV: REACCIONES EN MICROEMULSIONES 3.6. Electrosíntesis verde en microemulsiones Aceite Agua Agua Agua Aceite Agua Aceite Agua Microemulsión de aceite en agua Microemulsión bicontinua DISOLVENTE MAYORITARIO: AGUA Me Br N Me Surfactante: DDA B. Bromuro de didodecildimetilamonio EQ 3.6. ESOV: REACCIONES EN MICROEMULSIONES 3.6.1 Formación de enlaces C-C por electrocatálisis utilizando . microemulsiones J. Org. Chem. 61, 5972, 1996 EQ 3.6. ESOV: REACCIONES EN MICROEMULSIONES 3.6.2 Proceso Monsanto para la obtención de adiponitrilo 270,000 t/a Celda: Dividida Potencia (kW h 6.0 kg-1) No dividida (Emulsiones) 2.4 Hamann C.H. etal. Electrochemistry. Wiley, New York, 1998 EQ 3.6. ESOV: REACCIONES EN MICROEMULSIONES EQ 3.6.3 Electrosíntesis del verde de leuco- metileno empleando sono-emulsiones H N N Me2N H+, 2e- NMe2 Me2N S Cl NO2 Verde de metileno S NMe2 NO2 Verde de leuco-metileno Ventajas de utilizar emulsificación acústica: -No se utilizan surfactantes -Fácil separación del producto -La reacción electroquímica ocurre en una superficie muy grande Pure Appl.Chem. 73(12), 1947-1955, 2001 3.7 Evitar el uso de grupos protectores Electroreducción Regioselectiva Fry A.J. etal. J. Org. Chem. 35, 1232, (1970) 3.8. ESOV: ELECTROQUÍMICA DE FLUJO 3.8 ELECTROQUÍMICA DE FLUJO QUÍMICA DE FLUJO 3.8. ESOV: ELECTROQUÍMICA DE FLUJO Electrogeneración in situ de o-benzoquinona Chem. Commun., 2012, 48, 2806–2808 3.8. ESOV: ELECTROQUÍMICA DE FLUJO FLUJO DE CATIONES J. Am. Chem. Soc. 2001, 123, 7941-7942 4. preparación de moléculas complejas 4.PREPARACIÓN DE MOLÉCULAS COMPLEJAS EJÉMPLO DE UNA SÍNTESIS TOTAL CON DOS DISTINTAS METODOLOGÍAS: CONVENCIONAL Y ELECTROQUÍMICO ELECTROSÍNTESIS ORGÁNICA SÍNTESIS ORGÁNICA CONVENCIONAL A m ÁNODO n A B p CÁTODO B C q x ELECTRODO y 2 O N H Cl 1. OXIDACIÓN DE O ALCOHOLES A (EtO)2P ALDEHÍDOS OH O OEt E C O E O (EtO)2P O OEt C Cl H O (EtO)2P O OEt 2. REACCIÓN DE HORNER-EMMONS O (EtO)2P O OEt O Cl OEt C Cl E 3. AMIDACIÓN DE ÁCIDOS CARBOXÍLICOS O C OH O Cl O Cl OPPh3 O Cl OPPh3 N H C O 1. OXIDACIÓN DE ALCOHOLES A ALDEHÍDOS IPh3P N H OH OH E C E O H C O O H Ph3P N H 4. REACCIÓN DE WITTIG O 2 N H 4.PREPARACIÓN DE MOLÉCULAS COMPLEJAS Agustín Palma, Jorge Cárdenas and Bernardo A. Frontana-Uribe. Comparative study of the Nisobutyl-(2E,6Z)dodecadienamide chemical and electrochemical syntheses. Green Chem., 2009, 11, 283– 293 REACCIONES CONVENCIONALES REACCIÓNES ELECTROQUÍMICAS Ánodo R ROH TEMPOOX 2Br- 2e- TEMPORED Br2 Cátodo O (EtO)2P 4b: 95% R1 PCC 4a: 55% H 4b: 57% O (EtO)2P OEt O (EtO)2P O OEt 8 NaH O O OEt Cl 9 84% OEt 10a Ánodo O (EtO)2P 81% O OEt 9 1) LiOH/THF 2) H3O+ Ph3P -e- O Ph3P Cl OH O O Cl Cl OPPh3 i BuNH2 - Ph3PO 67% - i BuNH2 N H 12 Rendimiento total: 46% Rendimiento total: 10% O IPh3P 17, 81% - Ph3PO 27% 1) NaI 2) PPh3 18 OPPh3 O Cl Cátodo 17 NBS, PPh3 11, 88% -e-, -H+ X+e O 4a: 94% O 8 +e- ROH 3a = Cl(CH2)4 3b = CH3(CH2)5 N H NaNH2 O Cátodo 17 PROBASE +e- X EGB Ph3P 18 4b N H 60% 18 O Rendimiento global por ruta E/C: 22% 2 N H Rendimiento global por ruta C: 5% 4.PREPARACIÓN DE MOLÉCULAS COMPLEJAS Sowell C. G etal. Tetrahedron Lett.31, 485. 1990 5.PROPUESTA DE EXPERIMENTO 5. ¿CÓMO PODRÍAS INICIARTE EN LA ELECTROSÍNTESIS ORGÁNICA VERDE CON EQUIPO SENCILLO Y ECONÓMICO? BBB INCORPORAR AL MÁXIMO LOS POSTULADOS 5.PROPUESTA DE EXPERIMENTO 1. Seleccionar una reacción tradicional J. Chem. Ed. 75, (10), 1293-1294, 1998 5.PROPUESTA DE EXPERIMENTO 2. Investigar o desarrollar su versión electroquímica: Electrogeneración de bromo 5.PROPUESTA DE EXPERIMENTO 2. Incorporar al máximo los Postulados de la química verde Se evita manipulación de reactivo corrosivo y volátil: Br 2 Aprovechamiento de la energía: -Electrosíntesis apareada lineal -Agitación con aire 5.PROPUESTA DE EXPERIMENTO Aprovechamiento de la energía verde con fotocelda DISEÑO DE CELDA 5.PROPUESTA DE EXPERIMENTO EXPERIMENTO CUALITATIVO 6. conclusiones ELECTROSÍNTESIS Electrólisis directa, indirecta y apareada Mediadores Disolventes: LI, mE Electrolisis regioelectivas Aminoácidos Azucares Lignina Temperatura baja Electrólisis Reactivos apareada Electro-generados Mediadores Uso de energía renovable Electro-análisis ELECTROSÍNTESIS 7. BIBLIOGRAFÍA Bernardo A. Frontana-Uribe, R. Daniel Little, Jorge G. Ibanez, Agustín Palma and Ruben Vasquez-Medrano Organic electrosynthesis: a promising green methodology in organic chemistry Green Chem., 2010, 12, 2099-2119 153 referencias Diagrama básico de un ecosistema terrestre BIOMASA O O O O O O O O O O N N O Viva el curso de química verde