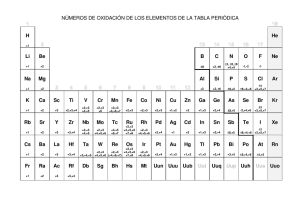
NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS
Anuncio
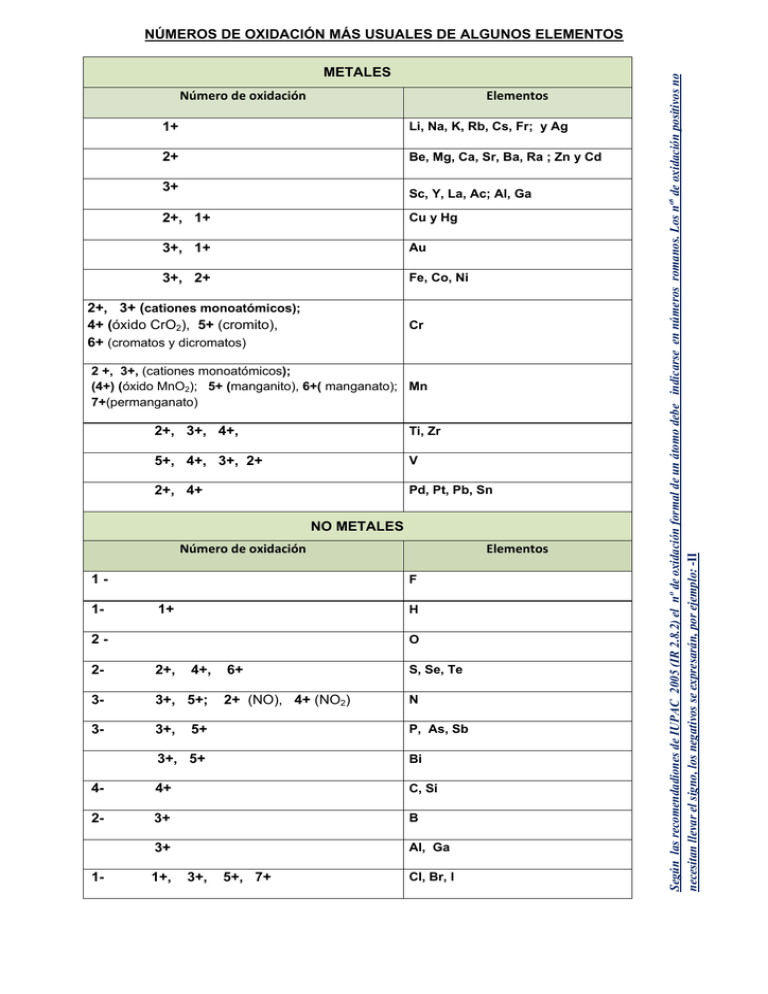
METALES Número de oxidación Elementos 1+ Li, Na, K, Rb, Cs, Fr; y Ag 2+ Be, Mg, Ca, Sr, Ba, Ra ; Zn y Cd 3+ Sc, Y, La, Ac; Al, Ga 2+, 1+ Cu y Hg 3+, 1+ Au 3+, 2+ Fe, Co, Ni 2+, 3+ (cationes monoatómicos); 4+ (óxido CrO2), 5+ (cromito), 6+ (cromatos y dicromatos) Cr 2 +, 3+, (cationes monoatómicos); (4+) (óxido MnO2); 5+ (manganito), 6+( manganato); Mn 7+(permanganato) 2+, 3+, 4+, Ti, Zr 5+, 4+, 3+, 2+ V 2+, 4+ Pd, Pt, Pb, Sn NO METALES Número de oxidación 11- Elementos F 1+ H 2- O 2- 2+, 4+, 3- 3+, 5+; 3- 3+, 6+ S, Se, Te 2+ (NO), 4+ (NO2) N 5+ P, As, Sb 3+, 5+ Bi 4- 4+ C, Si 2- 3+ B 3+ Al, Ga 1- 1+, 3+, 5+, 7+ Cl, Br, I Según las recomendadiones de IUPAC 2005 (IR 2.8.2) el nº de oxidación formal de un átomo debe indicarse en números romanos. Los nºs de oxidación positivos no necesitan llevar el signo, los negativos se expresarán, por ejemplo: -II NÚMEROS DE OXIDACIÓN MÁS USUALES DE ALGUNOS ELEMENTOS GRUPOS POLIATÓMICOS NH4+ ión (catión) amonio, azanio H3O+ ion (catión) oxonio, oxidanio AsH4* ion catión arsonio 1+ PH4+ ion fosfanio SbF4+ ion tetrafluorestibanio (nombre de sustitución); Tetrafluorantimonio(1+); Tetrafluorantimonio(V) (ambos son nombres de adición)