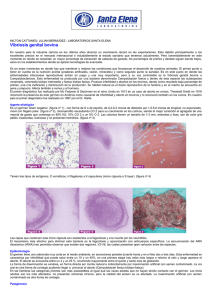
Tricomoniasis bovina
Anuncio

Trichomona foetus T.foetus es un protozoario flagelado que habita en el aparato reproductor, incluidos el prepucio y área distal del pene en toros, así como en la vagina y útero de las vacas. Es un organismo móvil aproximadamente el doble del tamaño de un glóbulo blanco (10-20 micras). Los protozoos son organismos unicelulares y estructuralmente más complejos que las bacterias, pero con muchas características biológicas similares, incluidas las multiplicación por fisión binaria. Este microorganismo puede ser identificado en un medio líquido a 100x donde se reconoce por su desigual y característico movimiento de saltos bruscos. Las tinciones no son necesarios para identificar el organismo vivo. Las estructuras de locomoción incluyen tres flagelos anteriores y un flagelo propulsor unido a una membrana ondulante sostenida por una costa. Recorriendo todo el cuerpo, desde los gránulos basales de los flagelos hasta el extremo posterior del cuerpo, y con frecuencia, proyectándose mas allá de el, existe un grueso bastoncillo transparente y cristalino llamado axostilo. Trichomonas foetus Note the undulating membrane (green arrows) along the surface of these trophozoites . La Tricomoniasis bovina es una enfermedad reproductiva del ganado que pueden tener un impacto económico significativo para la producción de vacas y terneros. Una vaca infectada esta sujeta a presentar muerte precoz de los embriones, aborto, piometra o infertilidad transitoria. En algunas regiones de América del Norte, América del Sur y Australia, donde la producción extensiva de carne vacuna es común, el 50% de los rebaños puede estar infectada. Aunque el microorganismo ha sido conocido por causar problemas de reproducción desde hace 100 años, ha habido una mayor conciencia de la enfermedad en los últimos años debido al impacto económico, haciendo que el uso de pruebas y el diagnostico sea mas frecuente. El impacto económico de la infección por tricomonas es grave. En las producciones de carne, e incluso a veces en las centrales lecheras, la producción de becerros se puede reducir hasta un 50% dependiendo del porcentaje de toros infectados y la susceptibilidad de las vacas en el hato. Además de la pérdida evidente de terneros, las pérdidas adicionales incluyen una temporada de cría prolongada o fechas posteriores al parto con un período de crecimiento más corto para los terneros, debido al aumento de repeticiones. Estas pérdidas combinadas pueden dar lugar a un numero tan alto como 35% en disminución de la rentabilidad económica por vaca en un hato infectado. T. foetus reside normalmente en la mucosa superficial del tracto reproductor del hospedador y su habilidad para adherirse al epitelio vaginal es fundamental en el establecimiento de la infección . La adhesión de T. foetus a la célula epitelial del tracto genital de la hembra bovina se inicia mediante el flagelo posterior y luego continua por su soma. El complejo molecular, adhesina Tf 190, ubicado en la superficie de T. foetus también favorecería la adhesión y citotoxicidad hacia la célula hospedador. El poder invasivo y la selectividad de T. foetus hacia las células huésped estaría determinado por el reconocimiento de receptores glicoproteícos en la matriz extracelular del hospedador a partir de lectinas del protozoo. Por otra parte, diversas endo y exoenzímas de T. foetus influyen en los mecanismos de patogenicidad. La cisteína proteínasa extracelular del protozoo favorece la invasión hacia la célula huésped debido a su capacidad para desintegrar epitelios, enzimas celulares y fibronectinas . A su vez, dicha enzima degrada isotipos de IgG, especialmente IgG2 y un componente del complemento (c3), ambos presente en secreciones genitales de la hembra bovina. La IgG2 y el complemento son importantes dentro de los mecanismos de defensa del bovino hacia organismos patógenos extracelulares . Sin embargo, la acción lítica de la cisteína proteínasa extracelular de T. foetus sobre la IgG2 y fracciones del complemento representaría un importante mecanismo de evasión del sistema inmune por parte del protozoo. Por otra parte, la resistencia de IgG2 a ser degradada por dicha enzima es regulada genéticamente. Por lo tanto, la presencia de animales con mayor capacidad para liberarse antes de la infección genital sería genéticamente determinada por la presencia de IgG2 resistente a la degradación enzimática. En los machos la sintomatología es inaparente. En la hembra el primer síntoma es la inflamación de la vagina. Inflamación del cuello del útero. Inflamación del útero. Aborto en el primer tercio de la gestación, el cual se puede dar de dos maneras: Cuando el feto sale junto con las membranas y el animal puede recuperarse. Cuando hay retención de la membranas, inflamación del útero y pérdida de la capacidad reproductiva. Repetición de celos a consecuencia de la muerte embrionaria No hay un signo observable que nos ayude con el diagnóstico de la enfermedad. El aborto puede llevar a un diagnóstico presuntivo, pero la confirmación del diagnóstico requiere la demostración del organismo en el tejido o con mayor frecuencia en cultivos. El diagnostico en el rebaño o de forma individual en los toros y vacas depende de la demostración precisa de T. foetus en el cultivo. Dos técnicas de cultivo se han empleado con éxito con resultados consistentes: en medio in vitro de Diamante, preparados específicamente para el cultivo de T. foetus, y el sistema de cultivo TF InPouch (BioMed Diagnostics, San Jose, CA). Este último es una bolsa de plástico muy práctica para uso en campo que contiene un medio de propiedad con una vida útil de 12-15 meses. Otras técnicas de diagnóstico, incluidos los métodos serológicos y las sondas de ADN carecen de la sensibilidad necesaria para el diagnóstico eficaz en la actualidad. Tanto Tritrichomona foetus como Campylobacter fetus pueden identificarse a partir de muestras colectadas del material prepucial y semen de toros y de mucus cérvico-vaginal y descargas uterinas de vacas y vaquillonas. Pancreatic Digest of Casein 15.0gm Yeast Extract 12.0gm Glucose 5.5gm Sodium Chloride 2.5gm L-Cystine 0.5gm Sodium Thioglycollate 0.5gm Gentamicin Amphotericin B 80.0mg 2.0mg Penicillin G 1,000,00 0U Horse Serum 120.0ml Agar 0.75gm Ingredients per 880ml of deionized water:* Final pH 7.0 +/- 0.3 at 25 degrees C. Hasta la actualidad no existen agentes terapéuticos eficaces contra la Tricomoniasis bovina, pero numerosos tratamientos fueron ensayados por investigadores argentinos e internacionales . Drogas como el dimetridazole, metronidazole o nitrimidazina fueron administradas en toros por vía oral, sistémica y local. Sin embargo, el uso indiscriminado o erróneo en condiciones de campo de dicha droga, hizo que se detectaran fallas en la efectividad terapéutica y presencia de cepas de T. foetus quimioresistentes. A su vez, las drogas tricomonicidas no están exentas de toxicidad siendo sospechosas de poseer algunas de ellas actividad cancerígena. Además, dichas drogas no se encuentran extensamente elaboradas por la industria y algunas no están aprobadas legalmente para su uso en bovinos . Recientemente, se reportó una considerable eficacia tricomonicida in vitro, sobre T. foetus y Trichomonas vaginalis, de un nuevo agente terapéutico denominado péptido d-hecate; sin embargo, se desconoce su desempeño en situaciones reales. Infusiones de lugol, cloramina, nitrato de plata, Nitroimidazoles por vía oral. En los últimos años, gracias a la identificación y purificación de un antígeno superficial de T. foetus denominado Tf 1.17 fue desarrollada una nueva vacuna experimental (BonDurant y col. 1993; Anderson y col. 1996; Corbeil y col. 1998). Tf 1.17 es un antígeno glicoproteíco presente en cepas de T. foetus de diferentes regiones geográficas del mundo. Además, estudios in vitro mencionan que anticuerpos monoclonales contra Tf 1.17 fueron capaces de inmovilizar, aglutinar, evitar la adhesión celular y destruir por la vía del complemento a T. foetus. Se desconoce la eficacia en condiciones naturales de una vacuna contenedora de Tf 1.17, pero su aplicación en vaquillonas desafiadas experimentalmente con T. foetus evidenció una pronta liberación de la infección, protección contra la inflamación y producción de IgA específicas en las secreciones genitales. Aunque no es probable, la transmisión es posible gracias a la inseminación artificial con esperma congelado. El organismo normalmente no habitan en la uretra, pero podría encontrarse en el semen si el líquido drenado del prepucio infecciosas en la vagina artificial, en el momento de recogida de esperma. Las tricomonas pueden sobrevivir las técnicas de dilución y congelación y descongelación, junto con los espermatozoides, aun así la IA es un método recomendado para tratar con un rebaño infectado si se realiza con la técnica adecuada y con semen de empresas que prueben regularmente a sus toros .