QUÍMICA FÍSICA AVANZADA Convocatoria Junio 2º Parcial 9
Anuncio

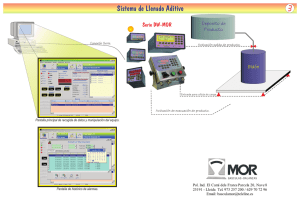
QUÍMICA FÍSICA AVANZADA Convocatoria Junio 2º Parcial 9-6-2005 APELLIDOS..............................................................................NOMBRE....................................... GRUPO: ............... ========================================================================= NOTA : No se permite el uso de libros, formularios, solucionarios o cualquier otra documentación. 1. La enzima acyl-CoA-dehidrogenasa cataliza el primer paso de la β-oxidación de los ácidos grasos, tal y como aparece en el siguiente esquema: O N N NH NH N N Ha O O O Ha H O C1 C1 C2 Hb O- N N SCoA C2 SCoA H O- O O Glu OHb Glu La siguiente figura muestra la superficie de energía potencial para este proceso en función de la distancia entre el carbono 1 y el hidrógeno a (R1) y la distancia carbono 2- hidrógeno b (R2). Tenga en cuenta que las líneas isoenergéticas aparecen espaciadas cada 2 kcal/mol y las distancias vienen en angstroms. 1.5 3.0 1 R1 0.5 2.0 0 -0.5 1.5 -1 1.0 -1.5 -1 1.0 -0.5 0 1.5 R2 0.5 1 2.0 1.5 1.1 Indique la geometría (R1 y R2) y la energía de las estructuras estacionarias (reactivos, productos, intermedios y estructuras de transición) que aparecen sobre la superficie de energía potencial. 1.2 Dibuje la evolución de la energía con la coordenada de reacción, mostrando los valores aproximados de la energía de activación y de reacción. 1.3. Calcule la magnitud del efecto cinético isotópico a 25º C cuando uno de los hidrógenos transferidos durante la reacción se sustituye por deuterio sabiendo que la frecuencia de vibración del enlace C-H es de 2800 cm-1.(suponga que la masa atómica de la molécula es mucho mayor que la del hidrógeno y/o deuterio). 1.4. Sabiendo que la etapa de reacción es monomolecular y que la entropía de activación a 25ºC es de -8.5 cal/mol K, determine el factor preexponencial de Arrhenius en la constante de velocidad (Nota, ΔH ‡ = E a − nRT , siendo n la molecularidad). 2. Resuelva las siguientes cuestiones 2.1. Se preparan las siguientes disoluciones acuosas a) NaCl 1M; b) Acido oleico 10-3M; c) agua pura; d) Acetona 10-3 M. Ordene las disoluciones de mayor a menor concentración de exceso superficial de soluto.(Nota: suponga que la interfase presenta comportamiento ideal) 2.2. Comente de forma breve pero razonada la siguiente afirmación: “Es posible tener vapor de agua sobresaturado porque en las primeras gotas microscópicas de agua líquida la tensión superficial alcanza valores muy altos” 2.3. Comente de forma breve pero razonada la siguiente afirmación: “Las dispersiones de coloides se inestabilizan al añadir electrolito debido a que aumenta la repulsión entre las partículas coloidales” 2.4. En un electrómetro capilar con un disolución de NaCl 1M se determina el máximo electrocapilar a -0,5 V. Se realizan medidas de tensión superficial a distintos potenciales a) V=-0,6V; b) V=-0,5V; c) V=0,4V d) V=-0,7V. De acuerdo con el modelo de doble capa difusa ordenar de mayor a menor el resultado de la medida de la densidad de carga superficial sobre el electrodo de mercurio. 3. Se estudió experimentalmente la reacción de hidrogenación de etileno sobre un catalizador de níquel: C2H4 (g) +H2 (g) ↔ C2H6 (g). Partiendo de reactivos puros se midió la velocidad inicial v0 (con unidades de atm s-1g-1) en función de la presión inicial de etileno P0 (atm), manteniéndose constante la presión de hidrógeno a 2,5 atm. Los resultados, a dos temperaturas distintas, se ajustaron de la siguiente forma: 1 25,51 T=300 º C = + 28,57 v0 P0 1 17,11 = + 3,20 T=360º C v0 P0 3.1. Considerando que el hidrógeno reacciona sin disociación ni adsorción y que la adsorción del producto es despreciable, determinar las expresiones de la velocidad inicial en función de las presiones de reactivos en el caso de que la etapa controlante sea la adsorción de etileno o la reacción superficial. Comparando con los datos experimentales, determinar cuál es la etapa limitante y los valores de las constantes que aparezcan en las ecuaciones cinéticas a la dos temperaturas de trabajo. 3.2. ¿Cuál será la energía de activación de la reacción global en los límites de presiones iniciales de etileno muy bajas y muy altas? 3.3. ¿Qué significado tiene una energía de activación negativa? ¿Cómo podría conseguirse, para esta reacción, una energía de activación negativa? ¿Cómo podría interpretarse una energía de activación negativa en esta reacción a partir del mecanismo de reacción propuesto? 4. Conteste de forma breve pero razonada a las siguientes cuestiones. 4.1.- En un recipiente de 1L a 298 K se introduce una cierta cantidad de adsorbente sólido. Si la constante de adsorción es de 0.8 atm-1, ¿qúe presión de gas será necesaria para que la fracción de recubrimiento alcance el 50%?. Si el volumen necesario para cubrir la monocapa es de 250 cm3 (en condiciones normales), ¿qué tanto por ciento del gas total se encuentra adsorbido?. Suponga válida la isoterma de Langmuir. 4.2. Determinar el peso molecular promedio en número de una muestra de poliestireno que presenta un peso molecular promedio en peso de 375.500 g/mol y un índice de polidispersidad de 1,5. Ordena de mayor a menor los pesos moleculares promedio en peso, viscoso, en número, z y z+1. 4.3.- Señalar sin ambigüedad la respuesta correcta (2 puntos). Una respuesta errónea puntuará como -0.5 puntos: La temperatura de transición vítrea es aquella que: (a) es característica de los polímeros cristalinos. (b) por bajo de la cual los compuestos poliméricos están en estado sólido rígido. (c ) la macromolécula presenta sus dimensiones sin perturbar. (d) es característica de los polímeros termoestables mientras que no existe en polímeros termoplásticos 4.4.- En general, en un proceso de quimisorción: (a) La entalpía de adsorción es negativa y la energía de activación es nula (b) La energía de activación es negativa y la entalpía de adsorción es positiva. (c ) La entalpía de adsorción es negativa y la energía de activación es positiva. (d) La energía de activación es nula y la entalpía de adsorción es nula 4.5.- En general, en un proceso de fisisorción: (a) La velocidad es menor que en un proceso de quimisorción. (b) Si aumenta la presión del gas no se produce la condensación, al contrario que en la quimisorción. (c ) Los productos que se desorben son distintos de los adsorbidos. (d) En valor absoluto, la entalpía de adsorción es menor que en un proceso de quimisorción. Fórmulas q kT kr = h qB ‡ ⎛ Δε ‡ NA V exp⎜⎜ − 0 qC ⎝ kT NA V NA V ‡ kT 0 1 − n (C ) exp⎛⎜⎜ − ΔG h ⎝ RT ⎛ ∂γ ⎞ ⎜ ⎟ = −RTΓ ⎝ ∂ ln c ⎠ kr = γ = γ max − ⎞ ⎟⎟ ⎠ ⎞ ⎟⎟ ⎠ ε 2x D ν = φe 2 1 2π K μ ∂ ln kr ∂T ∂ ln K ΔH = RT 2 ∂T E a = RT 2 Constantes y factores de conversión. 1 Debye = 3.335 64 10 -30 Cm 1 cal = 4.184 J R=8.31451 JK-1mol-1 ε0 = 8.8541878 10-12 C2N-1m-2 NA=6,02214 1023 mol-1 h = 6.62608 10-34 Js k=1.38066 10-23 JK-1 c=2,9979 108 m s-1 Pº=105 Pa