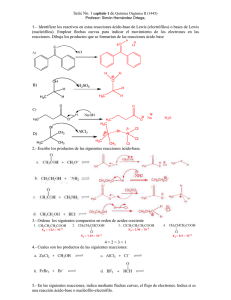
1. conceptos de ácido y base
Anuncio

REACCIONES ÁCIDO-BASE 1. 2. 3. 4. 5. 6. 7. Conceptos de ácido y base. Fuerzas de ácidos y bases. Concepto de pH. Hidrólisis. Disoluciones reguladoras. Volumetrías ácido-base. Indicadores. Química 2º bachillerato Reacciones ácido-base 1 0. CONOCIMIENTOS PREVIOS Los conocimientos previos que son necesarios dominar y ampliar son: • Los iones. • El enlace covalente e iónico. • El equilibrio. • La constante de equilibrio. Química 2º bachillerato Reacciones ácido-base 2 1. CONCEPTOS DE ÁCIDO Y BASE BASES: ÁCIDOS: • Tienen sabor agrio. • Son corrosivos para la piel. • Enrojecen ciertos colorantes vegetales. • Atacan a los metales desprendiendo H2. • Disuelven sustancias • Pierden sus propiedades al reaccionar con bases. Química 2º bachillerato • Tiene sabor amargo. • Suaves al tacto pero corrosivos con la piel. • Dan color azul a ciertos colorantes vegetales. • Precipitan sustancias disueltas por ácidos. • Disuelven grasas. • Pierden sus propiedades al reaccionar con ácidos. Reacciones ácido-base 3 1. CONCEPTOS DE ÁCIDO Y BASE Según la teoría de Arrhenius: •Ácido: sustancia que al disolverse en una disolución acuosa se disocia produciendo protones (H+) y aniones (iones negativos). HA H A H 2O •Base: sustancia que al disolverse en una disolución acuosa se disocia produciendo hidróxilos (HO-) y cationes (iones positivos). BOH B HO H 2O La neutralización (reacción entre un ácido y una base) sería: H HO H 2O Química 2º bachillerato Reacciones ácido-base 4 1. CONCEPTOS DE ÁCIDO Y BASE Según la teoría de Brönsted-Lowry: •Ácido: sustancia que cede protones (a una base). •Base: sustancia que acepta protones (a un ácido) La neutralización es una reacción de transferencia de protones (surge la idea del par ácido-base conjugado): HA B A HB En una disolución acuosa tengo: A1 B2 B1 A2 HA H 2O A H 3O B H 2O BH HO Química 2º bachillerato Reacciones ácido-base 5 1. CONCEPTOS DE ÁCIDO Y BASE Los ácidos pueden ser: • Monoprótico (ceden un protón). • Diprótico (ceden dos protones). … • Poliprótico (ceden n protones). Los iones que encontramos son: • H3O+ iones hidronio u oxonio. • HO- iones hidróxido, oxidrilo o hidróxilo. Química 2º bachillerato Reacciones ácido-base 6 1. CONCEPTOS DE ÁCIDO Y BASE Según la teoría de Lewis: •Ácido: sustancia capaz de aceptar y compartir un par de e(aportados por una base). •Base: sustancia capaz de ceder y compartir un par de e(aceptados por un ácido). La reacción de neutralización consiste en la formación de un enlace covalente coordinado: H H O H O H Química 2º bachillerato Reacciones ácido-base 7 1. CONCEPTOS DE ÁCIDO Y BASE Una sustancia anfótera es una sustancia capaz de comportarse como ácido y como base en función de con quién reaccione. HO HO C C CH2 O C O + H2O - O C O HO + HO - C - C CH2 O OH O O C CH2 O - + H2O O CH2 O C O O - + H3O + HA H 2O A H 3O B H 2O BH HO Química 2º bachillerato Reacciones ácido-base 8 1. CONCEPTOS DE ÁCIDO Y BASE Un anfolito es una sustancia capaz de experimentar simultáneamente dos disociaciones electrolíticas de signo contrario, actúa simultáneamente como un ácido y como una base. O O C OH R HC C O - R HC NH2 + NH3 H 2O H 2O H3O HO Química 2º bachillerato Reacciones ácido-base 9 1. CONCEPTOS DE ÁCIDO Y BASE Química 2º bachillerato Reacciones ácido-base 10 EJERCICIO-EJEMPLO a) Aplicando la teoría de Brönsted-Lowry y la de Arrhenius, explique razonadamente, utilizando las ecuaciones químicas necesarias, si las siguientes especies químicas se comportan como ácidos o como bases: KOH, NH3, CH3-COOH, CN–, HCO3–. b) Señale en cada caso la base o el ácido conjugado. Química 2º bachillerato Reacciones ácido-base 11 RELACIÓN DE EJERCICIOS ÁCIDOS Y BASES Química 2º bachillerato Reacciones ácido-base 12 2. FUERZAS DE ÁCIDOS Y BASES Para un ácido tengo: HA H 2O A H 3O A H 3O Ke Ka HA •Un ácido fuerte está completamente disociado en una disolución diluida (↑Ka, α≈1). HA H A H 2O •Un ácido débil está parcialmente disociado en una disolución diluida (↓Ka,α<1) . Pueden ser fuertes o débiles. HA H A H 2O Química 2º bachillerato c - - - c c c - - c-x X X c(1-α) c α Reacciones ácido-base cα 13 2. FUERZAS DE ÁCIDOS Y BASES Ácido fuerte [HA] [A–] Ácido débil [H+] [HA] [HA] [A–] Química 2º bachillerato Reacciones ácido-base [H+] 14 2. FUERZAS DE ÁCIDOS Y BASES HO B Para un base tengo: K e Kb B H 2O BH HO BOH •Una base fuerte está completamente disociado en una disolución diluida (↑Kb, α≈1). •Una base débil está parcialmente disociado en una disolución diluida (↓Kb, α<1) . Pueden ser fuertes o débiles. Química 2º bachillerato BOH B HO H 2O c - - - c c BOH B HO H 2O c - - c-x X X c(1-α) c α Reacciones ácido-base cα 15 2. FUERZAS DE ÁCIDOS Y BASES Cuanto más fuerte sea un ácido más débil será su base conjugada (y viceversa). H 2O H 2O H 3O HO HA H 2O A H 3O A H 2O HA HO Química 2º bachillerato K w H 3O HO 1014 A H 3O Ka HA K a Kb K w HA HO Kb A Reacciones ácido-base 16 2. FUERZAS DE ÁCIDOS Y BASES El grado de disociación (α) es el cociente entre los moles que se han disociado y los moles iniciales de soluto. Es el tanto por uno de los moles que reaccionan. Varía entre o (una reacción nula) y 1 (una reacción total), aunque a veces se da como un %. El grado de disociación puede variar en función del disolvente. Química 2º bachillerato Reacciones ácido-base 17 2. FUERZAS DE ÁCIDOS Y BASES Un ácido fuerte es aquel que, en disolución acuosa, está totalmente disociado. Un ácido débil es aquel que, en disolución acuosa, está parcialmente disociado. Es análogo para las bases. Cuando hablamos de un ácido fuerte donde su base conjugada es débil se refiere aun ácido fuerte entre los débiles (ya que uno fuerte de verdad no da la reacción inversa de su base). Es análogo para las bases. Química 2º bachillerato Reacciones ácido-base 18 2. FUERZAS DE ÁCIDOS Y BASES ÁCIDOS FUERTES BASES FUERTES HCl Hidróxidos del grupo 1 HBr LiOH NaOH KOH RbOH CsOH HI HNO3 Hidróxidos del grupo 2 (excepto Be) H2SO4 Mg(OH)2 Ca(OH) 2 Sr(OH) 2 Ba(OH) 2 HClO4 Química 2º bachillerato Reacciones ácido-base 19 EJERCICIO-EJEMPLO Calcula la concentración de protones y de iones hidroxilos de las siguientes disoluciones: a) 250 ml de HCl 0,1 M b) 250 ml de HClO 0,1 M si su Ka = 3,2 · 10–8 Química 2º bachillerato Reacciones ácido-base 20 RELACIÓN DE EJERCICIOS FUERZAS DE ÁCIDOS Y BASES Química 2º bachillerato Reacciones ácido-base 21 3.CONCEPTO DE pH El pH es una forma de medir la concentración de protones de forma sencilla: pH log H 3O pH pOH 14 pOH log HO La disolución puede ser: [H3O+] < [HO-] pH > 7 pOH < 7 •Neutra: [H3O+] = [HO-] pH = 7 pOH = 7 [H3O+] > [HO-] pH < 7 pOH > 7 •Básica: •Ácida: . Química 2º bachillerato Reacciones ácido-base 22 3.CONCEPTO DE pH Las concentraciones de protones y de iones hidróxilos son inversas. En realidad nos referimos al tipo de iones que predominan en la disolución (siempre hay de los dos presentes), cuanto de más hay de uno respecto del otro. Al igual que el pH también tengo: pK=-log(K) Las disoluciones básicas también se denominan alcalinas. Química 2º bachillerato Reacciones ácido-base 23 3.CONCEPTO DE pH Química 2º bachillerato Reacciones ácido-base 24 EJERCICIO-EJEMPLO En un laboratorio se dispone de cinco matraces que contiene cada uno de ellos disoluciones de las que se tiene la siguiente información: a) b) c) d) e) pH = 7 [H3O+] = 10–3 pOH = 2 [OH–] = 10–6 pH = 1. Ordena dichos matraces de mayor a menor acidez. Realizar una tabla indicando el pH, el pOH y las concentraciones de protones y de iones hidroxilos de cada apartado. Química 2º bachillerato Reacciones ácido-base 25 EJERCICIO-EJEMPLO Se sabe que 100 ml de una disolución de ácido oxoclorico (I) (hipocloroso) que contiene 1,05 gramos, tiene un pH de 4,1. Calcula: a) La constante de disociación del ácido. b) El grado de disociación. Masas atómicas: Cl: 35,5; O: 16; H: 1. Química 2º bachillerato Reacciones ácido-base 26 EJERCICIO-EJEMPLO A 25ºC una disolución 0,1 M de amoniaco tiene un pH de 11,12. Determina la constante de basicidad del amoniaco y la de acidez del ion amonio. Química 2º bachillerato Reacciones ácido-base 27 RELACIÓN DE EJERCICIOS pH Química 2º bachillerato Reacciones ácido-base 28 4. HIDRÓLISIS Toda sal procede de una combinación de ácido con una base: HA BOH AB H 2O La hidrólisis es el proceso por el cual iones de una sal reaccionan con las moléculas de agua para regenerar el ácido o la base con la que están emparentados: A H 2O HA HO AB A B H 2O B H 2O BOH H Química 2º bachillerato Reacciones ácido-base 29 4. HIDRÓLISIS En la hidrólisis puedo encontrar diversos casos según la naturaleza de la sal: • Sal procedente de un ácido fuerte y de una base fuerte: La disolución es neutra. • Sal procedente de un ácido fuerte y de una base débil: La disolución es ácida. • Sal procedente de un ácido débil y de una base fuerte: La disolución es básica. • Sal procedente de un ácido débil y de una base débil: La disolución depende del valor de las constantes. Química 2º bachillerato Reacciones ácido-base 30 4. HIDRÓLISIS Sal procedente de un ácido fuerte y de una base fuerte: la disolución es neutra. A H 2O HA HO AB A B H 2O B H 2O BOH H Química 2º bachillerato Reacciones ácido-base 31 4. HIDRÓLISIS Sal procedente de un ácido fuerte y de una base débil: la disolución es ácida. A H 2O HA HO AB A B H 2O B H 2O BOH H KH Química 2º bachillerato BOH H O 3 Reacciones ácido-base B Ka 32 4. HIDRÓLISIS Sal procedente de un ácido débil y de una base fuerte: la disolución es básica. A H 2O HA HO AB A B H 2O B H 2O BOH H HO AH KH K b A Química 2º bachillerato Reacciones ácido-base 33 4. HIDRÓLISIS Sal procedente de un ácido débil y de una base débil: la disolución depende del valor de las constantes. A H 2O HA HO AB A B H 2O B H 2O BOH H Química 2º bachillerato Reacciones ácido-base 34 4. HIDRÓLISIS • Sales procedentes de un ácido fuerte y una base fuerte • - Como por ejemplo: NaNO3 o CaCl2. - Ni el anión ni el catión experimentan hidrólisis. - Sus disoluciones son neutras (pH=7). • Sales procedentes de un ácido débil y una base fuerte - Como por ejemplo: Na2CO3 o KCN. - Sólo se hidroliza el anión, dando iones OH-. - Sus disoluciones son básicas (pH>7). Química 2º bachillerato Sales procedentes de fuerte y una base débil un ácido - Como por ejemplo: NH4NO3 o FeCl3. - Sólo se hidroliza el catión, dando iones H3O+. - Sus disoluciones son ácidas (pH>7). • Sales procedentes de un ácido débil y una base débil - Como por ejemplo: NH4CN o CaCl2. - Se hidrolizan tanto el anión como el catión. - La disolución es ácida o básica según qué ion se hidrolice en mayor grado. Reacciones ácido-base 35 EJERCICIO-EJEMPLO Cómo será el pH de una disolución de 150 ml de NaClO 0,1 M. ¿Cuánto valdrá? Ka (HClO) = 3,2·10–8 Calcula el pH de una disolución 0,7 M de KCN sabiendo que Ka de HCN es de 7,2·10–10 . Química 2º bachillerato Reacciones ácido-base 36 RELACIÓN DE EJERCICIOS HIDRÓLISIS Química 2º bachillerato Reacciones ácido-base 37 5. DISOLUCIONES REGULADORAS Una disolución reguladora, amortiguadora, buffer o tampón son soluciones resistentes a la variación de pH, varían muy poco su pH cuando se les añade una pequeña cantidad de un ácido o una base. Según de lo que partimos hay dos tipos: •Partimos de un ácido débil y sal (proporciona su base conjugada y procede de una base fuerte): sal 0 pH pK a log acido 0 •Partimos de una base débil y sal (proporciona su ácido conjugado y procede de un ácido fuerte): sal 0 pOH pKb log base 0 Química 2º bachillerato Reacciones ácido-base 38 5. DISOLUCIONES REGULADORAS © Ed. Santillana Química 2º bachillerato Reacciones ácido-base 39 EJERCICIO-EJEMPLO ¿Cuál será el pH de una disolución formada por 100 ml de acetato sódico 0,250 M, 25 ml de ácido acético del 12 % y g/ , densidad 1,06 y cantidad ml suficiente de agua para completar 250 ml? Masas atómicas: Na: 23; C: 12; 0:16; H: 1; Ka (CH3COOH) = 1,8· 10–5. Química 2º bachillerato Reacciones ácido-base 40 RELACIÓN DE EJERCICIOS TAMPONES Química 2º bachillerato Reacciones ácido-base 41 6. VOLUMETRÍAS ÁCIDO-BASE Una volumetría o valoración es el proceso por el cual se determina la concentración de un ácido o de una base a través de la reacción de neutralización con otra disolución de concentración conocida (de una base o de un ácido respectivamente). En la reacción de valoración el número de equivalentes del ácido y de la base tienen que ser el mismo. Química 2º bachillerato Reacciones ácido-base 42 6. VOLUMETRÍAS ÁCIDO-BASE La normalidad de la disolución es una concentración que nos indica el número de equivalentes de soluto por litro de disolución. El equivalente es una medida de cantidad de sustancia que nos indica la reactividad de la sustancia. Su valencia depende del número de iones que utilice en la reacción específica (y no del número de iones totales que pueda llegar a utilizar). Química 2º bachillerato Reacciones ácido-base 43 6. VOLUMETRÍAS ÁCIDO-BASE El procedimiento consiste en: 1. Medir con exactitud el volumen de la disolución de concentración desconocida. 2. Añadir el indicador o pHmetro. 3. Añadir, gota a gota, la disolución de concentración conocida hasta el viraje (punto final o punto de equivalencia) del indicador o pHmetro. 4. Medir el volumen gastado de la disolución conocida. Química 2º bachillerato Reacciones ácido-base 44 6. VOLUMETRÍAS ÁCIDO-BASE pH 12 10 8 Zona de viraje fenolftaleína 6 4 2 20 Química 2º bachillerato 40 Reacciones ácido-base 60 V NaOH(ml) 45 6. VOLUMETRÍAS ÁCIDO-BASE Los cálculos estequiométricos que hay que realizar son: m H n A n B OH m Am Bn m n H 2O VA N A VB N B Química 2º bachillerato eqA eqB Reacciones ácido-base 46 6. VOLUMETRÍAS ÁCIDO-BASE Las valoraciones ácido-base se basan en un cambio brusco de pH que tiene lugar en las inmediaciones del punto de equivalencia. El pH del punto de equivalencia depende de las especies presentes. El pH en el punto de equivalencia no es necesariamente 7 Química 2º bachillerato Reacciones ácido-base 47 6. VOLUMETRÍAS ÁCIDO-BASE Química 2º bachillerato Reacciones ácido-base 48 6. VOLUMETRÍAS ÁCIDO-BASE Química 2º bachillerato Reacciones ácido-base 49 EJERCICIO-EJEMPLO Determinar la concentración de una disolución de 15 ml de ácido clorhídrico valorada usando rojo de metilo con una disolución 0.01 M de amoniaco donde se han gastado 272 ml. Masas atómicas: H:1; O:16; N:14: Cl:35.5. Química 2º bachillerato Reacciones ácido-base 50 EJERCICIO-EJEMPLO 250 ml de ácido nítrico concentrado del 32 % y densidad 1,19 g/ml, se colocan en un matraz aforado de 1 litro y se añade agua destilada hasta enrasar. ¿Cuántos ml de la disolución diluida de ácido nítrico serán necesarios para neutralizar 50 ml de una disolución de NaOH cuyo pH es 13,93? Masas atómicas: H: 1; O: 16; N: 14. Química 2º bachillerato Reacciones ácido-base 51 7. INDICADORES Un indicador es un ácido o una base débil que se caracteriza por tener distinto color en torno a pH=pKin por lo que debe escogerse el indicador cuyo punto final esté próximo al punto de equivalencia de la valoración. El indicador apropiado para una valoración será aquel que cambie de color en el intervalo de pH donde está el punto de equivalencia. El pHmetro es un instrumento capaz de medir el pH y sus cambios. Química 2º bachillerato Reacciones ácido-base 52 7. INDICADORES In- (aq) + H3O+ (aq) Forma básica (color 2) HIn (aq) + H2O (l) Forma ácida (color 1) La constante de acidez del indicador es: KIn = [In-] [H3O+] [HIn] [HIn] [H3O+] = [In-] KIn Con esta expresión se puede interpretar el “color” que presentará el indicador según el pH de la disolución. Así se tiene que cuando la concentración de H3O+ : • Sea mayor que K In pH << pK In [HIn] >> [In-] Color de la forma ácida • Sea menor que K In pH >> pK In [HIn] << [In-] Color de la forma básica • Sea igual que K In Química 2º bachillerato pH = pK In [HIn] = [In-] Color intermedio Reacciones ácido-base 53 7. INDICADORES La zona de viraje de un indicador es: pH = pK ± 1 EJEMPLOS DE INDICADORES ÁCIDO-BASE Nombre del indicador Azul de timol Color forma Color forma ácida básica Rojo Amarillo Rango pH de cambio color 1,2-2,8 pKin 1,7 Naranja de metilo Rojo Amarillo 3,2-4,2 3,4 Rojo de metilo Rojo Amarillo 4,8-6,0 5,0 Tornasol Rojo Azul 5,0-8,0 6,5 Azul de bromotimol Amarillo Azul 6,0-7,6 7,1 Azul de timol Amarillo Azul 8,0-9,6 8,9 Fenolftaleína Incoloro Rosa 8,2-10,0 9,4 Rojo Púrpura 11,0-12,4 11,7 Alizarina Química 2º bachillerato Reacciones ácido-base 54 RELACIÓN DE EJERCICIOS VOLUMETRÍAS Química 2º bachillerato Reacciones ácido-base 55