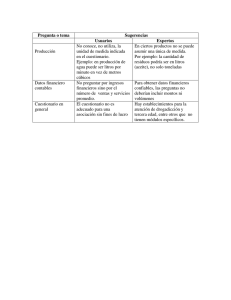
programa
Anuncio

1 UNIVERSIDAD DE SAN CARLOS DE GUATEMALA CENTRO UNIVERSITARIO DE OCCIDENTE DIVISIÓN CIENCIAS DE LA SALUD CARRERA DE MEDICO Y CIRUJANO PRIMER AÑO PLAN DE CURSO LABORATORIO DE QUÍMICA 2016 OBJETIVO GENERAL 1. Que el estudiante practique el contenido del programa teórico de química. 2. Que experimente los diferentes procesos químicos 3. Que conozca las técnicas básicas del laboratorio de química. 4. Que adquiera habilidad y destreza para los próximos laboratorios de los años siguientes. CONTENIDO OBJETIVOS LABORATORIO 1 1. Que el estudiante comprenda los cuidados, 1. INVESTIGACIÓ peligros y N: Medidas de comportamiento dentro seguridad en el del Laboratorio de laboratorio e Química. instrumentos 2. Presentar al estudiante de laboratorio. de nuevo ingreso el laboratorio de Química y 2. PRACTICA: ponerlo en contacto con Balanza e las instalaciones físicas y Instrumental equipo que básicamente volumétrico y habrá de usar. densidad. 3. Implementar el desarrollo de las siguientes prácticas de laboratorio. 4. Lograr que el estudiante principie a relacionarse con los instrumentos de laboratorio, los identifique unitariamente por su nombre y los clasifique en base de la sustancia de la cual están fabricados. 5. Usar de manera correcta la balanza del laboratorio. 6. Tomar y/o medir el peso de sustancias sólidas, liquidas y ACTIVIDADES 1. 2. 3. 4. Examen corto Clase magistral. Hoja de trabajo. Cuestionario. PROGRAMACIÓN Laboratorio No 1, Semana 1 , 2, 3 y 4 Semana 5 Recepción y calificación de trabajos e informes de laboratorio Primer Examen Parcial RECURSOS UTILIZADOS 1. 2. 3. 4. 5. 6. 7. 8. Biblioteca Guía de laboratorio Espátula Mechero Balanza Erlenmeyer Vidrio de reloj Capsula de porcelana 9. Varilla de agitación 10. Soporte universal 11. Rejilla de asbesto 12. Balón de fondo plano 13. Pizeta. 14. Beaker. 15. Pnzas. 16. Mechero de Bunsen 17. Buretas. 18. Probetas. 19. Balanza semianalítica 20. Vidrio Reloj 21. Beaker de 100 ml. 22.Balones aforados de 100 ml. Y 1000 ml 23.Probetas de 100 ml. 24.Agitador. INDICADORES 1. Guía de 2. 3. 4. 5. laboratorio. Cuadernos de apuntes de los estudiantes Exámenes cortos. Cuestionario. Hoja de trabajo RESULTADOS ESPERADOS 1. Alumnos de las diferentes secciones mejor preparados y capacitados para resguardar su seguridad, uso de instrumentos y verificar su teoría con la práctica. 2. El alumno utiliza correcta y adecuadamente balanzas granatarias, material volumétrico como, por ejemplo, vasos, matraces erlenmeyer, matraces aforados, probetas, pipetas o buretas entre otras. 2 gaseosas. 7. Contactar de manera referencial algunas clases de balanzas. 8. Manejar el concepto del menisco. 9. Medir distintos volúmenes de agua. 10.Usar de manera correcta: la bureta y la pipeta. 11.Tarar distintos instrumentos. 12.Pesar sustancias en el estado sólido y líquido. 13.Aplicar los conceptos de masa y volumen para el cálculo de la densidad de algunas sustancias. 14.Continuar desarrollando la destreza para el manejo de la balanza, la probeta, la bureta y la pipeta. 15.Utilizar adecuadamente el concepto de tara. 16.Pesar y medir el volumen de sustancias en estado de solido compactos regulares, irregulares y en polvo. 17.Calcular la densidad de las sustancias señaladas en el objetivo anterior y la del agua. 25. Capsula de porcelana 1. Balanza 2. Varilla de agitación 3. Probeta de 100 ml 4. Probeta de 25 ml 5. Termómetro 6. Pinza para termómetro 7. Beaker de 250 ml 8. Erlenmeyer 250 ml 9. Núcleos de ebullición 10.Soporte universal 11.Anillo 12.Rejilla de asbesto 13.Estufa. 14.Piseta 3 18.Comparar la densidad del agua midiendo volúmenes con distintos instrumentos. 19.Pronosticar qué instrumento volumétrico es más exacto en base de la densidad del agua. LABORATORIO 2 1. Iniciar el estudio de la nominación de las sustancias 1. INVESTIGACI correspondientes al ÓN: mundo material Lenguaje Químico. inorgánico. 2. PRACTICA: 2. Encontrar mecanismos de auto-aprendizaje de Reacciones un tema que muchas Químicas y veces se da por solubilidad e descontado. insolubilidad 3. Descubrir la importancia y factores que que tiene el lenguaje químico para el afectan. desarrollo de la carrera. 4. Interiorizar las formas de clasificación de las sustancias químicas y las reglas del lenguaje químico. 5. Interpretar los símbolos y formulas propias del lenguaje químico. 6. Reconocer el nombre implícito tanto de un símbolo químico como en una fórmula química. 7. Escribir formulas químicas correspondientes a sustancias químicas inorgánicas. 8. Manejar con propiedad y adecuadamente la LaboratorioNo 2, 1. 1. Examen corto 2. Clase magistral. 2. 3. Hoja de Semana 6, 7, 8, Y 9 3. trabajo. 4. 4. Práctica. 5. 5. Cuestionario 6. 7. Semana 10 8. Recepción y 9. calificación de 10. trabajos e 11. informes de laboratorio Segundo Examen Parcial 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. Tabla periódica. Libro de texto. Calculadora. Fe S AgNO3 K2CrO4 Na2CO3 HCI NaOH Fenolftaleína CuSO4 Zn BaCl2 HCl HNO3 H2SO4. Nitrato de niquel (II) Sulfuro de litio Cloruro de plata Fosfato de rubidio Acetato de plomo (II) Carbonato de estroncio Bromuro de mercurio (I) Sulfato de magnesio Clorato de magnesio 1. Guía de 2. 3. 4. 5. 1. El alumno reconoce los laboratorio. símbolos químicos y Cuadernos de escribe formulas químicas. apuntes de los estudiantes 2. El alumno comprende que Exámenes las reacciones químicas se cortos. dan a diario en nuestra Cuestionario. vida. Hoja de trabajo 4 nomenclatura y la notación química. 9. Diferenciar un cambio físico de un cambio químico. 10.Observar cuáles de las manifestaciones expuestas en la introducción, ocurren en cada una de las reacciones químicas propuestas en el procedimiento. 11.Determinar a qué tipo de reacción pertenece cada una de las que llevarán a cabo en la práctica. 12.Verificar cualitativamente la solubilidad y la insolubilidad en agua, éter, n-hexano y alcohol etílico de los solutos: nitrato de sodio, carbonato de sodio, parafina, benceno y ácido acético. 13.Medir relativamente la velocidad de solubilidad en agua de una misma sustancia en distintas condiciones. 14.Verificar la solubilidad de una misma sustancia sólida en distintos solventes líquidos. 5 LABORATORI O 3 1. INV EST IGA CIÓ N: Pre para ción de solu cion es. 2. PRA CTI CA: Valo raci ón o titul ació n de solu cion es. 1. Examen corto 2. Clase magistral. usando el método 3. Hoja de directo. trabajo. Desarrollar habilidades 4. Práctica. para el manejo de los instrumentos usados en 5. Cuestionario la preparación de las soluciones. Calcular las concentraciones de las soluciones preparadas usando distintos tipos de unidades. Poner en práctica la información teórica recibida (se dará una inducción a ello) acerca del tema de soluciones. Incentivar su curiosidad natural. Descubrir la acidez o la basicidad de dos medicamentos populares. Manejar con propiedad los instrumentos que se usan para valorar o titular una solución. Apreciar cualitativamente la función de un indicador. Verificar la concentración de soluciones preparadas, usando el proceso de titulación Laboratorio No 3 Semana 11, 12, 13 y 14. 1. Preparar soluciones 2. 3. 4. 5. 6. 7. 8. 9. Semana 15 Recepción y calificación de trabajos e informes de laboratorio Tercer Examen Parcial 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. NaCl NaOH KOH HCl HNO3 H2SO4 Balanza Balón Aforado Pipetas Buretas Probetas Vidrio Reloj 13. Soporte universal Pinzas. Reactivos preparados en la práctica 8 Pipetas Buretas Probetas Soporte universal Pinzas Pipetas Buretas Probetas Soporte universal Pinzas 1. Guía de 2. 3. 4. 5. laboratorio. Cuadernos de apuntes de los estudiantes Exámenes cortos Cuestionario. Hoja de trabajo 1. El alumno prepara soluciones, calculando su concentración en las unidades adecuadas, así como el margen de error admisible en las mismas. 6 1. Que el estudiante LABORATORI O 4 1. INVESTI GACIÓN: Qué es la destilaci ón y diferente s tipos de destilaci ón. 2. PRACTIC A: Partes e instalaci ón de un equipo de destilaci ón y funciona miento. 2. se familiarice con proyectos de investigación. Ponga en práctica los conocimientos adquiridos en la teoría de química inorgánica y orgánica Examen corto Clase magistr al. Hoja de trabajo. Práctica Cuestionario. 1. Informe del 1. Computadora. 2. Cañonera. 3. Equipo de No 4 Semana 16, 17, 18 y 19. Semana 20 Recepción y calificación de trabajos e informes de laboratorio destilación 2. 3. 4. 5. 6. Cuarto Examen Parcial LABORATORIO 5 1. INVESTIGA CIÓN: Metabolism o de la glucosa 2. PRACTICA: Reacciones de Benedict Laboratori o 1. 2. comprenda las reacciones que ocurren 3. 4. durante el metabolismo 5. 1. Que el estudiante de la glucosa. Ya que la glucosa es la principal fuente de energía para el metabolismo celular. 2. Que el alumno 3. comprenda que un aumento de glucosa en la sangre se produce cuando se consumen alimentos con alto contenido de hidratos de carbono Conocer un método practico y sencillo Laboratorio Examen corto Clase magistral. No 5 Semana Hoja de trabajo. 21,22,23 y 24, Práctica. Semana 25 Cuestionario Notas finales de laboratorio Quinto Examen Parcial 1. Informe del 2. 3. 4. 5. 6. 1. El alumno se prepara autónomamente sobre la teoría de la destilación y la pone en práctica en el laboratorio. trabajo de investigació n. Guía de laboratorio. Cuadernos de apuntes de los estudiantes Exámenes cortos. Cuestionari o. Hoja de trabajo 1. El alumno conoce la trabajo de importancia de los investigación. alimentos que ingiere y sus efectos. Guía de laboratorio. 2. El alumno puede medir la Cuadernos de glucosa en orina a través apuntes de los de los indicadores. estudiantes Exámenes cortos. Cuestionario. Hoja de trabajo 7 para medir los niveles de glucosa en la orina. EVALUACIÓN: La nota máxima del laboratorio de Química es de 15 puntos netos, los cuales estarán distribuidos de la manera siguiente: Exámenes cortos…………………………………. 0.75 Práctica, reporte y cuestionario (Por grupo)………..…. 0.75 Asistencia y disciplina………………………………..….... 0.50 Esta nota es por Laboratorio Investigación y hojas de trabajo……………….………… 1.00 TOTAL……………… 3.00 Exámenes cortos: Estos se realizarán en los primeros 10 minutos de la práctica y comprenden contenidos de la hoja de trabajo y la guía de la práctica a realizar.. ● Reportes: El reporte comprende lo siguiente; Caratula, introducción, objetivos, contenido de la práctica, resultados, análisis de los resultados, análisis de error (si los hubiera) conclusiones recomendaciones y bibliografía. Este reporte lo debe de entregar una semana después de realizada la práctica. Deberán estar escritos a máquina o computadora en papel tamaño carta. NO SE ACEPTAN DESPUÉS DE LA FECHA PROGRAMADA. ● 8 HORARIO Y DISTRIBUCIÓN DE SECCIONES PARA EL LABORATORIO DE QUÍMICA HORARIO LUNES 13:00 A 15:00 A 15:00 A 17:00 MIÉRCOLES G JUEVES E C B 17:00 A 19:00 MARTES H F D K J VIERNES Calificar los reportes y exámenes cortos de la semana CATEDRÁTICO Ing. Pablo Estrada Lic. Jorge Mario Aguilar V I L Inga. Surama Cifuentes R. CATEDRÁTICOS: Lic. Jorge Mario Aguilar Coordinador de laboratorio de Química Secciones B D F H Ing. Pablo Estrada Secciones G E C A Inga. Agra. Surama Cifuentes Ruiz Secciones I J K L laboratoriodequimicamedicinacunoc.blogspot.com JMAV/ 18‐1‐16