INTRODUCCIÓN A LA
MINERALOGÍA Y
CRISTALOGRAFÍA
Descripción breve
Estudiar la historia de la mineralogía y comprender el concepto de mineral. Entender la
constitución interna de la materia cristalina. Comprender la cristalización de los
sistemas químicos minerales.
Ambar Yuridia Gomez Mellado
ambar_gom91@hotmail.com
Contenido
Introducción a la mineralogía. ................................................................................................ 2
Analizar la evolución histórica de la mineralogía ............................................................... 2
Definición de mineral ......................................................................................................... 3
Introducción a la cristalografía. .............................................................................................. 4
Desarrollo de la cristalografía ............................................................................................. 5
Procesos de cristalización. ...................................................................................................... 6
Estructura interna de los cristales. ......................................................................................... 7
Simetría Cristalina................................................................................................................... 8
Eje de simetría .................................................................................................................... 9
Plano de simetría. ............................................................................................................. 10
Centro de simetría. ........................................................................................................... 10
Rotación con inversión. .................................................................................................... 10
Sistemas cristalográficos. ................................................................................................. 11
Índices de Miller ................................................................................................................... 13
Formas cristalinas ................................................................................................................. 14
Nombre de las formas ...................................................................................................... 14
Hábito cristalino. .................................................................................................................. 15
Clases cristalográficas. .......................................................................................................... 15
.............................................................................................................................................. 17
.............................................................................................................................................. 17
Proyecciones Cristalinas. ...................................................................................................... 17
Introducción a la mineralogía.
La mineralogía es el estudio de las sustancias cristalinas que se encuentran en la naturaleza,
es decir los minerales. Un conocimiento sobre qué son los minerales, cómo se han formado
y dónde se encuentran es básico para la comprensión de los minerales que son responsables
de nuestra actual cultura tecnológica. Todos los artículos inorgánicos que se comercializan,
si no son minerales en sí mismos, son de origen mineral.
Analizar la evolución histórica de la mineralogía
El surgir de la mineralogía como una ciencia es relativamente reciente, pero la práctica de
las artes mineralógicas es tan antigua como la civilización humana. En las pinturas rupestres
realizadas por hombres primitivos ya se utilizaron pigmentos naturales hecho de hematite
roja y óxido de manganeso negro, y las herramientas de pedernal eran posesiones preciosas
durante la Edad de Piedra.
Al filósofo griego Theophrastus (372-287 a.C.) le debemos el primero trabajo escrito
sobre minerales.
Durante los 1300 años siguientes, los pocos trabajos que se publicaron sobre minerales
contenían más fábulas y ficción popular que información verídica.
El nacimiento de la mineralogía como ciencia, sería la publicación en el año 1556 del
libro De Re Metallica escrito por el médico alemán, Georgius Agricola. Este libro
relata con todo detalle la práctica de la minería de su época e incluye la primera
recolección de minerales.
En 1669 Nicolas Steno contribuyó notablemente al desarrollo de la cristalografía con
su estudio de los cristales de cuarzo. Observó que a pesar de las diferencias de
procedencia, tamaño, o constitución, los ángulos entre las caras correspondientes
eran constantes.
En 1780, Carangeot inventó un mecanismo (goniómetro de contacto) para la medida
de ángulos interfaciales de un cristal.
En 1783, Romé de L’Isle realizó medidas angulares en los cristales y formuló la lye
de la constancia del ángulo interfacial.
En 1784, René J. Hauy demostró que los cristales estaban construidos por
acumulación de pequeños bloques idénticos, a los que él llamó moléculas integrales.
A principios del siglo XIX sucedieron rápidos avances en el campo de la mineralogía.
En 1809, Wollaston inventó el goniómetro de reflexión, que permitió una alta
exactitud y medidas precisas de las posiciones de las caras del cristal. Estos datos
hicieron de la cristalografía una ciencia exacta.
En 1848, Berzelius, un químico suizo, y sus discípulos estudiaron la química de los
minerales y desarrollaron los principios de la actual clasificación química de los
mismos.
En 1815, el naturalista francés Cordier, observó a través de su microscopio,
fragmentados de mineral triturado sumergidos en agua.
En 1828, el escocés William Nicol, inventó un dispositivo de polarización que
permitió el estudio sistemático del comportamiento de la luz en las sustancias
cristalinas. El microscopio de luz polarizada es todavía, un instrumento
determinante y muy importante en los estudios mineralógicos.
A finales del siglo XIX, Ferodov, Schoenflies y Barlow, trabajando independientemente y casi
al mismo tiempo, desarrollaron las teorías para la simetría interna y la ordenación en el
interior de los cristales que fueron los fundamentos para el trabajo posterior en la
cristalografía de rayos X.
En 1912 en un experimento efectuado por Friedrich y Max von Laue, demostró que
los cristrales podían difractar los rayos X. De esta forma se probó por primera vez la
distribución ordenada y regular de los átomos en un material cristalino.
En 1914, fueron publicadas por W.H. Bragg y W.L. Bragg las primeras
determinaciones de la estructura de un cristal.
El equipo moderno de difracción de rayos X asociado a computadores especialmente
diseñados ha hecho posible la determinación relativamente rápida de las estructuras
altamente complejas de un cristal.
En 1960, el advenimiento del microensayo electrónico al comienzo de la década,
aplicado al estudio de la química de los minerales a nivel de microescala, es otro
instrumento muy importante que ahora se utiliza rutinariamente para el estudio de
la química mineral, compuestos sintéticos y vidrios.
Desde 1970, el microscopio electrónico de transmisión, puede aumentar la
arquitectura interna de los minerales en millones de veces, ha producido imágenes
visuales de gran potencia de las estructuras atómicas.
El campo de la mineralogía abarca ahora un área muy amplia de estudio que incluye rayos
X, electrones y difracción de neutrones por minerales, síntesis de minerales, física de
cristales, evaluación de la estabilidad termodinámica de minerales, petrografía (estudio de
rocas y minerales en secciones delgadas), petrología (estudio de rocas), petrología
experimental y aspectos de metalurgia y cerámica.
Definición de mineral
Un mineral es un sólido homogéneo por naturaleza con una composición química definida
(pero generalmente no fija) y una disposición atómica ordenada. Normalmente se forma
mediante un proceso inorgánico.
Cuando decimos por naturaleza estamos distinguiendo entre sustancias formadas por
procesos naturales.
La definición de mineral también establece que un mineral es un sólido homogéneo. Esto
significa que consta de una única sustancia sólida que no puede ser subdividida físicamente
en simples componentes químicos. La cualidad de sólido excluye a los gases y a los líquidos.
El hecho de que un mineral deba tener una composición química definida implica que éste
puede expresarse mediante una fórmula química específica. Por ejemplo, la composición
química del cuarzo se expresa de la forma SiO2; el cuarzo solo contiene a los elementos
químicos, silicio y oxígeno, y tiene una fórmula definida, por lo tanto se considera con
frecuencia como una sustancia pura. Sin embargo, la mayoría de los minerales no tienen
una composición perfectamente definida. La dolomita CaMg(CO3)2 no es siempre un
carbonato puro de Ca y Mg, ya que pueden contener cantidades considerables de Fe y Mn
en lugar de Mg. Como estas cantidades varían, se dice que la composición de la dolomita
oscila entre ciertos límites, y por lo tanto, no es fija.
Una disposición atómica ordenada indica la existencia estructural de un entramado de
átomos (o iones) ordenados según un modelo geométrico regular. Así, pues, como éste es
el criterio necesario para considerar un sólido cristalino, los minerales son cristalinos.
De acuerdo con la definición tradicional, un mineral se forma mediante procesos
inorgánicos. En la definición dada de mineral, hemos utilizado el adverbio normalmente
para poder incluir dentro del dominio de la mineralogía los pocos compuestos producidos
orgánicamente que se acoplan a la definición de mineral. El ejemplo más destacado es el
del carbonato cálcico de las conchas de los moluscos. La concha de una ostra y la perla que
ésta puede llevar en su interior están en su mayor parte constituidas por aragonito, que es
idéntico al mineral formado por procesos inorgánicos. Aunque diversas formas de CaCO3
(calcita, aragonito, vaterita) y monohidrocalcita, CaCO3 ∙ H2O, son los minerales biogénicos
(“minerales formados por organismos”) más comunes. Existen muchas otras especies
biogénicas, el opal (una forma amorfa del SiO2), la magnetita (Fe3O4), la fluorita (CaF2), así
como el azufre elemental, son ejemplos de minerales que pueden ser precipitados por
organismos.
Introducción a la cristalografía.
Los minerales, con pocas excepciones, poseen la distribución interna ordenada
característica de los sólidos cristalinos. Cuando las condiciones son favorables, pueden estar
limitados por caras planas y pulidas y adquirir formas geométricas regulares conocidas
como cristales. La mayor parte de los cristalógrafos emplean hoy en día el término cristal al
referirse a cualquier sólido con estructura interna ordenada, posea éste o no caras externas,
pues éstas, en general, no son más que un accidente de su desarrollo y su ausencia no
modifica en absoluto las propiedades fundamentales de un cristal. Podemos, por tanto,
trazar una definición más amplia de un cristal considerándolo como un sólido homogéneo
que posee un orden interno tridimensional de largo alcance. El estudio de los sólidos
cristalinos y las leyes que gobiernan su crecimiento, forma externa y estructura interna, se
denomina cristalografía.
Desarrollo de la cristalografía
Las primeras indicaciones sobre la regularidad de dislocación de las partículas materiales
esféricas que componen el cristal se hallan en los trabajos del célebre astrónomo J. Kepler
(año 1619) y de Robert Hooke (año 1665), inventor del microscopio.
En 1669, Nicolás Stenon, descubrió la primera ley fundamental de cristalografía, ley
de la constancia de los ángulos diedros entre las caras de los cristales.
En 1660, el científico holandés Christian Huyghens, estudiando las propiedades
ópticas de los cristales de la calcita (CaCO3), emitió la hipótesis de que las
propiedades observadas podrían ser explicadas por la estructura interna regular de
la sustancia cristalina.
En 1711, M. Lomonósov, ofreció la posibilidad de explicar perfectamente la ley de la
constancia de los ángulos diedros: yuxtaponiéndose consecutivamente las capas de
corpúsculos al creceré el cristal, las caras se desplazan paralelamente a sí mismas.
En 1774, R. J. Haüy descubrió la segunda ley fundamental de la cristalografía, ley de
la racionalidad. Haüy supuso que las moléculas que constituyen el cristal, tienen la
forma constante de paralelepípedos.
En el primer decenio del s. XIX empezaron los trabajos de mediciones sistemáticas de los
ángulos diedros de los cristales naturales, minerales. En este período la cristalografía estaba
estrechamente vinculada con la mineralogía y era una de sus partes. Muchos mineralogistas
se dedicaban a la medición de los cristales, principalmente de los naturales, minerales
(Weiss, Neumann y Miller). Miller empezó a aplicar la en cristalografía los métodos de la
geometría analítica y creó un simbolismo racional para la notación de las caras mediante
índices.
La medición de los cristales se hacía con goniómetros de aplicación (de contacto) y, después,
con goniómetros de reflexión. Estos aparatos los inventaron Carangeot, en 1782, el primer
tipo, y Wollaston, en 1809, el segundo tipo.
A comienzos del s. XIX se crearon las bases de la ciencia de la simetría de los cristales, se
descubrió la ley de las zonas y se procedió a la clasificación de los cristales.
En 1830, Hessel, fue el primero en deducir todas las formas posibles de simetría de
los cristales.
En 1867, el académico A. Gadolin, basándose en las leyes geométricas dedujo los 32
tipos de simetría de los cristales.
A partir de la segunda mitad del s. XIX empieza la investigación de los cristales obtenidos
artificialmente. La cristalografía se va separando gradualmente de la mineralogía, se acerca
a la física y química y se convierte en una ciencia independiente. Se establecen las
regularidades de la cristalografía química, del isomorfismo y polimorfismo, se estudian
minuciosamente las propiedades ópticas de los cristales.
A finales del s. XIX se elaboraron las teorías geométricas de la estructura de los cristales.
En 1912, el físico M. Laue consiguió demostrar experimentalmente la exactitud de
la teoría reticular.
Después del descubrimiento, muchos físicos y cristalógrafos de renombre empezaron a
aplicar los rayos X al estudio de la estructura de los cristales y elaboraron una serie de
nuevos métodos originales de investigación.
Procesos de cristalización.
Los cristales se formar a partir de disoluciones, fundidos y vapores. Los átomos en estos
estados desordenados tienen una disposición al azar, pero al cambiar la temperatura,
presión y concentración pueden agruparse en una disposición ordenada característica del
estado cristalino.
Como ejemplo, de cristalización a partir de una disolución, consideraremos el cloruro sódico
(sal común) disuelto en agua. Si se deja que el agua se evapore, la disolución contiene cada
vez más Na+ y Cl por unidad de volumen. Finalmente, se llegará a un punto en el cual la
cantidad de agua presente no podrá retener toda la sal en solución y aquella empezará a
precipitar. Si se preparan las condiciones de forma tal que la evaporación del agua se realice
muy lentamente, los iones de sodio y clore, conforme se vayan separando de la solución, se
irán agrupando y, gradualmente formarán uno o unos pocos cristales con formas
características y a menudo con orientación común. Si la evaporación es rápida, aparecen
muchos centros de cristalización y los cristales resultantes serán pequeños y orientados al
azar.
Los cristales pueden formarse también a partir de una solución por descenso de la
temperatura o de la presión. El agua caliente, por ejemplo, disolverá algo más de sal que la
fría y si la solución caliente se deja enfriar, se llegará a un punto en que la solución se
sobresaturará a su temperatura y la sal cristalizará. Por otra parte, cuanto mayor sea la
presión a la que se someta el agua, mayor será la cantidad de sal que aquélla podrá
mantener en solución. Así, con el descenso de la presión de una solución saturada, se
producirá una sobresaturación y consecuentemente se formarán cristales. Por lo tanto, en
general, los cristales pueden formarse de una solución por la evaporación del disolvente,
por el descenso de la temperatura o por el descenso de la presión.
Un cristal se forma también a partir de una masa fundida de la misma manera que a partir
de una solución. El ejemplo más familiar de cristalización de una fusión es la formación de
cristales de hielo cuando el agua se congela. Aunque ordinariamente no se considere así, el
agua es hielo fundido. Cuando la temperatura es suficientemente baja, las moléculas de
agua que estaban libres para moverse en cualquier dirección ahora se quedan quietas y se
disponen mutuamente en un orden definido para formar una masa sólida, cristalina.
Aunque la cristalización a partir de un vapor es menos corriente que de una disolución o de
una fusión, los principios básicos son muy parecidos para ambos. A medida que el vapor se
enfría, los átomos o moléculas separadas se van aproximando entre sí, hasta formar
eventualmente un sólido cristalino. Los ejemplos más familiares de este tipo de
cristalización son la formación de copos de nieve a partir del aire saturado de vapor de agua
y la formación de cristales de azufre en la base de las fumarolas o en el cuello de los
volcanes.
Estructura interna de los cristales.
El orden interno o estructura cristalina de un mineral puede considerarse como la repetición
de un motivo (o grupo de átomos) sobre una red (que es una distribución periódica de
puntos en el espacio).
El motivo o grupo de átomos tiene una cierta simetría que puede reflejarse en la forma
externa del cristal.
El primer científico que demostró que la forma
cristalina externa de un mineral (su morfología) era
una expresión de su orden interno fue René-Just
Haüy.
La figura 1. ilustra el concepto de Haüy de
“moléculas integrales”, que se apilan regularmente
para dar lugar diversas formas desarrolladas. Haüy
acuñó la palabra “molécula” para designar lo que
para él significaba el concepto moderno de celda
unitaria. Una celda unitaria es la unidad más
pequeña de una estructura (o modelo) que puede
repetirse indefinidamente para generar todo el
sistema (o para generar la huella completa de un
modelo.
Fig. 1. Formas externas distintas producidas
por el apilamiento sistemático de celdas
unitarias cúbicas.
Un orden interno tridimensional de un cristal puede
considerarse como la repetición de un motivo (una unidad de
diagrama), de tal modo que los alrededores de cada motivo
son idénticos.
Fig. 2. Estructura atómica de la
calcita.
La figura 2. Ilustra la distribución (ordenada) de grupos
triangulares (CO3)2- y iones Ca2+ en la estructura de perfil
romboédrico de una célula unitaria de calcula (CaCO3).
Simetría Cristalina.
El lugar geométrico que ayuda a la visualización de la simetría de una distribución ordena
recibe el nombre de elemento de simetría.
Los ejes, planos y centro de simetría son ejemplos de los elementos de simetría. Las
operaciones de simetría correspondientes a cada uno de estos elementos son: rotación
alrededor de un eje, reflexión sobre un plano e inversión alrededor de un punto. Los
procesos de rotación alrededor de un eje, de reflexión en un plano o de inversión alrededor
de un punto central se denominan colectivamente operaciones de simetría.
La rotación alrededor de un eje imaginario y según un ángulo Ø, puede generar otro motivo
o varios motivos.
En la figura 3 el ángulo Ø de 180° genera un modelo con dos manos. Un eje de rotación es
una línea imaginaria alrededor de la cual puede girar un motivo patrón y repetirse a sí
mismo apareciendo una o varias veces durante una rotación completa.
Fig. 3. (a) Generación de un diagrama por rotación de un motivo a través de un ángulo de 180°. (b) Motivos derecho e izquierdo
relacionados por la reflexión en un plano. (c) Motivos relacionados por inversión a través de un centro. (d) Motivos relaciones por
una rotación de 180° y por la subsiguiente inversión; esta última operación se llama también roto-inversión.
Eje de simetría
La simetría de rotación se expresa generalmente
mediante cualquier número entero (n), desde 1 a
infinito. El numero n expresa el número de veces
que un motivo se repite durante una rotación
completa (360°). Una simetría de rotación de n=1
significa que después de una rotación completa de
360° alrededor de un eje, todos los aspectos de un
objeto o figura coinciden consigo mismo al menos
una vez. El otro caso de límite de simetría de
rotación es el de un eje de rotación de orden infinito
(n = ∞). Un objeto que posee este tipo de eje entra
en coincidencia consigo mismo para cualquier
ángulo de rotación, pues es la cantidad de rotación
necesaria infinitamente pequeña.
La figura 4 muestra como un cilindro hueco es
compatible con un eje de rotación, paralelo a la
generatriz del cilindro, (n = ∞). En cambio el mismo
cilindro hueco con una simple muesca posee una
simetría rotacional de n=1.
Fig. 4. Simetría rotacional.
Los tipos encontrados en el orden interno de los cristales y también expresados en su forma
externa (morfología) son primarios (Ø = 360º), binarios (Ø = 180), ternarios (Ø =120º),
cuaternarios (Ø = 90º) y senarios (Ø = 60º).
Los posibles ejes de rotación están
representados en la figura 5 con los
símbolos gráficos utilizados para
representarlos.
El
número
de
apariciones del motivo durante una
rotación de 360° da su nombre al eje de
rotación. Por ejemplo, dos unidades
equivalentes a una rotación de 360°
están relacionadas con un eje de
rotación binario.
Fig. 5. Ejes de simetría de un cristal.
La rotación produce modelos en los cuales el motivo original y los generados en el proceso
son idénticos en orientación entre sí. Dicho de otro modo, el motivo original y el generado
son de la misma mano. Por ello, se dice que el motivo original y el generado por rotación
son congruentes.
Plano de simetría.
Otro elemento de simetría, llamado plano de simetría, produce mediante la operación de
reflexión, una imagen igual a la primera, como si él plano fuera un espejo (fig. 6). El motivo
que se refleja es el opuesto al motivo original y jamás podrán superponerse entre sí. Es la
misma relación que existe entre la mano derecha y la mano izquierda y así se constituye lo
que se llama un par enantiomorfo.
Fig. 6 Plano de simetría.
Los planos de simetría pueden estar o no presentes en un cristal y para buscarlos debemos
mirar que superficie imaginaria puede cortar el cristal en dos partes exactamente iguales.
Los planos pueden pasar por aristas o cortarlas en su punto medio, pueden pasar por
vértices o cortar las caras en su mitad.
Centro de simetría.
Un tercer elemento de simetría es el Centro de simetría y está relacionado con la operación
de inversión. Una inversión implica el dibujo de líneas imaginarias trazadas desde cada
punto del objeto que pasando por el centro de inversión alcanzan distancias iguales al otro
lado de dicho centro. El objeto invertido se recrea conectando los puntos extremos de estas
líneas.
Rotación con inversión.
Además del orden simétrico engendrado por los ejes de
rotación, existen rotaciones de orden 1, 2, 3, 4 y 6 que
pueden combinarse con inversiones y que por ello se
conocen con el nombre de ejes de rotoinversión. Los ejes de
rotación han sido ilustrados por motivos que residen en el
mismo plano, como en la Fig. 7. Combinando la rotación con
la inversión es más fácil observar el orden de un diagrama
en tres dimensiones.
Fig. 7. Rotoinversión
Ejes cristalográficos.
En la descripción de los cristales resulta conveniente referir las formas externas o la simetría
interna a una serie de tres (o cuatro) ejes de referencia. Estas líneas de referencia
imaginarias, denominadas ejes cristalográficos, se toman paralelas a las aristas de
intersección de las caras cristalinas principales. Además, las posiciones de los ejes
cristalográficos vienen más o menos fijadas por la simetría de los cristales, pues en la mayor
parte de los cristales nos encontramos que coinciden con los ejes de simetría o con las
normales a los planos de simetría. Para algunos cristales puede haber más de una
posibilidad de ejes cristalográficos cuando la selección se hace sólo por la morfología. En el
caso ideal deben ser paralelos y sus longitudes proporcionales a las aristas de la celda
unidad.
Todos los cristales, con excepción de los que pertenecen al sistema hexagonal se refieren a
tres ejes cristalográficos designados como a, b y c. En el caso general (sistema triclínico)
todos los ejes tienen diferentes longitudes y son oblicuos entre sí. Los extremos de cada eje
se designan con más o menos (+ o -); el extremo frontal de a, el extremo derecho de b y el
extremo superior de c son positivos; los extremos opuestos son negativos. Los ángulos que
forman los extremos positivos de los ejes se designan convencionalmente con las letras
griegas α, β y γ.
Sistemas cristalográficos.
Los seis sistemas cristalinos están referidos a las siguientes direcciones axiales y ángulos
axiales.
Triclínico. Tres ejes desiguales que se cortan todos según ángulos oblicuos.
Monoclínico. Tres ejes desiguales, dos de los cuales forman entre sí un ángulo oblicuo,
siendo el tercero perpendicular al plano de los otros dos.
Ortorrómbico. Tres ejes mutuamente perpendiculares, todos ellos de diferente longitud.
Tetragonal. Tres ejes mutuamente perpendiculares, dos de los cuales (los ejes horizontales)
son de igual longitud (a1 y a2), pero el eje vertical es más corto o más largo que los otros
dos.
Hexagonal. Cuatro ejes cristalográficos; tres ejes horizontales iguales (a1, a2 y a3) se cortan
bajo ángulos de 120°, el cuarto (vertical) es de longitud diferente y perpendicular al plano
de los otros tres.
Isométrico. Tres ejes mutuamente perpendiculares de longitudes iguales (a1, a2 y a3).
Fig.8 Ilustraciones del sistema convencional de ejes cristalográficos adoptados para cada uno de los
seis sistemas cristalinos.
Índices de Miller
Se han planeado diversos métodos de notación para expresar las intersecciones de las caras
cristalinas en los ejes cristalinos. Pero el más universalmente empleado es el sistema de
índices propuesto por W.H. Miller.
Los índices de Miller de una cara consisten en una serie de números enteros que han sido
deducidos de las intersecciones por su inversión y, si es necesario, por la subsiguiente
reducción de fracciones. Los índices de una cara se expresan siempre de forma que los tres
números (cuatro en el sistema hexagonal) se refieran a los ejes a, b y c, respectivamente y,
por consiguiente, las letras que indican los diferentes ejes se omiten. Los índices expresan
una relación, pero al objeto de simplificar, el signo de la relación se omite también.
Para las dos caras superiores de la Fig. 9 que cortan los
segmentos positivos de los ejes cristalográficos, las
intersecciones son 1a, 1b, 1c y 2a, 2b, 2c/3
respectivamente. Invirtiendo estos parámetros, resulta:
1/1, 1/1, 1/1 y 1/2, 1/2, 3/2 respectivamente. Con el objeto
de eliminar fraccionarios en la segunda expresión,
multiplicamos por dos, quedando entonces los índices de
Miller de (111) para la cara unidad, y (113) para la otra
cara.
Generalmente los números que expresan los índices de
Fig. 9. Índices de Miller
Miller son enteros pequeños. Cuando estos números son
de dos dígitos, se utiliza la coma para separarlos, por ejemplo: (1, 12, 4), y se lee: “uno,
doce, cuatro”. Si la cara corta a alguno de los ejes cristalográficos en forma negativa, se
coloca una raya encima del número que corresponde a dicho corte, por ejemplo: (1 1̅ 1), y
se lee: “uno, menos uno, uno”.
Nótese que los índices que estamos expresando corresponden a caras del cristal, y por eso
se colocan entre paréntesis. Si vamos a dar los índices de una forma cristalina, la expresión
contiene el símbolo de llaves: {1 1 1}.
Cuando no se conocen las intersecciones exactas, se usa el símbolo general (hkl), sabiendo
que en su orden representan los recíprocos de sus intersecciones a lo largo de los ejes a, b
y c. La expresión (hkl) indica que una cara corta desigualmente a los tres ejes.
Si una cara es paralela a uno de los ejes y corta a los otros dos, el símbolo general se escribe
(0kl), (h0l) o (hk0), según sea el caso particular. Si la cara es paralela a dos ejes y corta sólo
a uno, esa medida se considera una distancia unidad, y los índices serían: (100), (010), (001),
con sus equivalentes negativos: (1̅00), (01̅0) y (001̅).
Formas cristalinas
En su significado más familiar el término forma se usa para indicar el aspecto externo
general. En cristalografía, se forma externa se designa con la palabra hábito, mientas que
forma consiste en un sentido especial y restringido. Así, una forma consiste en un grupo de
caras cristalinas, todas las cuales tienen la misma relación con los elementos de simetría y
exhiben las mismas propiedades físicas y químicas, pues todas tienen debajo los mismos
átomos en el mismo orden geométrico.
Externamente, las caras que componen una forma, pueden tener diferentes tamaños,
debido a la imperfecta formación del cristal.
Para reconocerlas, normalmente nos ayudamos por la observación de estrías naturales,
figuras de corrosión o crecimientos. A veces es necesario someter el cristal a un ataque
químico, que revele estas evidencias.
Nombre de las formas
Pedión (monoedro). Forma que comprende una sola cara (1).
Pinacoide (paraleloedro). Forma abierta constituída por dos caras paralelas (2).
Domo (diedro). Formado por dos caras no paralelas, simétricas con relación a un plano de
simetría (m). Es una forma abierta (3).
Esfenoide (diedro). Dos caras no paralelas simétricas respecto a un eje de rotación binario
(4).
Prisma. Forma abierta que puede estar compuesta por tres, cuatro, seis, ocho o doce caras,
todas ellas paralelas al mismo eje. El número de caras depende del sistema al cual pertenece
el cristal (5-11).
Pirámide. Así se denomina a la forma abierta compuesta de 3, 4, 6 ,8 o 12 caras no paralelas
entre sí que se cortan en un punto (12-18).
Bipirámide. Forma cerrada de seis, ocho, doce, dieciséis o veinticuatro caras, según sea el
sistema. Pueden considerarse como formadas por dos Pirámides, unidas por reflexión, la
una sobre la otra a través de un plano de simetría horizontal.
Trapezoedro. Formas cerradas de 6, 8 o 12 caras con 3,4 o 6 caras superiores giradas con
respecto de las 3, 4 o 6 caras inferiores.
Escalenoedro. Forma cerrada de 8 o 12 caras agrupadas en pares simétricos.
Romboedro. Seis caras que constituyen una forma cerrada. Tres de ellas de la parte superior
alternan con las otras tres de la parte inferior giradas entre sí 60°.
Biesfenoide. Es una forma cerrada constituida por caras superiores que alterna con dos
caras inferiores, separadas entre sí 90°.
Hábito cristalino.
El término hábito se usa para designar las formas generales de los cristales como cúbica,
octaédrica, prismática. Debido a que el hábito es controlado por el medio ambiente en el
que se crecen los cristales, puede variar con la localidad. En un sitio puede ser normal y en
otros tabular o fibroso. Los cristales presentan sólo raramente una forma geométrica ideal.
Pero aun en cristales mal formados o defectuosos la evidencia de la simetría está presente
en el aspecto físico de las caras y en la disposición simétrica de los ángulos interfaciales. En
la Fig.10 se indican varias formas cristalinas, primero desarrolladas idealmente y luego
defectuosas.
Fig. 10. Ejemplos de algunos hábitos cristalinos en el sistema isométrico.
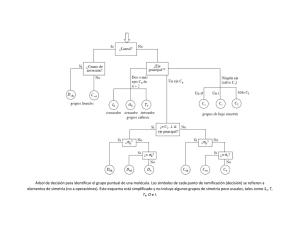
Clases cristalográficas.
Los elementos de simetría sin translación se combinan de treinta y dos manera distintas y
dan lugar a las 32 clases cristalinas o grupos puntuales existentes.
Recordemos que la expresión (hkl) representa los índices de Miller de la Forma general, que
corta de manera diferente a los tres ejes cristalográficos.
El nombre que recibe la Forma general, es el nombre que se dará a la clase, por ejemplo:
(hkl) en la simetría: 2/m 2/m 2/m es la Forma llamada Bipirámide rómbica. El nombre de la
Clase será entonces Bipiramidal rómbica.
En la simetría 4/m 3 2/m, (hkl) es la Forma general llamada Hexaquisoctaedro, por tanto, el
nombre de la Clase será Hexaquisoctaédrica.
La cantidad de especies minerales que cristalizan en cada uno de los seis sistemas cristalinos
es muy variable. Se ha encontrado la siguiente distribución:
Sistema Cúbico o Isométrico
Sistema Hexagonal
Sistema Tetragonal
Sistema Ortorrómbico
Sistema Monoclínico
Sistema Triclínico
26%
19%
12%
20%
21%
2%
Se ha encontrado también que la mayor cantidad de especies minerales se encuentra en la
clase cristalina de más alta simetría de cada sistema.
Estas clases son: 1 en el Triclínico, 2/m en el Monoclínico; 2/m 2/m 2/m en el Rómbico; 4/m
2/m 2/m en el Tetragonal; 3 2/m en el Hexagonal, división Romboédrica; 6/m 2/m 2/m en
el Hexagonal, división Hexagonal y 4/m 3 2/m en el Cúbico. Se agrega a esta lista, las clases
3 2 de la división Romboédrica del sistema Hexagonal; 4 3 2 y 2/m 3 del sistema Cúbico, por
representar especies minerales de marcada importancia, como son, Cuarzo, Esfalerita y
Pirita.En total son entonces 10 Clases, de las 32 que existen, las que se van a considerar,
como más importantes en este estudio. La tabla 1, muestra la distribución convencional de
los sistemas y clases cristalinas.
Tabla 1. Las 32 clases de cristales y su simetría característica.
Proyecciones Cristalinas.
Una proyección de un cristal es un medio de representar un cristal tridimensional en una
superficie plana bidimensional. Diferentes tipos de proyección se usan para fines distintos,
pero cada una de ellas se llevas a cabo según las reglas definidas de tal manera que la
proyección tiene una relación conocida y constante con el cristal. Los dibujos que se
presentan en el trabajo se conocen como proyecciones clinográficas y son de un tipo tal de
perspectiva que parecen una fotografía en dos dimensiones del cristal. Este es mejor
método para representar el cristal y muchas veces es superior a la fotografía.