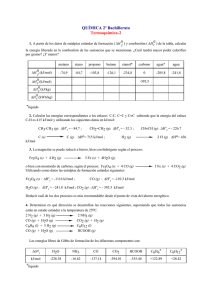
Relación de problemas 6: Termoquímica Ensayos Físico-Químicos 1. El CO2 puede obtenerse de la combustión de carbono: C(s) + O2 (g) CO2 (g) ΔH = -393,5 KJ/mol Este gas (CO2) también puede producirse sintetizando (CO) en una primera etapa y haciéndolo reaccionar luego con oxígeno en una segunda etapa. C(s) + ½ O2 (g) CO (g) CO(s) + ½ O2 (g) CO2 (g) ΔH = -110,6 KJ/mol ΔH = -282,9 KJ/mol Comprobar que la entalpía de formación es la misma independientemente del proceso analizado (combustión de carbono o proceso en 2 etapas). 2. A partir de las energías de enlace de la tabla determina la entalpía de las siguientes reacciones, indicando en cada caso si la reacción es endotérmica o exotérmica a) Hidrogenación del 1,3-butadieno para obtener butano (reacción sin ajustar estequiométricamente) CH2=CH-CH=CH2 + 2 H2 CH3-CH2-CH2-CH3 b) Combustión de propano (reacción sin ajustar estequiométricamente) CH3 – CH2 – CH3 + O2 CO2 + H2O c) Formación de amoniaco a partir de sus elementos (reacción sin ajustar estequiométricamente): N2 + H2 NH3 d) Cloración de etino para obtener 1,2-dicloroeteno C2H2 + Cl2 ClCH=CHCl e) Oxidación de metanol (reacción sin ajustar estequiométricamente): CH3OH (liq) + O2 CO2 + H2O f) Formación de agua a partir de H2 y O2: H2 + ½ O2 H2O Enlace C–C C–H O–H H–H O=O C=C C=O C≡C C–O N≡N N–H Cl – Cl C - Cl C.F.G.S. Análisis y Control de Calidad Energía (KJ/mol) 346 411 459 432 494 610 799 835 352 946 389 243 339 1 Ensayos Físico-Químicos Relación de problemas 6: Termoquímica 3. Determinar la entalpía de formación del cloruro de aluminio anhídro (Al 2Cl6 (s)) a partir de Al (s) y Cl2 (g), teniendo en cuenta los datos siguientes: a) 2 Al (s) + 6 HCl (aq) Al2Cl6 (aq) + 3 H2 (g) ΔHº= -240,0 Kcal b) H2 (g) + Cl2 (g) 2 HCl (g) ΔHº = - 44,0 Kcal c) HCl(g) HCl (aq) ΔHº = - 17,5 Kcal d) Al2Cl6 (s) Al2Cl6 (aq) ΔHº = -153,7 Kcal 4. Combine las siguientes ecuaciones termoquímicas S (rómbico) + O2 (g) → SO2 (g) ΔHº298 = -70,944 kcal S (monoclínico) + O2 (g) → SO2 (g) ΔHº298 = -71,02 kcal Para predecir ΔHº298 de: S(rómbico) → S (monoclínico) Calcular la entalpía de combustión del propano gaseoso cuando forma dióxido de carbono gaseoso y agua líquida en condiciones estándar a partir de los calores de formación del dióxido de carbono, del propano y del agua. Datos: ΔHof, CO2(g)= -393,5 KJ; ΔHof, C3H8(g)= -103,8 KJ; ΔHof, H2O(l) = -285,8 KJ 5. 6. Muchos encendedores contienen butano líquido. Empleando entalpías de formación, calcule la cantidad de calor que se produce cuando 1g de butano se quema por completo con aire. Datos: ΔHof, CO2(g)= -393,5KJ; ΔHof, C4H10(g)= -147,6 KJ; ΔHof, H2O(l)= -285,8KJ 7. Calcular el cambio de entalpía estándar para la combustión completa de 1 mol de etanol (l). Datos: ΔHof, C2H5OH(l)= -277,7 kJ.mol-1 ; ΔHof , CO2(g)= -393,5 kJ.mol-1 , ΔHof,H2O(l)= -287,1 kJ.mol-1, ΔHof,O2(g)= 0 kJ.mol-1 8. La entalpía de combustión de C(s) a dióxido de carbono (g) es -393,5 KJ/mol de C y la entalpia de combustión del monóxido de carbono a dióxido de carbono es -283,0KJ/mol de monóxido de carbono. Utilizando estos datos calcule la entalpía de combustión de carbono a monóxido de carbono. 9. Calcule el ΔH de reacción de: 2 Cs + H2 (g) → C2H2 (g) Dadas las siguientes reacciones que se deben balancear y sus respectivos cambios de entalpía: C.F.G.S. Análisis y Control de Calidad 2