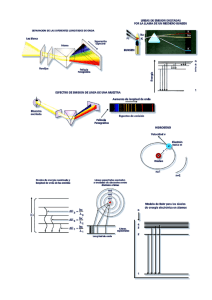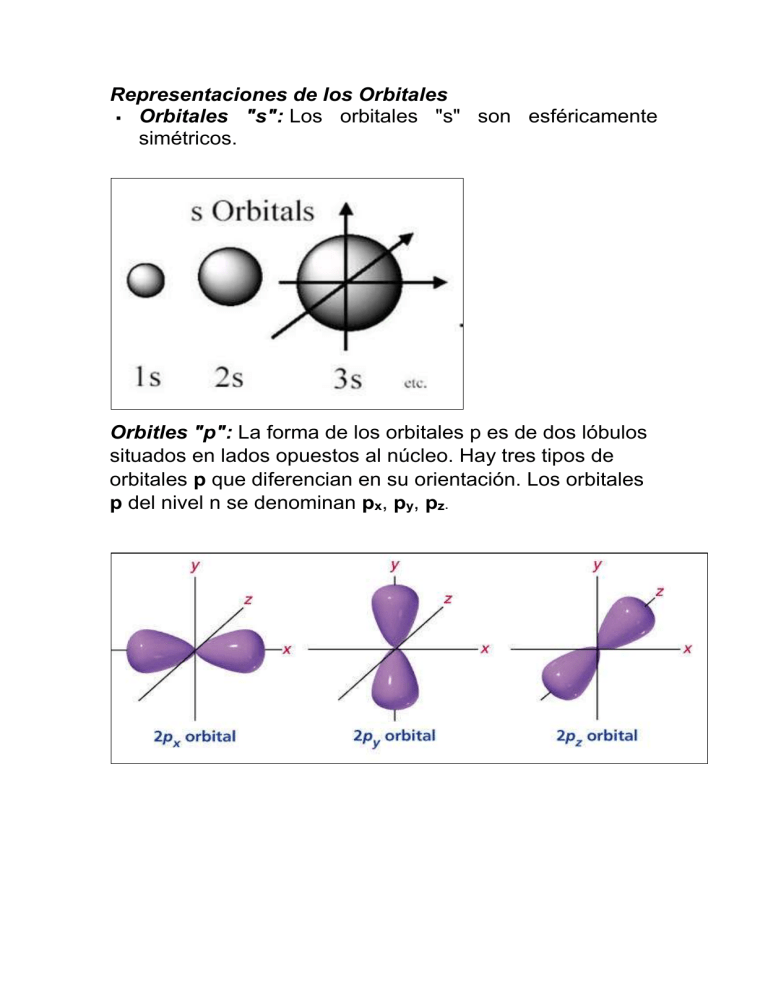
Representaciones de los Orbitales Orbitales "s": Los orbitales "s" son esféricamente simétricos. Orbitles "p": La forma de los orbitales p es de dos lóbulos situados en lados opuestos al núcleo. Hay tres tipos de orbitales p que diferencian en su orientación. Los orbitales p del nivel n se denominan px, py, pz. Orbitales "d": En el tercer subnivel tenemos 5 orbitales atómicos con diferentes orientaciones en el espacio tal y como vemos en la figura. Cuatro de los cinco orbitales d tienen forma de trébol de cuatro hojas, tal como se muestra en la figura de abajo; el quinto orbital d posee el aspecto de una mancuerna alargada con una rosca en torno a su centro. Piense en el orbital como una fotografía del átomo tomada con baja velocidad: el orbital debería aparecer como una nube borrosa indicando la región del espacio alrededor del núcleo donde ha estado el electrón. En esta imagen podemos ver el núcleo en el centro (Color verde) y 3 tipos de orbitales a su alrededor.