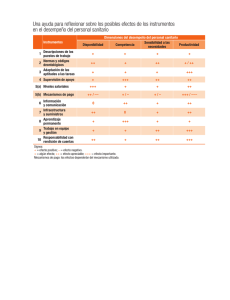
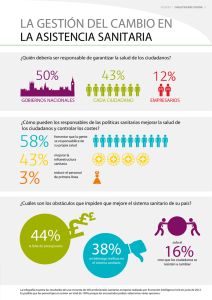
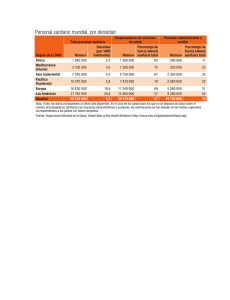
OBTENCIÓN DE REGISTRO SANITARIO DE ALIMENTOS DE CONSUMO HUMANO MBA Ing. Pamela Díaz Romani CONTENIDO Normativas sanitaria para alimentos y bebidas Registro Sanitario: - Significado e Importancia - Verificación del Producto - Base Legal para la obtención de Registro Sanitario. - Requisitos para la inscripción en el Registro Sanitario - Procedimiento y Trámite ante DIGESA - Costos - Casos: Renovación y modificaciones (transferencia) - Datos adicionales I. NORMATIVAS LEGALES: 1) Normativa Nacional: DECRETO SUPREMO Nº 007-98-SA REGLAMENTO SOBRE VIGILANCIA Y CONTROL SANITARIO DE ALIMENTOS Y BEBIDAS * LOS ALIMENTOS DE ORIGEN ANIMAL * LA FABRICACION DE ALIMENTOS Y BEBIDAS *CONTROL DE CALIDAD SANITARIA E INOCUIDAD * LOS ALIMENTOS DE ORIGEN VEGETAL * LA ESTRUCTURA FISICA E INSTALACIONES DE LAS FABRICAS *HIGIENE DEL PERSONAL Y SANEAMIENTO * LA DISTRIBUCION DE AMBIENTES Y UBICACION DE EQUIPOS REGISTRO SANITARIO DE ALIMENTOS Y BEBIDAS INDUSTRIALIZADOS DIGESA: Dirección General de Salud Ambientales e Inocuidad Alimentaria I. NORMATIVAS Y CAMBIOS LEGALES: 2) El 30 de marzo de 2014 el diario El Peruano publica el Decreto Supremo N°004-2014 SA en el que se muestran las siguientes exigencias: Artículo 58-A.- Certificación de la Validación Técnica Oficial del Plan HACCP Artículo 58-B.- Certificación de Principios Generales de Higiene del Codex Alimentarius (PGH) I. NORMATIVAS Y CAMBIOS LEGALES : 2) El 30 de marzo de 2014 el diario El Peruano publica el Decreto Supremo N°004-2014 SA en el que se muestran las siguientes exigencias: DISPOSICIONES COMPLEMENTARIAS FINALES: Segunda.- Plazo para la obtención de la Certificación de Principios Generales de Higiene (PGH) La micro y pequeña empresa (MYPE) deberá en el plazo de dos (2) años, contado a partir de la entrada en vigencia del artículo 2° del presente Decreto Supremo, obtener la certificación de Principios Generales de Higiene del Codex Alimentarius (PGH). Dicho plazo no exime el cumplimiento de la normativa sanitaria. Tercera.- Plazo para que las micro y pequeña empresa (MYPES) obtenga la Certificación de la Validación Técnica Oficial del Plan HACCP Las micro y pequeñas empresas (MYPEs) deberán en el plazo de cuatro (4) años, contados a partir de la entrada en vigencia del artículo 2° del presente Decreto Supremo, obtener la certificación de la Validación Técnica Oficial del Plan HACCP. Dicho plazo no exime el cumplimiento de la normativa sanitaria. I. NORMATIVAS Y CAMBIOS LEGALES : 3) El 29 de diciembre de 2016 el diario El Peruano Publica: Decreto Legislativo nº 1290: Artículo 3.- De la habilitación sanitaria emitida por la Dirección General de Salud Ambiental e Inocuidad Alimentaria - DIGESA: 3.1 El análisis del riesgo alimentario para la salud es el patrón de referencia para el control y la vigilancia sanitaria de los establecimientos habilitados para la fabricación de alimentos elaborados industrialmente destinados al consumo humano. El Ministerio de Salud mediante Resolución Ministerial aprobará el listado de alimentos o grupos de alimentos en base al mencionado patrón de referencia. 3.2 La habilitación sanitaria se otorga por establecimiento a través de la DIGESA. Asimismo, para su obtención y vigencia debe implementarse permanentemente un sistema preventivo de riesgo alimentario que incluyan las Buenas Prácticas de Manufactura o el Plan HACCP. DISPOSICIONES COMPLEMENTARIAS MODIFICATORIAS …. La referida autorización sanitaria es de aprobación automática… I. NORMATIVAS Y CAMBIOS LEGALES : 3) El 29 de diciembre de 2016 el diario El Peruano Publica: Decreto Legislativo nº 1290: I. NORMATIVAS Y CAMBIOS LEGALES : 3) El 29 de diciembre de 2016 el diario El Peruano Publica: Decreto Legislativo nº 1290: II. HABILITACIÓN SANITARIA: 2.1 BPM: Las Buenas Prácticas de Manufactura son una herramienta básica para la obtención de productos seguros para el consumo humano, que se centralizan en la higiene y la forma de manipulación. •Ubicación de las Instalaciones •Estructura Física e Instalaciones •Distribución de ambientes y ubicación de equipos •Abastecimiento de agua, desagüe y eliminación de desechos •Higiene del personal, limpieza y desinfección de las instalaciones •Aspectos operativos •Materias primas, aditivos alimentarios y envases •Almacenamiento •Retiro de Producto •Transporte II. HABILITACIÓN SANITARIA: 2.2 El Análisis de Peligros y Puntos Críticos de Control (APPCC o HACCP, por sus siglas en inglés) 1.Formar el equipo de trabajo: 2.Describir los productos: 3.Identificar el uso esperado del producto por los consumidores: 4.Desarrollar el diagrama de flujo y la descripción del proceso: 5.Realizar el análisis de peligros asociados a la producción e identificar las medidas preventivas 6.Identificar los puntos de control críticos (PCC) Establecer límites críticos para cada PCC. 7.Establecer límites críticos para cada PCC 8.Establecer un sistema de supervisión o vigilancia 9.Establecer las acciones correctoras 10.Establecer sistema de registro y archivo de datos 11.Establecer un sistema de verificación del sistema 12. Realizar una revisión del sistema III. REGISTRO SANITARIO 3.1. Importancia Es la garantía que acredita al empresario que los productos que ofrece en el mercado nacional, son aptos para el consumo humano. Para las PYMES consolidar un producto apto para el consumo humano es importante ya que tendrían mayores oportunidades de ofrecer dichos productos a muchos mercados. Representa un activo intangible en su empresa, que aporta valor agregado al producto, y así mismo brinda mayor competitividad III. REGISTRO SANITARIO 3.1. ¿Qué es el Registro Sanitario? Es un documento que autoriza a una persona natural o jurídica para fabricar, envasar e importar un producto destinado al consumo humano. Son regulados a través del Ministerio de Salud y dentro de este a través de la Dirección General de Salud Ambiental (DIGESA). Para efectos del Registro Sanitario, se considera alimento o bebida industrializado al producto final destinado al consumo humano, obtenido por transformación física, química o biológica de insumos de origen vegetal, animal o mineral y que contiene aditivos alimentarios. III. REGISTRO SANITARIO III. REGISTRO SANITARIO III. REGISTRO SANITARIO 3.2. Verificación de Producto Según el acta 31 de la COMPIAL (Comisión Multisectorial Permanente de Inocuidad Alimentaria) en abril de 2013 se estableció que NO es competencia de Digesa el siguiente grupo de productos: - Productos de procesamiento primario. - Productos de origen pesquero y acuícola. - Productos con propiedades en salud (medicinales): Productos dietéticos, herbarios o con propiedades en salud. III. REGISTRO SANITARIO 3.2. Verificación de Producto III. REGISTRO SANITARIO 3.2. Verificación de Producto Todos los ingredientes deben de ser de GRADO ALIMENTARIO. Verificar que el nombre del producto refleje su verdadera naturaleza en cumplimiento con lo establecido en Norma Codex Stan 01-1985 y Ley de Protección y Defensa del Consumidor n.° 29571. Respecto a los aditivos estos deben de cumplir con el Art. 63 del Reglamento sobre Vigilancia y Control Sanitario de Alimentos y Bebidas aprobado por D.S.007-98-SA, revisar norma CODEX y en su Defecto FDA, los mismos que deben ser declarados con el respectivo código SIN y la cantidad en mg/kg. III. REGISTRO SANITARIO 3.2. Verificación de Producto Según el Art. 104 del Reglamento sobre Vigilancia y Control Sanitario de Alimentos y Bebidas aprobado por D.S. -007 -98 -SA, el Registro Sanitario se otorga por producto o grupo de productos y fabricante. Se considera grupo de productos aquellos elaborados por un mismo fabricante, que tienen la misma composición cualitativa de ingredientes básicos que identifica al grupo y que comparten los mismos aditivos alimentarios. Sólo puede ingresar por expediente un Producto o Grupo de productos. Ejemplo: III. REGISTRO SANITARIO 3.2. Verificación de Producto Según el Art. 104 del Reglamento sobre Vigilancia y Control Sanitario de Alimentos y Bebidas aprobado por D.S. -007 -98 -SA, el Registro Sanitario se otorga por producto o grupo de productos y fabricante. Se considera grupo de productos aquellos elaborados por un mismo fabricante, que tienen la misma composición cualitativa de ingredientes básicos que identifica al grupo y que comparten los mismos aditivos alimentarios. Sólo puede ingresar por expediente un Producto o Grupo de productos. Ejemplo: III. REGISTRO SANITARIO 3.2. Verificación de Producto Ejemplo 2: Ejemplo 3: III. REGISTRO SANITARIO 3.3. Base Legal La inscripción del registro sanitario se rige en función a las siguientes Leyes y Decretos: Ley N° 26842, Ley General de Salud, del 20/07/97, Artículo 91° y 92° Decreto Supremo N° 007-98-SA, Reglamento sobre Vigilancia y Control Sanitario de Alimentos y Bebidas, del 25/09/98,Artículo 101°, 103°, 104°, 105°, 107°, 108°, 110°, 111°, 113° y del 115° al 119° y Cuarta Disposición Complementaria, Transitoria y Final. Decreto Legislativo N° 1062, Ley de Inocuidad de los alimentos, del 28/06/08. Decreto Supremo N° 034-2008-AG, Reglamento de la Ley de Inocuidad de los alimentos, del 17/12/08. Ley N° 28314, Ley que dispuso la fortificación de la Harina de Trigo con micronutrientes, del 03/08/04. Decreto Supremo N° 012-2006-SA, Reglamento de la Ley que dispuso la fortificación de la Harina de Trigo con micronutrientes, del 25/06/06. Decreto Supremo N° 012-2009-SA, Reglamento de la Ley N° 28681, Ley que regula la comercialización, consumo y publicidad de bebidas alcohólicas, del 11/07/09, Artículo18°. Ley N° 28405, Ley de Rotulado de Productos Industriales manufacturados, del 30/11/04, Artículo 5°. Ley N° 29571, Código de Protección y Defensa del Consumidor, del 02/09/10. Decreto Supremo N° 010-2010-MINCETUR, establecen disposiciones reglamentarias referidas a la VUCE del 09/07/10, Artículo 2°, 4° y 5°. Ley N° 27444, Ley del Procedimiento Administrativo General, del 11/04/01 Artículo 44°. Reglamento sobre vigilancia y control sanitario de los alimentos y bebidas. Art.102. III. REGISTRO SANITARIO 3.3. Base Legal Reglamento sobre Vigilancia y Control Sanitario de Alimentos y Bebidas aprobado por D.S. -007 -98 – SA: Lo pueden obtener de la misma página de Digesa en la sección Normas Sanitarias, colocar en “Seleccione Dirección”: Inocuidad Alimentaria, página 8, con fecha 25 de septiembre de 1998: http://www.digesa.minsa.gob.pe/NormasLegales/Normas/DS007_98.pdf III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a) Solicitud Única de Comercio Exterior (SUCE) www.vuce.gob.pe. Para Obtener N° de SUCE deberá tramitarlo con su Código de Pago Bancario (CPB), esta solicitud tiene carácter de Declaración Jurada e incluye la siguiente información: a.1) Nombre o razón social, domicilio y número de Registro Único de Contribuyente de la persona natural o jurídica que solicita la inscripción o reinscripción. Ejemplo: Razón Social: Grupo Perumex S.A.C Domicilio: Av. Los Aires 319 La Victoria. RUC: 20105588521 Nombre: Pedro Villena Fuentes Domicilio: Jr. Los Jazmines 302 Lince. RUC: 10405965434 III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: Sea empresa o sea persona natural deben verificar que entre las actividades que realiza y que están registradas en la Sunat debe estar la de “Elaboración de productos alimenticios”. a.2) Nombre que refleje la verdadera naturaleza del producto y marca del producto. El nombre debe ser específico, no genérico. Ejemplo 1: - Nombre que refleje la verdadera naturaleza del producto: Yogurt bebible sabor fresa - Denominación comercial: Yogurt frutado - Marca: Deliyogurt. Ejemplo 2: - Nombre que refleje la verdadera naturaleza del producto: Hojuelas de plátano fritas y saladas (con ají). - Denominación comercial: Chifles (Picantes) - Marca: Inka Chips III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.4) Resultados de los análisis físico-químico y microbiológicos del producto terminado, procesado y emitido por laboratorio acreditado por el Instituto Nacional de Calidad - INACAL Entre los recomendados: SGS, La Molina Calidad Total Laboratorios, CERPER, INASA, CERTIFICAL. http://www.inacal.gob.pe/inacal/files/acreditacion/LE/Directorio%20de%20Acredita dos/Rev_449_Directorio_LE_Acreditados_11_Marzo_2016.pdf III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.4.1. Resultados de análisis Microbiológicos: El resultado de análisis deberá estar vigente al momento de efectuar el trámite. Los datos deben corresponder a la empresa o persona natural, la dirección del establecimiento de fabricación y nombre del producto. Verificar que los resultados de los análisis microbiológicos cumplan con los criterios establecidos en la Norma Sanitaria aprobada por la R.M. 591- 2008 MINSA. En el siguiente enlace, según Grupo de Alimentos, se muestran los análisis microbiológicos que se debe realizar a las muestras enviadas y los límites máximos que deben tener. http://www.senasa.gob.pe/senasa/wpcontent/uploads/2015/07/CRITERIOS-MICROBIOLOGICOS-RM-5912008-MINSA.pdf III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: Ejemplo 1: En este caso los límite máximo está dado por “m” no por “M”. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: Modelo de resultado microbiológico. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.4.2. Resultados de análisis Físico-químico: El resultado de análisis deberá estar vigente al momento de efectuar el trámite. (En el caso de documentos extranjeros el tiempo de vigencia es de 1 año). Los datos deben corresponder a la empresa o persona natural, la dirección del establecimiento de fabricación y nombre del producto. Verificar que los resultados de los análisis físicos químicos cumplan con los parámetros establecidos en las normas específicas del CODEX Alimentarius, normas sanitarias nacionales o FDA Ejemplo Leche: pH y Sólidos totales Polvo: Humedad y Cenizas III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: Modelo de resultado físico. químico. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.7) Condiciones de conservación y almacenamiento. Es necesario haber realizado las pruebas de conservación y almacenamiento al producto que vamos a registrar, ya que esas mismas consideraciones irán publicadas en la etiqueta y deben ser reportados en el momento de realizar el trámite. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.8) Datos sobre el envase utilizado, considerando tipo, material y presentaciones. El envase debe ser acorde a las características del producto: Tipo de envase: bolsas, frascos, botellas, cajas, etc. Material: plástico, vidrio, cartón, etc Presentación: Se debe tener una lista de todas las posibles presentaciones que tendrá el producto. 125g, 250 g, 500 g, etc. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.9) Periodo de vida útil del producto en condiciones normales de conservación y almacenamiento. Se debe realizar las pruebas necesarias para saber cuánto tiempo va durar el producto, 1 año, 6 meses, 3 semanas, etc. Y esto está representado en la etiqueta como Fecha de Vencimiento. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.10) Sistema de identificación del Lote de producción. Cada lote producido debe tener un código de identificación (letras y números) que la persona natural o empresa designe según su criterio y características del proceso. Si en caso se prefiera se puede usar la Fecha de Vencimiento como identificación de Lote, pero esto también debe ser registrado en el momento del trámite. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: a.11) Proyecto de rotulado, conforme las disposiciones del presente Reglamento. Se presenta un borrador del proyecto de etiqueta con la información del producto que se detalló anteriormente. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: Datos a considerar: En la declaración de los ingredientes y aditivos empleados en la elaboración del producto se debe consignar los ingredientes que generan hipersensibilidad de ser necesario sombreándola en negrita. Cuando un ingrediente sea a su vez producto de dos o más ingredientes, dicho ingrediente compuesto podrá declararse como tal en la lista de ingredientes, siempre que vaya acompañado inmediatamente de una lista entre paréntesis de sus ingredientes. Todos los datos exigidos en el Art. 117 del Reglamento deben estar en idioma español. III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: El SIN (Sistema Internacional de Numeración de Aditivos Alimentarios) tiene por objeto servir como sistema de identificación de los aditivos alimentarios de uso aprobado en uno o más países miembros. Ejemplo: Sorbato de potasio: SIN= (202) III. REGISTRO SANITARIO 3.4. REQUISITOS PARA LA INSCRIPCIÓN EN EL REGISTRO SANITARIO: III. REGISTRO SANITARIO 3.5. PROCEDIMIENTO Y TRÁMITE ANTE DIGESA: Teniendo toda la información detallada anteriormente proceda a realizar el trámite entrando a la ´pagina de DIGESA : http://www.digesa.sld.pe/ Opción VUCE y seguir los pasos que se mencionan a continuación: III. REGISTRO SANITARIO 3.5. PROCEDIMIENTO Y TRÁMITE ANTE DIGESA: III. REGISTRO SANITARIO 3.6. COSTOS: Ejemplo: Trámite de Inscripción del Registro Sanitario S/.389.90 III. REGISTRO SANITARIO 3.6. COSTOS: III. REGISTRO SANITARIO 3.7. CASOS: RENOVACIONES, MODIFICACIONES (TRANSFERENCIAS): A) RENOVACIONES: El registro sanitario tiene un tiempo de vigencia de 5 años y por lo menos 1 mes antes del vencimiento debo iniciar el proceso de renovación, al igual que en la inscripción debo acceder a la VUCE y seguir el proceso para acceder a la renovación, lo importante es que debemos mantener las mismas características del producto que consideramos en un inicio, si hacemos un cambio, sea en el nombre o en la formulación podría ser observada nuestra solicitud. III. REGISTRO SANITARIO 3.8. DATOS ADICIONALES: Para consultas técnicas pueden escribir al correo: consultas@digesa.minsa.gob.pe o pedir una cita y presentar sus consultas en la misma Digesa en mesa de partes, la respuesta es por currier enviando la respuesta a la dirección fiscal de la empresa en estos casos la demora en las respuesta puede ser de hasta un mes. Visitando esta página pueden ir monitoreando el estado del expediente, o consulta. http://www.digesa.minsa.gob.pe/Expedientes/Consulta_AnexoExpediente.aspx FINALMENTE: Por último: Según Artículo 104 del Decreto Supremos 007: Facultades y obligaciones derivadas del Registro Sanitario: “La obtención del Registro Sanitario de un producto faculta su fabricación o importación y comercialización por el titular del Registro, en las condiciones que establece el presente reglamento. El titular del Registro Sanitario es responsable por la calidad sanitaria e inocuidad del alimento o bebida que libera para su comercialización.”