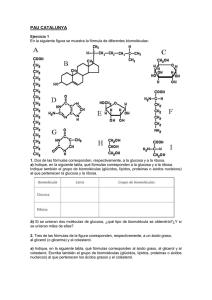
Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 50 MARCEL SAYOL Médico Especialista en Medicina Familiar y Comunitaria Miembro de la Sociedad Española de Medicina de Urgencias y Emergencias Ingeniero Técnico Profesor numerario de IES FUNDAMENTOS Y TÉCNICAS DE ANALISIS BIOQUÍMICO QUÍMICA CLÍNICA CICLO FORMATIVO DE GRADO SUPERIOR “LABORATORIO DE DIAGNÓSTICO CLÍNICO” CRÉDITO 4 Año 2005 Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 2 51 ESTUDIO DEL METABOLISMO DE LOS LÍPIDOS CONTENIDOS Estructura, funciones y clasificación de los lípidos Metabolismo de los lípidos Lípidos séricos. Lipoproteínas Procedimientos de medida de la concentración de lípidos Patrones de alteración del metabolismo lipídico OBJETIVOS ESPECÍFICOS Describir la estructura química de cada una de las clases de lípidos, y clasificarlos según este criterio Describir los procesos de absorción y digestión de las grasas Describir el proceso de oxidación de los ácidos grasos y la formación de cuerpos cetónicos Describir el proceso de biosíntesis de los ácidos grasos y del colesterol Clasificar las lipoproteínas plasmáticas en función de su movilidad electroforética, densidad, velocidad de sedimentación, tamaño y contenido Definir las apolipoproteínas en función de su localización Describir el proceso de transporte de los lípidos endógenos y de los exógenos Enumerar los pasos a efectuar en el proceso de medida de la concentración de lípidos Describir las clases de aspectos del suero Definir los procedimientos más comunes de medida del colesterol y de los TG Definir los criterios de valoración de riesgo de enfermedades cardiovasculares Clasificar las hiperlipoproteinemias y las hipolipoproteinemias Clasificar las anormalidades lisosómicas de lípidos de presentación más frecuente Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 52 1. Estructura, funciones y clasificación de los lípidos 1.1. Química de los lípidos Desde el punto de vista de su estructura química, los lípidos son compuestos orgánicos hidrocarbonados que constituyen ésteres reales o potenciales de ácidos grasos. Todos ellos tienen dos propiedades comunes: ser insolubles en agua y ser extraíbles de las células y de los tejidos por disolventes no polares tales como el cloroformo, el éter y el benceno entre otros. Existen diversas clases de lípidos según su constitución química, así pues cabe destacar en primer lugar a los ácidos grasos, compuestos esenciales de la mayor parte de los lípidos, los triglicéridos que son los más abundantes, los fosfolípidos, formados por la adición de un grupo fosfórico, los esfingolípidos formados por la unión de un ácido graso con una molécula de esfingosina, los glucolípidos formados por la unión con un hidrato de carbono, los lípidos insaponificables en los que se incluyen los esteroides y los terpenos, las ceras formadas por la unión de un ácido graso y un alcohol de cadena larga, y por último las lipoproteínas combinación de un lípido y una proteína, muy abundantes en el plasma. Las funciones de cada una de estas clases de lípidos es diferente, pero cabe destacar como las más relevantes la de constituir la forma más importante de almacenar energía y la de formar las membranas celulares. 1.2 Ácidos grasos Son ácidos alifáticos de cadena larga y constituyen las unidades básicas de varias clases de lípidos, además son los responsables del aspecto graso o aceitoso que poseen todos los lípidos. Los ácidos grasos no se encuentran en estado libre sino que aparecen como producto de la hidrólisis de los lípidos o unidos a ellos por enlaces covalentes. Poseen una larga cadena hidrocarbonada con un grupo carboxilo Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 53 terminal, ejemplo de ello son el ácido palmítico y el ácido oleico representados en la figura 2.1 Los ácidos grasos tienen una fórmula común: R-COOH, donde R representa la larga cadena hidrocarbonada que puede tener de 4 a 26 átomos de carbono, o bien más detalladamente: CH3-(CH2)n-COOH. Su nombre sistemático deriva del hidrocarburo con el cual está emparentado sustituyendo la terminación o por la de oico final. Cuando tiene un doble enlace la sustitución es por cenoico, si tiene dos enlaces dobles la sustitución es por dienoico, y con tres dobles trienoico. El símbolo 18:0 quiere decir un ácido graso con 18 átomos de carbono sin enlaces dobles, el símbolo 18:2 significa un ácido graso de 18 carbonos con dos dobles enlaces, etc. Los átomos de carbono se numeran a partir del extremo carboxilo y a los átomos número 2 y 3 se les llama a veces carbono α y carbono β respectivamente y al último carbono (el carbono metilado del extremo distal de la cadena), carbono ω. La posición del doble enlace viene representada por el símbolo Δm por ejemplo Δ10 indica que hay un doble enlace entre los carbonos números 10 y 11. En el caso de haber más de un doble enlace, la notación Δm indicará la posición del primero de ellos, quedando los siguientes en las posiciones más cercanas posibles al primero, teniendo en cuenta que los enlaces dobles no se hallan nunca conjugados, es decir no tienen la forma: (-CH=CH-CH=CH-), sino que se encuentran separados por un grupo metileno: (-CH=CH-CH2-CH=CH-). Así pues, la notación que correspondería al ácido linoleico sería 18:2 Δ6, igualmente para el ácido linolénico sería: 18:3 Δ3, y para el ácido araquidónico: 20:4 Δ6. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 54 Figura 2.1 Dos ejemplos de la estructura de un ácido graso Figura 2.1 Ácido esteárico O C CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2-CH2- CH2- CH2- CH2- CH2-CH3 HO Ácido oleico O C CH2 -CH2-CH2- CH2-CH2- CH2-CH2 -CH CH- CH2-CH2-CH2 - CH2- CH2-CH2-CH2-CH3 HO La cadena hidrocarbonada de la cual están formados los ácidos grasos puede ser de tres tipos, saturada, con uno o más enlaces dobles y con enlaces triples. Los ácidos grasos saturados son aquellos que poseen enlaces simples entre sus átomos de carbono, los ácidos grasos monoinsaturados son aquellos que tienen un solo enlace doble y los ácidos grasos poliinsaturados son aquellos que tienen dos o más enlaces dobles en su cadena. Los ácidos grasos con algún enlace triple son escasos en la naturaleza. Los ácidos grasos difieren entre sí por la longitud de su cadena y por el número y la posición de sus enlaces insaturados. La mayoría de los ácidos grasos naturales poseen un número par de átomos de carbono y los que contienen 16 o 18 átomos de carbono son los que más abundan. Una característica muy importante de los ácidos grasos es la de tener un extremo, el carboxilo, muy polar e hidrófilo, mientras que el otro extremo es no polar e hidrófobo. Esta característica se manifiesta claramente cuando se ponen en contacto Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 55 un ácido graso y agua, el ácido graso forma entonces una capa monomolecular sobre la superficie del agua, de manera que el grupo carboxilo se introduce en el agua y la cadena no polar sobresale por encima de la superficie sin contactar por lo tanto con el agua. Se denominan ácidos grasos esenciales aquellos que siendo imprescindibles para el funcionamiento del organismo, se deben incluir en la dieta puesto que el metabolismo carece de los mecanismos para su síntesis endógena. Los ácidos grasos esenciales son tres: el ácido linoleico, el ácido linolénico y el ácido araquidónico, aunque respecto a este último hay autores que no lo consideran esencial debido a que se puede sintetizar a partir del ácido linoleico y por lo tanto sería sólo esencial si existiera carencia de éste. Los ácidos grasos más abundantes que se hallan en la naturaleza se resumen en las tablas 2.1 y 2.2 siguientes. TABLA 2.1 ÁCIDOS GRASOS SATURADOS Nº de Estructura química Nombre átomos de Nombre trivial sistemático carbono 12 CH3(CH2)10COOH n-dodecanoico Ácido láurico 14 CH3(CH2)12COOH n-tetradecanoico Ácido mirístico 16 CH3(CH2)14COOH n-hexadecanoico Ácido palmítico 18 CH3(CH2)16COOH n-octadecanoico Ácido esteárico 20 CH3(CH2)18COOH n-eicosanoico Ácido araquídico 24 CH3(CH2)22COOH n-tetracosanoico Ácido lignocérico Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 56 TABLA 2.2 ÁCIDOS GRASOS INSATURADOS Nº de átomos de Estructura química carbono 16 Nombre trivial CH3(CH2)5CH=CH(CH2)7COOH Ácido palmitoleico 18 CH3(CH2)7CH=CH(CH2)7COOH Ácido oleico 18 CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH Ácido linoleico 18 CH3CH2CH=CHCH2CH=CHCH2CH=CH(CH2)7COOH Ácido linolénico 20 CH3(CH2)4CH=CHCH2CH=CHCH2CH=CHCH2CH=CH(CH2)3COOH Ácido araquidónico 1.3 Triglicéridos Son compuestos que contienen ácidos grasos como constituyentes, son los más sencillos y abundantes de entre todos los lípidos. Para su designación también se emplean los sinónimos siguientes: lípidos neutros, grasas y triacilglicéridos y suelen representarse por las siglas TG. Químicamente son ésteres del alcohol glicerina y de tres moléculas de ácidos grasos (R1, R2, R3). En la figura 2.2 se representa la estructura general de los triglicéridos y como ejemplo uno de ellos, la tripalmitina. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 57 Figura 2.2 Estructura general de los triglicéridos. Ejemplo: tripalmitina Estructura general de un ácido graso H H H H C C C O O O C R1 H C C O R2 C Glicerina O R3 Tripalmitina Glicerina H O H O O C CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2-CH3 O H C O C CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2-CH3 O H C O C CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2- CH2- CH2- CH 2- CH2-CH3 H Res iduos de palmítico Figura 2.2 Los TG no poseen carga eléctrica, y por lo tanto no son polares pero sí hidrofóbicos y tienen una densidad más baja que la del agua. Constituyen los componentes principales del depósito graso de reserva en las células animales y en las plantas, pero no se encuentran formando las membranas celulares. Existen dos grupos de TG, los simples y los mixtos. Los primeros contienen los tres ácidos grasos iguales, mientras que los mixtos contienen dos o más ácidos grasos distintos. Si los TG se someten a ebullición o se mezclan con ácidos o con bases, se hidrolizan, proceso que recibe el nombre de saponificación. El proceso resumido se representa en el siguiente esquema: 3NaOH TG → Glicerina + 3 ácido graso-Na Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 58 Existen enzimas pancreáticos llamados lipasas que también tienen acción hidrolizante sobre los TG. Los TG que proceden de fuentes animales suelen tener cadenas de ácidos grasos cortas y saturadas y se solidifican a temperatura ambiente, los que proceden de fuentes vegetales suelen tener cadenas más largas y poliinsaturadas y permanecen en estado líquido incluso a temperaturas bajas. Cuando los TG se exponen al aire puede ocurrir un proceso llamado auto-oxidación consistente en que el oxígeno molecular puede atacar a los ácidos grasos que tienen dos o más enlaces dobles rindiendo productos complejos (éstos son los responsables del sabor desagradable de las grasas rancias). El proceso de auto-oxidación no tiene lugar normalmente en las células puesto que lo impide la acción de la vitamina E, algunos enzimas y posiblemente también la acción de la vitamina C, pero puede ocurrir que en algunas enfermedades en las que se producen depósitos lipídicos anormales en los tejidos, el proceso de auto-oxidación sí tenga lugar. La principal función de los TG es la de constituirse como lípidos de reserva, para ello se localizan en el citoplasma celular en forma de gotitas aceitosas microscópicas dispersadas y emulsionadas. En los adipocitos o células grasas, los TG se encuentran almacenados en grandes cantidades en forma de gotitas de grasa que ocupan prácticamente todo el citoplasma. El poder de almacenar energía es mucho mayor en los TG que en el glucógeno ya que a igualdad de masa, rinden más del doble de calorías los primeros que el segundo. Otra función importante de los TG que se encuentran almacenados en los adipocitos, es servir de aislante térmico frente a temperaturas muy bajas, función que se hace especialmente patente en algunos animales como las focas y las morsas entre otros. El tejido adiposo sirve también como tejido de relleno que ocupa los espacios existentes entre los órganos internos. 1.4 Fosfolípidos Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 59 Llamados también lípidos polares, son compuestos sólidos que tienen un aspecto céreo y se localizan casi exclusivamente en las membranas celulares y en el plasma, aunque se pueden encontrar trazas en los depósitos grasos. Su función principal, como se deduce, es pues de tipo estructural. Los fosfolípidos son ésteres del glicerol que contienen un grupo de ácido fosfórico en uno de los átomos de ca Como características de los fosfolípidos, hay que distinguir en primer lugar la existencia de una cabeza hidrofílica muy polar junto con una carga negativa en el grupo P (a pH=7), además los grupos R que tuviese la molécula de fosfolípido, pueden aportar otra u otras cargas eléctricas adicionales. Las colas hidrocarbonadas son de tipo no polar, esto hace que puedan formar micelas en el agua. Los fosfolípidos pueden experimentar hidrólisis por la acción de ácidos, bases y por enzimas llamadas fosfolipasas. rbono terminales de la cadena del glicerol. Pueden tener además otros grupos enlazados a la porción fosfato como por ejemplo si hay una molécula de colina, se llamará fosfatidilcolina (figura 2.3), si contiene una etanolamina se llamará entonces fosfatidiletanoamina, etc. Figura 2.3 Fosfatidilcolina. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 60 + N(CH 3) 3 Figura 2.3 CH 2 Colina CH 2 Cabeza polar O O P O - O H H CH 2 C C O O C Cola no pol ar O H C CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH CH 2 CH CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 3 CH3 O 1.5 Esfingolípidos Este tipo de lípidos contienen una sustancia llamada esfingosina que es un aminoalcohol de cadena larga, o en su defecto un análogo, unida a una molécula de ácido graso también de cadena larga y un alcohol polar. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 61 Los esfingolípidos se clasifican en: 1) esfingomielinas que contienen una fosfocolina o fosfoetanolamina y fósforo, por lo que también se las puede clasificar como fosfolípidos, son las más abundantes y se hallan en las membranas de las células animales y en la cubierta que rodea las células nerviosas, (figura 2.4). 2) Los cerebrósidos contienen una glucosa o una galactosa y no contienen fósforo ni tampoco poseen carga eléctrica. 3) Los gangliósidos contienen un oligosacárido y es muy frecuente que una o más de sus unidades de monosacárido terminales sea el ácido N-acetilneuramínico llamado también ácido siálico, los gangliósidos tampoco tienen fósforo y constituyen el 6% aproximadamente de los lípidos de las membranas en la materia gris del cerebro, así como también se encuentran en los lugares específicos situados en la superficie de las neuronas que sirven de unión a los neurotransmisores sinápticos. 1.6 Glucolípidos Son lípidos que contienen un azúcar en su molécula, pero carecen de grupo fosfórico, los más sencillos son los glucosildiacilglicéridos que se encuentran en las plantas y en determinados microorganismos. Se da la circunstancia que los cerebrósidos y los gangliósidos se pueden clasificar como esfingolípidos, tal como se ha visto en el apartado anterior, y también como glucolípidos puesto que contienen a la vez azúcar y esfingosina. Figura 2.4 Estructura de la esfingomielina Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol CH3 CH 3 N+ CH 3 CH 2 Figura 2.4 62 Cabeza de fosfocolina CH 2 O O P - O O CH 2 H C H C HC Esfingosina NH OH C O CH 2 CH CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH CH2 CH CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH2 CH 2 CH 3 CH 2 Ácido gra so CH 2 CH 3 1.7 Ceras Las ceras constituyen una clase de lípidos que se forman por la esterificación de un ácido graso con un alcohol de cadena larga, saturados y no saturados. La mayor parte de ellos se encuentran formando diferentes estructuras del organismo humano y de los animales. Son segregados por las glándulas sebáceas de la piel a modo de recubrimiento de la misma y para mantenerla flexible, impermeable y lubrificada. El Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 63 pelo, el vello y la lana de los animales además de las plumas, también contienen ceras, así como en las hojas de muchas plantas, en las frutas, en algunos insectos y en la cera de las abejas en forma de ácido palmítico. 1.8 Lípidos insaponificables La característica más relevante de esta clase de lípidos es que no experimentan hidrólisis. Se clasifican en dos grupos los esteroides y los terpenos que describimos a continuación. a) Los esteroides son moléculas derivadas del núcleo de un compuesto llamado perhidrociclopentanofenantreno cuya estructura Representa en la figura 2.5. 26 CH3 25 HC Figura 2.5 27 CH3 24 CH2 23 CH2 22 CH2 18 CH3 12 11 C 19 CH3 1 2 HO 14 A B 5 4 17 D 16 15 9 10 3 13 20 CH3 HC 21 8 Núcleo del perhidrociclopentanofenantreno 7 6 Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 se Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 64 Existen numerosos compuestos en el metabolismo humano con estructura de esteroide, entre ellos resulta importante destacar los ácidos biliares, las hormonas sexuales, tanto masculinas como femeninas, las hormonas de la corteza adrenal y los esteroles como el colesterol (figura 2.5) y el lanosterol Cabe destacar también la existencia de algunos esteroides constituyendo los venenos de los sapos. b) Los terpenos derivan del isopreno (2-metil-1,3-butadieno) y pueden ser moléculas lineales o cíclicas. Un terpeno importante es el β-caroteno, sustancia aceitosa de color rojo-pardo muy abundante en las zanahorias, formada por 8 residuos de isopreno y que es un precursor de la vitamina A o retinol. Las otras tres vitaminas liposolubles, la vitamina E, la vitamina K y la vitamina D, pertenecen también a este grupo. 1.9 Lipoproteínas Son asociaciones de ciertas proteínas con lípidos, las más importantes son las proteínas plasmáticas de las que trataremos más extensamente en el apartado 3. Una característica de las lipoproteínas es que no existe enlace covalente entre el lípido y la proteína que la forma. Pueden contener lípidos polares, lípidos neutros o colesterol y sus ésteres. Actúan como vehículos de transporte de los lípidos desde el intestino delgado hasta el hígado y de éste a los depósitos grasos y a otros tejidos. 1.10 Micelas lipídicas En los sistemas acuosos (al igual que en los jabones), los lípidos polares se dispersan para formar las llamadas micelas constituidas por asociaciones de estos lípidos dispuestos uno al lado de otro formando un compartimento cerrado, (figura 2.6). Cada lípido posee un extremo polar o hidrófilo y un extremo no polar o hidrófobo, razón por la cual se disponen de la manera descrita cuando se hallan dispersos en agua. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol Figura 2.6 Micela lipídica, monocapa y bicapa lipídica Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 65 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 66 También pueden formar monocapas en las superficies acuosas con sus cabezas hidrofílicas proyectadas hacia el interior de la fase acuosa y las colas hidrocarbonadas hidrofóbicas expuestas al aire. Otra posibilidad es también la formación de bicapas que son estructuras cooperativas que se mantienen juntas mediante muchas interacciones reforzantes de tipo no covalente, así como por fuerzas atractivas existentes entre cadenas adyacentes. Actualmente se acepta que las propiedades de las bicapas son muy semejantes a las de las membranas biológicas formadas por una bicapa fosfolipídica con proteínas específicas y enzimas. Los liposomas o vesículas lipídicas son de forma esférica ligeramente alargadas con un diámetro de varios cientos de angstroms (Ǻ) y con un grosor de cada capa de unos 50 Ǻ. En su interior pueden quedar atrapados iones o moléculas. Tienen interés farmacológico. 1.11 Funciones del tejido adiposo El tejido adiposo está constituido fundamentalmente por un conjunto de células que contienen gran cantidad de triglicéridos formando la llamada gota lipídica que ocupa prácticamente todo el citoplasma. El tejido adiposo tiene cinco funciones: 1) Constituir el material de reserva energética. 2) Aislamiento térmico que protege de las pérdidas de calor hacia el exterior del organismo. 3) Acolchonamiento de determinadas partes del cuerpo como las plantas de los pies y las palmas de las manos que amortiguan la presión ejercida sobre ellas. 4) Función de relleno entre los órganos internos. Éstos al no poseer formas geométricas regulares dejan espacios virtualmente vacíos entre sí que se rellenan de grasa. Sucede a veces en individuos muy delgados, por ejemplo en la anorexia nerviosa, que los espacios situados debajo de los riñones al ser deficientes Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 67 en grasa, impiden el sostenimiento adecuado de estos órganos y se desplazan hacia abajo (ptosis renal), localizándose en una posición anómala. 5) Configuración de la silueta externa del organismo, que si bien es una función muy importante en algunos animales, en el humano se limita a contribuir en la diferenciación de la forma corporal entre los dos sexos. 2. Metabolismo de los lípidos 2.1 Digestión y absorción de grasas Los lípidos constituyen una parte muy importante de la nutrición y se obtienen a partir de la grasa animal en forma de triglicéridos y colesterol fundamentalmente, y de los vegetales como lípidos poliinsaturados y de fitosterol, que es el equivalente al colesterol de las plantas. Los lípidos exógenos se incorporan al organismo en tres fases: la digestión, la absorción y el transporte. En la fase de la digestión, que tiene lugar en la luz intestinal, juega un importante papel la bilis formada sobretodo por ácidos biliares anfipáticos *(2), que actúan sobre los acúmulos de lípidos deglutidos transformándolos en pequeñas micelas más fácilmente accesibles a la acción de los enzimas digestivos (proceso que se conoce con el nombre de emulsión) *(3). Los enzimas digestivos que se producen en el páncreas son la lipasa pancreática *(4), la colesterolesterasa y la fosfolipasa A, el primero actúa sobre los triglicéridos liberando ácidos grasos formando monoglicéridos, diglicéridos y glicerol, la segunda actúa sobre los enlaces estéricos liberando ácidos grasos y colesterol libre, y el último tiene acción hidrolizante sobre los fosfolípidos *(5). En la fase de absorción, los lípidos atraviesan la mucosa intestinal y alcanzan el interior de las células mucosas por un mecanismo de pinocitosis. La mayor parte de Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 68 las grasas ingeridas pasa a los vasos linfáticos antes de alcanzar el sistema sanguíneo. Los TG así absorbidos se distribuyen fundamentalmente en el tejido subcutáneo, localizándose en el interior de los adipocitos. 2.2 Oxidación de los ácidos grasos Como ya se ha mencionado los triglicéridos tienen fundamentalmente la función de proveer de energía a los humanos y animales, por término medio proporcionan más del 40% de la energía que necesita diariamente un individuo de un país desarrollado, y abastecen de forma significativa a órganos como el hígado, el corazón y el músculo esquelético. Cada gramo de peso proporciona unas 9 kilocalorías, energía que se almacena en los enlaces de los ácidos grasos en su mayor parte, mientras que el glicerol contribuye sólo en un 5%. Los ácidos grasos se activan y se oxidan en la mitocondria de los hepatocitos por pérdida sucesiva de fragmentos de dos carbonos mediante la llamada beta-oxidación en la cual el átomo de carbono en posición beta se oxida y produce un β-cetoácido. Los ácidos grasos que alcanzan el hepatocito tienen dos procedencias, unos vienen de la sangre unidos a la albúmina y otros proceden de la hidrólisis de los TG por acción de las lipasas. Cuando los ácidos grasos se encuentran en el citoplasma deben someterse a la acción de las sintetasas de acil-CoA que catalizan la reacción esquematizada en la figura 2.7, puesto que como ácidos grasos libres no pueden atravesar la membrana mitocondrial. Figura 2.7 Preparación de un ácido graso para su entrada en la mitocondria Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 69 Figura 2.7 ATP R-COOH + CoA-SH AMP R C S CoA O (Acil-CoA) En esta reacción se forma un enlace tioéster entre el grupo carboxilo del ácido graso y el grupo tiol del CoA, generando acil-CoA, éstos no pueden todavía atravesar la membrana mitocondrial, pero la acción de dos enzimas, la carnitín-aciltransferasa-I y la carnitín-aciltransferasa-II catalizan la unión del acil-CoA con la carnitina pudiendo ahora atravesar la membrana. La carnitina es sintetizada por los humanos a partir del aminoácido lisina y se encuentra en la matriz interna de la mitocondria. El acil-CoA se encuentra ahora en disposición de poderse oxidar y lo hace en dos fases. En la primera fase los ácidos eliminan fragmentos de 2 carbonos, iniciándose en el extremo carboxilo de la cadena mediante una serie de repeticiones de acciones enzimáticas que consiguen separar una unidad de acetilo de 2 carbonos cada vez, (figura 2.8). Por ejemplo el ácido palmítico se somete a siete pases enzimáticos, y en cada uno se separa una unidad de 2 carbonos en forma de acetil-CoA. Al final de los siete pases queda una unidad de 2 carbonos en forma de acetil-CoA, rindiendo globalmente 8 fragmentos de 2 carbonos en forma de acetil-CoA. En la segunda fase los restos de acetil-CoA entran en el ciclo de Krebs. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 70 La oxidación completa del ácido palmítico produce 129 moléculas de ATP, de los cuales 96 proceden de las ocho moléculas de acetil-CoA, 21 de las 7 moléculas de NADH oxidadas en la cadena respiratoria, y 14 de las 7 moléculas de FADH2 *(6) también oxidadas en la cadena respiratoria, (obsérvese que en conjunto suman 131 moléculas de ATP, pero en el proceso de activación del ácido palmítico se consumen 2 moléculas, por lo que el resultado neto es de 129). Los ácidos grasos de cadena impar, liberan propionil-CoA (H3C-CH2-CO-S-CoA) en la etapa final de la tiolisis. Figura 2.8 β-oxidación de los ácidos grasos Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 71 O R CH 2 CH 2 CH 2 S C CoA (Acil-CoA) FAD 1) Oxidación FADH2 R CH 2 C H O C C S CoA (Enoil-CoA) H H 2O R CH 2 2) Hidratación OH H O C C C H H + NAD CoA S (L-hidroxiacil-CoA) 3) Oxidación H + + NADH O R CH 2 C O CH2 CoA-SH C S CoA 4) Tiolisis O R CH 2 (Cetoacil-CoA) C O S (Acil-CoA acortado en 2 átomos de C) CoA + H3 C C S CoA (Acetil-CoA) Figura 2.8 2.3 Formación de cuerpos cetónicos El acetil-CoA formado en la oxidación de los ácidos grasos tiene como destino entrar en el ciclo de Krebs, pero para ello es necesario que exista un equilibrio en las degradaciones de grasas y de hidratos de carbono. Para que el acetil-CoA pueda Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 72 entrar en el ciclo de Krebs dependerá de sí el oxalacetato es asequible para unirse al acetil-CoA y formar citrato. Si la degradación de grasas es mucho mayor que la degradación de hidratos de carbono, tal como sucede en la diabetes mellitus y en el ayuno prolongado, la concentración de oxalacetato será baja debido a que éste se utiliza para la formación de glucosa (gluconeogénesis). Por otra parte en la diabetes, los tejidos no pueden utilizar la glucosa como fuente de energía y es por eso que en su lugar utilizarán a las grasas. De todo ello se deduce que habrá poco oxalacetato y no podrá condensarse con el acetil-CoA, entonces éste se degradará por otra vía formando los llamados cuerpos cetónicos, (figura 2.9). Los cuerpos cetónicos se forman a partir de dos moléculas de acetil-CoA según el esquema representado en la figura 2.10. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol Figura 2.9 Vías metabólicas del acetil-CoA con déficit de oxalacetato Figura 2.9 [Oxalacetato] Gluconeogénesis + Acetil-CoA Cuerpos cetónicos Ciclo de Krebs Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 73 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 74 Figura 2.10 Formación de cuerpos cetónicos H HO NAD C + + NAD H + H CH3 O + H C CH3 CH 2 CH 2 COO COO D-3-hidroxibutirato Acetoacetato D-3-hidroxibutirato CO 2 O CH 3 C CH 3 Acetona D-3-hidroxibutirato Acetoacetato Acetoacetato Acetona Hepatocito Sangre Tejidos Figura 2.10 En las mitocondrias de las células hepáticas, dos moléculas de acetil-CoA de hidratan y dan acetoacetato más dos moléculas de CoA y un hidrogenión, el acetoacetato así formado se convierte en D-3-hidroxibutirato, o bien en acetona que pasan a la sangre y posteriormente a los tejidos donde puede tener lugar también la conversión de acetoacetato a D-3-hidroxibutirato y acetona. Estos tres compuestos se les llama comúnmente cuerpos cetónicos, una producción excesiva de cuerpos cetónicos se denomina cetosis. El acetoacetato y el D-3-hidroxibutirato constituyen combustibles normales de las células, sobretodo las del músculo cardíaco y de la corteza renal. En los tejidos periféricos, el acetoacetato se combina con el succinil-CoA y después de varias reacciones se convierte en dos moléculas de acetil-CoA que se incorporan al ciclo de Krebs para su oxidación completa. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 75 2.4 Biosíntesis de ácidos grasos La biosíntesis de ácidos grasos tiene lugar en el citoplasma celular a partir del acetilCoA, transformándose éste en diversas sustancias intermedias y finalmente en ácido palmítico. Se precisa además la intervención de ATP y de NADPH. La síntesis de ácidos grasos no tiene lugar por la ruta inversa a su degradación, sino que ambos ocurren por vías distintas. Además la síntesis tiene lugar en el citoplasma en lugar de la matriz mitocondrial como ocurre en la oxidación. El acetil-CoA se combina con el dióxido de carbono y en presencia de ATP, dando malonil-CoA, ADP, y fósforo inorgánico (Pi), en una reacción irreversible: Acetil-CoA + ATP + CO2 → Malonil-CoA + ADP + Pi La reacción es catalizada por el enzima acetil-CoA-carboxilasa que contiene un grupo prostético (ver unidades 3 y 5) llamado biotina *(7) que es una vitamina. La biotina funciona como transportador de CO2. El malonil-CoA de tres átomos de carbono es un precursor de las unidades de dos carbonos con las que se construye la cadena de ácido graso. La molécula de acetilCoA funciona como cebador o iniciador del proceso en el cual el extremo carboxilo pasará a formar el carbono número 15 del ácido palmítico formado, mientras que el grupo metilo pasará a formar el carbono número 16. Por lo tanto el crecimiento de la cadena se hace posible por la adición sucesiva de restos acetilo al extremo carboxílico de la cadena, estos grupos acetilo derivan de los dos átomos de carbono del malonilCoA, el tercer carbono del malonil-CoA se pierde en forma de CO2. En este proceso es muy importante la participación de una proteína transportadora de acilos, llamada abreviadamente ACP. El ácido palmítico formado se puede alargar para formar otros ácidos grasos saturados por la acción de dos sistemas enzimáticos situados, uno en la mitocondria y Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 76 el otro en el retículo endoplasmático. La prolongación se obtiene por adiciones sucesivas de acetil-CoA en el primer sistema enzimático, y de malonil-CoA en el segundo. A partir del ácido palmítico también pueden formarse ácidos grasos insaturados, pero no existen enzimas en los mamíferos para introducir dobles enlaces entre carbonos a partir del carbono número 9, motivo por el cual no se pueden sintetizar los llamados ácidos grasos esenciales 2.5 Biosíntesis de colesterol El colesterol es sintetizado en forma endógena por el hígado a razón de aproximadamente unos 1,5 gramos diarios. Mientras que el colesterol aportado de forma exógena por la dieta es solamente de 0,15 a 0,3 gramos diarios, hecho que hay que resaltar si se considera la importancia que se le atribuye al exceso de colesterol en el organismo como causa de enfermedad cardiovascular. El colesterol tiene tres funciones básicas: 1) Está presente en las membranas de las células eucariotas, pero no de las procariotas. 2) Forma parte de las lipoproteínas plasmáticas. 3) Es un precursor de las hormonas esteroideas (progesterona, testosterona, estradiol, cortisol, etc.). 3) Es un precursor de las sales biliares. El colesterol procede del acetil-CoA *(8). El Acetil-CoA, molécula de 2 carbonos se convierte a través de sucesivas transformaciones bioquímicas en una molécula de colesterol de 27 átomos de carbono, (tabla 2.3). El paso de acetil-CoA a mevalonato de 6 carbonos, es irreversible y está catalizado por el enzima 3-hidroxi-3metilglutaril-CoA-reductasa (abreviadamente HMG-CoA-reductasa), que es un enzima limitante de la biosíntesis del colesterol, por lo que su actividad será el principal factor en la regulación de la producción endógena de colesterol. Algunos fármacos del grupo de las estatinas, como la lovastatina, la simvastatina o la pravastatina inhiben la actividad de este enzima y producen consecuentemente una disminución de la producción de colesterol endógeno. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 77 TABLA 2.3 Nombre Número de átomos de carbono Acetil-CoA 2 Mevalonato 6 Isopentenilpirofosfato 5 Farnesilpirofosfato 15 Escualeno 30 Lanosterol 30 Colesterol 27 3. Lípidos séricos. Lipoproteínas 3.1 Introducción Los lípidos plasmáticos están formados por las siguientes sustancias: Colesterol, el 30% en forma libre y el 70% en forma esterificada Triglicéridos Fosfolípidos Ácidos grasos libres El transporte de estos compuestos se lleva a cabo de forma tal que los ácidos grasos libres van unidos a la albúmina, mientras que los restantes van unidos a las lipoproteínas plasmáticas. El estudio de las lipoproteínas tiene especial interés por el hecho de haberse demostrado que la cardiopatía isquémica, primera causa de muerte en los países desarrollados, guarda una estrecha relación con los niveles plasmáticos de dichas sustancias. Los lípidos procedentes de la ingesta o de la producción endógena tienen que ser transportados a través de la sangre, desde el intestino y desde el hígado Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 78 respectivamente, hasta la célula, lugar de consumo o almacenamiento, pero ocurre que el colesterol y los triglicéridos son muy hidrofóbicos y por ello no pueden ser transportados de manera directa en la sangre sino que se hace necesario un sistema de transporte que posibilite su solubilización. Este sistema de transporte está constituido por un conjunto de moléculas llamadas lipoproteínas. 3.2 Lipoproteínas plasmáticas Las lipoproteínas constan de los siguientes componentes, (figura 2.11): 1) Cubierta anfipática. Constituida por una capa de fosfolípidos con cabezas polares dirigidas hacia el exterior de la partícula, y por ácidos grasos dirigidos hacia el interior de la misma formando el núcleo apolar. Además la cubierta presenta algunas moléculas de colesterol libre con su grupo hidroxilo dirigido hacia las cabezas polares de los forfolípidos. 2) Apolipoproteínas. Formadas por cadenas polipeptídicas que desarrollan una función estructural y sobretodo dirigen el metabolismo de las lipoproteínas además de constituir el lugar específico de reconocimiento por parte de los receptores de membrana celulares. 3) Núcleo apolar. Se trata de un microentorno de carácter hidrofóbico que está constituido por lípidos no polares, ésteres de colesterol y triglicéridos. Hay que constatar que las lipoproteínas no presentan una estructura estática, sino que se encuentran en continua reorganización. Esta dinámica depende del estado metabólico de cada partícula en cada momento concreto, esto hace que en los procesos metabólicos de estas partículas existan notables intercambios entre los lípidos y las proteínas que las forman. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 79 Figura 2.11 Estructura general de una lipoproteína Figura 2.11 Colesterol no esterificado Triglicéridos Apolipoproteínas Fosfolípidos Ésteres de colesterol Las lipoproteínas plasmáticas fueron en un principio, aisladas y caracterizadas según su densidad mediante ultracentrifugación, clasificándose según su velocidad de sedimentación en unidades Svedberg (ver unidad didáctica número 15 del libro Fundamentos y Técnicas de Análisis Bioquímico-Técnicas Instrumentales del mismo autor), originándose de ello una terminología que todavía se sigue usando. Posteriormente las lipoproteínas del plasma se pudieron aislar también mediante técnicas electroforéticas dando lugar a la clasificación en lipoproteínas alfa, beta, y pre-beta. Esta clasificación tiene una correlación muy exacta con la clasificación mediante las siglas HDL, LDL, VLDL respectivamente, (tabla 2.4). Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 80 TABLA 2.4 Nombre originado por ultracentrifugación Quilomicrones Unidades Svedberg (S) Tamaño (nm) Contenido 75-1200 90% deTG y 4% de colesterol 62% de TG y 18% de colesterol 35% de TG y 35% de colesterol 10% de TG y 60% de colesterol 10% de TG y 60% de colesterol 36% de TG y 14% de colesterol Nombre originado por electroforesis Sin movilidad Densidad (δ) (g/cm3) VLDL Pre-β 0,93 < δ < 1,006 IDL Pre-β 1,006< d < 1,019 LDL β 1,019 < δ< 1,063 Lp(a) β y pre-β 1,050 < δ < 1,12 26-30 HDL α 1,063 < δ < 1,21 5-12 δ < 0,93 20-400 28-75 25-35 0-20 18-25 Las siglas VLDL significan lipoproteínas de muy baja densidad, las LDL significan lipoproteínas de baja densidad y las HDL significan lipoproteínas de alta densidad. Las siglas Lp(a) hacen referencia a la lipoproteína a que últimamente se ha relacionado como factor de riesgo independiente en cuanto a enfermedad cardiovascular, (parece ser que a partir de niveles superiores a 30 mg/dL tiene una correlación muy positiva con los infartos de miocardio). La Lp(a) es una lipoproteína parecida a la LDL pero difiere en el tipo de apoproteína. Migra a la región pre-β en la electroforesis, su tamaño es intermedio entre las VLDL y las LDL y su densidad se encuentra en el rango de la HDL. Tiene una homología molecular considerable con el plasminógeno y los genes de ambas proteínas se encuentran en el cromosoma 6 muy próximos entre sí. El papel de transportador es distinto en cada una de las lipoproteínas, de manera que fundamentalmente el colesterol es transportado por las LDL y las HDL, mientras que los triglicéridos lo son por las VLDL y por los quilomicrones. Los quilomicrones son las fracciones de lipoproteínas que tienen mayor tamaño y además son las de menor densidad debido a su alto contenido en TG y bajo contenido Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 81 en proteínas. Cuando se deja reposar una muestra de suero lipémico a una temperatura de 4 a 6° C durante 12-16 horas, se puede observar una capa cremosa en la parte superior debido a que tienen menor densidad que las otras lipoproteínas. Los quilomicrones se sintetizan en el epitelio intestinal y se liberan al sistema linfático alcanzando posteriormente el sistema sanguíneo a través del conducto torácico y la vena yugular. Las VLDL son moléculas sintetizadas por el hígado a partir de remanentes de quilomicrones, son cofactores necesarios para que la lipoproteinlipasa hidrolice a los TG, que pasan a los tejidos dando lugar a moléculas IDL. 3.3 Apolipoproteínas Constituyen la parte proteica de las lipoproteínas y cada una de ellas puede contener varios tipos de apoproteínas. Las más importantes son las siguientes: la Apo B que tiene dos variantes: la Apo B100 de síntesis hepática y la Apo B48 de síntesis intestinal, la primera se encuentra en la LDL, VLDL e IDL, la segunda forma parte de los quilomicrones. La Apo E se encuentra en todas las clases de lipoproteínas excepto en la LDL, se sintetiza en el hígado y su función principal es el reconocimiento de las lipoproteínas por parte de receptores de membrana. La Apo C es una familia de péptidos de síntesis hepática y se encuentra sobretodo en las VLDL, en los quilomicrones y en las HDL. Otras clases de apoproteínas son la Apo AI, la Apo AII y la Apo A IV. 3.4 Transporte de lípidos de origen exógeno Los lípidos procedentes de la absorción intestinal son reesterificados en la célula de la mucosa intestinal formando de nuevo TG, fosfolípidos y ésteres de colesterol que se unen a las apoproteínas y forman un quilomicrón. Éste pasa a la linfa y después a la sangre. Una clase de apoproteína del tipo Apo C permite al quilomicrón interaccionar con la lipasa endotelial (LPL) situada en el endotelio vascular y se hidrolizan los TG del quilomicrón liberando ácidos grasos que pasan al tejido correspondiente para ser Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 82 utilizados o almacenados. El quilomicrón va perdiendo su contenido de TG y de Apo C y consecuentemente pierde también su capacidad de interacción con la LPL, lo que queda de ello será el quilomicrón residual. El quilomicrón residual es captado por el hígado a través de un receptor específico que reconoce a la Apo E de esta misma partícula. 3.5 Transporte de lípidos endógenos Los lípidos de origen hepático junto con la Apo B100, la Apo E y la Apo C forman las VLDL, éstas son objeto de acción de la LPL en el plasma haciendo que pierdan gran parte de sus TG, la parte restante de ellas son las IDL. Las IDL entonces, pueden seguir dos vías distintas, una parte de ellas será captada por el hígado a través del receptor para su Apo E (llamado receptor Apo B100, E de Goldstein-Brown) y el resto se transformará en LDL. Por otra parte se sabe que las LDL son las encargadas de abastecer de colesterol a los tejidos de forma que éste se introduce en las células por un mecanismo que depende del receptor Apo B 100, E. Se ha podido comprobar que existe otro mecanismo de entrada de colesterol a las células independiente del receptor Apo B 100, E, es el llamado receptor scavenger que se encuentra en los macrófagos, las células musculares lisas y en el endotelio fundamentalmente. Para que la LDL se pueda unir a este receptor es necesario que esté oxidada ya que en este estado tiene bloqueados los sitios de unión con la Apo B 100, E pero no con el receptor scavenger. Esto implica que con la LDL oxidada todo el colesterol se vaya acumulando en las células musculares lisas de la pared vascular hasta convertirlas en células espumosas que se depositarán en el vaso produciendo la placa de ateroma. Además las LDL oxidadas adquieren unas propiedades citotóxicas y quimiotácticas sobre el sistema monocito-macrófago que producirán un aumento de la lesión ateromatosa. De todo ello se deduce que la Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 83 fracción oxidada de LDL juega un papel importantísimo en la producción de lesiones ateromatosas. Las causa de oxidación de la LDL se deben en general a que sus ácidos grasos puedan sufrir procesos de oxidación a través de mecanismos mediados por radicales libres dando lugar a compuestos que se unen a la Apo B produciendo un cambio de carga en la LDL. Este proceso de oxidación se puede desencadenar por la presencia de cationes divalentes y sobretodo por metabolitos, como el anión superóxido, liberados por algunas células como los monocitos y las plaquetas, así como por las células endoteliales y musculares lisas. El colesterol que se encuentra en exceso se elimina por vía biliar ya que no existen enzimas capaces de intervenir en su degradación. Para que llegue el colesterol al hígado y por lo tanto pueda ser eliminado por la bilis, debe de existir un sistema de transporte que permita trasladarlo desde los tejidos periféricos hasta este lugar. Este transporte corre a cargo de la HDL y por lo tanto parece ser que a partir de un cierto valor de concentración, dicha lipoproteína tenga efectos protectores frente a las enfermedades que se relacionan con los depósitos tisulares de colesterol. 4. Procedimientos de medida de la concentración de lípidos 4.1 Preliminares Las dos determinaciones que se deben hacer inicialmente son el colesterol y los triglicéridos, para ello debe efectuarse la extracción sanguínea después de un periodo de ayuno de 12 horas para evitar que la hiperquilomicronemia postprandrial interfiera con la determinación de la trigliceridemia. En aquellos estudios en los que sólo se deba determinar la colesterolemia, no será necesario el ayuno previo, pero sí lo será, en aquellos que además se deba determinar la fracción HDL. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 84 La tercera prueba que a continuación se aconseja hacer es la del aspecto del suero, para ello se deberá mantener éste en un tubo de ensayo en posición vertical a 4°C durante 12 horas. En general el aspecto del suero se suele describir con una de las siguientes calificaciones: claro, lactescente, opalescente, ámbar, hemolizado, ictérico o formando un anillo de quilomicrones. Un suero claro y transparente correspondería a un suero normal y por lo tanto descarta la presencia de hipertrigliceridemia, pero nos previene de posibles errores de laboratorio o de interferencias que son muy frecuentes al determinar los TG. Un aspecto opalescente indica la presencia de VLDL o de partículas remanentes de VLDL en cantidades importantes. Si se observa plasma en lugar de suero puede dar lugar a confusión ya que la eventual hiperfibrinogenemia puede ofrecer un aspecto semejante. Un aspecto lactescente advierte de la presencia de quilomicrones o de VLDL muy grandes, pero no descarta la presencia de grandes cantidades de VLDL normales. Un aspecto ámbar, difícil de valorar, hace sospechar la presencia de altas concentraciones de LDL o de betacarotenos. Se emplea poco porque es difícil de sistematizar. Un aspecto hemolizado revela posibles interferencias en la medida de otros parámetros de laboratorio y en estos casos se recomienda practicar una nueva extracción, a la vez que suspender el estudio en curso. Un aspecto ictérico también nos previene de la existencia de posibles artefactos en las demás pruebas de laboratorio efectuadas y además indica posibles afectaciones hepático-biliares o procesos hemolíticos. En el caso de observar un suero lactescente u opalescente, está indicado hacer un estudio del aspecto del suero refrigerado, para lo cual se recomienda utilizar una Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 85 cantidad de unos 10 mL en un tubo de vidrio ancho (de unos 2 cm). En este caso habrá dos opciones: 1) En el caso de un suero opalescente, puede que sea uniformemente opalescente (traslúcido), luego esto indicará la presencia de grandes cantidades de VLDL o de remanentes y nos descarta la presencia de quilomicrones, o bien en el caso de existir una pequeña capa superior de material blanco, indicaría la presencia de remanentes de quilomicrones. 2) En el caso de un suero con aspecto lactescente, acabado de obtener, también hay dos posibilidades: que aparezca una capa cremosa o lechosa en la parte superior y el resto del suero sea claro o poco turbio, que nos descartará la presencia de cantidades importantes de VLDL, y la otra posibilidad es que haya la misma capa cremosa pero el resto del suero sea francamente turbio, en este caso existiría la presencia combinada de quilomicrones con un aumento de VLDL. Conociendo la colesterolemia, la trigliceridemia y el aspecto del suero, podremos orientar fácilmente el diagnóstico de una hiperlipidemia. La cuarta determinación que deberemos hacer es la fracción HDL, prueba que resultará muy útil para valorar el riesgo cardiovascular, ya que su concentración guarda una relación inversamente proporcional con dicha patología. Una vez se ha determinado la fracción HDL-colesterol, podemos calcular con bastante aproximación el valor de la fracción LDL-colesterol mediante la fórmula de Friedewald siguiente: [LDL colesterol ] = [colesterol total ] − ( [HDL colesterol ] + [TG ] ) 5 o bien: Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol [LDL colesterol ] = [colesterol total ] − ( [HDL colesterol ] + 86 [TG ] ) 2,2 Si las unidades se expresan en mmol/L. Las fórmulas son válidas sólo si la concentración de triglicéridos no supera los 500 mg/dL. A continuación se realizará la quinta prueba, es decir la electroforesis de las lipoproteínas que generalmente se hace sobre un soporte electroforético de gel de poliacrilamida (ver unidad didáctica número 12 del libro del mismo autor antes citado), a también en acetato de celulosa. Las bandas así obtenidas se tiñen con un colorante como por ejemplo el aceite rojo 7B o azul brillante de Coomasie, y aparecen reveladas sobre el soporte electroforético de tal manera que se les designan nombres análogos a las bandas de las proteínas séricas según la tabla 2.4. Los valores normales para cada fracción respecto del total de lípidos son las siguientes: αlipoproteínas: 16-46%; pre β-lipoproteínas: 3-30%; β-lipoproteínas: 39-65%. Hay que considerar que la técnica es esencialmente cualitativa pero resulta así mismo útil para la cuantificación de las fracciones y para el seguimiento de las hiperlipemias. 2.2 Procedimientos de medida del colesterol Existen varios métodos colorimétricos para la determinación del colesterol, uno de los más antiguos es el método de Liebermann-Burchard que se basa en formar un compuesto coloreado por la acción del ácido sulfúrico concentrado sobre el colesterol en medio anhidro. El medio anhidro se consigue con ácido acético y el producto final obtenido es el colesterileno de color verdoso cuya absorbancia se compara con la de un estándar de colesterol, calculándose posteriormente la concentración de colesterol de la muestra. La reacción es la siguiente: Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 87 Medio anhidro Colesterol + H2SO4 colesterileno → Ácido acético La técnica consiste en pipetear en tres tubos de ensayo los volúmenes de reactivos de acuerdo con el cuadro siguiente: Muestra Estándar Reactivo de Liebermann H2O destilada Blanco 4 mL Problema 0,1 mL 4 mL 0,1 mL Patrón 0,1 mL 4 mL - - A continuación se incuban los contenidos de los tubos durante 20 minutos a temperatura ambiente, ajustándose el espectrofotómetro al cero con el blanco y se efectúan lecturas de absorbancias en los tubos problema (Ax) y patrón (Ap) a 620 nm, teniendo en cuenta que las soluciones obtenidas son estables durante 40 minutos. Posteriormente se calcula la concentración de colesterol sabiendo que el estándar suele tener una concentración de 200 mg/dL, del modo siguiente: [Colesterol ] = Ax · 200 Ap La muestra a emplear debe ser suero en ayunas y sin haber sufrido hemólisis. El reactivo de Liebermann contiene: 240 mL de ácido acético 7,5M; anhídrido acético 5,2M; y ácido dimetil-benzeno sulfónico 50 mmol/L que se debe mantener refrigerado durante su almacenamiento, además hay que tener en cuenta que se trata de productos cáusticos por lo que se deberán tomar precauciones en su manejo. Otra técnica para la determinación del colesterol es la técnica de Allain que se fundamenta en las reacciones siguientes: Colesterolesterasa 1) Ésteres de colesterol + H2O → Colesterol + ácidos grasos Colesteroloxidasa 2) Colesterol + O2 + H2O → Colestenona + H2O2 Peroxidasa 3) H2O2 + fenolampirona → Quinona + H2O Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 88 La técnica consiste en pipetear en tubos de ensayo cantidades adecuadas de reactivo (contiene los enzimas, fenolampirona y un tampón), muestra (suero o plasma) y estándar. Se mezclan los tubos durante 10 minutos a temperatura ambiente, se ajusta al cero el espectrofotómetro mediante el blanco y se leen las absorbancias a 500 nm. Seguidamente se calcula la concentración problema de modo análogo al anterior método teniendo en cuenta que el rango de linealidad es válido hasta 700 mg/dL. Se debe tener en cuenta además, las posibles interferencias que pudieran ocasionar sustancias como el ácido ascórbico, la hemoglobina y la bilirrubina a dosis elevadas, así como por la eventual presencia de ciertos fármacos. La determinación de la fracción HDL de colesterol se determina basándose en el hecho que las lipoproteínas LDL y VLDL precipitan en presencia de fosfotungstato e iones magnesio, mientras que las HDL permanecen en la solución pudiéndose determinar en el sobrenadante. La técnica consiste en centrifugar el suero con el reactivo precipitante durante 20 minutos a un mínimo de 4000 rpm y determinar el colesterol del sobrenadante mediante la técnica de Allain descrita anteriormente. El reactivo precipitante suele contener además de fosfotungstato y magnesio, un potenciador de color que hace resaltar más visiblemente el sobrenadante. 4.3 Procedimientos de medida de los triglicéridos La mayoría de métodos utilizados para la determinación de los triglicéridos se basan en las reacciones siguientes: Lipasa 1) TG → Glicerol + ácidos grasos libres Glicerol kinasa 2) Glicerol + ATP → Glicerol-1P + ADP Glicerol-1P deshidrogenasa 3) Glicerol-1P + NAD+ → Dihidroxiacetona-P + NADH + H+ Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 89 A veces se suele añadir un reactivo especial como por ejemplo la hidrazina que forma un complejo con la dihidroxiacetona-P y desplaza el equilibrio de la reacción hacia la derecha forzando a que la reacción termine. Seguidamente se lee la absorbancia del NADH a 340 nm (ver unidad didáctica número 4 del libro citado anteriormente). Existen otros métodos que generan glicerol-3P y éste a su vez, genera peróxido de hidrógeno que por acción de una peroxidasa se convierte en una sustancia coloreada. 4.4 Procedimientos de medida de las apolipoproteínas La cuantificación de las apolipoproteínas se efectúa mediante nefelometría (ver unidad 7 de la obra citada), midiéndose la dispersión luminosa debida a la formación de grandes complejos antígeno-anticuerpo. 5. Patrones de alteración del metabolismo lipídico 5.1 Generalidades Es muy importante el papel que juegan los lípidos en la producción de enfermedades que afectan al sistema cardiovascular, según estadísticas las enfermedades cardiovasculares son la primera causa de muerte a partir de los 45 años en los países industrializados, los síntomas y las defunciones se producen cuando el exceso de lípidos que no se elimina o no se utiliza, se deposita en tejidos y paredes arteriales obstruyendo el normal flujo de sangre a órganos vitales. Cuando la restricción del flujo sanguíneo se produce en las arterias coronarias, sobreviene el angor o angina de pecho, en caso de compromiso circulatorio relativamente leve, o el infarto de miocardio cuando la obstrucción es total. Si la obstrucción ocurre en algún vaso cerebral se produce un accidente vascular cerebral (AVC) con necrosis de tejido neuronal. El exceso de lípidos produce también su acumulación en órganos sobretodo Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 90 en hígado y en riñón y puede impedir su normal funcionamiento, si se acumulan en la piel forman los llamados xantomas. El perfil analítico de lípidos que se obtiene en el laboratorio representa solamente un aspecto de la valoración de riesgo de enfermedad cardiovascular, tan importantes como éste, son el consumo de tabaco, la hipertensión arterial, el sedentarismo, y la obesidad que en conjunto se les clasifica en factores de riesgo susceptibles de ser modificados. Otros factores de riesgo no modificables son la edad, el sexo (los hombres tienen más riesgo que las mujeres) y los antecedentes familiares, así como otras enfermedades concomitantes como por ejemplo la diabetes mellitus. En cuanto a la valoración de riesgos a través de parámetros analíticos hay que señalar que las concentraciones de LDL colesterol están en relación directa con el riesgo, mientras que las concentraciones de HDL colesterol lo están en relación inversa. Obsérvese la tabla 2.5 como guía orientativa en la valoración del riesgo cardiovascular en función del perfil lipídico. TABLA 2.5 Determinación Nivel deseable Nivel límite Nivel indeseable Colesterol total < 200 mg/dL 200-249 mg/dL ≥250 mg/dL HDL colesterol ≥55 mg/dL 35-54 mg/dL <35 mg/dL LDL colesterol <130 mg/dL 130-159 mg/dL ≥160 mg/dL Triglicéridos <250 mg/dL 250-500 mg/dL >500 mg/dL Las principales enfermedades relacionadas con la acumulación de lípidos en los tejidos se clasifican en tres grandes grupos: las hiperlipoproteinemias, las hipolipoproteinemias y las anormalidades lipídicas lisosómicas. Las primeras se dividen a su vez en primarias y secundarias, las primarias se clasifican por el sistema Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 91 de Frederickson enumerándose mediante números romanos del I al V y se describen a continuación. 5.2 Hiperlipoproteinemias primarias Hiperlipoproteinemia tipo I. Llamada también quilomicronemia familiar, se transmite de forma autosómica dominante. Puede ser debida a tres tipos de errores congénitos, la deficiencia del enzima LPL, la deficiencia de la apolipoproteína C II y en tercer lugar la presencia de un inhibidor de la lPL. La enfermedad se manifiesta con una hipertrigliceridemia plasmática de 500 a 2000 mg/dL y sus síntomas clínicos al igual que en otros tipos de hipertrigliceridemia son en primer lugar el dolor abdominal, presente ya desde la infancia localizado en el epigastrio y la zona periumbilical con irradiación lumbar, la pancreatitis aguda que suele ser frecuente en este tipo de enfermos, así como la hepatoesplenomegalia debida al depósito de triglicéridos en las células del sistema mononuclearfagocítico. También es frecuente encontrar células espumosas en la médula ósea por el mismo motivo. La acumulación de TG en la piel produce la aparición de xantomas eruptivos que se manifiestan como pequeñas pápulas amarillentas en las zonas sometidas a presión. Cuando la hipertrigliceridemia supera los 2000 mg/dL se puede observar la llamada lipemia retinalis, la cual es observable en el fondo del ojo donde las vénulas y las arteriolas adquieren un color rosa pálido, pero que no produce ninguna alteración de la función visual. Por otra parte pueden aparecer alteraciones neuropsiquiátricas de difícil explicación etiopatogénica, como la demencia, la depresión y la pérdida de memoria reciente. El diagnóstico se puede hacer en primer lugar por el aspecto de “sopa de tomate” que adquiere la sangre y el aspecto lechoso del suero obtenido después del ayuno de 12 horas. La analítica demuestra un aumento de los TG con un colesterol normal. También la “prueba del refrigerador” resulta útil, ésta Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 92 consiste en dejar durante 12 horas el suero en una nevera a 4°C y observar después que los quilomicrones forman una capa cremosa en la parte superior del tubo mantenido verticalmente. Adicionalmente las concentraciones de LDL y HDL suelen ser normales. El diagnóstico definitivo de la falta del enzima LPL se confirma mediante el estudio de la actividad del enzima. La deficiencia de la apo C II se confirma mediante separación de las apolipoproteínas de la VLDL por electroforesis. En los casos que la enfermedad sea debida a la presencia de un inhibidor de la LPL, éste se puede objetivar observando que la actividad enzimática no se corrige añadiendo apo C II, siendo dicha actividad normal en el tejido adiposo. Hiperlipoproteinemia tipo II. Consiste en un incremento de las LDL y se divide en tres formas: 1) hipercolesterolemia poligénica, llamada también hipercolesterolemia primaria grave, 2) hipercolesterolemia familiar combinada y 3) hiperlipemia familiar combinada. En la primera no existe defecto identificable y se cree debida a factores ambientales y cursa con niveles de colesterol total superiores a 300 mg/dL. Las formas familiares se heredan a través de genes autosómicos dominantes que conllevan a una incapacidad de los receptores celulares que impiden la unión de la LDL para su eliminación. El pronóstico de esta enfermedad dependerá fundamentalmente de ser homocigoto o heterocigoto para el gen en cuestión. Hiperlipoproteinemia tipo III. Llamada también enfermedad de la “β ancha”. El proteinograma electroforético realizado en estos enfermos resalta la existencia de una proteína presente en concentraciones patológicamente elevadas que ocupa la zona comprendida entre la β y la pre-β (LDL y VLDL respectivamente) del lipoproteinograma y que corresponde a la lipoproteína IDL. Esta enfermedad se llama también disbetalipoproteinemia familiar y se transmite genéticamente de Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 93 forma autosómica recesiva causando una mutación en la secuencia de aminoácidos de la apo-E que la hace irreconocible para sus receptores hepáticos. El perfil diagnóstico completo de esta enfermedad será: 1) Elevación paralela y simultánea de la colesterolemia y la trigliceridemia. 2) En la electroforesis con acetato de celulosa o agarosa se observa una banda β ancha. 3) Cociente: VLDL colesterol > 0,3 (criterio válido si TG < 1000 mg/dL). TG 4) La electroforesis por isoelectroenfoque constituye la prueba de confirmación del diagnóstico donde se demuestra la existencia de las isoformas anormales en un alelo de la apo-E de las IDL. Los individuos que padecen esta enfermedad presentan xantomas cutáneos de dos tipos, unos llamados xantomas planos de coloración anaranjada que típicamente se localizan en las palmas y en los pliegues interdigitales y otros, los xantomas tuberoeruptivos localizados en codos y rodillas. También presentan aterosclerosis generalizada, prematura y grave con afectación de las arterias coronarias, carótida interna, aorta abdominal y arteria femoral que causan frecuentemente cardiopatía isquémica e insuficiencia vascular cerebral, en hombres la patología aparece a partir de los 20 años de edad y en las mujeres a partir de la menopausia. Hiperlipoproteinemia tipo IV. Se hereda con rasgo autosómico dominante o como parte del síndrome de hiperlipidemia familiar combinada. Cursa con un incremento de los niveles de VLDL y el defecto parece ser un aumento en su producción o una disminución en su depuración o ambas. Los síntomas aparecen en la edad adulta presentando afectaciones coronarias prematuras. El aumento de los niveles de VLDL da lugar a una banda electroforética pre-β ancha junto con la ausencia de la banda de los quilomicrones. Los niveles de TG están elevados y el colesterol es normal. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 94 Hiperlipoproteinemia tipo V. Corresponde a un aumento de las VLDL y de quilomicrones. Esta afectación provoca niveles de TG muy altos ya sea por la incapacidad de eliminar las lipoproteínas ricas en TG, o por el exceso de producción o por ambas cosas. Se desconoce el mecanismo genético de esta forma familiar. El aspecto del suero incluye un anillo cremoso en la parte superior y el patrón electroforético consiste en la presencia de bandas anchas de quilomicrones y pre-β. Los niveles de LDL y de HDL son normales o bajos, pero los de colesterol total y TG están aumentados. En general los pacientes presentan síntomas a partir de los 20-50 años que suelen ser dolor abdominal y xantomas eruptivos, pero no se detectan afectaciones coronarias prematuras. 5.3 Hiperlipoproteinemias secundarias Las hiperlipoproteinemias secundarias consisten en niveles aumentados de lípidos asociadas a otras afecciones primarias que se corrigen al tratar éstas. Las más frecuentes son debidas al mal funcionamiento hepático o las de origen periférico, entre las primeras cabe destacar la hepatitis biliar, la obstrucción biliar, la cirrosis y la pancreatitis aguda, mientras que dentro de las segundas se pueden incluir el infarto de miocardio, la insuficiencia renal, la gota, la anemia perniciosa y la diabetes mellitus. 5.4 Hipolipoproteinemias Las hipolipoproteinemias también constituyen un grupo de enfermedades importantes, entre ellas destaca en primer lugar la ausencia de LDL o abetalipoproteinemia que se debe a la incapacidad de secreción de lipoproteínas que contienen apo B, o a la incapacidad de su síntesis, o a ambos factores. Se trata de una situación muy grave pues carecen totalmente de LDL y el problema fundamental es la malabsorción de grasas, incluidas las vitaminas liposolubles. Un hecho característico es la presencia de células repletas de vacuolas lipídicas de gran tamaño Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 95 en la mucosa intestinal. Presentan manifestaciones neuromusculares como debilidad, ataxia e hiporreflexia, también puede producirse ceguera. El frotis de sangre muestra un 50-70% de eritrocitos en forma de espinas (llamados acantocitos). La malabsorción de vitamina K no suele producir problemas de hemorragias pero si que presentan un tiempo de protrombina anormalmente alargado. La enfermedad de Tangier consiste en la ausencia de HDL que provoca una acumulación de ésteres de colesterol en el sistema reticuloendotelial, pero no afecta al funcionamiento de los órganos principales. El perfil analítico pone de manifiesto unas cantidades muy bajas, a veces indetectables de HDL, de LDL y de colesterol total, así como ausencia de la banda α en el lipidograma electroforético, siendo los TG normales o elevados. La clínica correspondiente a estos enfermos consiste en amígdalas y adenoides de gran tamaño de color naranja-amarillento, presentan además hepatoesplenomegalia, debilidad y atrofia muscular, neuropatías periféricas con depresión de los reflejos tendinosos, pero lo más grave en estos casos es la aterosclerosis. Los depósitos de ésteres de colesterol se pueden demostrar por biopsia rectal. 5.5 Anormalidades lisosómicas de lípidos Los lisosomas constituyen verdaderas “bolsas” intracelulares de enzimas que hidrolizan lípidos y otros constituyentes bioquímicos, estas vías catabólicas generalmente constan de diversos pasos cada uno de ellos catalizado por un enzima, cuando uno de éstos está ausente o en menor cantidad, se acumula el sustrato en el punto de la deficiencia. Las afectaciones de este tipo se describen a continuación. Enfermedad de Gaucher. Es la más frecuente, se debe a la ausencia del enzima βglucocerebrosidasa que hace que se acumule glucocerebrósido. El diagnóstico de laboratorio incluye la presencia de células de Gaucher que son histiocitos Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 96 cargados de lípidos en la médula ósea, acompañado de elevación sérica de fosfatasa ácida. Enfermedad de Niemann-Pick. Llamada lipidosis de esfingomielina, consistente en la deficiencia de esfingomielinasa que provoca acumulación de esfingomielina. En el laboratorio, a menudo se detectan células de apariencia espumosa en el frotis de médula ósea, tratándose de histiocitos sobrecargados. Al contrario de la enfermedad descrita anteriormente, la fosfatasa ácida sérica es normal. Enfermedad de Krabbe. Llamada también lipidosis de galactocerebrósido o leucodistrofia de células globoides. La deficiencia es el enzima galactocerebrósidoβ-galatosidasa que produce una acumulación de galactocerebrósidos. Afecta principalmente al sistema nerviosa central (SNC) provocando deterioro mental y motor graves. En el análisis se detecta un aumento de las proteínas del líquido cefalorraquídeo (LCR) y la presencia de células globoides que son histiocitos multinucleados de gran tamaño. En general es una enfermedad mortal a partir de los 6-12 meses del inicio. Distrofia metacromática. Se debe al defecto de arilsulfatasa A que provoca la acumulación de 3-sulfato-galatosilcerebrósido. Produce parálisis progresiva y deterioro mental. Enfermedad de Fabry. Llamada también angioqueratoma corporal difuso universal. Se produce por la acumulación de trihexósido de ceramida en el SNC como consecuencia de la falta del enzima lisosómico α-galactosidasa. Se hereda como rasgo ligado al cromosoma X y se produce un exantema maculopapular con dolor y quemazón en las extremidades, opacidades corneales, insuficiencia renal e infartos cerebrales y de miocardio. Enfermedad de Tay-Sachs. Llamada también gangliosidosis Gm2. Generalmente se trata de lactantes que acumulan gangliósido GM2 en las neuronas debido al déficit Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 97 de hexoaminidasa A. Los enfermos sufren deterioro psicomotor y muchas veces demencia. Existe una variante: la gangliosidosis GM1. Fucosidosis. Es la deficiencia de α-fucosidasa que produce el acúmulo de esfingolípidos que contienen fructosa y fragmentos de glucoproteínas. El tipo I se asocia con insuficiencia respiratoria, retraso psicomotor piel gruesa, sialorrea, cardiomegalia e hipersudoración, el tipo II es más leve, pero aparecen angioqueratomas. _____________________________________________________ APÉNDICE *(1) Anfipático significa que es hidrofílico e hidrofóbico a la vez. *(2) Los ácidos biliares conocidos son el ácido taurocólico y el ácido glicocólico, derivados del ácido cólico de naturaleza esteroide unido a los aminoácidos taurina y glicina respectivamente. Estos ácidos son aniones a pH 7 y actúan como detergentes puesto que su grupo hidrofílico es soluble en agua mientras que su grupo hidrofóbico (su porción esteroide), lo es en las grasas, esto hace que la parte hidrofóbica pueda disolverse en las gotitas de grasa, dejando que la parte hidrofílica permanezca en el exterior de la superficie de las gotitas de grasa, así adquieren carga negativa y al repelerse entre sí se mantienen separadas. De esta manera su superficie aumenta con relación a su volumen (cuanto más pequeñas sean las gotitas, mayor será su superficie relativa) y consecuentemente aumentará la superficie de contacto entre las fases acuosa y lipídica. Todo ello tiene un sentido: los enzimas digestivos son hidrosolubles y por lo tanto no pueden penetrar en el interior de las gotitas de grasa, pero al aumentar la superficie de contacto, éstas resultan ser más accesibles a la acción de los enzimas. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 98 *(3) Se ha sugerido también la presencia de una lipasa en el intestino delgado, segregada posiblemente por éste, ya que los individuos pancreatectomizados pueden digerir pequeñas cantidades de lípidos. *(4) Es importante saber que no existe lipasa en la saliva y por lo tanto no se produce ninguna digestión de grasas en la boca. También se ha detectado la existencia de una lipasa en el estómago pero debido a que su funcionamiento sólo tiene lugar a un pH de alrededor de 7, parece dudosa su eficacia ya que el jugo gástrico suele tener un pH mucho más bajo. De ello se deduce pues, que el proceso de digestión de las grasas solamente tiene lugar es el intestino delgado. *(5) En el año 1891 Munk observó por casualidad en un individuo que tenía una fístula linfática (canal que comunica el sistema linfático con el exterior del organismo), que en ayunas, la linfa que recogía a través de la fístula era líquida y de color claro, mientras que después de una comida rica en grasas aparecía de aspecto lechoso por el hecho de tener gotitas de lípidos en suspensión. Estas gotitas recibieron el nombre de quilomicrones. *(6) FADH2 son las siglas del compuesto flavin adenin dinucleótido reducido. *(7) La biotina se encuentra ampliamente difundida en los alimentos y no suele ser causa de enfermedad carencial. Se sabe que en las dietas que contienen grandes cantidades de albúmina de huevo crudo pueden ser perjudiciales puesto que una proteína, la avidina, de la albúmina de huevo se combina con la biotina e impide su absorción. Se conoce la anécdota de un único caso de un individuo con déficit natural de biotina, corresponde a un hombre que hacía una dieta estrictamente formada por una docena de huevos crudos diarios y varios litros de vino. *(8) En el año 1940, Konrad E. Bloch inyectó acetato marcado radiactivamente a las ratas de experimentación y comprobó posteriormente que el colesterol contenía el isótopo de carbono marcado, de lo que dedujo que el acetato es un precursor del Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 99 colesterol, hecho que le valió el premio Nobel del año 1964 compartido con Feodor Lynen). ACTIVIDADES DE AUTOEVALUACIÓN PRUEBA OBJETIVA DE SELECCIÓN ALTERNATIVA MÚLTIPLE Sólo es válida una de las cuatro respuestas de cada pregunta. 1) Cuando el aspecto del suero es hemolizado se recomienda una de las siguientes conductas: a) mantener refrigerado el suero a 4°C durante 6 horas y volver a observarlo b) anotar que se trata de suero con lisis de hematíes y seguir efectuando las demás pruebas de laboratorio con normalidad c) repetir la extracción sanguínea y suspender la práctica de otras pruebas de laboratorio d) anotar la presencia de betacarotenos y sospechar altas concentraciones de VLDL 2) El símbolo 20:2 significa que se trata de un ácido graso: a) con 20 átomos de carbono y con enlaces simples b) con 20 átomos de carbono y un enlace doble en el carbono número 2 c) con 20 átomos de carbono y algún enlace doble d) con 2 enlaces dobles, uno en el carbono número 20 y el otro en el número 2 3) Las micelas están formadas por: a) terpenos b) esteroides c) lipoproteínas d) ceras Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 100 4) Una de las siguientes enfermedades no es una anormalidad lisosómica lipídica: a) enfermedad de Fabry b) enfermedad de Krabbe c) enfermedad de Tay-Sachs d) abetalipoproteinemia 5) La denominada lipemia retinalis consistente en la observación de vénulas de color rosa pálido en el fondo del ojo, se pone de manifiesto cuando: a) los niveles de TG superan los 2000 mg/dL b) los niveles de colesterol superan los 250 mg/dL c) los niveles de HDL están por debajo de los 100 mg/dL d) los niveles de quilomicrones superan los 20.000 mg/dL 6) El método más apropiado, entre los siguientes, para la determinación de las apolipoproteínas es: a) volumetría polarográfica b) nefelometría c) polarimetría d) fotometría de llama 7) El reactivo de Liebermann-Burchard para la determinación colorimétrica del colesterol contiene todos los componentes siguientes menos uno, señalarlo: a) ácido acético b) ácido dimetil-benzeno sulfónico c) peroxidasa d) anhídrido acético 8) Está totalmente comprobado que una de las siguientes sustancias a dosis altas interfiere con la prueba de Allain, señalarla: a) vitamina E Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 101 b) vitamina C c) Ca++ d) ácido pantoténico 9) Los ácidos grasos poliinsaturados son aquellos que: a) tienen dos o más enlaces dobles b) tienen solamente un enlace doble c) tienen un o más enlaces triples d) tienen todos los enlaces simples 10) Las lipoproteínas que contienen aproximadamente la misma cantidad de TG que de colesterol son: a) las VLDL b) las LDL c) las HDL d) las IDL PROBLEMAS 1) Aplicando el método de Liebermann-Burchard, se efectúan lecturas de absorbancia a 620 nm para una muestra de suero y un estándar, dando los valores de 0,842 y 0,432 respectivamente. La concentración del estándar utilizado es de 150 mg/dL. Calcular la concentración de colesterol de la muestra y compararlo con los valores normales. 2) A partir de una muestra de plasma se han obtenido unos valores de colesterol total de 225 mg/dL, de la fracción HDL-colesterol de 59 mg/dL y de TG de 265 mg/dL. Calcular a partir de los datos disponibles, la concentración de LDLcolesterol. Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401 Fundamentos y Técnicas de Análisis Bioquímico. Química Clínica. Marcel Sayol 102 3) Con la intención de diagnosticar la hiperlipoproteinemia tipo III (disbetalipoproteinemia familiar), se determinan los valores de colesterolemia y trigliceridemia obteniéndose los resultados de 360 y 880 mg/dL respectivamente. La fracción VLDL-colesterol, obtenida por ultracentrifugación, resultó ser de 354 mg/dL. Enumerar las pruebas y efectuar los cálculos que se deberán realizar para establecer el correcto diagnóstico. ________________________________________________________ CRITERIOS Y ACTIVIDADES DE EVALUACIÓN Definir la estructura de los ácidos grasos, triglicéridos, fosfolípidos, esfingolípidos, glucolípidos, ceras, lípidos insaponificables, lipoproteínas y micelas lipídicas Describir las funciones del tejido adiposo Definir el proceso de oxidación de los ácidos grasos y el de formación de cuerpos cetónicos Definir el proceso de biosíntesis de los ácidos grasos y del colesterol Describir la estructura de las lipoproteínas plasmáticas y las apolipoproteínas Describir el transporte de lípidos exógenos y endógenos Seleccionar los métodos apropiados para la determinación del colesterol y los TG Enumerar los procesos patológicos que cursan con valores anormales de colesterol y sus fracciones HDL y LDL Clasificar las hiperlipoproteinemias y las hipolipoproteinemias primarias Clasificar las anormalidades lisosómicas lipídicas PROPUESTA DE ACTIVIDADES DE REFUERZO Contestar detalladamente a las siguientes preguntas: ¿Cuál es la conducta a seguir delante de la observación de un suero con aspecto lactescente? ¿Cómo se pueden clasificar los esfingolípidos? ¿Cuáles son las causas más habituales de producción de cetosis? ¿Cuál es el proceso y la causa atribuidos a la formación de la placa de ateroma? ¿Preguntas?: msayol@xtec.cat Registro General de la Propiedad Intelectual. Número de asiento registral: 02/2006/4401