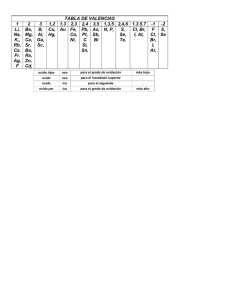
Union internacional de química pura y aplicada. Nomenclatura • http://www.slideshare.net/luitzin/01-quimicacano • http://www.slideshare.net/luitzin/02-quimicacano-b Cuadro de obtención de compuestos inórganicos a partir de metales y no metales. stock Nom este Formulación de compuestos inorgánicos binarios • Una fórmula química es la representación simbólica de la molécula de un elemento químico. Las fórmulas están compuestas por símbolos, que representan a los elementos cuyos átomos entran a formar parte en el compuesto. El número de átomos de cada elemento se indica con subíndices. • Compuestos binarios • Son compuestos en los que intervienen dos elementos químicos diferentes. Para formular los compuestos binarios se escribe primero el metal y luego el no metal, mientras que para nombrarlos se invierten los términos. • Existen tres métodos de nomenclatura: nomenclatura tradicional, nomenclatura sistemática o estequiométrica y numerales de Stocks Formas de nombrarlos • Nomenclatura tradicional: requiere conocer la valencia o estado de oxidación de los elementos y la relación en que se combinan los átomos. • K2O, óxido de potasio u óxido potásico. • Nomenclatura sistemática (IUPAC): utiliza los prefijos para indicar el número de átomos de cada elemento, sin requerir el conocimiento de las valencias. • Ca5F (PO4)3 = fluoruro tris (fosfato) de calcio • Nomenclatura de Stock: se indica con números romanos entre paréntesis la valencia del metal. • Fe2+3S3-2, sulfuro de hierro (III) Combinaciones binarias del hidrógeno • El hidrógeno da lugar a las siguientes combinaciones binarias: • Combinaciones con F, Cl, Br, I, S, denominadas hidrácidos. • Su fórmula general es XnH. Se denominan con el nombre del elemento terminado en -uro seguido de «de hidrógeno». • Combinaciones con otros no metales o hidruros no metálicos. Su fórmula general es XHn y tienen nombres específicos. • Combinaciones con metales o hidruros metálicos. Su fórmula general es XHn. Se denominan como hidruros anteponiéndose al nombre del metal. Hidrácidos Compuesto Nombre sistemático Disolución acuosa HCI Cloruro de hidrógeno Ácido clorhídrico HI Yoduro de hidrógeno Ácido yodhídrico H2S Sulfuro de hidrógeno Ácido sulfhídrico Hidruros no metálicos Compuesto Nombre común NH3 Amoníaco H2O Agua CH4 Metano PH3 Fosfina Nombre sistemático Trihidruro de nitrógeno Dihidruro de oxígeno Tetrahidruro de carbono Trihidruro de fósforo Hidruros metálicos Compuesto Nombre sistemático NaH Monohidruro de sodio Dihidruro de calcio CaH2 CuH Monohidruro de cobre Nombre stock Hidruro de sodio Hidruro de calcio Hidruro de cobre (I) Combinaciones binarias del oxígeno • Los óxidos son la combinación de un elemento con el oxígeno. Si el elemento es un metal, son óxidos propiamente dichos. Si se trata de un no metal, reciben el nombre de anhídridos. Su fórmula general es X2On. • Según la nomenclatura clásica, para nombrarlos se utiliza la expresión óxido seguida del nombre del elemento, al cual se le añadirá un sufijo u otro según la valencia con la que actúe. • Por ejemplo, el cloro puede actuar con cuatro estados de oxidación (+1,+ 3, +5,+ 7), por lo que puede formar los siguientes oxidos: • Cl2O Cl2O3 Cl2O5 Cl2O7 • Los nombres según la nomenclatura de la IUPAC o sistemática, se escriben usando los prefjos mono, di, tri, etc, indicando la cantidad de átomos de cada elemento. • Según la de Stocks se nombran con la expresión «óxido de» seguida del nombre del elemento y si éste posee más de un estado de oxidación, se añadirá entre paréntesis y con números romanos el número de oxidación con el que actúa,. • Y según la tradicional si el elemento sólo tiene dos estados de oxidación, se añade la terminación -ico cuando actúa con el mayor y -oso cuando actúa con el menor. Si tiene 4, se añaden los prefijos: hipo y per , para la menor y mayor, respectivamente Para el ejemplo del cloro, sería: Cl2O Óxido de dicloro Cl2O3 Trióxido de Oxido de dicloro cloro (III) Oxido cloroso Cl2O5 Pentóxido de dicloro Oxido clórico Cl2O7 Heptaóxido Oxido de Oxido de dicloro cloro (VII) perclórico Oxido de cloro (I) Oxido de cloro (V) Oxido hipocloroso Oxidos ácidos y básicos Compuesto Nombre sistemático Nombre stock BaO Monóxido de bario Óxido de bario Al2O3 Trióxido de dialuminio Óxido de aluminio SO2 Dióxido de azufre Óxido de azufre (IV) As2O3 Trióxido de diarsénico Óxido de arsénico (III) Sales binarias • Las sales binarias son la combinación de un metal con un no metal. Su fórmula general es AxBy. Para designarlas, se utiliza el nombre del no metal terminado en -uro, seguido del nombre del metal. Compuesto NaCl CaF2 Nombre sistemático Nombre stock Cloruro de Cloruro de sodio sodio Fluoruro de Difluoruro de calcio calcio Formulación de compuestos inorgánicos ternarios • Las combinaciones ternarias son aquellas en cuyas moléculas intervienen átomos de tres elementos distintos. Normalmente, forma parte de su combinación el oxígeno, que actúa con número de oxidación -2. Dentro de los compuestos ternarios se distinguen tres grupos principales: hidróxidos o bases, oxoácidos u oxácidos y sales u oxisales. Hidróxidos o bases • Los hidróxidos o bases resultan de la combinación de un catión, generalmente metálico, con el ion hidróxido, OH-. • Su fórmula general es X(OH)n. donde n es el estado de oxidación del metal • Nomenclatura tradicional: se denominarían como «hidróxido de», seguido del nombre del metal y añadiendo una terminación indicativa de su valencia. Esta terminación sigue las mismas reglas que en los compuestos binarios. • Nomenclatura sistemática: se nombrarían con la palabra «hidróxido», precedida de un prefijo, que indica el número de grupos (OH) de la molécula y el nombre del metal Oxoácidos u oxácidos • Los oxoácidos se obtienen de la combinación de un no metal con hidrógeno y oxígeno. Su fórmula general es HaXbOc. Como norma práctica, en la mayoría de los casos se obtienen de los anhídridos u óxidos de los no metales, a los que se suma una molécula de agua. • Así, el ácido nítrico se forma a partir de la adición de una molécula de agua al óxido de nitrógeno (V). • N2O5 + H2O → H2N2O6 → HNO3 • Lo mismo sucede con el ácido sulfúrico: • SO3 + H2O → H2SO4 • Los oxoácidos se nombran utilizando la nomenclatura tradicional. Por ejemplo: • Cl2O + H2O → H2Cl2O2 → HClO • ácido hipocloroso • Cl2O3 + H2O → H2Cl2O4 → HClO2 • ácido cloroso • Cl2O5 + H2O → H2Cl2O6 → HClO3 • ácido clórico • Cl2O7 + H2O → H2Cl2O8 → HClO4 • ácido perclórico Sales u oxisales • Las sales u oxisales resultan de la sustitución de los hidrógenos de los oxácidos por un metal. • Se denominan de acuerdo con el nombre del ácido, añadiendo al no metal la terminación -ito, cuando el ácido acaba en -oso, y -ato, cuando el ácido acaba en -ico, seguido de la preposición «de» y del nombre del metal. Si éste tiene más de un número de oxidación, o bien se le añade entre paréntesis y con números romanos el número de oxidación con el que actúa, nomenclatura stock. • Por ejemplo, NaNO3 , resulta de la sustitución en HNO3 del hidrógeno por el metal sodio. Como procede del ácido nítrico, se nombra como «nitrato». Dado que el sodio sólo tiene una valencia, se añade la terminación «de sodio». Ejemplos de compuestos inorgánicos ternarios LiOH Al(OH)3 Trihidróxido de hierro o hidróxido de hierro (III) Hidróxido de litio Hidróxido de aluminio HClO Ácido hipocloroso H2SO3 HNO Ácido sulfuroso Ácido hiponitroso H2CO3 Na2SO4 Ácido carbónico Sulfato de sodio Fe(NO3)2 Nitrato de hierro (II) Al(ClO3)3 CaCO3 Clorato de aluminio Carbonato de calcio Fe(OH)3 • • • • • • • • • • • • • • • • • • • • • • • • I. Escribe la fórmula a los siguientes compuestos 1. Ácido clorhídrico 2. Yoduro de hidrógeno 3. óxido de estroncio 4. hidruro de aluminio 5. sulfuro de hidrógeno 6. oxido de potasio 7. anhídrido hipoyodoso 8. ácido bromhídrico 9. oxido de bario 10. hidruro de cesio 11. óxido aurico 12. anhídrido hiposelenioso 13. anhídrido sulfuroso 14. oxido de calcio 15. hidruro de plata 16. agua 17. trihidruro de hidrógeno 18. anhídrido peryódico 19. anhídrido sulfúrico 20. telenuro de hidrógeno. 21. oxido de oro (I) 22. oxido de cobalto (III) • • • • • • • • • • • • • • • • • • • • • • • • Escribe el nombre de los siguientes compuestos: 1. HF 2. HgO 3. CaH2 4. CO2 5. Rb2O 6. I2O 7. SO3 8. Br2O7 9. As2O5 10. Na2O 11. ZnO 12. PtO2 13. SiO2 14. CsH 15. HI 16. CdH2 17. HCl 18. I2O 19. CuO 20. Au2O3 21. LiH 22. SO2 Compuestos organicos Alcanos • En el sistema IUPAC, un nombre químico tiene al menos tres partes principales: prefijo(s), padre y sufijo. • El o los prefijos especifican el número, localización, naturaleza y orientación espacial de los sustituyentes y otros grupos funcionales de la cadena principal. • El padre dice cuantos átomos de carbono hay en la cadena principal y el sufijo identifica al grupo funcional más importante presente en la molécula. • Prefijo(s) – Padre – Sufijo Alcanos lineales • Estos consisten de cadenas no ramificadas de átomos de carbono, con sus respectivos hidrógenos, unidos por enlaces simples como se ilustra a continuación. • El nombre general de estos compuestos es alcano; el sufijo es la terminación: ano. Alcanos ramificados Alquenos Otros compuestos • Todos los compuestos que contienen un solo grupo funcional se nombran siguiendo el procedimiento descrito para alcanos. Sólo que ahora la cadena principal debe contener al grupo funcional y este determina el sufijo del compuesto. Además, la cadena principal se debe numerar de tal forma que el grupo (o grupos) funcional reciba el índice más bajo posible. Alcoholes • La cadena principal del compuesto debe contener al carbono enlazado al grupo OH y ese carbono debe recibir el índice más bajo posible. La terminación o del alcano correspondiente a la cadena principal se sustituye por ol para indicar que se trata de un alcohol. De forma análoga a los alquenos, se antepone un prefijo al nombre padre para especificar la posición del grupo funcional, en este caso el OH. Aldehídos • Los nombres de los aldehídos se derivan del nombre del alcano con el mismo número de átomos de carbono. La o final del alcano se reemplaza con el sufijo al. Ya que este grupo funcional está siempre al final de una cadena, no es necesario especificar su posición en el nombre, pero su presencia sí determina la numeración de la cadena. Aldehídos más complejos en donde el grupo –CHO está enlazado a un anillo utilizan el sufijo carbaldehído en lugar de al. Acido carboxílico El nombre de estos compuestos se forma anteponiendo la palabra ácido y cambiando la o final del alcano correspondiente por oico. El carbono carboxílico siempre lleva el índice 1. Para compuestos con el grupo –COOH enlazado a un anillo se usa el sufijo carboxílico. El carbono al que está enlazado el carboxilo lleva el índice 1 y el carbono carbonílico no se numera en este sistema. Aminas Aminas primarias simples se nombran agregando el sufijo amina al nombre del sustituyente alquílico (metil, etil, etc.). Aminas primarias simples se nombran agregando el sufijo amina al nombre del sustituyente alquílico (metil, etil, etc.). Aminas asimétricas se nombran como aminas primarias N-sustituidas. Se escoge el grupo alquilo más largo como padre y los otros grupos alquilo se consideran sustituciones en el átomo de nitrógeno. Los sustituyentes en el átomo de nitrógeno se indican con el prefijo N-.