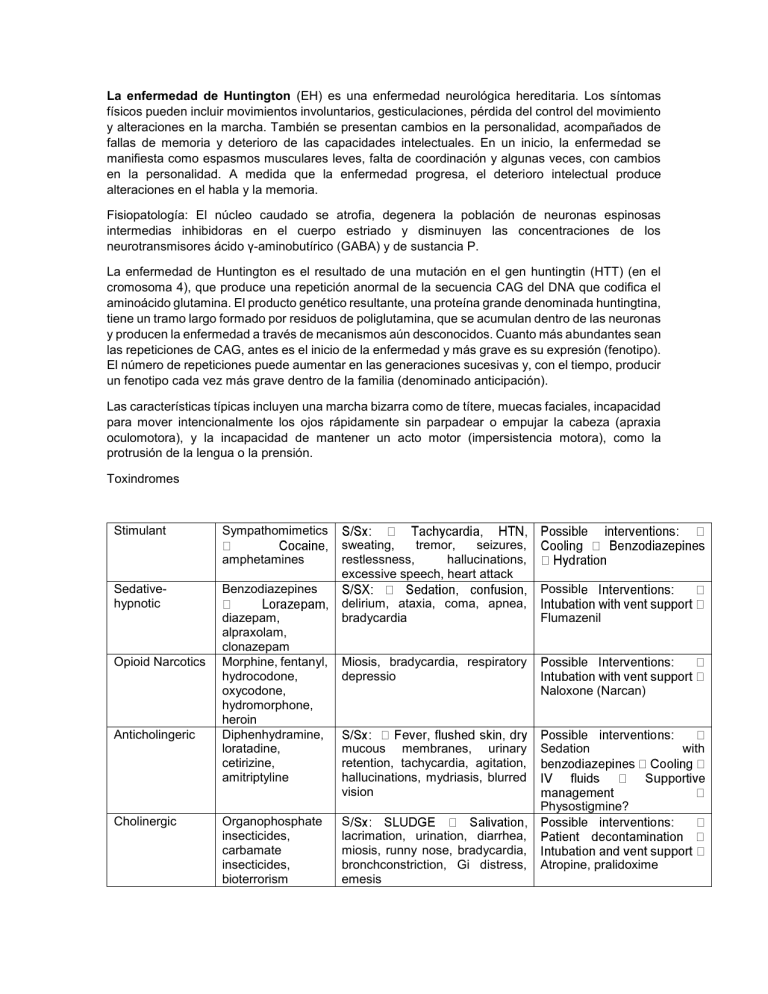
La enfermedad de Huntington (EH) es una enfermedad neurológica hereditaria. Los síntomas físicos pueden incluir movimientos involuntarios, gesticulaciones, pérdida del control del movimiento y alteraciones en la marcha. También se presentan cambios en la personalidad, acompañados de fallas de memoria y deterioro de las capacidades intelectuales. En un inicio, la enfermedad se manifiesta como espasmos musculares leves, falta de coordinación y algunas veces, con cambios en la personalidad. A medida que la enfermedad progresa, el deterioro intelectual produce alteraciones en el habla y la memoria. Fisiopatología: El núcleo caudado se atrofia, degenera la población de neuronas espinosas intermedias inhibidoras en el cuerpo estriado y disminuyen las concentraciones de los neurotransmisores ácido γ-aminobutírico (GABA) y de sustancia P. La enfermedad de Huntington es el resultado de una mutación en el gen huntingtin (HTT) (en el cromosoma 4), que produce una repetición anormal de la secuencia CAG del DNA que codifica el aminoácido glutamina. El producto genético resultante, una proteína grande denominada huntingtina, tiene un tramo largo formado por residuos de poliglutamina, que se acumulan dentro de las neuronas y producen la enfermedad a través de mecanismos aún desconocidos. Cuanto más abundantes sean las repeticiones de CAG, antes es el inicio de la enfermedad y más grave es su expresión (fenotipo). El número de repeticiones puede aumentar en las generaciones sucesivas y, con el tiempo, producir un fenotipo cada vez más grave dentro de la familia (denominado anticipación). Las características típicas incluyen una marcha bizarra como de títere, muecas faciales, incapacidad para mover intencionalmente los ojos rápidamente sin parpadear o empujar la cabeza (apraxia oculomotora), y la incapacidad de mantener un acto motor (impersistencia motora), como la protrusión de la lengua o la prensión. Toxindromes Stimulant Sympathomimetics amphetamines Sedativehypnotic Opioid Narcotics Anticholingeric sweating, tremor, seizures, restlessness, hallucinations, excessive speech, heart attack Benzodiazepines diazepam, alpraxolam, clonazepam Morphine, fentanyl, hydrocodone, oxycodone, hydromorphone, heroin Diphenhydramine, loratadine, cetirizine, amitriptyline Possibl delirium, ataxia, coma, apnea, bradycardia Flumazenil Miosis, bradycardia, respiratory depressio Naloxone (Narcan) mucous membranes, urinary retention, tachycardia, agitation, hallucinations, mydriasis, blurred vision Sedation Physostigmine? Cholinergic Organophosphate insecticides, carbamate insecticides, bioterrorism S lacrimation, urination, diarrhea, miosis, runny nose, bradycardia, bronchconstriction, Gi distress, emesis Atropine, pralidoxime with Hallucinogen Hypoglycemic Lyseric acid diethylamide (LSD), phencyclidine (PCP), ketamine Insulin (Lantus, Levemir, Novolog, Sulfonylureas (glipizide, glyburide) dysphoria, mydriasis ety, hyperthermia, management sweating, tachycardia, hypertension, seizures, strange behavior, slurred speech Specific overdoses Benzodiazepines Methamphetamine Diphenhydramine Fase 1: Reacciones de Fase I y II: metabolismo del benceno. El benceno, substancia lipófila, muy poco soluble en agua, sufre en el organismo distintas reacciones de oxidación catalizadas por CYP1A1 y CYP2E1, dando origen a derivados fenólicos (reacción de Fase I). Dichos metabolitos son ciertamente más polares y reactivos, pero no poseen la suficiente hidrosolubilidad que garantice una fácil eliminación. El fenol, metabolito mayoritario, es conjugado con ácido glucorónico (reacción de Fase II) lo que aumenta notablemente su hidrosolubilidad y es fácilmente eliminado por vía renal. Otros ejemplos de fase I son: procaína, aspirina, clofibrato, lidocaína, procainamida, indometacina. Furosemida: Biotransformación: se une en un 70 % a proteínas en plasma, su efecto máximo es a 30 a 45 minutos, su metabolización es el hígado en un 90 %. El 10 % se excreta por vía renal sin alteración. Fase II: ejemplos acetaminofén, morfina, diazepam, esteroides, metildopa, sulfonamida, isoniazida, dapsona, clonazepam Terminal presináptica: transmisión Sináptica La transmisión sináptica se refiere a la propagación de los impulsos nerviosos de una célula hacia otra. Esto ocurre en una estructura especializada de la célula conocida como la brecha sináptica, un sitio de encuentro entre el axón de la neurona pre-sináptica y la neurona post-sináptica. La terminación de un axón pre-sináptico, que se encuentra opuesto a la neurona post-sináptica, se agranda y forma una estructura conocida como el botón terminal. Un axón puede hacer contacto a través de cualquier lugar en la segunda neurona: en las dendritas (una sinapsis axo-dendrítica), en el cuerpo celular (una sinapsis axo-somática) o los axones (una sinapsis axo-axonal). Los impulsos nerviosos son transmitidos en la brecha sináptica por la liberación de químicos denominados neurotransmisores. Cuando el impulso nervioso, o el potencial de acción llega al final del axón pre-sináptico, las moléculas del neurotransmisor son liberadas hacia la brecha sináptica. Los neurotransmisores son un grupo diverso de compuestos químicos, desde aminas simples como la dopamina y amino ácidos tales como el ácido gamma-amino butírico (GABA), hasta polipéptidos como las encefalinas. Los mecanismos por los cuales se produce una respuesta en ambas neuronas pre-sinápticas y post-sinápticas son tan diversos como los mecanismos usados por el factor de crecimiento y los receptores de citocinas. La liberación de neurotransmisores es iniciada por la llegada de un impulso nervioso (o potencial de acción), y se produce mediante un proceso muy rápido de secreción celular: en el terminal nervioso presináptico, las vesículas que contiene los neurotransmisores permanecen ancladas y preparadas junto a la membrana sináptica. Cuando llega un potencial de acción se produce una entrada de iones calcio a través de los canales de calcio dependientes de voltaje. Los iones de calcio inician una cascada de reacciones que terminan haciendo que las membranas vesiculares se fusionen con la membrana presináptica y liberando su contenido a la hendidura sináptica. Los receptores del lado opuesto de la hendidura se unen a los neurotransmisores y fuerzan la apertura de los canales iónicos cercanos de la membrana postsináptica, haciendo que los iones fluyan hacia o desde el interior, cambiando el potencial de membrana local. El resultado es excitatorio en caso de flujos de despolarización, o inhibitorio en caso de flujos de hiperpolarización. El que una sinapsis sea excitatoria o inhibitoria depende del tipo o tipos iones que se canalizan en los flujos postsinápticos, que a su vez es función del tipo de receptores y neurotransmisores que intervienen en la sinapsis.