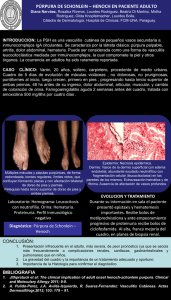
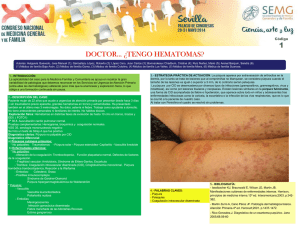
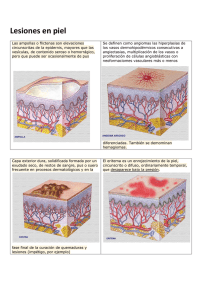
Actualizaciones Púrpura J.M. Carrascosa y C. Ferrándiz Servei de Dermatologia. Hospital Universitari Germans Trias i Pujol. Universitat Autònoma de Barcelona. Badalona. Barcelona. La púrpura puede ser el resultado de alteraciones de cualquiera de los elementos que condicionan la hemostasia: plaquetas, factores de coagulación o vasos sanguíneos. Las púrpuras secundarias a alteraciones en el número o funcionalismo de las plaquetas se manifestarán casi siempre en forma de petequias. Por el contrario, la aparición de áreas equimóticas deberá alertar sobre un trastorno en los factores de la coagulación, en particular sobre la posibilidad de una coagulación intravascular diseminada. La púrpura palpable es la forma clínica más frecuente y representativa de las vasculitis cutáneas de vaso pequeño. La púrpura no palpable de origen vascular puede ser de etiología inflamatoria –angiocapilaritis–, por incremento de la presión intravascular o asociada a la alteración estructural de los vasos sanguíneos. Se entiende por púrpura el cambio de coloración de la piel o de las mucosas que resulta de la extravasación de hematíes1. La púrpura puede aparecer por trastornos de cualquiera de los elementos que condicionan la hemostasia: plaquetas, factores de coagulación o vasos sanguíneos. En función del tamaño de las lesiones purpúricas, éstas recibirán la denominación de petequias –hemorragias puntiformes de menos de 2 mm de diámetro–, púrpura –de 2 mm a 1 cm– o equimosis –lesiones mayores de 1 cm–. Las características clínicas de la púrpura permiten, en muchas ocasiones, sospechar cuál de los citados elementos se encuentra implicado. De este modo, las alteraciones plaquetarias se manifestarán casi siempre en forma de petequias, mientras que los trastornos de la coagulación darán lugar a áreas equimóticas. Las lesiones inflamatorias de los vasos –vasculitis y angiocapilaritis– representan la causa más frecuente de púrpura localizada y persistente, siendo posible casi siempre identificar a la inspección un componente eritematoso e inflamatorio. Por definición, las lesiones purpúricas no desaparecen a la vitropresión, característica clínica que permite diferenciarlas de otras erupciones eritematosas. En la presente revisión se expondrán las características más relevantes de aquellos cuadros clínicos asociados a púrpura, tomando como hilo conductor la clasificación propuesta en la tabla 1. Para finalizar se desarrollarán, atendiendo a sus características distintivas, la púrpura en el neonato, la asociada a enfermedades sistémicas y la secundaria a procesos infecciosos. En la tabla 2 se exponen las exploraciones complementarias que pueden estar indicadas en el estudio etiológico de un cuadro purpúrico. Púrpuras secundarias a alteraciones en el número o funcionalismo de las plaquetas Púrpura trombocitopénica idiopática o enfermedad de Werlhof2-6 Palabras clave: Púrpura. Trombocitopenia. Coagulación intravascular diseminada. Vasculitis. 19 Es un trastorno que resulta de la destrucción autoinmune de las plaquetas circulantes de forma secundaria a anticuerpos antiplaquetarios, casi siempre de tipo IgG o IgM. Se han descrito dos formas. La forma aguda, de etiología postinfecciosa y más frecuente en la edad infantil, se presenta como FMC-Formación Médica Continuada en Atención Primaria 215 Volumen 8, Número 4, Abril 2001 TABLA 1. Clasificación de las púrpuras TABLA 2. Exploraciones complementarias indicadas en el estudio de las púrpuras Alteraciones en el número o funcionalismo de las plaquetas 1. Púrpura trombocitopénica idiopática Aguda Crónica 2. Púrpura trombocitopénica secundaria o sintomática Déficit en la producción (leucemias, anemia aplásica, mieloma, mielofibrosis, tóxicos, uremia) Fármacos Infecciones Secuestro plaquetario (esplenomegalia, síndrome de Kasabach-Merrit) Consumo excesivo (púrpura trombótica trombocitopénica, síndrome hemolítico urémico, coagulación intravascular diseminada) 3. Alteraciones de la función plaquetaria Enfermedad de Von Willebrand Síndrome de Hermansky-Pudlak Síndrome de Ehler-Danlos 4. Trombocitosis Alteraciones de la coagulación Hemofilias Alteraciones del complejo de la protrombina Coagulación intravascular diseminada y purpura fulminans Púrpura por afección de los vasos (púrpura vascular) 1. Vasculitis cutánea de pequeño vaso (púrpura palpable) 2. Púrpura no palpable Dermatosis pigmentarias purpúricas Púrpura por incremento de la presión intravascular (tos, vómitos, estasis venosa) Púrpura por alteraciones estructurales de los vasos (púrpura senil, lesión actínica, púrpura por corticoides, escorbuto, síndrome de Ehler-Danlos) Púrpura tóxica (fármacos y sustancias químicas) Infecciones Miscelánea Púrpuras secundarias a enfermedades sistémicas Púrpuras secundarias a procesos infecciosos Púrpuras neonatales Síndrome de autosensibilización eritrocitaria una erupción espontánea petequial o en forma de áreas equimóticas en la piel y mucosas que pueden acompañarse de ampollas hemorrágicas en las encías y labios. El pronóstico, casi siempre benigno, puede, sin embargo, verse ensombrecido por el desarrollo de hemorragias viscerales, en particular hemorragia intracraneal. Las formas crónicas son más frecuentes en pacientes adultos y se encuentran, en alrededor del 20% de los casos, alteraciones analíticas diagnósticas del síndrome antifosfolípido: alargamiento del tiempo parcial de tromboplastina, anticoagulante lúpico y anticuerpos anticardiolipina. La clínica de las formas crónicas es similar a la referida en las formas agudas, si bien su presentación puede ser más larvada y la presencia de ampollas hemorrágicas en la mucosa oral debe considerarse rara. De este modo, las hemorragias de carácter ginecológico pueden constituir el pri216 FMC-Formación Médica Continuada en Atención Primaria Recuento plaquetario Tests de resistencia capilar Tiempo de hemorragia Batería de factores de coagulación Estudio histopatológico mer y único síntoma de púrpura trombocitopénica idiopática en mujeres de edad media. El tratamiento de las formas agudas no es siempre preciso y, aunque se ha preconizado la utilidad de los corticoides o las inmunoglobulinas en las formas graves, no está claro si el concurso de estos tratamientos modifica la tendencia a la hemorragia o la mortalidad. En las formas crónicas, por el contrario, la esplenectomía sigue siendo el tratamiento de elección en dos tercios de los casos. Otras posibilidades terapéuticas, como glucocorticoides, inmunoglobulinas intravenosas, danazol o fármacos inmunosupresores se consideran, aún hoy, reservadas para aquellos casos en los que la esplenectomía fracase o bien esté contraindicada1. Púrpura trombocitopénica secundaria o sintomática (figs. 1 y 2)7-12 La lesión estructural y funcional de la médula ósea en el curso de enfermedades como leucemias, anemias aplásicas, carcinomatosis, mieloma múltiple o mielofibrosis es causa frecuente de trombocitopenia por déficit en su síntesis. A mecanismos parecidos se atribuye la trombopenia asociada al contacto con tóxicos como el benzol, la mostaza nitrogenada o trastornos metabólicos como la uremia. Existe una larga lista de fármacos que se han asociado a trombocitopenia, si bien en muchos casos el mecanismo por el que ésta ocurre no está bien establecido. Los fármacos citados con mayor frecuencia son la quinina, quinidina, oro, heparina, sulfamidas, tiacidas, indometacina, bismuto, arsenicales y rifampicina. El concurso de procesos infecciosos también debe considerarse en el diagnóstico diferencial de las trombocitopenias (véase posteriormente). La esplenomegalia puede dar lugar a púrpura por secuestro plaquetario. Este mecanismo también explicaría la inclusión en este apartado del síndrome de Kasabach-Merrit, definido por el desarrollo de trombocitopenia y diátesis hemorrágica en el contexto de un hemangioma cavernoso gigante. Los angiomas, que pueden ser únicos o múltiples pero en general de gran tamaño, secuestran y destruyen las plaquetas en su interior. La púrpura trombótica trombocitopénica y el síndrome hemolítico urémico son distintas expresiones de un mismo proceso caracterizado por la formación de trombos de plaquetas en la microvasculatura, hecho que condiciona ane20 J.M. Carrascosa y C. Ferrándiz.– Púrpura mia hemolítica y alteraciones vasculares con afección renal –síndrome hemolítico urémico– o del sistema nervioso –púrpura trombótica trombocitopénica–. En el tratamiento de estos procesos se han empleado con éxito variable glucocorticoides, heparina, inmunoglobulinas intravenosas o vincristina. Debe recordarse que la transfusión de plaquetas ha de evitarse siempre en este proceso por el riesgo de agravarlo. Alteraciones de la función plaquetaria Se han descrito diversos síndromes en los que el desarrollo de cuadros hemorrágicos se debería a alteraciones de la función plaquetaria, siendo normal la cifra de plaquetas. En este apartado se incluyen la enfermedad de Von Willebrand –proceso autosómico dominante en el que existe un déficit de la actividad coagulante del factor VIII y del antígeno asociado–, el síndrome de Hermansky-Pudlak –enfermedad transmitida con un patrón autosómico dominante que combina albinismo oculocutáneo tirosinasa positivo, diátesis hemorrágica y depósitos ceroides en el sistema reticuloendotelial–, el síndrome de Ehler-Danlos, el seudoxantoma elástico, la insuficiencia renal crónica y la anemia grave. Trombocitosis13 De forma aparentemente paradójica, la trombocitemia puede ser causa de hemorragia, en particular cuando el número de plaquetas supera la cifra de 1.000 × 109/l. Debe sospecharse esta posibilidad cuando la púrpura se acompañe de áreas parcheadas de livedo reticular, acrocianosis, eritromelalgia u otros síntomas vasculares de obstrucción, incluyendo gangrena. Alteraciones en los factores de la coagulación Hemofilias6,14 Tanto en la hemofilia A –déficit del factor VIII– como en la hemofilia B –déficit del factor IX– pueden detectarse manifestaciones hemorrágicas ya presentes en el período neonatal. Desde el punto de vista clínico, resulta característico observar hemorragias profusas tras mínimas heridas, así como el desarrollo de hematomas y extensas sufusiones hemorrágicas, en particular sobre prominencias óseas. Con frecuencia la hemorragia cede de forma espontánea para reaparecer pasados algunos minutos o incluso horas. Las hemartrosis, que representan la principal causa de morbilidad, se desarrollarán a partir del cuarto año de vida. Otras hemorragias viscerales frecuentes son las hematurias y la hemorragia digestiva, mientras que la localizada en el sistema nervioso ocurre de forma infrecuente. 23 Figuras 1 y 2. Petequias y enantema en una púrpura trombopénica por fármacos. Alteraciones del complejo de la protrombina Éste incluye a los factores II, VII, IX y X, que son sintetizados en el hígado de forma dependiente de la vitamina K. Podrán ser causa de púrpura todos aquellos procesos que cursen con déficit de esta vitamina, como una dieta inadecuada, malabsorción intestinal, toma de anticoagulantes de tipo cumarínicos o inmadurez metabólica en el recién nacido (enfermedad hemorrágica del recién nacido). FMC-Formación Médica Continuada en Atención Primaria 217 Volumen 8, Número 4, Abril 2001 TABLA 3. Situaciones clínicas que pueden complicarse con coagulación intravascular diseminada Liberación de tromboplastina tisular al compartimiento intravascular Accidentes obstétricos: desprendimiento precoz de placenta, placenta previa, retención de feto muerto, retención placentaria, preeclampsia, eclampsia, etc. Neoplasias diseminadas: leucemias agudas promielocíticas, etc. Infecciones: sepsis por gérmenes gramnegativos, infecciones por bacterias grampositivas, Rickettsia y virus Complejos antígeno-anticuerpo: accidentes transfusionales, procesos autoinmunes Estasis sanguínea Coagulación intravascular diseminada6,15-18 La coagulación intravascular diseminada (CID) se define como una brusca activación de la cascada de la coagulación, circunstancia que puede ocurrir en el contexto de enfermedades muy diversas. El resultado es un depósito intravascular de fibrina que condiciona trombosis, isquemia tisular y necrosis. La activación secundaria de la fibrinólisis condiciona una depleción de plaquetas y de otros factores de la coagulación, lo que lleva, de forma aparentemente paradójica, a un estado de hipocoagulabilidad. Las situaciones clínicas que pueden conducir a CID se exponen en la tabla 3. La presentación clínica es heterogénea. De este modo, mientras que en las formas leves sólo se observarán escasas petequias y áreas equimóticas, en las graves se desarrollarán hematomas subcutáneos, ampollas hemorrágicas y áreas de necrosis cutáneas. El cuadro clínico puede complementarse con hemorragias gastrointestinales, genitourinarias y viscerales. En general, las manifestaciones derivadas de la hipocoagulabilidad superan en extensión y gravedad a las derivadas de la hipercoagulabilidad. En los estudios de laboratorio se detec- Figura 3. Purpura fulminans en meningococemia. 218 FMC-Formación Médica Continuada en Atención Primaria tarán trombopenia y alargamiento del tiempo de protrombina y del tiempo parcial de tromboplastina. El diagnóstico de laboratorio se completará con el hallazgo de títulos disminuidos de fibrinógeno e incremento de sus productos de degradación. Se ha afirmado que el déficit congénito o adquirido de proteínas S y C representaría un factor de riesgo para el desarrollo de este cuadro. La purpura fulminans es una forma grave de CID desencadenada tras un proceso infeccioso (p. ej., escarlatina, infecciones estreptocócicas, varicela o rubéola) y se caracteriza por la aparición súbita de extensas áreas equimóticas. Las lesiones, iniciadas en el tercio distal de las extremidades y en las zonas de presión, tienden a crecer de forma centrífuga dando lugar a grandes placas necróticas con tendencia a la necrosis central y a la formación de ampollas hemorrágicas (fig. 3). La afección visceral puede derivar en hematuria, hemorragias gastrointestinales, shock, coma y muerte. El pronóstico de la purpura fulminans debe considerarse invariablemente grave, ya que puede conducir a la muerte del individuo en 2 o 3 días. Sin embargo, las posibilidades terapéuticas disponibles en la actualidad –tratamiento del shock y administración de plaquetas, fibrinógeno y plasma fresco– han permitido reducir la tasa de mortalidad a un 20-35% de los casos, siempre y cuando el tratamiento se instaure de forma temprana. Existen algunos ensayos en marcha para investigar la utilidad en este proceso de la antitrombina III o de inhibidores de la C1-esterasa. Púrpura por afección de los vasos (púrpura vascular) Vasculitis cutánea de vaso pequeño (púrpura palpable)19-30 Dentro de este concepto se incluye un amplio grupo de entidades, tanto primarias como secundarias –desencadenadas por fármacos, infecciones, neoplasias o enfermedades autoinmunes subyacentes– en las que las lesiones cutáneas pueden aparecer aisladas o acompañarse de la afección vasculítica en otros órganos y sistemas. El variado espectro de lesiones cutáneas, la más característica de las cuales es la púrpura palpable, será la traducción de la inflamación y necrosis de los vasos cutáneos de pequeño calibre: arteriolas, capilares y, de forma especialmente significativa, vénulas poscapilares. Desde hace años se conoce la implicación de los inmunocomplejos, bien circulantes o formados in situ, en la patogenia de las vasculitis cutáneas de vaso pequeño (VCPV) a través de un mecanismo de hipersensibilidad de tipo III. De este modo, se considera en la actualidad que este mecanismo es el predominante en las VCPV y justificaría la génesis de buena parte de los cuadros incluidos en esta denominación, como las vasculitis desencadenadas por fármacos, infeccio24 J.M. Carrascosa y C. Ferrándiz.– Púrpura TABLA 4. Clasificación de las vasculitis cutáneas de pequeño vaso (VCPV) en función de factores desencadenantes y procesos subyacentes VCPV desencadenadas por infecciones Bacterianas (estreptotoco betahemolítico, estafilococo dorado, Mycobacterium leprae) Virales (hepatitis A, B, C, virus del herpes simple, virus Influenza) Fúngicas (Candida albicans) Protozoos (Plasmodium malariae) Helmínticas (Squistosoma haematobium, Squistosoma mansoni, Onchocerca volvulus) VCPV desencadenadas por fármacos Insulina, penicilina, hidantoínas, estreptomicina, ácido aminosalicílico, sulfamidas, tiacidas, fenotiacidas, fenilbutazona, quinina, estreptocinasa, tamoxifeno, vacunas anti-Influenzae, anticonceptivos orales, suero VCPV desencadenadas por sustancias químicas (insecticidas, derivados del petróleo) VCPV asociadas a alergenos alimentarios (proteínas de la leche, gluten) VCPV asociadas a enfermedades crónicas subyacentes (lupus eritematoso sistémico, síndrome de Sjöegren, artritis reumatoide, enfermedad de Behçet, estados hiperglobulinémicos, crioglobulinemia, síndrome del bypass intestinal, colitis ulcerosa, fibrosis quística, cirrosis biliar primaria) VCPV asociadas a neoplasias Enfermedades linfoproliferativas (enfermedad de Hodgkin, micosis fungoide, linfosarcoma, leucemia T del adulto, mieloma múltiple) Tumores sólidos (cáncer pulmonar, carcinoma de colon, próstata, renal, de cabeza y cuello, de mama) VCPV como signo de vasculitis sistémica (granulomatosis de Wegener, síndrome de Churg-Strauss, poliangitis microscópica) Cuadros idiopáticos de VCPV (vasculitis urticarial, eritema elevatum diutinum, vasculitis nodular, vasculitis livedoide, atrofia blanca, poliarteritis nudosa cutánea) nes, neoplasias o enfermedades autoinmunes. Sin embargo, en la actualidad se conoce que no es el único mecanismo posible. De este modo, pueden comprobarse lesiones clínica y microscópicamente idénticas a las anteriores, por ejemplo, en las vasculitis mediadas por anticuerpos anticitoplasma del neutrófilo (ANCA). En general, se considera que puede encontrarse un factor causal subyacente o desencadenante en el 30-70% del total de casos de VCPV (tabla 4), siendo los citados con mayor frecuencia los fármacos –p. ej., penicilina–, las infecciones bacterianas –p. ej., estreptococo– o virales –p. ej., virus de la hepatitis C–, las enfermedades autoinmunes –en particular el lupus eritematoso y la artritis reumatoide– o las neoplasias subyacentes –sobre todo las hematológicas–. También puede ser que la clínica cutánea se integre dentro del cortejo sindrómico de una vasculitis sistémica –p. ej., granulomatosis 25 Figura 4. Púrpura palpable (vasculitis leucocitoclástica). de Wegener, vasculitis de Churg-Strauss o vasculitis de Shönlein-Henoch. La forma de presentación cutánea más frecuente en las VCPV es la púrpura palpable, en forma de pápulas o placas purpúricas que no desaparecen a la vitropresión (fig. 4). La púrpura palpable ocurre en más del 90% de los casos y representa la traducción clínica más fiable de la inflamación y necrosis de los vasos de pequeño calibre. El grado de inflamación puede condicionar que las lesiones de púrpura palpable evolucionen hacia ampollas hemorrágicas, placas necróticas o úlceras (fig. 5). Por el contrario, si el proceso inflamatorio es discreto, las lesiones presentarán un aspecto eritematoedematoso que remeda a la urticaria –vasculitis urticarial– (fig. 6). El desarrollo de nódulos o de livedo reticular –lesiones mucho más infrecuentes– indicará la presencia de vasculitis de vaso de tamaño intermedio, lo que obliga a descartar la presencia de una afección sistémica (figs. 7 y 8). La distribución de las lesiones suele ser bilateral y simétrica, de forma que casi siempre se afectan las extremidades inferiores (60-90%), pudiendo extenderse al tronco (30%) o a las extremidades superiores (5-10%). Las lesiones cutáneas evolucionan durante varios días, aunque si aparecen brotes FMC-Formación Médica Continuada en Atención Primaria 219 Volumen 8, Número 4, Abril 2001 Figura 7. Nódulos cutáneos por vasculitis. Figura 5. Ampollas hemorrágicas en vasculitis leucocitoclástica. Figura 8. Livedo reticular. Figura 6. Vasculitis urticarial. reiterados el aspecto clínico puede ser de cronicidad. La erupción puede ser asintomática o acompañarse de prurito (40%) o dolor (30%). El cuadro clínico puede acompañarse de fiebre (30%) o de síndrome tóxico (25%). La afección de órganos y sistemas extracutáneos durante el proceso inflamatorio ocurre en alrededor del 20 al 50% de los casos, siendo el sistema osteoarticular –artralgias/artritis– 220 FMC-Formación Médica Continuada en Atención Primaria y el renal los implicados con mayor frecuencia. Sin embargo, en este último órgano la lesión vasculítica condiciona en su mayoría microhematuria o proteinuria microscópica, siendo excepcional el desarrollo de una insuficiencia renal franca. Mucho menos frecuentes son el compromiso del aparato digestivo –prominente en procesos tales como el síndrome de Shönlein-Henoch–, del sistema nervioso o del aparato respiratorio. En el estudio analítico, las alteraciones más frecuentes son inespecíficas, en forma de leucocitosis o incrementos de la velocidad de sedimentación globular (VSG). Los estudios de inmunofluorescencia sobre biopsias cutáneas pueden ser de utilidad, ya que su positividad será indicativa de la implicación de fenómenos de hipersensibilidad de tipo III en la patogenia del proceso, si bien se trata de una determinación de escasa sensibilidad, en particular si la lesión biopsiada es de más de 24 h de evolución. Por otro lado, la visualización de depósitos de IgA será muy indicativa, en un contexto clínico adecuado, de vasculitis de Shönlein-Henoch (VSH). Otras determinaciones inmunológicas –complemento sérico, anticuerpos antinucleares (ANA), factor reumatoide– pueden ayudar a caracterizar una enfermedad autoinmune subyacen26 J.M. Carrascosa y C. Ferrándiz.– Púrpura te. También serán útiles, en el estudio etiológico, las determinaciones de crioglobulinas o de ANCA. Desde el punto de vista microscópico, el hallazgo fundamental es la inflamación y necrosis del endotelio, siendo característico observar un depósito periendotelial de fibrina –necrosis fibrinoide–. Alrededor del vaso se constituye un infiltrado inflamatorio de predominio neutrofílico con polvo nuclear –leucocitoclasia– en las fases iniciales, y mixto o incluso de predominio linfocitario en fases más evolucionadas. Teniendo en cuenta que las VCPV son un grupo heterogéneo de entidades, el pronóstico será muy variable y deberá valorarse de forma individualizada en cada caso. En conjunto, se considera que las VCPV evolucionarán de forma aguda en el 50% de los casos. En el extremo contrario, alrededor del 10% de los pacientes presentarán brotes durante más de 10 años. La mortalidad asociada a las VCPV es escasa, habiéndose determinado que menos del 2% de los pacientes acabarán muriendo a causa de complicaciones extracutáneas de la vasculitis. Considerando las VCPV como enfermedades con un espectro de gravedad muy variable, se juzga adecuado llevar a cabo un protocolo de estudio que permita establecer la extensión y gravedad de la afección extracutánea y el diagnóstico de posibles desencadenantes o procesos subyacentes (tabla 5). La vasculitis de Shönlein-Henoch es una variante de la VCPV en la que, a las lesiones cutáneas, casi siempre en forma de púrpura palpable, se suman la implicación de grandes articulaciones (75-85%), síntomas gastrointestinales –dolor cólico, vómitos, melenas y hematemesis– (60-75%) y signos de compromiso renal –hematuria microscópica y proteinuria, glomerulonefritis segmentaria y focal– (40-50%). El dato más característico es el hallazgo de valores elevados de IgA en suero y depósitos de esta inmunoglobulina y de complemento en las lesiones cutáneas. La VSH es un proceso de predominio en la infancia, con un pico entre los 4 y 8 años, aunque puede aparecer en la edad adulta. El curso de la enfermedad acostumbra ser recurrente, precediéndose con frecuencia los brotes de una infección estreptocócica o de un catarro de vías altas. El pronóstico, condicionado por la magnitud de la lesión renal, debe considerarse bueno en la infancia y reservado en la edad adulta. La vasculitis urticarial es una variante de la VCPV de predominio en mujeres jóvenes, definida por el aspecto eritematoedematoso de las lesiones que recuerda a los habones de la urticaria. Sin embargo, el estudio microscópico demostrará una vasculitis leucocitoclástica en todos los casos. A diferencia de lo que ocurre en la urticaria, las lesiones evolucionan durante más de 24 h, son dolorosas en vez de pruriginosas y pueden dejar hiperpigmentación postinflamatoria al resolverse. La vasculitis urticarial cursa en forma de brotes recurrentes durante años, a menudo acompañados de artralgias. En el estudio inmunológico resulta característico en27 TABLA 5. Propuesta de protocolo de estudio en las vasculitis cutáneas de pequeño vaso Datos clínicos Antecedentes etiológicos Fármacos Procesos infecciosos Enfermedades sistémicas Neoplasias Lesiones cutáneas Tiempo de evolución Tipo de lesiones (pápulas, placas, ampollas hemorrágicas, úlceras, nódulos y urticaria) Localización Curso del proceso (agudo, recurrente, crónico) Afección sistémica General (fiebre, astenia, anorexia o pérdida de peso) Muscular (mialgias) Articular (artritis y artralgias) Gastrointestinal (dolor abdominal, vómitos y diarreas) Neurológica (paresias, parestesias, neuralgias, cefalea y alteraciones visuales) Cardiovascular (angina y claudicación) Exploraciones complementarias Hemograma y velocidad de sedimentación globular Coagulación Bioquímica general incluyendo función renal y hepática y enzimas musculares Proteinograma Bioquímica de orina incluyendo determinación de hematíes crenados Inmunología (ANA, anti-ADN, dosificación del complemento, FR, crioglobulinas, ANCA, ICC y dosificación de inmunoglobulinas) Serologías (ASLA, HBsAg, VHC y lúes) Radiografía de tórax Otras exploraciones según hallazgos (biopsia renal o hepática y endoscopia pulmonar) Estudio histológico Biopsia-punción de 4 mm para tinción de hematoxilinaeosina y para inmunofluorescencia directa ANA: anticuerpos antinucleares; FR: factor reumatoide; ANCA: anticuerpos anticitoplasma del neutrófilo; ICC: inmunocomplejos circulantes; ASLA: antiestreptolisinas; HBsAg: antígeno de superficie del virus de la hepatitis B; VHC: virus de la hepatitis C. contrar hipocomplementemia y, en ocasiones, alteraciones indicativas de enfermedad autoinmune –ANA, descenso del complemento–. De hecho, en algunos casos puede subyacer una auténtica enfermedad autoinmune, en particular un lupus eritematoso o una enfermedad de Sjöegren. El eritema elevatum diutinum es una forma infrecuente de VCPV, caracterizada por el desarrollo de placas purpúricas distribuidas de manera bilateral y simétrica en las áreas de extensión de las extremidades, que evolucionan de forma crónica durante meses o años. La etiopatogenia de las lesioFMC-Formación Médica Continuada en Atención Primaria 221 Volumen 8, Número 4, Abril 2001 percusión negativa que los factores físicos derivados del ortostatismo ejercen en el desarrollo de las lesiones. Los antihistamínicos anti-H1, empleados en las formas leves, no sólo permitirán disminuir los síntomas, sino también bloquear la adhesión de los inmunocomplejos al endotelio, favorecida por la histamina. La colquicina –de 0,5 a 1,5 mg diarios– y la sulfona –50 a 200 mg diarios– son los fármacos más empleados en los casos con afección cutánea predominante. Otras posibilidades terapéuticas, como los corticoides sistémicos, el metotrexato, la azatioprina o la ciclosporina A, suelen reservarse para aquellos casos en los que fallan los anteriores, o cuando se detecta una importante afección extracutánea. Púrpura no palpable Dermatosis pigmentarias purpúricas (angiocapilaritis purpúricas pigmentarias)31-35 Figura 9. Púrpura de Schamberg. nes cutáneas, todavía en discusión, podría justificarse por una reacción de hipersensibilidad frente a antígenos estreptocócicos. En algunos casos se ha descrito la asociación del eritema elevatum diutinum con gammapatía policlonal IgA, IgM o IgG. Desde el punto de vista terapéutico, en todos los casos de VCPV debe recomendarse reposo para contrarrestar la re- Figura 10. Púrpura pigmentaria anular. 222 FMC-Formación Médica Continuada en Atención Primaria Las púrpuras pigmentarias son un grupo de dermatosis de etiología desconocida, definidas por la presencia en el examen microscópico de capilaritis acompañada de una extravasación discreta de hematíes y de depósito extravascular de hemosiderina. Desde el punto de vista clínico, se presentan en forma de erupciones constituidas por máculas milimétricas confluentes en placas de coloración eritematoanaranjada. La variante más frecuente es la púrpura pigmentaria progresiva o enfermedad de Shamberg (fig. 9), entidad de curso crónico-recurrente, más frecuente en los varones, en la que la clínica cutánea acostumbra iniciarse en las extremidades inferiores para extenderse luego al resto del tegumento cutáneo. Dentro del conjunto de púrpuras pigmentarias se incluye una serie de variantes que, al menos en muchos casos, basan sus diferencias en modificaciones morfológicas difíciles de establecer en la práctica y con escasa o nula implicación pronóstica. Así, se habla de púrpura pruriginosa o eccematoide de Doucas y Kapetanakis si la púrpura se acompaña de cambios eccematosos; de enfermedad de Majocchi si las lesiones adoptan contornos anulares (fig. 10), de dermatitis de Gougerot y Blum cuando aparecen asociadas pápulas liquenoides, o de púrpura gravitacional o dermatitis ocre de Favre para referirse a una capilaritis limitada a las extremidades inferiores y asociada a insuficiencia venosa (fig. 11). El liquen aureus es un término empleado para referirse a una variante localizada de angiocapilaritis de evolución prolongada. Aunque en la mayoría de casos la etiología del cuadro es desconocida, los hallazgos histopatológicos indican la implicación de un mecanismo de hipersensibilidad de tipo IV, habiéndose descrito en relación al carbomal, aditivos alimentarios o por eccema de contacto alérgico a tintes de la ropa. La mayoría de las dermatosis purpúricas son muy resistentes al tratamiento y pueden evolucionar durante años. Se 28 J.M. Carrascosa y C. Ferrándiz.– Púrpura Figura 11. Dermatitis ocre. han probado, con éxito en casos aislados, los antihistamínicos orales, venotónicos, hemorreológicos, los corticoides tópicos, la PUVA-terapia, la ciclosporina o la griseofulvina. Púrpura por aumento de la presión intravascular36 La púrpura cutánea, en particular en forma de exantema petequial, puede ocurrir en el curso de procesos que condicionen un incremento de la presión intravascular. De este modo, resulta típica la aparición de petequias alrededor de los tejidos laxos de labios y párpados tras maniobras de Valsalva desencadenadas por vómitos o accesos de tos (fig. 12). De igual modo, pueden observarse máculas purpúricas con un patrón reticulado en las zonas de presión de prendas de vestir, o máculas purpúricas redondeadas en las zonas de aplicación de electrodos después de un electrocardiograma. La estasis venosa o cualquier dermatosis que curse con vasodilatación es causa frecuente de púrpura en las extremidades inferiores en pacientes de edad avanzada. En los niños, la aparición de zonas purpúricas en las áreas genitales debe alertar acerca de la posibilidad de abusos sexuales. Figura 12. Púrpura por maniobras de Valsalva. móticas en zonas expuestas, bien de forma espontánea o más a menudo desencadenadas por pequeños traumatismos (fig. 13). En la alteración estructural de los vasos sanguíneos estaría también el origen de la púrpura que puede verse en enfermedades del tejido conectivo, como el síndrome de Ehler-Danlos, y en enfermedades carenciales como el escorbuto. Púrpura por alteración estructural de los vasos sanguíneos37 La alteración estructural de los vasos sanguíneos secundaria a la edad, al daño actínico crónico o a fármacos como los corticoides puede condicionar el desarrollo de áreas equi29 Figura 13. Púrpura senil. FMC-Formación Médica Continuada en Atención Primaria 223 Volumen 8, Número 4, Abril 2001 Miscelánea Púrpuras secundarias a enfermedades sistémicas1 Diversas enfermedades sistémicas, como la insuficiencia renal, diabetes, hepatopatías, hemocromatosis, carcinomatosis, malnutrición o afecciones endocrinológicas, pueden cursar con púrpura por mecanismos diversos y con frecuencia no bien conocidos. En la amiloidosis, el desarrollo de placas purpúricas en la cara interna de los párpados representa una imagen clínica típica que puede ayudar al diagnóstico (fig. 14). En esta enfermedad, el origen de la púrpura puede deberse a enfermedad hepática, a alteraciones plaquetarias o al depósito del amiloide en los capilares. El desarrollo de petequias o de placas purpúricas distales acompañadas de livedo reticular constituye un signo característico de la enfermedad por émbolos de colesterol (fig. 15). Esta grave complicación debe sospecharse en pacientes con factores de riesgo para aterosclerosis que presenten las citadas manifestaciones clínicas, en particular tras el antecedente de un proceso invasivo intravascular diagnóstico o terapéutico (p. ej., una arteriografía). Púrpura secundaria a procesos infecciosos38-45 La púrpura se incluye en el amplio abanico de manifestaciones cutáneas asociadas a procesos infecciosos (tabla 6). En estos casos, los mecanismos patogénicos implicados pueden ser variados e incluyen la invasión directa del endotelio, vasculitis por hipersensibilidad, púrpura trombopénica, embolización séptica o lesión del endotelio mediada por toxinas liberadas por los organismos infecciosos. En la meningococia, las lesiones cutáneas son el signo de presentación entre el 70 y el 90% de los casos. En el 50% se trata de un exantema purpúrico o petequial, mientras que la purpura fulminans ocurrirá en unos pocos casos. La meningococia crónica también puede dar lugar a pápulas o nódulos de características purpúricas. En la escarlatina, el desarrollo de líneas petequiales sobre las zonas de flexión constituye uno de los signos característicos de la enfermedad (signo de Pastia). Las sepsis bacterianas, en especial las mediadas por microorganismos gramnegativos, pueden ser también causa de purpura fulminans. Las lesiones purpúricas en las endocarditis bacterianas pueden ser secundarias a fenómenos embólicos o a vasculitis mediadas por inmunocomplejos. La ectima gangrenosa es una manifestación cutánea secundaria a la sepsis por Pseudomonas aeruginosa, que co- TABLA 6. Principales agentes infecciosos descritos en asociación a púrpura Figura 14. Amiloidosis sistémica. Bacterianos Neisseria meningitidis N. gonorrhoeae Haemophilus influenzae Staphylococcus aureus Escherichia coli Streptococcus pyogenes Streptococcus pneumoniae Pseudomonas aeruginosa Rickettsia spp. Mycoplasma pneumonia Salmonella spp. Shigella spp. Legionella spp. Brucella spp. Virales Varicela zoster Coxsackie virus Echovirus Rotavirus Hepatitis A, B, C Citomegalovirus Virus de Epstein-Barr Sarampión Parvovirus B19 Hongos Candida spp. Mucor spp. Aspergillus spp. Cryptococcus spp. Figura 15. Enfermedad por émbolos de colesterol. 224 FMC-Formación Médica Continuada en Atención Primaria Parásitos Strongyloides stercoralis Acanthamoeba spp. 30 J.M. Carrascosa y C. Ferrándiz.– Púrpura TABLA 7. Diagnóstico diferencial en la púrpura neonatal Eritropoyesis extramedular Defectos en los factores de la coagulación Déficit de proteínas C y S (purpura fulminans neonatal) Enfermedad hemorrágica del recién nacido Alteraciones plaquetarias Destrucción autoinmune de plaquetas (trombocitopenia neonatal aloinmune, trombocitopenia autoinmune materna, trombocitopenia por fármacos) Figura 16. Síndrome de las pápulas purpúricas en guante y calcetín. Defectos primarios en la producción o función plaquetaria (trombocitopenia por ausencia de radio, síndrome de Wiskott-Aldrich, anemia de Fanconi, trombocitopenia congénita amegacariocítica, trombocitopenia recesiva ligada al X, síndromes de las plaquetas gigantes, trisomía 13 o 18, síndrome de Alport, tromboastenia de Glanzmann, síndrome de Hermansky-Pudlak) Síndrome de Kasabach-Merrit Infecciones Congénitas (TORCH)* Sepsis Virus de la inmunodeficiencia humana Parvovirus B19 Traumatismo *T: toxoplasmosis; R: rubéola; C: citomegalovirus; H: herpes simple tipos I y II. Figura 17. Síndrome de las pápulas purpúricas en guante y calcetín. mienza en forma de una mácula eritematosa y asintomática que evoluciona hasta dar lugar a una úlcera centrada por una escara necrótica. Algunas infecciones virales incluyen dentro de su espectro clínico erupciones purpúricas, en la mayoría de los casos de características inespecíficas. Una excepción a esto sería el síndrome de las pápulas purpúricas en guantes y calcetín, proceso definido por un exantema petequial pruriginoso en manos y pies limitado proximalmente casi en su totalidad por muñecas y tobillos, y descrito en asociación a la infección por Parvovirus B19, citomegalovirus, sarampión, hepatitis B o virus Coxsackie (figs. 16 y 17). Púrpura en el recién nacido46-49 La púrpura en el neonato es una situación de urgencia que debería alertar al médico acerca de la posible existencia de una enfermedad grave subyacente. Aunque buena parte de las causas de púrpura se superponen a las descritas en los distintos apartados previos, existen algunas peculiaridades que deben tenerse en cuenta (tabla 7). En la evaluación de la púrpura neonatal, resulta impor31 tante obtener información sobre las enfermedades maternas, ingestión de fármacos, historia familiar de hemorragias, evolución de los embarazos previos y administración profiláctica o no de vitamina K. Además, debe llevarse siempre a cabo una exploración pormenorizada en busca de alteraciones congénitas, organomegalias o alteraciones de la temperatura, siendo asimismo necesario adoptar las medidas diagnósticas adecuadas para descartar una sepsis. La enfermedad hemorrágica del recién nacido es un término utilizado para referirse a cualquier hemorragia neonatal atribuible al descenso de los valores de los factores II, VII, IX y X por déficit de vitamina K. El neonato afectado presentará áreas equimóticas con hemorragias umbilicales, gastrointestinales, genitourinarias y del sistema nervioso central. La administración profiláctica de vitamina K a la madre permite prevenir el cuadro. Las púrpuras trombocitopénicas congénitas pueden ocurrir en el contexto de infecciones (p. ej., rubéola, citomegalovirus, toxoplasmosis), o por el paso de anticuerpos antiplaquetarios a través de la placenta en madres afectadas de púrpura trombopénica idiopática, trombopenia mediada por fármacos o en casos de incompatibilidad inmunológica maternofetal. Otras causas congénitas de trombopenia neonatal aparecen expuestas en la tabla 6. FMC-Formación Médica Continuada en Atención Primaria 225 Volumen 8, Número 4, Abril 2001 Petequias Áreas equimóticas Púrpura inflamatoria Solicitar Recuento plaquetario Tiempo de protrombina (TP) Tiempo parcial de tromboplastina activada (TPTA) Tiempo de sangría (TS) Sin alteraciones Púrpura por aumento de la presión intravascular Púrpura por alteración estructural de los vasos TS alargado Resto normal Trombocitopatías (alteración en el funcionalismo de las plaquetas) No palpable Palpable Angiocapilaritis Vasculitis cutánea de pequeño vaso Biopsia cutánea (opcional) Véase tabla 5 TP alargado TS alargado Alteraciones de los factores II, V, VII, X, y fibrógeno por ejemplo Insuficiencia hepática Déficit de vitamina K Anticoagulantes orales Síndrome de autosensibiliza- Otras determinaciones ción eritrocitaria Estudios de adhesión plaquetaria Determinación del tamaño plaquetario Estudios supervivencia plaquetaria TP alargado TPTA alargado Coagulación intravascular diseminada TP alargado Plaquetopenia Alteración de los factores VIII, IX, XI XII, II, V, X Púrpura trombocitopénica idiopática Púrpura trombocitopénica secundaria Otras determinaciones Fibrinógeno Factores V y VIII Dímero D Otras determinaciones Test de Coombs Anticuerpos antinucleares Estudios de vida plaquetaria Estudio del volumen plaquetario Estudio de médula ósea Anticuerpos plaquetarios Figura 18. Algoritmo diagnóstico de la púrpura cutánea en función de las características clínicas de las lesiones. Síndrome de autosensibilización eritrocitaria50 Es una entidad clínica infrecuente, caracterizada por el desarrollo de lesiones dolorosas, eritematosas y purpúricas desarrolladas de forma predominante en las piernas y que se atribuyen a un mecanismo de hipersensibilidad frente al ADN del individuo o frente a antígenos eritrocitarios. Se trata de un cuadro propio de adultos jóvenes y de mujeres de mediana edad en quienes destacan casi siempre antecedentes psiquiátricos. 226 FMC-Formación Médica Continuada en Atención Primaria En definitiva, la púrpura es un signo cutáneo inespecífico que puede corresponderse con un número variado de entidades, algunas de ellas muy graves (tabla 8). Para el diagnóstico de cada uno de estos procesos, resulta fundamental la evaluación de las características clínicas de las lesiones, la cual orientará acerca de las exploraciones complementarias pertinentes en función de la sospecha diagnóstica (fig. 18)51,52. En la tabla 9 se describen aquellos signos que obligan a una valoración urgente en pacientes con púrpura cutánea. 32 33 Petequias y/o equimosis Livedo reticular, acrocianosis, eritromelalgia, gangrena Extensas sufusiones hemorrágicas y hemorragias profusas tras pequeños traumatismos Trombocitosis Hemofilias Erupción asintomática o discretamente pruriginosa constituida por máculas milimétricas confluentes en placas de coloración eritematoanaranjada Aparición de áreas equimóticas en zonas expuestas tras pequeños traumatismos Angiocapilaritis Púrpura por alteración estructural de los vasos No No No Exantema petequial pruriginoso en manos y pies limitado por muñecas y tobillos en el contexto de proceso febril No Petequias en labios, párpados y cuello tras maniobras de Valsalva Petequias lineales coincidiendo con área de presión Petequias en extremidades inferiores coincidiendo con estasis venosa Púrpura por aumento de la presión intravascular Sí, urgente en función de la presentación clínica Síndrome de las pápulas purpúricas en guante y calcetín Púrpura palpable en forma de pápulas y/o placas distribuidas de manera bilateral y simétrica; con menor frecuencia placas urticariales, ampollas hemorrágicas, úlceras, nódulos o livedo reticular Afección visceral por la vasculitis (20-50%): artritisartralgias, hemorragia digestiva, dolor abdominal, hematuria, parestesias, etc. Vasculitis cutánea de pequeño vaso Sí, urgente Sí, urgente Petequias y áreas equimóticas en las formas leves Aparición súbita de áreas equimóticas en el tercio distal de las extremidades y zonas de presión con tendencia a la necrosis central y a la formación de ampollas en las formas graves Hemorragias viscerales (gastrointestinales, genitourinarias, etc.) Coagulación intravascular diseminada Sí, urgente Sí, urgente en función de la presentación clínica Sí Sí, urgente en función de la presentación clínica Su sospecha requiere derivación Enfermedad por émbolos de colesterol Petequias o placas purpúricas distales acompañadas de livedo reticular en pacientes con aterosclerosis tras proceso invasivo endovascular Exantema purpúrico o petequial, en ocasiones acompañado de pápulas o nódulos inflamatorios en el contexto de signos y síntomas sépticos Púrpura en el contexto de sepsis bacterianas Hemorragia visceral frecuente (hemartrosis, hematuria, hemorragia digestiva, etc.) Petequias y, en menor medida, equimosis espontáneas Ampollas hemorrágicas en mucosas (forma aguda) Sangrado visceral (sistema nervioso central, renal, ginecológico) Clínica Púrpura trombocitopénica idiopática Entidad Tratamiento No requiere Descoagulación Tratamiento del estado general No requiere Antihistamínicos orales, corticoides tópicos, venotónicos hemorreológicos No requiere En casos graves con afección multiorgánica: metotrexato, azatioprina, ciclosporina A, ciclofosfamida, etc. Reposo, colquicina, sulfona, corticoides orales Tratamiento del agente desencadenante Tratamiento del shock Perfusión de plaquetas, fibrinógeno y plasma fresco, reposición de proteína C; heparina (casos seleccionados), antifibrinolíticos sintéticos, antitrombina III, fármacos antifuncionalismo plaquetario Tratamiento antibiótico según germen Tratamiento del estado general Administración de crioprecipitados de factor VIII o IX, concentrados de factor VIII, factor VIII recombinante; desmopresina Antifibrinolíticos en profilaxis y tratamiento de complicaciones Abstención terapéutica antiagregantes, hidroxiurea, interferón, 32P Formas agudas: conducta expectante, corticoides, inmunoglobulinas Formas crónicas: esplenectomía, glucocorticoides, inmunoglobulinas, danazol TABLA 8. Manifestaciones clínicas, tratamiento y criterios de derivación de algunas de las entidades asociadas con púrpura cutánea J.M. Carrascosa y C. Ferrándiz.– Púrpura FMC-Formación Médica Continuada en Atención Primaria 227 Volumen 8, Número 4, Abril 2001 TABLA 9. Signos que obligan a una valoración urgente en pacientes con púrpura cutánea Púrpura en la edad neonatal Presencia de extensas áreas equimóticas Hemorragias en mucosas Signos directos –hematuria, hematemesis, hemoptisis– o indirectos –hipotensión, anemia, taquicardia, shock, etc.– de hemorragia visceral Signos o síntomas de septicemia Signos o síntomas de afección extracutánea en púrpura palpable Púrpura acral acompañada de livedo reticular tras el antecedente de un proceso invasivo intravascular (enfermedad por émbolos de colesterol) Bibliografía 1. Dowd PM, Champion RH. En: Champion RH, Burton DL, Burns DA, Breathnach SM, editores. Textbook of Dermatology (6.a ed.). Milán: Blackwell Science, 1998; 2141-2154. 2. Macro M, Boutard P, Leporrier M. Purpura thrombopenique auto-immune. Modalites therapeutiques. Presse Med 1997; 26: 439-443. 3. Sutor AH, Gaedicke G. Acute autoimmune thrombocytopenia. Baillieres Clin Haematol 1988; 11: 381-389. 4. Winiarski J. Mechanisms in childhood idiopathic thrombocytopenic purpura (ITP). Acta Paediatr Suppl 1998; 424: 54-56. 5. Porcelijn L, Von dem Borne AE. Immune-mediated thrombocytopenias: basic and immunological aspects. Baillieres Clin Haematol 1998; 11: 331-341. 6. Castillo Cofiño R, Ordinas Bauza A, Reverter Calatayud JC, Vicente García V, Roche Hernando E. Enfermedades de la hemostasia. En: Farreras P, Rozman C, editores. Medicina interna (13.a ed.). Barcelona: Mosby-Doyma, 1995; 1770-1880. 7. Esterly NB. Kasabach-Merritt syndrome. J Am Acad Dermatol 1983; 8: 504-513. 8. Maceyko RF, Camisa C. Kasabach-Merritt syndrome. Pediatr Dermatol 1991; 8: 133-136. 9. Ridolfi RL, Bell WR. Thrombotic thrombocytopenic purpura. Review of 25 cases and review of the literature. Medicine (Baltimore) 1981; 60: 413-428. 10. Schachne JP, Glasser N, Lee S, Kress Y, Fisher M. Hermansky-Pudlak syndrome: case report and clinicopathological review. J Am Acad Dermatol 1990; 22: 926-932. 11. Hardisty RM. Platelet disorders. En: Hoffbrand AV, Lewis SM, editores. Postgraduate haematology (3.a ed.). Oxford: Heinemann, 1989; 598626. 12. Debourdeau P, Zammit C, Souleau B, Vedrine L, Farge-Bancel D. Traitment des microangiopathies thrombotiques. Ann Med Interne 1999; 150: 374-387. 13. Amblard P, Lèques B, Seigneurin D. Manifestations cutanées des thrombocytémies. Ann Derm Vénéréol 1977; 104: 115-120. 14. Buchanan GR. Hemofilias. Clin Med N Am (ed. esp.) 1980; 21: 313-331. 15. Auletta MJ, Headington JT. Purpura fulminans. A cutaneous manifestation of severe protein C deficiency. Arch Dermatol 1988; 124: 1387-1391. 16. Baglin T. Disseminated intravascular coagulation: diagnosis and treatment. Br J Med 1996; 312: 683-687. 17. Amstutz P, Moyo JS. Les coagulations intra-vasculaires diseminees. Cah Anestesiol 1996; 44: 219-228. 18. Darmstadt GL. Acute infectious purpura fulminans: pathogenesis and medical management. Pediatr Dermatol 1998; 15: 169-183. Puntos clave • La esplenectomía continúa considerándose el tratamiento de elección en la púrpura trombocitopénica idiopática crónica. • No está bien establecido si el empleo de corticoides o inmunoglobulinas administrados por vía intravenosa mejora el pronóstico en las formas agudas de púrpura trombocitopénica idiopática. • La trombocitosis puede ser, de forma aparentemente paradójica, causa de hemorragia cuando el número de plaquetas supera la cifra de 1.000 × 109/ l. • La púrpura trombótica trombocitopénica y el síndrome hemolítico urémico se consideran en la actualidad distintas expresiones de un mismo proceso caracterizado por la formación de trombos en la microvasculatura. • Aunque el pronóstico de la purpura fulminans debe considerarse invariablemente grave, la aplicación de medidas terapéuticas de forma temprana permite reducir la mortalidad a un 20-35% de los casos. • Se ha afirmado que el déficit congénito o adquirido de proteínas S y C representaría un factor de riesgo para el desarrollo de coagulación intravascular diseminada. • En las vasculitis cutáneas de pequeño vaso, cuya manifestación clínica más característica es la púrpura • • • 228 palpable, debe investigarse la extensión y gravedad de la afectación extracutánea y los factores desencadenantes o procesos subyacentes. Se considera que puede encontrarse un factor causal subyacente o desencadenante en el 30-70% del total de casos de vasculitis cutáneas de pequeño vaso. La mayoría de las dermatosis purpúricas pigmentarias son muy resistentes al tratamiento habiéndose intentado, con éxito en casos aislados, los corticoides tópicos, la PUVA-terapia, la ciclosporina o la griseofulvina. La púrpura en el neonato es una situación de urgencia que debería alertar al médico acerca de la posible existencia de una enfermedad grave subyacente. FMC-Formación Médica Continuada en Atención Primaria 34 J.M. Carrascosa y C. Ferrándiz.– Púrpura 19. Lotti T, Ghersetich I, Comacchi C, Jorizzo JL. Cutaneous small-vessel vasculitis. J Am Acad Dermatol 1998; 39: 667-686. 20. Sneller MC, Fauci AS. Pathogenesis of vasculitis syndromes. Adv Rheumatol 1997; 81: 221-242. 21. Lotti T, Comacchi C, Ghersetich I. Cutaneous necrotizing vasculitis. Int J Dermatol 1996; 35: 457-474. 22. Gammon R. Leucocytoclastic vasculitis. Clin Rheumatic Dis 1982; 8: 397-413. 23. Callen JP. Cutaneous vasculitis: What have we learned in the past 20 years? Arch Dermatol 1998; 134: 355-357. 24. Ekenstam E, Callen JP. Cutaneous leukocytoclastic vasculitis. Clinical and laboratory features of 82 patients seen in private practice. Arch Dermatol 1984; 120: 484-488. 25. Sánchez NP, Harriet MVH, Daniel Su WP. Clinical and histopathologic spectrum of necrotizing vasculitis. Arch Dermatol 1985; 121: 220-224. 26. Carrascosa JM. Placas purpúricas, artralgias y dolor abdominal en un varón de 54 años. Rev Esp Reumatol 1996; 23: 311-313. 36. Alcalay JA, Ingber A, Sandbank M. Mask phenomenon: postemesis facial purpura. Cutis 1986; 38: 28. 37. Feinstein RJ, Halprin KM, Penneys NS, Taylor JR, Schenkman J. Senile purpura. Arch Dermatol 1973; 108: 229-232. 38. Shneiderman P. The vascular purpuras. En: Beuler E, Lichtman MA, Coller BS, Kipps TJ, editores. Williams Hematology (5.a ed.). Nueva York: McGraw-Hill, 1995; 1402-1412. 39. Kingston ME, Mackey D. Skin clues in the diagnosis of life-threatening infections. Rev Infect Dis 1986; 8: 1-11. 40. Marzouk O, Thomson APJ, Sills JA, Hart CA, Harris F. Features and outcome in meningococcal disease presenting with maculopapular rash. Arch Dis Child 1991; 66: 485-487. 41. Goldenhersh MA. Petechiae caused by streptococcal pharyngitis. J Am Acad Dermatol 1992; 27: 456-457. 42. Harms M, Feldmann R, Saurat JH. Papular-purpuric “gloves and socks” syndrome. J Am Acad Dermatol 1990; 23: 850-854. 27. Jeanette ChJ, Milling DM, Falk RJ. Vasculitis affectin the skin. A review. Arch Dermatol 1994; 130: 899-906. 43. Carrascosa JM, Bielsa I, Ribera M, Ferrándiz C. Papular-purpuric gloves-and-socks syndrome related to cytomegalovirus infection. Dermatology 1995; 19: 269-270. 28. Sais G, Vidaller A, Jucglà A, Servitje O, Condom E, Peyrí J. Prognostic factors in leukocytoclastic vasculitis. A clinicopathologic study in 160 patients. Arch Dermatol 1998; 134: 309-315. 44. Pérez-Ferriols A, Martínez-Aparicio A, Aliaga-Boniche A. Papularpurpuric “gloves and socks” syndrome caused by measles virus. J Am Acad Dermatol 1994; 30: 291-292. 29. Carrascosa JM. Vasculitis necrosantes cutáneas: consideraciones conceptuales y patogenéticas. Piel 1998; 13: 163-169. 45. Feldmann R, Harms M, Saurat JH. Papular-purpuric “gloves and socks” syndrome: not only parvovirus B19. Dermatology 1994; 188: 85-87. 30. Bielsa I, Carrascosa JM, Hausmann G, Ferrándiz C. An immunohistopathologic study in cutaneous necrotizing vasculitis. J Cutan Pathol 2000; 27: 130-135. 31. Ratnam KV, Su WP, Peters MS. Purpura simplex (inflammatory purpura without vasculitis): a clinicopathologic study of 174 cases. J Am Acad Dermatol 1991; 25: 642-647. 32. Ghersetich I, Lotti T, Bacci S, Comacchi C, Campanile G, Romagnoli P. Cell infiltrate in progressive pigmented purpura (Schamberg’s disease): immunophenotype, adhesion receptors, and intercellular relationships. Int J Dermatol 1995; 34: 846-850. 46. Baselga E, Drolet BA, Esterly NB. Purpura in infants and children. J Am Acad Dermatol 1997; 37: 673-705. 47. Skacel PO, Contreras M. Neonatal alloimmune thrombocytopenia. Blood Rev 1989; 3: 174-179. 48. Juif JG, Stoll C, Korn R. Thrombopenie hypoplasique congénitale avec aplasie du radius. Arch Fr Pediatr 1972; 29: 513-526. 49. Omerod AD. The Wiskott-Aldrich syndrome. Int J Dermatol 1985; 24: 77-81. 33. Wong WK, Ratnem KV. A report of two cases of pigmented purpuric dermatosis treated with PUVAtherapy. Acta Derm Venereol (Stock) 1991;71: 68-70. 50. Berman DA, Roenigk HH, Green D. Autoerythrocyte sensitization syndrome (Psycogenic purpura). J Am Acad Dermatol 1992; 27: 829832. 34. Okada K, Ishikawa O, Miyachi Y. Purpura pigmentosa chronica succesfully treated with oral cyclosporin A. Br J Dermatol 1995; 134: 180-181. 51. Lusher JM. Screening and diagnosis of coagulation disorders. Am J Obstet Gynecol 1996; 175: 778-783. 35. Tamaki K, Yasaka N, Osada A, Shibagaki U, Furue M. Succesfully treatment of pigmented purpuric dermatosis with griseofulvin. Br J Dermatol 1995; 132: 159-160. 52. Bader-Meunier B, Dreyfus M. Exploration des troubles de l’hémostase de l´enfant (en dehors de la période néonatale). Arch Pédiatr 1999; 6: 1086-1091. 35 FMC-Formación Médica Continuada en Atención Primaria 229