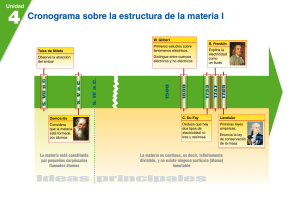
17/03/2020 HISTORIA DE LOS MODELOS ATOMICOS PROFESORA: Paula Cufré FECHA DE ENTREGA: 25/ 03/2020 Observa los videos, atomistas griegos (https://www.youtube.com/watch?v=st1in9yXOyQ )y modelos atómicos(https://www.youtube.com/watch?v=TlDDLA6RlRE) (https://www.youtube.com/watch?v=wiePxx847Wo) y luego responde: 1) ¿Qué ocurriría si dividiéramos un trozo de materia muchas veces? ¿llegaríamos hasta una parte indivisible o podríamos seguir dividiendo indefinidamente? 2) Explica con tus palabras que significa “atomismo”. 3) ¿Cómo describe Demócrito al átomo? 4) Las siguientes ilustraciones corresponden a modelos de Thomson (1898) y Rutherford (1911). MODELO ATOMICO THOMSON MODELO ATOMICO DE RUTHERFOTD a) Investiga en internet, en que experiencias se basaron Thomson y Rutherford para postular estos modelos? b) ¿Qué partículas descubrieron ambos científicos? c) Si el modelo atómico de Thomson se parece a un budín de pasas de uvas, ¿qué representa el budín y las pasas? d) ¿A que otro modelo te recuerda el modelo atómico de Rutherford? ¿Por qué? e) ¿En qué se parecen y en qué se diferencian el modelo de Thomson y el de Rutherford? f) Teniendo en cuenta la evolución de los modelos atómicos, ¿cuál es tu opinión sobre los modelos científicos? ¿son inamovibles o se reformulan a la luz de nuevos descubrimientos? 5) En 1913, Niels Bohr, discípulo de Rutherford, mejoró el modelo atómico: propuso que los electrones se encuentran distribuidos en diferentes niveles energéticos. Representa la ubicación por niveles de los electrones de los siguientes átomos. Considera el núcleo como una pequeña esfera y las orbitas circulares. Para tener en cuenta: cada orbita o nivel de energía (n) admite un número máximo de electrones: n1=2, n2=8, n3=18, n4=32. Litio = 3 Oxigeno = 6 Sodio = 11 Bromo = 35 6) Explica la diferencia fundamental entre el modelo atómico de Rutherford y el de Bohr. 7) ¿Cómo creen que el desarrollo de la tecnología contribuye al desarrollo del conocimiento científico?