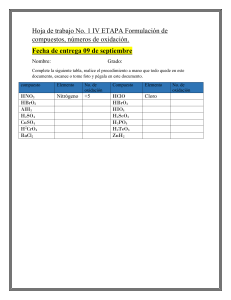
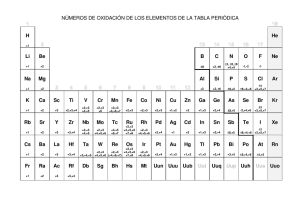
Reglas para calcular los números de oxidación. Nava Rios Alexa Guadalupe El número de oxidación de un elemento libre es cero Familia 1 siempre trabaja con 1+, familia 2 siempre con 2+ En los iones de un único átomo, el estado de oxidación o número de oxidación de dicho átomo coincide con la carga del ión. Ej: Li+ Ca+2 El número de oxidación del flúor, es siempre -1 El número de oxidación del aluminio, es siempre 3+ El número de oxidación del oxígeno es siempre -2, excepto cuando: o Cuando se combina con F, entonces su número de oxidación será +2 o Cuando el O, está formando un peróxido, donde su número de oxidación es -1 El número de oxidación del hidrógeno es siempre +1, excepto en los hidruros metálicos que es -1 Algunos elementos tienen distinto estado de oxidación en función del compuesto que están formando La suma algebraica de los números de oxidación de los elementos de un compuesto ha de ser igual a su carga: si es un compuesto neutro, la suma algebraica deberá ser igual a 0. Si es un catión o un anión será igual a la carga del ión, Ej: en el caso del anión ClO3- la suma algebraica de los números de oxidación deberá ser -1. Aquí el oxígeno tiene estado de oxidación -2, por lo que (-2)·3 = -6. De este modo, para que la suma algebraica sea -1, el estado de oxidación del cloro ha de ser +5. Bibliografía: Reglas de determinación del número de oxidación [Internet]. Quimitube.com. 2012 [citado el 4 de septiembre de 2021]. Disponible en: https://www.quimitube.com/teoriaredox/normas-determinacion-numero-oxidacion/ de Sonora IT. REGLAS PARA ASIGNAR NÚMEROS DE OXIDACIÓN [Internet]. Slideshare.net. [citado el 4 de septiembre de 2021]. Disponible en: https://es.slideshare.net/tango67/reglas-para-asignar-nmeros-de-oxidacin