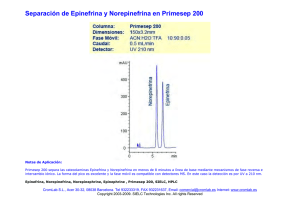
Efecto de la epinefrina en concentraciones fisiológicas sobre los factores de virulencia de Mannheimia haemolytica. Rosales Resendiz Michelle Tutor: Erasmo Negrete Abascal La familia Pasteurellaceae alberga a un amplio grupo de bacterias relacionadas con enfermedades económicamente importantes para la industria ganadera, causantes de infecciones zoonóticas en humanos. Los organismos colonizan principalmente las membranas mucosas, Mannheimia haemolytica (Mh) ha sido aislada del tejido que compone el tracto respiratorio superior, orofaringe, tracto reproductivo y, en ocasiones, de partes del tracto intestinal de un amplio grupo de especies. 6, 13, 29 Mh es una bacteria patógena anteriormente nombrada como Pasteurella haemolytica. y agrupada en el género Mannheimia; incluye a los serotipos A 1, 2, 5-9, 12-14, 16 y 27, aislados únicamente de rumiantes. Morfológicamente se identifica a Mh como un cocobacilo Gram negativo, no móvil, encapsulado que forma colonias lisas de color blanco grisaceo de 1-2 mm de diametro después de incubación en medio TSB. Es mesófila, de metabolismo aerobio o anaerobio facultativo, oxidasa positiva e indol negativa, de igual manera es negativa para pruebas de rojo metilo, gelatinasa y Voges-Proskauer. Crece en agar McConkey y en medios enriquecidos como agar chocolate o agar sangre, produciendo beta hemólisis (agar sangre de bovino), y es parcialmente resistente a la fagocitosis debido a las propiedades de su cápsula. 2, 7, 20. Mh está estrechamente relacionado con las infecciones del tracto respiratorio de bovinos y ovinos, se considera un habitante común de las criptas amigdalinas de ganado sano que en situaciones de estrés se multiplica e invade el tejido pulmonar durante la inhalación, provocando infección activa en el epitelio alveolar. De igual forma se relaciona con procesos neumónicos, septicémicos y de mastitis. Suele afectar a animales menores de un año recién transportados y, con mayor incidencia, a becerros de 1 a 5 meses de edad; aunque también puede ser aislada de organismos sanos. En la industria ganadera, las enfermedades respiratorias son la causa principal de morbilidad, mortalidad y de pérdidas de ganado vacuno destinado al consumo. 3, 22, 23, 27, 32. En Mh se han reportado toxinas relacionadas directamente con la especificidad con su hospedero así como con sus factores de virulencia sobre el mismo. Las leucotoxinas (Lkt) son un grupo de exotoxinas cuyo efecto primario se ejerce contra los leucocitos, específicamente sobre células polimorfonucleares. Estas proteínas provocan un amplio rango de efectos secundarios sobre los leucocitos, su producción se ha relacionado directamente con el crecimiento de Mh en infecciones pulmonares, así mismo, se ha evidenciado que la actividad citotóxica del extracto de Mh fue mayor en leucocitos y plaquetas de rumiantes que en caballos, cerdos y humanos.12-14, 27, 35. La epinefrina, comúnmente conocida como adrenalina, es un neurotransmisor perteneciente al grupo de las catecolaminas de interés clínico. Estos compuestos están formados por un grupo catecol (orto-dihidroxibenceno) y una cadena lateral con un grupo amino, se sintetizan en la médula adrenal de las glándulas suprarrenales y son liberadas directamente al torrente sanguíneo. Se caracterizan por sus funciones en la regulación de procesos fisiológicos al estimular los receptores adrenérgicos de las células receptoras. En el sistema respiratorio, la epinefrina mediante los receptores β2 adrenérgicos produce efectos broncodilatadores y reduce las secreciones bronquiales (efecto α-adrenérgico).9, 31. En 2018, Pillai et al. desarrollaron un modelo in-vitro de la biopelícula formada por Mh bajo el efecto de compuestos estresantes: epinefrina (E), norepinefrina (NE) y sustancia P (SP), donde E tuvo la mayor efecto en la dispersión de la biopelícula, seguido de NE y SP. Ellos concluyen que este modelo, aplicado in-vivo, implicaría a estos agentes como coadyuvantes en las primeras etapas de la neumonía causada por Mh. Betancourt (2020) determinó el impacto de E y NE en el crecimiento poblacional, la expresión de proteínas, la actividad proteolítica y la formación de biopelículas de Actinobacillus seminis. En su trabajo se reporta que, aunque las catecolaminas utilizadas no indujeron cambios significativos en el crecimiento de A. seminis, existen cambios en los patrones de proteínas, zimogramas e inmuno reconocimientos, así como un aumento en la dispersión de biopelículas. Se ha estudiado ampliamente el efecto de las hormonas en miembros de la familia Pasteurellaceae. Al estar relacionado con enfermedades económicamente importantes para la industria ganadera, es importante estudiar los factores que afectan la virulencia de Mh, como lo es la epinefrina. OBJETIVO GENERAL ● Determinar el efecto de la Epinefrina sobre el crecimiento y la expresión proteíca de Mannheimia haemolytica. OBJETIVOS PARTICULARES ● Determinar el efecto de la epinefrina sobre el crecimiento de M. haemolytica. ● Determinar los patrones de proteínas totales y secretadas por Mannheimia haemolytica en presencia de epinefrina a diferentes concentraciones. ● Observar el efecto de los diferentes tratamientos de epinefrina sobre la actividad proteolítica de Mannheimia haemolytica. MATERIALES Y MÉTODOS. CRECIMIENTO BACTERIANO. La obtención de la cepa y el mantenimiento del cultivo se llevó a cabo de acuerdo a lo reportado por Mortes-García (2015) y Betancourt (2020), así como todas las técnicas reportadas. Para el crecimiento bacteriano se utilizó medio Infusión de Cerebro y Corazón (BHI), donde se realizó un pre-cultivo de la cepa de Mh (ATCC 31612) donada por el Dr. Edgar Zenteno (Facultad de Medicina, UNAM) en un tubo de ensayo con 3 ml de BHI y se dejó creciendo en agitación (150 rpm) a 37° C durante 24 horas. Posteriormente se sembró en agar sangre para su mantenimiento. CINÉTICA DE CRECIMIENTO. La determinación del efecto de los diferentes tratamientos de epinefrina en el crecimiento de Mh se realizó una cinética de crecimiento; se cultivó la cepa de Mh en 3 mL de caldo BHI, una alícuota de este cultivo se diluyó en 3 mL de caldo para llevarlo a una concentración del 10% y se incubó a 37 y 39 °C en agitación hasta alcanzar una densidad óptica de 0.1. En ese momento se añadirán 10, 20, 30, 40 y 50 ng/ml de E y como control se uso medio sin epinefrina. Se realizaron mediciones cada hora durante 6 h a 600 nm, la última medición fue leída a las 24 h. Se realizó prueba de pureza sobre placas de agar BHI y estas fueron incubadas a 37ºC durante 24 h.34 OBTENCIÓN DE PROTEÍNAS. Las proteínas totales y secretadas se obtuvieron mediante cultivos en 100 mL de medio con la cepa ATCC 31612. Una vez alcanzada la densidad óptica de 0.1 a 600 nm se agregaron 10, 20, 30, 40 y 50 ng/ml de E, estos cultivos se incubaron a 37 y 39 °C. Los cultivos se centrifugaron a 10500 rpm durante 25 minutos a 8°C, el sobrenadante de cultivo fue precipitado con 100 ml de etanol para recuperar las proteínas secretadas. La pastilla celular fue resuspendida con una solución de HEPES 10 mM pH 7.8 con lisozima (1 mg/mL) y se incubaron en agitación a 150 rpm a 37°C durante 1 hora, posteriormente las células se sonicaron 10 ciclos (15 segundos de sonicación por 10 segundos de descanso) en baño frío. Las muestras se centrifugaron a 13400 rpm durante 3 minutos para separar las células enteras, se recuperará el sobrenadante (proteínas totales). CUANTIFICACIÓN DE PROTEÍNAS Y ELECTROFORESIS. Para identificar los cambios en los patrones de proteínas inducidos por los diferentes tratamientos y su peso molecular relativo, se realizó una separación electroforética en geles de poliacrilamida con dodecil sulfato de sodio (SDS-PAGE) al 10%. Previo a ello se determinó la concentración de proteína por muestra por método de Bradford y se cargaron 10 μg de proteína por carril. Se corrieron a 90V durante 120 min y posterior a ello se tiñeron los geles con una solución de Azul de Coomassie (R-250 0.1%, metanol 40% y ácido acético 10%), se utilizó una solución de ácido acético al 10% para retirar el exceso de colorante.8, 16. ACTIVIDAD PROTEOLÍTICA. La actividad proteolítica se identificó mediante zimogramas en geles SDS-PAGE al 10% con 0.1% de gelatina porcina. Posterior a la separación electroforética, los geles de sustrato se incubaron en agitación durante 1 h en una solución de tritón X-100 al 2.5%. Enseguida, los geles fueron incubados en Tris 20 mM CaCl 210 mM toda la noche a 37 °C para activar las posibles proteasas que degradan el sustrato. Los geles fueron teñidos con azul de Coomassie y las actividades proteolíticas fueron observadas como zonas blancas contra un fondo azul.15, 28. WESTERN BLOT Cuando obtenemos la separación electroforética, se realizó una electrotransferencia a una membrana de nitrocelulosa. Ésta se bloqueó con leche al 5% en PBS-Tween20 al 0.5% y tras lavar la membrana con Buffer PBS-Tween-20, se adicionó como anticuerpo primario suero bovino agudo y agitó a 80 rpm durante dos horas a temperatura ambiente. Después, se recuperó el suero y se lavó la membrana, se adicionó suero α (anti) bovino como anticuerpo secundario y se dejó en agitación durante dos horas. Finalmente, se realizó un revelado químico de la membrana para su posterior análisis.25 CRECIMI M. haemolytica ATCC CINÉTIC BHI 3ml, alícuota de 10%. 37 y 39 °C OBTENC BHI 100 ml, 37 y 39 °C Control, 10, 20, 30, 40 y PROTEÍN EXTRAC Método Gel SDS- ELECTR Gel SDS- ZIMOGR WESTER Figura 1. Diagrama de metodología utilizada para la evaluación de los factores de virulencia de Mannheimia haemolytica. RESULTADOS Se evaluó el crecimiento y el patrón proteico de de Mh. incubada a 37°C bajo concentraciones fisiológicas de epinefrina (100, 200 y 500 pg) y en concentraciones mil (10, 20 y 50 ng) y un millón veces mayor (1, 10 y 20 μg) encontrando mayores una respuesta más significativa en concentraciones mil veces mayores a las fisiológicas (datos no mostrados). 10, 33, En la evaluación del crecimiento de Mh a 37 °C se observó que las concentraciones de 10, 20, 30, 40 y 50 ng/ml epinefrina no favorecen el crecimiento respecto al control (Gráfico 1); esto ocurre también en el crecimiento a 39 °C, únicamente en la concentración de 50 ng/ml de epinefrina el crecimiento se ve desfavorecido respecto al control (Gráfico 2). Gráfico 1. Cinética de crecimiento de Mannheimia haemolytica a 37°C en presencia de epinefrina (Control, 10, 20, 30, 40 y 50 ng/ml). Gráfico 2. Cinética de crecimiento de Mannheimia haemolytica a 39°C en presencia de epinefrina (Control, 10, 20, 30, 40 y 50 ng/ml). En el patrón de proteínas de extractos totales se pudieron observar cambios en la expresión de proteínas, principalmente en todas las muestras a las que se les añadieron diferentes volúmenes de epinefrina y que se incubaron a 39°C. En el gel se presentan cambios en las bandas en pesos aproximados de 24, 27, 60 y 75 kDa que no se aprecian visiblemente en el control. Así mismo, las bandas con tratamiento de epinefrina con peso molecular de 100 kDa se muestran con mayor intensidad respecto al control (Figura 2). No se apreciaron cambios trascendentes en los tratamientos incubados a 37°C. 25 15 0k 0k D 10 D 75 0k kD D 3 7° C 3 9° C 50 kD 37 kD 25 kD 20 kD con trol 10 20 ng/ ng/ ml ml SDS-Page 30 40 50 ng/ ng/ ng/ ml ml al 10%. Patrónmlde con trol 10 20 ng/ ng/ mltotales ml proteínas 30 40 50 ng/ ng/ ng/ ml ml ml de Mannheimia Figura 2. Gel haemolytica en presencia de epinefrina (10 - 50 ng/ml) De la igual forma, en el patrón de proteínas secretadas se presentaron cambios en la expresión de proteínas de ambos ensayos (37 y 39°C). En ambas temperaturas se pueden observar cambios en las bandas a un peso de 21 y 25 kDa en los volúmenes de 30 y 50 ng/ml de los ensayos a 37°C y en los volúmenes de 30, 40 y 50 ng/ml de epinefrina de los ensayos a 39°C; también a 39°C se puede observar que se presentan cambios en las bandas a un peso de 35 y 100 kDa en las muestras con epinefrina (Figura 3). 37 °C 39 °C 25 0 15 k 0 D k 10 D 0 75 k k D D 50 k D 37 k D 25 k D 20 k D Figura co 10 20 30 40 50 co 10 20 30 40 50 nt 3. Gel de proteínas secretadas por Mannheimia nt SDS-Page ng/ ng/al 10%. ng/ Patrón ng/ ng/ ng/ ng/ ng/ ng/ ng/ ro ml ng/ml) presencia de (10 ro haemolytica ml ml en ml ml mlepinefrina ml - 50 ml ml ml l l Se realizó un zimograma con sustrato de gelatina porcina para identificar la actividad proteolítica de las proteínas secretadas por Mh incubada a 37 y 39°C en presencia de epinefrina. En él se pudo observar alta actividad en el tratamiento de 10 ng/mL a 39°C distribuida en pesos moleculares de 50 a 80 kDa aproximadamente. De igual forma se presenta ligera actividad en los tratamientos de 30 y 40 kDa a 37°C en los pesos moleculares de 45 y >250 kDa (Figura 4). 25 15 0k 0k D 10 D 75 0k k D D 3 7 ° C 3 9 ° C 50 k D 37 k D 25 k D 20 k con 10 20 30 40 50 con 10 20 30 40 50 D Figura 4. Zimograma (Gel SDS-Page al 8%)ng/ de lasng/muestras trol ng/ con ng/ gelatina ng/ porcina ng/ ng/ trol ng/ ng/ ng/ de proteínas secretadas haemolyticamlen presencia epinefrina. ml mlpor Mannheimia ml ml ml ml ml de ml ml Por último, se realizó un western blot para confirmar la presencia de proteínas tipo proteasas dentro de las muestras, la inmunogenicidad se determinó usando suero de bovino agudo. Con ello se observó reconocimiento a 10, 55 (más intensa), 45, 40, 35, 27, 25, 23 (más débil) kDa en los tratamientos con epinefrina a 37 y 39°C (Figura 5). 25 15 0k 0k 10 D D 75 0k kD D 37 °C 39 °C 50 kD 37 kD 25 kD 20 kD Figura 5. con trol 10 20 30 40 50 con 10 20 30 40 ng/ ng/ ng/ ng/ ng/ trol ng/ ng/ ng/ ng/ Inmuno ml reconocimiento de ml proteínas ml ml de mllas muestras ml ml secretadas ml ml Mannheimia haemolytica en presencia de epinefrina. 50 ng/ por ml DISCUSIÓN Aunque actualmente se conoce mucho acerca de los factores de virulencia de Mh y cómo estos le ayudan a causar infecciones en rumiantes al pasar de hospedero de su microbiota a un importante patógeno, aún es poco explorado el comportamiento de estos factores frente a agentes estresantes, como lo es el aumento de la epinefrina.19 Mh es ampliamente estudiada por ser un organismo de alta importancia en la industria ganadera, pues se ha aíslado de ganado joven con cuadros de neumonía aguda; así mismo, en esta industria el ganado se somete a muchos procedimientos que alteran las concentraciones de hormonas relacionadas al estrés debido al impacto que la manufactura tiene sobre los animales, por ello es importante evaluar el comportamiento de Mh frente a estas variaciones. 11, 18, 26. Anteriormente se ha reportado un efecto positivo en el crecimiento de bacterias patógenas gram negativas inducida por las catecolaminas relacionadas al estrés que son secretadas por el sistema nervioso entérico, sin embargo, en este trabajo el crecimiento de Mh en presencia de epinefrina no se ve favorecido. Esto concuerda con lo reportado por Betancourt (2020), que tampoco observó efectos significativos en el crecimiento de Actinobacillus seminis en presencia de epinefrina y norepinefrina. Por otro lado, los factores de virulencia de Mh son otro aspecto importante a evaluar debido a su intervención en el proceso de infección. Las proteasas son productos secretados por las bacterias que pueden tener un papel importante en el proceso de patogénesis, su alcance como factor de virulencia reside en su capacidad para actuar como un factor tóxico que promueve la colonización en el hospedero.1, 30. La actividad proteolítica obtenida presentó pesos moleculares de 50 a 80 kDa a 39°C y 45 y >250 kDa a 37°C en presencia de epinefrina; las proteasas reportadas previamente para Mh se señalaron a pesos moleculares de 35.2 kDa y 64 kDa. 4,36 Esto podría indicar que se trata de proteasas similares, sin embargo, se recomienda identificar el tipo de proteasas a partir de inhibidores. Finalmente, la leucotoxina es el factor de virulencia más estudiado en Mh debido a su papel principal en la lisis de leucocitos y por tanto en la disminución de la capacidad inmunológica del animal. En la prueba de inmuno reconocimiento se pudo observar una intensa banda alrededor de 100 kDa, similar a la reportada por Morales-Álvarez (2004), esto sugiere que la leucotoxina se hace presente aun en presencia de epinefrina. CONCLUSIONES ➔ La epinefrina a en volúmenes de ng/mL no favorece el crecimiento de Mannheimia haemolytica. ➔ A una temperatura de 39°C se ve favorecida la expresión de proteínas en presencia de volúmenes de epinefrina de 10 a 50 ng/mL. ➔ Un volumen de epinefrina a 10 ng/mL favorece la producción de probables proteasas. ➔ A concentraciones de 10 a 50 ng/ml de epinefrina a 90 ng/mL se favorece la expresión de leucotoxina. ➔ La leucotoxina sigue presente aun en presencia de volúmenes de epinefrina en ng/mL a 37 y 39°C REFERENCIAS 1. Abdullah, K. M., Lo, R. Y., & Mellors, A. L. A. N. (1991). Cloning, nucleotide sequence, and expression of the Pasteurella haemolytica A1 glycoprotease gene. Journal of bacteriology, 173(18), 5597-5603. 2. Angen, O.; Mutters, R.; Caugant, D. A.; Olsen. J. E. y Bisgaard, M. 1999. Taxonomic relationships of the [Pasteurella] haemolytica complex as evaluated by DNA–DNA hybridizations and 16S rRNA sequencing with proposal of Mannheimia haemolytica gen. nov., comb. nov., Mannheimia granulomatis comb. nov., Mannheimia glucosida sp, nov., Mannheimia ruminalis sp, nov. and Mannheimia varigena sp, nov. International Journal of Systematic and Evolutionary Microbiology, 49(1): 67-86. 3. Angen, O.; Quirie, M.; Donachie, W. y Bisgaard, M. 2002. Investigations on the species specificity of Mannheimia (Pasteurella) haemolytica serotyping. Veterinary Microbiology, 65(4): 283-290. 4. Bernardino, S., Alanis, E., Morales Alvarez, J. F., Jaramillo Mesa, L., & Aguilar Romero, F. (1995). Evaluation of leukotoxin production from Pasteurella haemolytica strains, with different origin. Veterinaria Mexico (Mexico). 5. Betancourt, P. B. (2020). Efecto de epinefrina y norepinefrina en la expresión de proteínas de Actinobacillus seminis [Tesis de Licenciatura]. Facultad de Estudios Superiores Iztacala. Tlalnepantla Edo. de México. 6. Boyce, J. D.; Harper, M.; Wilkie I. W. y Adler, B. 2010. Pasteurella. Pathogenesis of Bacterial Infections in Animals, 4: 325-346. 7. Boyce, J.; Lo, R.; Wilkie, I. y Adler, B. 2004. Pasteurella and Mannheimia. Pathogenesis of bacterial infections in animals, ed Giles, C. L.; Prescott, J. F.; Songer, J. G.y Thoen, C. O., (Carlton, Australia: Blackwell Publishing), 273–294. 8. Bradford, M. M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding. Anal.Biochem.,72:248-254. 9. Brandan, N.; Llanos, I.; Ruiz, D. A. N. D. y Rodríguez, A. 2010. Hormonas catecolaminicas adrenales. Cátedra de Bioquímica Facultad de Medicina.[acceso: 4 de abril de 2015]. URL: http://med.unne.edu.ar/sitio/multimedia/imagenes/ckfinder/files/files/CarreraMedicina/BIOQUIMICA/catecolaminas.pdf 10. Burdick, N. C., Carroll, J. A., Randel, R. D., Willard, S. T., Vann, R. C., Chase Jr, C. C., ... & Welsh Jr, T. H. (2011). Influence of temperament and transportation on physiological and endocrinological parameters in bulls. Livestock Science, 139(3), 213-221. 11. Burdick, N. C., Randel, R. D., Carroll, J. A., & Welsh, T. H. (2011). Interactions between temperament, stress, and immune function in cattle. International Journal of Zoology, 2011. 12. Chang, Y. F.; Ma, D. P.; Shi, J. y Chengappa, M. M. 1993. Molecular characterization of a leukotoxin gene from a Pasteurella haemolytica-like organism, encoding a new member of the RTX toxin family. Infection and immunity, 61(5): 2089– 2095. 13. Christensen, H. y Bisgaard, M. 2008. Taxonomy and biodiversity of members of Pasteurellaceae. Pasteurellaceae: Biology, Genomics and Molecular Aspects. Caister Academic Press, 1-26. 14. Davies, R. L., y Baillie, S. 2003. Cytotoxic activity of Mannheimia haemolytica strains in relation to diversity of the leukotoxin structural gene lktA. Veterinary microbiology, 92(3): 263-279. 15. De la Cruz, M. A. H. (2015). Caracterización de proteasas de Actinobacillus seminis [Tesis de Licenciatura]. Facultad de Estudios Superiores Iztacala. Tlalnepantla Edo. de México. 16. Fredheim, E. G. A.; Klingenberg, C.; Rohde, H.; Frankenberger, S.; Gaustad, P.; Flægstad, T. y Sollid, J. E. 2009. Formación de biopelículas por Staphylococcus haemolyticus. Journal of Clinical Microbiology, 4(4):1172-1180. 17. Freestone, P. P., Haigh, R. D., & Lyte, M. (2007). Specificity of catecholamineinduced growth in Escherichia coli O157: H7, Salmonella enterica and Yersinia enterocolitica. FEMS microbiology letters, 269(2), 221-228. 18. Freestone, P. P., Williams, P. H., Haigh, R. D., Maggs, A. F., Neal, C. P., & Lyte, M. (2002). Growth stimulation of intestinal commensal Escherichia coli by catecholamines: a possible contributory factor in trauma-induced sepsis. Shock, 18(5), 465-470. 19. García Gomez, Elizabeth. (2004). Identificación y caracterización de proteasas secretadas por Mannheimia (pasteurella) haemolytica aislada de pollo [Tesis de Licenciatura]. Universidad Nacional Autónoma de México, México. 20. Jaramillo-Arango, C.; Trigo-Tavera, F. J. y Suárez-Güemes, F. 2009. Mannheimiosis bovina: etiología, prevención y control. México. Veterinaria, 40(3): 293-314. 21. Laemmli, U. K. 1970. Cleavage of structural proteins during the assembly of the head of bacteriophage T4. Nature, 227(5259): 680-685. 22. Lo, Ry. 2001. Genetic analysis of virulence factors of Mannheimia (Pasteurella) haemolytica A1. Veterinary microbiology, 83(1): 23-35. 23. Marshall, B. M. y Levy, S. B. 2011. Food Animals and Antimicrobials: Impacts on Human Health. Clinical microbiology reviews, 24(4): 718–733. 24. Miyoshi, S. I., & Shinoda, S. (2000). Microbial metalloproteases and pathogenesis. Microbes and infection, 2(1), 91-98. 25. Montes-García, J. F. (2015, enero). Identificación de proteínas amiloides expresadas por Mannheimia haemolytica. [Tesis de Maestría]. Facultad de Medicina Veterinaria y Zootecnia. D. F. México. 26. Morales Alvarez, José Francisco. (2004). Evaluación de mecanismos de patogenicidad de aislados de Mannheimia haemolytica A2 productores de neumonias en ovinos [Tesis de Doctorado]. Universidad Nacional Autónoma de México, México. 27. Narayanan, S.; Nagaraja, T.; Chengappa, M. y Stewart, G. 2002. Leukotoxins of gram-negative bacteria. Veterinary microbiology, 84(4): 337-356.