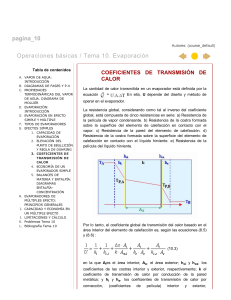
Coeficientes térmicos
Anuncio

PRÁCTICAS DE TERMODINÁMICA DETERMINACIÓN DE COEFICIENTES TÉRMICOS.− La variación de alguna de las variables de Estado de un sistema termodinámico influye en el resto de las variables de Estado. Los coeficientes térmicos del sistema nos indican dicha variación. Supongamos, para ello, un sistema de un componente y una sola fase. El volumen del sistema vendrá expresado en función de la presión y la temperatura mediante su ecuación térmica de estado : V = V(p,T) La variación que experimenta el volumen del sistema como consecuencia de la variación simultánea de presión y temperatura, la calculamos a partir de la expresión anterior, en forma diferencial : "V "V dV = _ dT + _ dp "TP "pT El cambio relativo de volumen será : dV 1 "V 1 "V _ = _ _ dT + _ _ dp V V "TP V "pT Al coeficiente de dT que representa la variación relativa de volumen en función de la temperatura en un proceso isobaro, se le denomina coeficiente de dilatación, y se representa mediante la letra : 1 "V =__ V "TP Al coeficiente de dp, cambiado de signo, que representa la variación relativa de volumen con respecto a la presión en un proceso isotermo, se le denomina coeficiente de compresibilidad isoterma y se representa con letra K : 1 "V k=−__ V "pT Por analogía con los anteriores definimos el coeficiente piezotérmico, como la variación relativa de presión del sistema en función de la temperatura en un proceso isocoro. 1 Los anteriores coeficientes están relacionados entre si por la expresión : = pK Los coeficientes térmicos de todos los sólidos disminuyen al bajar la temperatura, lo que indica que se hacen más rígidos y, por tanto menos compresibles y dilatables a medida que la temperatura desciende ( agua convertida en hielo ). Sin embargo, su variación con respecto a la temperatura y presión, para sólidos y líquidos, es muy reducida en los intervalos considerados normalmente, por lo que, en una primera aproximación pueden considerarse constantes. Así, el valor de para el caso de sólidos, es del orden de 10−5 ºC−1 y de 10−4 ºC−1 para líquidos. En el caso de que consideremos constante, la integración de dV a partir de la ecuación de a presión constante, conduce a la expresión : Ln V = t + Ln Vo Siendo t, la temperatura del sistema en ºC y Vo, el volumen del mismo a la temperatura de 0 ºC. La representación gráfica de la ecuación anterior es una recta cuya pendiente es el valor de Ln V Ln Vo t ºC Método operativo.− En el comienzo de la práctica y con la totalidad de los instrumentos necesarios, procedemos a calcular el volumen de agua inicial. Para ello tomamos el peso del matraz Erlenmeyer junto con su tapón de goma (con el termómetro y tubo de vidrio) antes y después de su llenado, la diferencia entre ambos pesos es de 124.81 g, conocida la densidad del agua, d = 1g/cc, obtenemos el volumen igual a 124.81cc. Una vez hallado el volumen, señalamos la altura inicial del agua en el tubo de vidrio y procedemos a su calentamiento. Por cada incremento de temperatura equivalente a 5 ºC, medimos y marcamos la altura. Este procedimiento lo llevamos a cabo entre 10 y 65 ºC. Y realizamos la siguiente tabla : T(ºC) 10 15 20 25 30 35 40 45 50 55 60 65 L(cm) 0 0,25 0,75 1,35 2,1 2,75 3,65 4,3 5,55 6,7 7,95 9,4 V(cm3) 124,81 124,88 125,02 125,19 125,4 125,58 125,84 126,02 126,38 126,7 127,06 127,47 Ln V 4,82679258 4,82735328 4,82847372 4,82983258 4,83150863 4,83294301 4,83501126 4,83644062 4,83929324 4,84182209 4,84465942 4,84788104 2 El volumen V se ha calculado mediante : V = Vo + R2 0.25 el radio tomado es de 0.3. Finalmente construimos la gráfica : Realizamos la misma operación con el alcohol etílico, teniendo en cuenta que la densidad del alcohol etílico es d = 0.81 g/cc obtenemos la tabla : T(ºC) 10 15 20 25 30 35 40 45 50 55 L(cm) 0 1,6 3,45 5,55 7,65 9,75 12,1 14,85 17,3 20,85 V(cm3) 119,46 119,91 120,43 121,03 121,62 122,21 122,88 123,66 124,35 125,35 Ln V 4,78298159 4,78674146 4,79106867 4,79603845 4,80090143 4,80574088 4,81120827 4,81753586 4,82310017 4,83110982 con su correspondiente gráfica : 3 Finalmente observamos que el coeficiente de dilatación del agua es bastante menor que el del alcohol etílico. 4