fisicoquimica - Escuela en Tandil
Anuncio

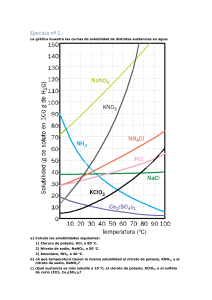
Escuela de Educaion Agraria Nº1 Segundo SB “C” Físico Química Profesora: Emilia Montero ACTIVIDADES SOLUCIONES 1) Defina los siguientes términos: a) Punto de fusión b) Punto de ebullición c) Densidad d) Concentración e) Solubilidad f) Volumen g) Masa h) Peso 2) La solubilidad del Nitrato de Potasio (KNO3) es 31,6 a 20ºC, que tipo de solución se formara si disuelvo en 100 gr de agua: a) ¿Qué significa el numero 31,6? b) ¿Por qué se informa la temperatura? c) 20 gr de nitrato de potasio. d) 31,6 gr de nitrato de potasio. e) 50 gr de nitrato de potasio. f) Explique las soluciones formadas en c), d) y e) 3) ¿Se puede seguir agregando soluto indefinidamente y siempre obtener una solución? 4) Sabiendo que el oro es una solución (aleación), realice una hipótesis del significado del oro 18 kilates. 5) ¿Qué factores modifican la solubilidad de un sólido? ¿Y de los gases? Explique. 6) Indica el %v/v de una solución que se preparó mezclando 60 ml de alcohol con 180 ml de agua. 7) Se disuelven 4 gr de azúcar en 196 gr de agua ¿Cuál es la concentración de la solución en % m/m? 8) Repasar las actividades de la carpeta. INTRODUCCIÓN A REACCIONES QUÍMICAS 1) ¿Qué es una reacción química? 2) ¿Cómo se representan? 3) ¿Qué significan el signo + y la flecha en las ecuaciones químicas? 4) Explique la ley de conservación de la masa. ¿Cómo se aplica esto a las ecuaciones químicas? 5) Sabiendo que: los cambios químicos son cambios en donde las sustancias que los sufren cambian para convertirse en otras y que los cambios físicos al producirse no cambian la identidad de la sustancia, cite ejemplos de cada uno. 6) Explique de que se tratan las reacciones de: a) síntesis b) descomposición c) precipitación d) oxidorreducción e) combustión 7) Busque ejemplos para cada una de las reacciones anteriores. 8) Como se clasifican las reacciones teniendo en cuenta la energía. Explique.