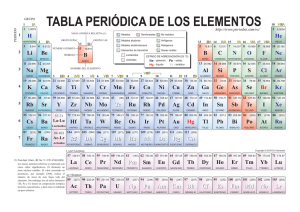
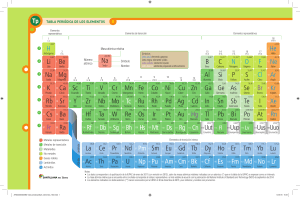
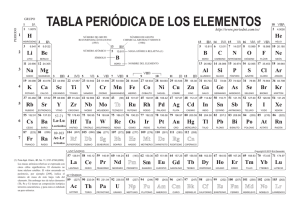
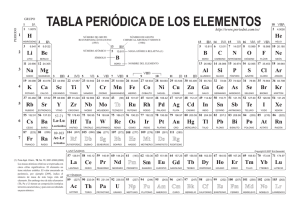
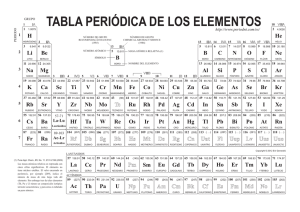
Elementos de transición de la tabla periódica.
Anuncio

ELEMENTOS DE TRANSICIÓN Desde la antigüedad, muchos de los metales de transición han sido utilizados en diferentes actividades del ser humano, en la fabricación de armas y herramientas, y en la elaboración de finos y delicados adornos. También son parte importante en la construcción, pues metales como el hierro se diseñan estructuras para construir casas, grandes edificaciones y puentes. Los elementos de transición se ubican en la parte central de la tabla periódica se designan con números romanos y la letra B. Los elementos de transición son todos metales se caracterizan porque tienen llenos o semillenos los orbitales d. Las propiedades de los metales de transición son muy similares entre si. Los compuestos de éstos metales son por lo general, de colores brillantes y se emplean para dar color a las pinturas. El mercurio es el único metal de transición líquido a temperatura ambiente, se emplea en la fabricación de termómetros. El cromo se utiliza en las aleaciones del acero, también para cubrir las superficies de otros metales con el fin de evitar la oxidación y la corrosión . El zinc se utiliza para galvanizar el hierro, en la fabricación de pilas secas y en aleaciones con el cobre, como el latón. Elementos de transición interna. Los elementos de transición interna también se denominan tierras raras. Corresponden a las dos filas de elementos de la parte interior de la tabla periódica, estos elementos tienen llenos o semillenos los orbitales f y algunos tienen sus subniveles d parcialmente ocupados, sus electrones de valencia pertenecen a sus tres niveles más externos. Los elementos de transición interna comprenden dos series : los lantánidos y los actínidos. Serie de los elementos lantánidos. La serie de los lantánidos comprende desde el elemento 58 al elemento 71; éstos tienen dos electrones externos en el subnivel 6s, más electrones adicionales en el subnivel 4f. El cerio(Ce) es el principal metal de esta serie, forma aleaciones con el hierro y con el magnesio, esta última se utiliza para fabricar motores de avión. Otro elemento presente en esta serie es el neodimio(Nd) que es empleado para decolorar el vidrio. El europio(Eu), el gadolinio8GD)y el disprosio(DY) absorben neutrones y por eso son utilizados para controlar los reactores nucleares. El prometio (Pm) es el único elemento de esta serie que es sintético. Serie de los elementos actínidos. La serie de los actínidos se llama asé por el actinio un elemento radiactivo comprende los elementos desde el 90 hasta el 103 presentan dos electrones en el subnivel 7s, más electrones adicionales en el subnivel 5f. El plutonio(pu) es uno de los elementos que se obtienen a partir del uranio cuando se utiliza como combustible nuclear; también se emplea como fuente de energía en los marcapasos. Algunos actínidos tienen aplicaciones en la medina por ejemplo el californio(Cf), de masa 246, se usa en el tratamiento del cáncer. El uranio pertenece a la serie de los elementos actínidos , es radiactivo y tóxico presenta tres radioisótopos naturales : el 238U, el más abundante, el 235U, el 234U, 235U es el más fisionable, se utiliza como combustible y explosivo nuclear. Los lantánidos y actinidos tienen propiedades similares.- Estos metales son blandos y maleables, y se emplean en la fabricación de piedras para encendedores, láseres , vidrio de alta calidad ysus colorantes también se usan en aleaciones y en la producción de superconductores de cerámica. Existen otros elementos, desde el 104 hasta el 118, a los cuales no se ha podido comprobar sus propiedades, debido a que su tiempo de vida media es muy corto. Períodos Los períodos corresponden a las filas horizontales de la tabla periódica y se designa con números arábigos del 1 al 7. Cada período indica la iniciación del llenado de un nuevo nivel de energía y se caracteriza por el número cuántico principal .