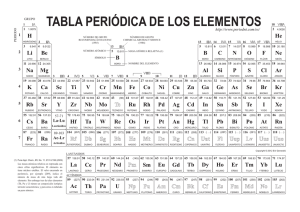
TEMA 22 LOS METALES DEL BLOQUE f: LANTÁNIDOS Y
Anuncio

1
TEMA 22
LOS METALES DEL BLOQUE f: LANTÁNIDOS Y ACTÍNIDOS
1.- Introducción
En este capítulo se estudian los metales del bloque f y sus compuestos. Hay dos series
de metales: lantánidos (los 14 elementos que siguen al lantano en la tabla periódica) y
actínidos (los 14 elemntos que siguen al actinio). Lantánidos y actínidos (Tabla 24.1) se
conocen en conjunto como metales de transición interna, mientras que escandio, itrio,
lantano y lantánidos se denominan conjuntamente metales de las tierras raras. Aunque
en sentido estricto La y Ac son metales del grupo 3, la similitud química del La con los
elementos Ce-Lu y la del Ac con Th-Lr significa que el La se clasifica normalmente con
los lantánidos y el Ac con los actínidos.
Se utiliza a menudo el símbolo Ln para hacer referencia genérica a los elementos La-Lu.
Los lantánido se parecen entre sí mucho más que los miembros de una fila de metales d.
La química de los actínidos es más complicada y además solo Th y U tienen isótopos
naturales. El estudio de los elementos transuránidos (los de Z> 92) requiere técnicas
2
especiales. La abundancia de los isótopos artificiales entre los elementos del bloque f
puede verse en el Apédice 5: todos los actínidos son inestables con respecto a la
desintegración radiactiva (véase Sección 25.9), aunque la vidamedia de los isótopos más
abundantes de torio y uranio (232Th y 238U, t1/2= 1.4x104 y 4.5x109 años,
respectivamente) es tan larga que a efectos prácticos su radiactividad puede
despreciarse.
Los elementos transuránidos son los que tienen número atómico mayor que el U (Z>
92).
2.- Orbitales f y estados de oxidación
Para un orbital f los números cuánticos son n= 4, l= 3 y ml= +3, +2, +1, 0, -1, -2, -3; un
conjunto de orbitales f está degenerado siete veces. Los orbitales f son ungerade.
Un conjunto de orbitales f está degenerado siete veces y hay más de un modo de
representarlo. Se utiliza normalmente el conjunto cúbico y se relaciona fácilmente con
el campo ligando teraédrico, octaédrico y cúbico. El conjunto cúbico comprende los
orbitales atómicos fx3, fy3, fz3, fxyz, fz(x2-y2), fy(z2-x2) y fx(z2-y2); la Figura 24.1 recalca cómo
se relaciona la dirección de los lóbulos del orbital atómico fxyz con los vértices de un
cubo. Cada orbital f contiene tres planos nodales.
La capa de valencia de un elemento lantánido contiene orbitales atómicos 4f y la de un
actínido, orbítales 5f: la configuración electrónica en el estado fundamental de los
elementos del bloque f se da en la Tabla 24.1. Un orbital atómico 4f no tiene ningún
nodo radial, mientras que un orbital atómico 5f tiene un nodo radial (véase Sección 1.6).
Una diferencia crucial entre los orbítales 4f y 5f es el hecho de que los orbitales
atómicos 4f están muy ocultos y los electrones 4f no están disponibles para el enlace
covalente. Normalmente, tampoco es posible, desde el punto de vista energético, la
ionización más allá del ión M3+ y esto conduce a un estado de oxidación característico
de +3 en toda la fila desde La hasta Lu.
Los elementos La a Lu se caracterizan por un estado de oxidación +3 y su química es
fundamentalmente la del ión Ln3+.
Los estados de oxidación conocidos de los actínidos se muestran en la Tabla 24.2. La
existencia de al menos dos estados de oxidación para casi todos estos metales implica
que las energías de ionización sucesivas (véase Apéndice 8) difieren probablemente
menos que las de los lantánidos. Para los estados de oxidación más elevados, con toda
seguridad debe intervenir el enlace covalente. Esto puede ocurrir bien porque los
3
orbitales atómicos 5f se extienden más lejos del núcleo que los orbitales atómicos 4f y
están disponibles para el enlace, o bien poruqe la separación de energía entre los
orbitales atómicos 5f, 6d, 7s y 7p es lo suficientemente pequeña como para que se
alcancen fácilmente los estados de valencia adecuados para el enlace covalente. Las
pruebas de que los orbitales atómicos 5f tienen una mayor extensión espacial que los
orbitales atómicos 4f vienen de la estructura fina del espectro ESR del UF3 (en una red
de CaF2) que se origina por la interacción del espín electrónico del U3+ y los iones F-; el
NdF3 (la correspondiente especie lantánida) no muestra tal efecto.
La Tabla 24.2 muestra que los primeros actínidos exhiben un amplio rango de estados
de oxidación, pero del Cm al Lr los elementos se parecen a los lantánidos. Esto es una
consecuencia de que la energía de los orbitales atómicos 5f disminuye al atravesar el
periodo y por tanto se estabilzan los electrones 5f.
3.- Tamaño de átomos e iones
Contracción de los lantánidos
La contracción de los lantánidos es la disminución constante de tamaño a lo largo de la
serie de elementos La-Lu.
La disminución global de los radios atómicos e iónicos (Tabla 24.1) de La a Lu tiene
importantes consecuencias en la química de los metales de la tercera fila del bloque d
(véase Sección 22.3). La contracción es análoga a la observada en un periodo de metales
del bloque d y se atribuye al mismo efecto: el apantallamiento incompleto de un
electrón por otro en la misma subcapa. Sin embargo, el apantallamiento de un electrón
4f por otro es menor que el de un electrón d por otro y, al aumentar la carga nuclear de
La a Lu, hay una disminución bastante regular en el tamaño de la subcapa 4fn.
Los radios iónicos para los lantánidos en la Tabla 24.1 se refieren a iones de
coordinación 8, y los de los actínicdos a coordinación 6. Los valores deben utilizarse
solo como guía; aumentando al hacerlo el número de coordinación y de ninguna manera
son valores absolutos.
Números de coordinación
En la Sección 19.7, estudiamos los números de coordinación hasta 9. El gran tamaño de
los metales lantánidos y actínidos significa que, en sus complejos, son comunes los
números de coordinación elevados (> 6). El desdoblamiento del conjunto de orbitales f
degenerados en el campo cristalino es pequeño (∆o ≈ 1 KJmol-1) y las consideraciones
de estabilización del campo cristalino son de poca importancia en la química de
4
lantánidos y actínicos. Las preferencias entre diferentes números de coordinación y
geometrías suelen star controladas por efectos estéricos.
4.- Propiedades espectroscópicas y magnétcias
Espectros electrónicos y momentos magnétiscos
El lector debe consultar el Cuadro 20.6 para los símbolos de términos para átomos e
iones libres. La interpretación de los espectros electrónicos 4fn se basa en los principios
explicados para los iones metálicos del bloque d (véase Sección 20.6) pero hay
importantes diferencias. Para los lantánidos, el acoplamiento espín-órbita es más
importante que el dedoblamiento del campo cristalino y los términos que se diferencian
solo en el valor de J tienen una energía lo suficientemente distinta como para estar
separados en el espectro electrónico. Además como l=3 para un electrón f, ml puede ser
3, 2, 2, 0, -1, -2 o –3 dando lugar a valores elevados de L para algunos iones fn: por
ejemplo, para la configuración f2 la aplicación de la regla de Hund da el estado
fundamental (con L=5, S= 1) como 3H4. Como también los términos S, P, D, F y G son
posibles muchos de ellos con valores positivos diferentes de J, el número de
transiciones posibles es grande, incluso después de tener en cuenta las limitaciones
impuestas por las reglas de selección. Como resultado, los espectros de los iones Ln3+
contienen con frecuencia un gran número de absorciones. Al estar los electrones 4f bien
apantallados y no afectados por el entorno del ión, las bandas originadas por
transiciones f-f son finas ( y no anchas como las absorciones d-d) y su posición en el
espectro se ve poco afectada por la formación de complejos. La intensidad de las
absorciones es baja, lo que indica que la probabilidad de las transiciones f-f es baja, es
decir, hay poca mezcla d-f. Las absorciones debidas a las transiciones 4f-5d son anchas
y están afectadas por el entorno de los ligandos. Se utilizan pequeñas cantidades de
sales de lagunos lantánidos en fósforos para tubos de televisión (véase luminiscencia a
continuación) debido a la nitidez de sus transciones electrónicas.
En los espectros electrónicos de los iones de metales lantánidos, las absorciones debidas
a transiciones f-f son finas, pero las bandas debidas a transiciones 4f-5d son anchas.
Los colores típicos de los iones Ln3+ en disolución acuosa se recogen en la Tabla 24.3.
Normalmente (pero no siempre ) las especies fn y f14-n tienen colores similares.
5
Los momentos magnéticos (véase Sección 20.8) de los iones Ln3+ se dan en la tabla
24.3. En general, los valores experimentales concuerdan con los calculados a partir de
las fórmulas (véase Ecuación 20.14) basándose en la suposición de acoplamiento de
Russell-Suanders y constantes de acoplamiento espín-órbita grandes, a consecuencia de
lo cual solo los estados con valor de J más bajo están poblados. Esto no se cumple para
Eu3+ y no del todo para Sm3+. Para Eu3+, la constante de acoplamiento espín-órbita λ es
≈ 300 cm-1, solo ligeramente mayor que KT (≈ 200 cm-1); el estado fundamental del ión
f6 es 7F0 (que es diamagnético, ya que J= 0), pero los estados 7F1 y 7F2 también están
poblados en cierta medida y dan lugar al momento magnético observado. Como era de
esperar, a baja temperatura, el momento de Eu3+ es próximo a cero. La variación de m
con n (número de electrones desapareados) en la Tabla 24.3 surge del cumplimiento de
la tercera rega de Hund (véase Cuadro 20.6): J= L-S para una capa menos que semillena
pero J= L+S para una capa más que semillena; en consecuencia, J y gJ (véase Ecuación
20.15) para estados fundamnetales son ambas mayores en la segunda mitad que en la
primera mitad de la serie de los lantánidos.
Luminiscencia de los complejos lantánidos
La irradiación con luz UV de muchos complejos de Ln3+ provoca su fluorescencia. En
algunas especies se necesitan temperaturas bajas para observar este fenómeno. La
fluorescencia lleva al uso de los lantánidos en fósforos para televisión y luces
fluorescentes. El origen de la fluorescencia son las transicones 4f-4f; no son posibles las
transiciones para f0, f7 (prohibidas por espín) y f14. La irradicación produce Ln3+ en un
estado excitado que pasa al estado fundamental bien con emisión de energía (observada
como fluorescencia) o por mecanismo sin readiación. Los iones comercialmente
importantes por sus propiedades de emisión son Eu3+ (emisión roja) y Tb3+ (emisión
verde).
Espectros electrónicos y momentos magnéticos: actínidos
Las propiedades espectroscópica y magnéticas de los actínidos son complicadas y solo
las mencionaremos brevemente. Las absorciones debidas a transiciones 5f-5f son
débiles, pero son algo más anchas y más intensas (y considerablementa más
dependientes de los ligandos presentes) que las debidas a transicones 4f-4f. La
6
interpretación de los espectros electrónicos la complican las constantes de acoplamiento
grandes espín-órbita (aproximadamente el doble que las de los lantánidos) que tiene
como resultado que el esquema de acoplamiento Russell-Suanders falle parcialmente.
Las propiedades magnéticas muestran una similitud global a las de los lantánidos en la
variación del momento magnéticos con el número de electrones desapareados, pero los
valores para especies lantánidas y actínidas isoelectrónicas, por ejemplo Mn(VI) y
Ce(III), Np(V) y Pr(III), Np(IV) y Nd(III), son más bajos para los actínicos lo que
indica una anulación parcial de la contribución orbital por efecto del campo cristalino.
5.- Fuentes de lantánidos y actínidos
Abundancia y separación de los lantánidos
Todos los lantánidos excepto el Pm se encuentran en la natutaleza. El isótopo más
estable del promecio, 147Pm (emisor β, t1/2= 2.6 años) se forma como producto en la
fisión de núcleos pesados y se obtiene en cantidades de mg a partir de productos de las
reactores nucleares.
Bastnasita y monacita son las principales menas de La y los lantánidos. Todos los
metales (excluyendo Pm) pueden obtenerse a partir de la monacita, un fosfato mixto
(Ce, La, Nd, Pr, Th, Y...)PO4). La bastnasita, (Ce, La,...)CO3F, es una fuente de los
lantánidos más ligeros. La primera etapa en la extracción de los metales a partir dela
monacita es la eliminación de fosfato y torio. La mena se calienta con sosa caústica y,
después de enfriar, se disuelve el Na3PO4 en agua. Los óxidos hidratados de Th(IV) y
Ln(III) residuales se tratan con HCl acuoso, caliente; el ThO2 no se disuelve, pero los
óxidos de Ln(III) dan disolución de MCl3 (M= La, Ce,...) que se purifica a continuación.
Partiendo de la bastnasita, la mena se trata con HCl diluido para eliminar el CaCO3 y
después se convierte en una disolución acuosa de MCl3 (M= La, Ce,...). La semejanza
de tamaño y propiedades de los iones de los lantánidos hace que la separación sea
difícil. Losmétodos modernos de separación de lantánidos implican la extracción con
disolventes utilizando (nBuO)3PO (véase Cuadro 6.3) o el intercambio iónico (véase
sección 10.6).
Una resina típica de inetrcambio catiónico es poliestireno sulfonado o su sal de Na+.
Cuando se vierte una disolución que contiene iones Ln3+ en una columna con resina, los
cationes se intercambian con los iones H+ o Na+ (Ecuación 24.1).
Ln3+ (aq) + 3H+ (resina)
Ln3+ (resina) + 3H+(aq)
(24.1)
El coeficiente de distribución en el equilibrio entre la resina y la disolución acuosa
[[Ln3+(resina)]/[Ln3+(aq)] es grande para todos los iones, pero casi constante. Los iones
Ln3+ unidos a la resina se eliminan utilizando un agente de complejación como EDTA4(véase Ecuación 6.75). Las constantes de formación de los complejos EDTA4- de los
iones Ln3+ aumentan con regularidad desde 1015.3 para La3+ hasta 1019.2 para Lu3+. Si se
eluye con una disolución acuosa diluida de H4EDTA una columna en la que todos los
iones Ln3+ han sido absorbidos y se ajusta el pH a 8 con NH3, Lu3+ se compleja de
forma preferente, después Yb3+ y así sucesivamente. Utilizando una columna de
intercambio iónico larga, pueden separase componentes con una pureza del 99.9%
(Figura 24.2).
7
Los actínidos
A excepción del Th y U, los actínidos son artificiales y se producen en las reacciones
nucleares (véase capítulo 2). Los peligros de radicación de todos los elementos, menos
Th y U, conducen a dificultades técnicas en el estudio de los compuestos actínidos y, en
general, no son aplicables las técnicas experimentales convencionales.
Uranio y torio se ailslan de fuentes naturales. El torio se extrae de la monacita como
ThO2 (véase más arriba) y la fuente más importante de uranio es la pechblenda (U3O8).
La mena de uranio se calienta con H2SO4 en presencia de un aoxidante para dar el
sulfato del catión uranilo [UO2]2+, que se separa en una resina de intercambio aniónico,
eluyendo con HNO3 para dar [UO2][NO3]2. Después de una purificación adicional, el
uranio se precipiata como el complejo oxo-peroxo UO2(O2).2H2O o como “torta
amarilla” (composición aproximada [NH4]2[U2O7]). La descompsociónntérmica de UO3
amarillo que se convierte en UF4 (Reacción 2.19 y 2.20); la reducción com Mg da U
metal.
Los isótopos 227Ac y 231Pa pueden aislarse a partir de los productos de la desintegración
del 235U de la pechblenda, pero es mejor sintetizarlos por las reacción nucleares 24.2 y
24.3
-β-
(n,γ)
226
227
Ra
231
Th
Ac
(24.2)
-β-
(n,γ)
230
227
Ra
231
Th
Pa
(24.3)
La Ecuación 2.17 mostraba la síntesis del 239Np y 239Pu; la irradicación prolongada del
239
Pu en un reactor nuclear conduce a la formación sucesiva de pequeñas cantidades de
240
Pu, 241Pu, 242Pu y 243Pu. Este último un emisor β- (t1/2= 5 h) y se desintegra a 243Am
(t1/2= 7400 años) que da 244Cm por la Secuencia 24.4.
(n,γ)
243
Am
244
-β-
Am
244
Cm (24.4)
8
Tanto 243Am como 244Cm están disponibles en escala de 100 g y la captura múltiple de
neutrones seguida de desintegración β- de cantidades de miligramos de 249Bk, 252Cf,
253
Es y 254Es, además de 257Fm en cantidades de microgramos. La síntesis de los
actínicos más pesados se detalló en la Sección 2.6. En el Cuadro 24.3 se destaca un uso
cotidiano de 241Am.
6.- Metales lantánidos
El lantano y los lantánidos, excepto Eu, cristalizan en una o ambas de las estructuras de
empaquetamiento compacto; el Eu tiene una red bcc y el valor de rmetal dado en la Tabla
24.1 puede ajustarse a 205 pm para coordinación 12 (véase Sección 5.5). Es importante
señalar en la Tabla 24.1 que Eu e Yb tienen un radio metálico mucho mayor que los
otros lantánidos, lo que implica que Eu eYb (que tienen estados de oxidación inferiores
bien definidos) contribuyen con menos electrones al enlace M-M. Esto concuerda con
los valores más bajos de ∆H0a: Eu e Yb, 177 y 152 KJmol-1, respectivamente,
comparado con los otros lantánidos (206-430 KJmol-1). El valor más bajo en este rango
(206 KJmol-1) pertenece al Sm; como Eu e Yb, Sm también tiene un stado de oxidación
inferior bien definido pero a diferencia de Eu e Yb, el Sm no muestra anomalía en su
radio metálico. Además, Eu e Yb, pero no Sm, forman disoluciones azules en NH3
líquido debido a la Reacción 24.5 (véase Sección 8.6).
Ln
Ln2+ + 2e(solv)
Ln= Eu, Yb
(14.5)
Todos los lantánido son metales blandos de color blanco. Los últimos metales se
pasivan con un recubrimiento de óxido y son cinéticamente más inertes que los
primeros metales. Los valores de E0 para la Semirreacción 24.6 están en el intervalo –
2.0 a 2.4 V y la pequeña variación indica que las variaciones de la ∆H0a, EI y ∆Hhid (que
son considerables) se cancelan de hecho.
Ln3+ + 3e
Ln (24.6)
Todos los metales desprende H2 de ácidos diluidos o vapor. Arden en el aire para dar
Ln2O3 a excepción del Ce que forma CeO2. Al calentarlos, los lantánidos reaccionan
con H2 para dar una serie de compuestos entre hidruros metálicos (es decir,
conductores) LnH2 (mejor formulados como Ln3+(H-)2(e-)) e hidruros salinos LnH3. Los
hidruros no estequiométricoa están representados por “GdH3” que en realidad tiene
composiciones en el rango GdH2.85-3. El Eu forma solo EuH2. La aleación LaNi5 es un
“recipiente de almacenaje de hidrógeno” potencial (véase Sección 9.7 y Cuadro ).2)
porque absorbe reversiblemente H2 (Ecuación 24.7).
LaNi5
LaNi5Hx x ≈ 6 (24.7)
Los carburos Ln2C3 y LnC2 se forman al calentar los metales con carbono. Los carburos
LnC2 adoptan la misma estructura que CaC2 (véase Sección 13.7), pero los enalces C-C
(128 pm) son apreciablemente más largos (119 pm en CaC2). Son condutores metálicos
y están mejor formulados con Ln3+[C2]2-(e-). Los boruros lantánidos se estudiaron en la
Sección 12.10; los haluros se describen a continuación.
7.- Compuestos inorgánicos y complejos de coordinación de los lantánidos
9
La discusión en esta sección es necesariamente selectiva. La mayor parte de la química
está relacionada con el estado de oxidación +3, siendo Ce(IV) el único estado +4 estable
(Ecuación 24.8)
Ce4+ + e
Ce3+ E0= +1.27 V (24.8)
El estado de oxidación +2 está bien definido para Eu, Sm y Lu. Los valores estimados
de E0 para los pares Sm3+/Sm2+ y Yb3+/Yb2+ son –1.5 y 1.1 V, respectivamente, lo que
indica que Sm(II) e Yb(II) son muy inestables con respecto a la oxidación incluso con
agua. Para el par Eu3+/Eu2+, el valor de E0 (-0.35 V) es análogo al de Cr3+/Cr2+ (-0.41 V)
y las disoluciones incoloras de Eu(II) pueden utilizarse para estudios químicos, en
ausencia de aire.
Haluros
La reacción de F2 con Ln da LnF3 para todos los metales y, para Ce, Pr y Tb, también
LnF4. CeF4 puede preparase también por la reacción 24.9 o a temperatura ambiente en
HF anhidro (Ecuación 24.10). Las mejores rutas para PrF4 y TbF4 (Ecuaciones 24.11 y
24.12) tiene lugar lenta, pero cuantitativamente; el óxido “Th4O7” es en realidad una
mezcla en dos fases de Tb7O12 y Tb11O20.
F2, XeF2, ClF3
CeO2
CeF4
(24.9)
F2 en HF líquido 298 K, 6 días
CeF3
CeF4
(24.10)
F2 en HF líquido, 298 K, radiación UV, 11 días
Pr6O11
PrF4
(24.11)
F2 en HF líquido, 198 K, radiación UV, 25 días
Tb4O7
TbF4
(24.12)
Con Cl2, Br2 e I2, se forman LnX3. Sin embargo, la ruta genral a LnX3 es por reacción
de Ln2O3 con HX acuoso; esto da los haluros hidratados, LnX3(H2O)x (x= 6 o 7). El
tricloruro anhidro se prepara normalmente por deshidratación de LnCl3(H2O)x con
SO2Cl o NH4Cl; deshidratación térmica tiene como resultado la formación de
oxocloruros. La Reacción 24.13 da diyoduros metálicos con elevada conductividad
eléctrica; como con los dihidruros anteriores, estos diyoduros son en realidad Ln3+(I)2(e-). Pueden formarse LnX2 salinos (Ln= Sm, Eu, Yb; X= F, Cl, Br, I) por reducción
de LnX3 (por ejemplo, con H2).
Ln + 2LnI3
3LnI2 Ln= La, Ce, Pr, Gd (24.13)
La estructura en estado sólido de LnX3 contiene centros de Ln(III) con números de
coordinación elevados y, al disminuir rM3+ a lo largo de la fila, el número de
coordinación disminuye. En LaF3 cristalino, cdada centro de La3+ tiene coordinación 11
en un ambiente de prisma trigonal con cinco topes. Los cloruros LnCl3 para Ln= La a
Gd poseen estructura de UCl3; éste es un prototipo estructural que contiene centros
metálicos de prisma trigonal con tres topes. Para Ln= Tb a Lu, LnCl3 adopta una red en
capas de AlCl3 con Ln(III) octaédrico.
Compuestos como KCeF4, NaNdF4 y Na2EuCl5 se preparan por fusión de fluoruros
metálicos del grupo 1 y LnF3. Se trata de sales dobles y no contienen aniones
10
complejos. Se conocen varios aniones hexahaluro discretos de Ln(III), por ejemplo,
[YbI6]4-.
Hidróxido y óxidos
El hidróxido de lantano, aunque moderadamente soluble, es una base fuerte y absorbe
CO2 dando el carbonato. La fuerza y la solubilidad de la base disminuyen al atravesar la
serie de los lantánidos; Yb(OH)3 y Lu(OH)3 se disuelven en NaOH concentrado,
caliente (Ecuación 24.14).
Ln(OH)3 + 3[OH]-
[Ln(OH)6]3-
Ln= Yb, Lu
(24.14)
El hidróxido de cerio(III) es un sólido blanco y en el aire se forma lentamente Ce(OH)4
amarillo. La mayoría de los óxidos Ln2O3 se forman por descomposicón térmica de
sales de oxoácidos, por ejemplo Reacción 24.15, pero Ce, Pr y Tb dan óxidos superiores
por este método y se utiliza para reducir estos últimos a Ln2O3.
4Ln(NO3) 3
2Ln2O3 + 12NO2 + 3O2
(24.15)
La reacción de Nd2O3 y oleum (véase Sección 15.8) a 470 K tiene como resultado la
formación de Nd(S2O7)(HSO4), primer ejemplo de disulfato de un metal de las tierras
raras.
Complejos de Ln(III)
Los iones Ln3+ son duros y muestran preferencia por F- y ligandos dadores O-, por
ejemplo en complejos con [EDTA]4- (Sección 24.5). [Yb(OH)6]3- (Ecuación 24.24) y en
complejos de β-dicetonato (Cuadro 24.4). En sus acuocomplejos, los iones Ln3+ tienen
normalmente coordinación 9 y se ha confirmado una estructura de prisma trigonal con
tres topes en sales cristalinas como [Pr(H2O)9][OSO3Et]3 y [Ho(H2O)9][OSO3Et] 3. Lo
normal en complejos de Ln3+ son los números de coordinación elevados, siendo los más
elevados los correspondientes a los primeros lantánidos, entre los ejemplos están:
- coordinación 12: [La(NO3-O,O’)6]3-, [La(H2O)2(NO3-O,O’)5]2-;
- coordinación 11: [La(H2O)5(NO3-O,O’)3], [Ce(H2O)5(NO3-O,O’)3], [Ce(15-corona5)(NO3-O,O’) 3], [La(15-corona-5)(NO3-O,O’)3] (Figura 24.3a);
- coordinación 10: [Ce(CO3-O,O’)5]6- (Ce4+, Figura 24.3b), [Nd(NO3-O,O’)5]2-, [Eu(18corona-6)(NO3-O,O’)2]+;
-coordinación 9: [Ln(EDTA)(H2O)3]- (Ln= La, Ce, Nd, Sm, Eu, Gd, Tb, Dy, Ho),
[CeCl2(18-corona-6)(H2O)]+,
[PrCl(18-corona.6)(H2O)2]2+,
[LaCl3(18-corona-6)]
(Figura 24.3c), [Eu(tpy)3]+,[Nd(H2O)(CO3-O,O’)4]5-;
- coordinación 8: [Pr(NCS-N)8]5- (entre cúbica y antiprismática cuadrada);
- coordinación 7: (24.1);
- coordinación 6: cis-[GdCl4(THF)2]-[Ln(β-dicetonato)3] (véase Cuadro 24.4).
11
La variación que se encuentra en la geometría de coordinación para un número de
coordinación elevado determinado, es consistente con el razonamiento de que los
requisitos espaciales de un ligando y las limitaciones de coordinación de los ligandos
multidentados son factores determinantes; los orbitales atómicos 4f están muy ocultos y
juegan un papel pequeño en el enlace metal-ligando. De esta manera, la configuración
4fn no influye en el control del número de coordinación. Recientes avances en agentes
de contraste para RMI (véase Cuadro 2.6) suponen el estudio de complejos de Gd3+ que
contienen ligandos polidentados con dadores O- y N-.
Los números de coordinación inferiores pueden estabilizarse utilizando ligandos ariloxi
o amida, por ejemplo:
- coordinación 5: (24.2), (24.3);
- coordinación 3: [Nd{N(SiMe3)2}3].
En estado sólido [Nd{N(SiMe3)2}3] es piramidal trigonal pero esto puede ser una
consecuencia de las fuerzas de empaquetamiento cristalino (véase Sección 19.7).
12
8.- Complejos organometálicos de los lantánidos
La química organolantánida es un área de investigación que se amplía rápidamente y un
aspecto interesante de esta área es el número de catalizadores eficaces para
transformcaciones orgánicas que se han descubierto (véase Cuadro 24.5). A diferencia
de la extensa química de los carbonilos de metales del bloque d (véase Secciones 23.4 y
23.9), los metales lantánidos no forman complejos con CO en condiciones normales. Se
han preparado carbonilos inestables como Nd(CO)6 por aislamiento en matriz. Los
organolantánidos son normalmente sensibles al aire y a la humedad y algunos son
pirofóricos; el manejo de estos compuestos en atmósfera inerte es esencial.
Complejos con enlace σ
La Reacción 24.26 muestra un método general para formar enlaces σ Ln-C.
LnCl3 + 3LiR
LnR3 + 3LICl
(24.16)
En presencia de un exceso de LiR y con grupos R que no estén demasido impedidos
estéricamnete, la Reacción 24.16 puede seguir para dar [LnR4]- o [LnR6]3- (Ecuaciones
24.27 y 24.28).
THF, 218 K
YbCl3 + 4TbBuLi
LuCl3 + 6MeLi
[Li(THF) 3]+[YbtBu4]- + 3LiCl
DME, 195 K
[Li(DME)]3+[LuMe6]3- + 3LiCl
(24.17)
DME= 1,2-dimetoxietano (24.18)
En estado sólido, [LuMe6]3- es octaédrico (Lu-C= 253 pm) y se conocen análogos para
todos los lantánidos excepto Eu. En estas reacciones se necesita un disolvente de
coordinación como DME o Me2NCH2CH2NMe2 (TMED) para estabilizar el producto
con un ión Li+ solvatado. En algunos casos, el disolvente se coordina con el metal
lantánido, por ejemplo TmPh3(THF)3 (Reacción 24.19 y estructura 24.4).
en THF en presencia de TmCl3
Tm + HgPh2
TmPh3(THF)3
(24.19)
Los complejos que contienen grupos –C≡CR con enlace σ se han preparado por varias
rutas, por ejemplo Reacción 24.20.
HC≡CtBu en THF
[LutBu4(THF)4]-
t
- BuH
[Lu(C≡CtBu)4]-
(24.20)
13
Complejos ciclopentadienilo
Muchos organolantánidos contienen ligandos colcopentadienilo y la Reacción 24.21 es
una ruta general a Cp3Ln.
LnCl3 + 2NaCp
Cp3Ln + 3NaCl
(24.21)
La estructura en estado sólido de compuestos Cp3Ln varía con Ln, por ejemplo Cp3Tm
y Cp3Yb son monoméricos, mientras que Cp3La, Cp3Pr y Cp3Lu son poliméricos. Los
aductos con dadores como THF, piridina y MeCN se forman fácilmente, por ejemplo
(η5-Cp)3Tb(NCMe) y (η5-Cp)3Dy(THF) tetraédricos y (η5-Cp)3Pr(NCM3)2 (grupos
MeCN axiales) bipiramidal trigonal. Los complejos (η5-C5Me5)3Sm y (η5-C5Me5)3Nd
son reductores de un electrón: (η5-C5Me5)3Ln reduce Ph3P=Se a PPh3 y forma (η5C5Me5)2Ln(µ-Se)nLn(η5-C5Me5)2 (Ln= Sm, n= 1; Ln= Nd, n= 2) y (C5Me5)2. La
capacidad reductora se atribuye a la fuerte congestión estérica en (η5- C5Me5)3Ln,
siendo el agente reductor el ligando [C5Me5]-.
Alterando la proporción LnCl3:NaCp en la reacción 24.21, pueden aislarse (η5C5H5)2LnCl y (η5-C5H5)LnCl2. Si embargo, los datos cristalográficos revelan
estructuras más complejas de la que sugieren estas fórmulas: por ejmplo, (η5C5H5)ErCl2 y (η5-C5H5)YbCl2 cristalizan a partir de THF como aductos 24.5, (η5C5H5)2YbCl y (η5-C5H5)ErCl son díméricos (Fifura 24.4a) (η5- C5H5)2DyCl consiste en
cadenas poliméricas (Figura 24.4b).
Los Esquemas 24.22 y 24.23 muestran algunas reacciones de [(η5-C5H5)2LuCl]2 y [(η5C5H5)2YbCl]2; los disolventes de coordinación a menudo se incorporan a los productos
y pueden ocasionar la ruptura de puentes como en la Reacción 24.24.
14
Los compuestos del tipo (η5-Cp)2LnR (aislados como aductos de THF) pueden
prepararse directamente a partir de LnCl3, por ejemplo para Lu en la Reacción 24.25.
LuCl3 + 2NaCp + LiR
(η5-Cp)2LuR (R= CH2Ph, CH2tBu,4-MeC6H4
(24.25)
El uso del ligando pentametilciclopendienilo (más impedido estéricamente que el
ligando [C5H5]-) en la química organolantánida ha desempeñado un papel fundamental
en el desarrollo de este campo (véase Cuadro 24.5). Se ha visto que el aumento del
impedimento estérico del ligando [C5R5]- estabiliza los derivados de los primeros
metales lantánidos. Por ejemplo, la reacción de Na[C5HiPr4] con YbCl3 en 1,2dimetoxietano (DME) conduce a la formación del complejo monomérico 24.6.
Por el contrario, la reacción de LaCl3 o NdCl3 con dos equivalentes molares de
Na[C5HiPr4] en THF seguida de recristalización en Et2O conduce a complejos 24.7,
caracterizados en estado sólido. En estas especies diméricas, hay una asociación entre
los iones [(η5-C5HiPr4)2MCl2]- y Na+ solvatado.
Los metalocenos de lantánido(II) para Sm, Eu e Yb se conocen desde la década de 1980
y se estabilizan usando el ligando voluminoso [C5Me5]- (Ecuaciones 24.26-24.28): los
productos se obtienen como solvatos; los metalocenos sin solvatar tienen estructuras
angulares en estado sólido (Figura 24.4c) en lugar de un estructura tipo ferroceno. Para
Sm, Eu e Yb el método más conveniente para obtener (η5-C5Me5)2Ln parte de
LnI2.THF.
15
2Na[C5Me5] + YbCl2
2K[C5Me5] + SmI2
2 C5Me5H + Eu
(η5-C5Me5)2Yb + 2NaCl
(η5--C5Me5)2Sm + 2KI
(η5-C5Me5)2Eu + H2
(24.26)
(24.27)
(24.28)
El primer complejo organometálico de Tm(II) se conoción en 2002. Su estabilización
require un sustituyente C5R5 con más impedimento estérico que el necesario para los
metalocenos de Sm(II), Eu(II) e Yb(II). La Reacción 24.29 muestra la síntesis de {η5C5H3-1,3-(SiMe3)2}2Tm(THF) y el uso de una atmósfera de argón resulta esencial. La
Reacción 24.30 es un ejemplo de los efectos que tiene en la reacción utilizar el ligando
[C5Me5]- en lugar de [C5H3-1,3-(SiMe3)2]-.
16
Derivados bis(areno)
La condensación conjunta a 77 K de 1,3,5-tBu2C6H3 con vapores metálicos de Ln da los
derivados bis(areno) (η6-1,3,5-tBu3C6H3)2Ln. Los complejos son térmicamente estables
para Ln= Nd, Tb, Dy, Ho, Er y Lu, pero instables para Ce, Eu, Tm e Yb.
Complejos que contienen el ligando η8-ciclooctatetraenilo
En el capítulo 23 se describieron los complejos organometálicos sándwich y mediosandwhich que contiene ligandos con enlace π de hapticidad ≤7, por ejemplo [(η7C7H7)Mo(CO)3]+. El mayor tamaño de los lantánidos permite la formación de complejos
sándwich con el ligando plano, octogonal [C8H8]2- (véase Ecuación 24.52). Los cloruros
de lantánido(III) reaccionan con K2C8H8 para dar [(η8-C8H8)2Ln]- (Ln= La, Ce, Pr, Sm,
Tb, Yb). El cerio forma también (η8-C8H8)2Ce (24.8), un análogo del uranoceno (véase
Sección 24.11) y para lantánidos con un estado de oxidación estable +2, son aislables
las sales de K+ de [(η8-C8H8)2Ln]2- (Ln= Sm, Eu, Yb).
9.- Metales actínidos
El hecho de que todos salvo dos de los metales actínidos sean artificiales (véase Sección
24.5) afecta a la amplitud en la que se conocen sus propiedades y esto se diferencia en la
diferente cantidad de información que se proporciona para cada metal. La inestabilidad
de los actínidos con respecto a la desintegración radiactiva ya se ha mencionado y en la
Tabla 24.4 se recogen datos sobre los isótopos de vida más larga para cada elemento.
Todos los actínidos son muy tóxicos, siendo extremadamente peligrosa la ingestión de
emisores α de vida larga tales como 231Pa; las dosis letales son pequeñísimas.
17
El actino es un metal blando que brilla en la oscuridad. Se oxida fácilmente a Ac2O3 en
aire húmedo y desprende H2 del H2O. El torio es relativamente estable en el aire, pero es
atacado lentamente por el H2O y rápidamente por el vapor o el HCl diluido. Al
calentarlo, Th reacciona con H2 para dar ThH2, con halógenos para dar ThX4 y con N2 y
C para dar nitruros y carburos; forma aleaciones con una variedad de metales (por
ejemplo, ThZn2, CuTh2). El protactinio es dúctil y maleable, no se corroe en el aire,
pero reacciona con O2, H2 y los halógenos al calentar (Esquema 24.31) y con HF, HCl y
H2SO4 concentrados.
O 2, ∆
Pa
Pa2O5
H 2, ∆
PaH3
I 2, ∆
PaI5
(24.31)
El uranio experimenta corrosión en el aire; le ataca el agua y los ácidos diluidos pero no
los álcalis. El Esquema 24.32 da una selección de reacciones. Con O2 se produce UO2
pero al calentar se forma U3O8.
H 2, ∆
U
UH3
F2, D
UF6
Cl2, D
UCl4 + UCl5 + UCl6
H2O, 373 K
UO2
(24.32)
El neptunio es un metal reactivo que se empaña rápidamente en el aire. Reacciona con
ácidos diluidos desprendiendo H2, pero no le atacan los álcalis. A pesar de que la masa
crítica (véase Sección 2.5) de plutonio es < 0.5 Kg y de que es muy tóxico, su
utilización como combustible nuclear y explosivo hace que sea un elemento muy
estudiado. Reacciona con O2, vapor y ácidos pero es inerte frente a los álcalis; al
calentar, Pu se combina con muchos no metales para dar, por ejemplo, PuH2, PuH3,
PuCl3, PuO2, Pu3C2. El americio es un emisor α y γ muy intenso. Se empaña lentamente
en aire seco, reacciona con vapor y ácidos y al calentar forma compuestos binarios con
una serie de no metales. El curio se corroe rápidamente en el aire; solo pueden
manejarse cantidades mínimas (< 20 mg en condiciones controladas). Berquelio y
californio se comportan de manera similar al Cm y son atacados por el aire y los ácidos,
pero no por álcali. El curio y los últimos elementos se manejan solo en laboratorios de
investigación especializados.
En las secciones que quedan nos centraremos en la química de torio y uranio (los
actínidos para los cuales se ha desarrollado una química más extensa) y plutonio. Los
diagramas de potencial para Np, Pu y Am se incluyen en la Figura 24.6.
18
10.- Compuestos inorgánicos y complejos de coordinación de torio, uranio y
plutonio
Torio
La química del torio se refiere en gran mediada a Th(IV) y, en disolución acuosa, no
hay pruebas de ningún otro estado de oxidación. El valor de E0 para el par Th4+/Th es –
1.9 V.
Los haluros de torio(IV) se preparan por combinación directa de los elementos. ThF4,
ThCl4 y ThBr4, blancos, y ThI4, amarillo, cristalizan en redes en las cuales Th(IV) tiene
coordinación 8. La reacción de ThI4 con Th da ThI2 y ThI3 (ambos polimórficos) que
son conductores metálicos y se formulan como Th4+(I-)(e-)2 y Th4+(I-)3(e-),
respectivamente. El fluoruro de torio(IV) es insoluble en agua y en disoluciones acuosas
de fluoruros de metales alcalinos, pero puede preparase un gran número de fluoruros
dobles o complejos por combinación directa de sus constituyentes. Su estructura es
complicada, por ejemplo [NH4]3[ThF7] y [NH4][ThF8] contienen cadenas infinitas de
[ThF7]n3n- que consisten en Th(IV) prismático trigonal con tres topes, compartiendo
lados. El cloruro de torio(IV) es soluble en agua y se conocen una serie de sales que
contienen unidades [ThCl6]2- octaédricas, discretas (Reacción 24.33).
ThCl4 + 2MCl
M2ThCl6
Por ejemplo M= K, Rb, Cs
(24.33)
El ThO2 blanco se obtiene por descomposición térmica de Th(ox)2 o Th(NO3)4 y adopta
una red de CaF2 (Figura 5.18). Precipita en disolución neutra o incluso débilmente
ácida. Hoy en día, el ThO2 tiene aplicación como catalizador de Fischer-Tropsch, pero
la propiedad de emitir un resplandor azul al calentarlo condujo a su anterior uso para
mantas de gas incandescentes. Como era de esperar por su elevada carga formal en el
centro metálico, las disoluciones acuosas de las sales de Th(IV) contienen productos de
hidrólisis como [ThOH]3+, [Th(OH)2]2+. La adición de álcali a estas disoluciones da un
precipitado blanco gelatinoso de Th(OH)4 que se convierte en ThO2 a > 700 K.
Los complejos de coordinación de Th(IV) exhiben de modo característico números de
coordinación elevados y prefieren dadores duros tales como oxígeno, por ejemplo:
- coordinación 12: [Th(NO3,O,O’)6]2- (Figura 24.5), [Th(NO3-O,O’)5(OPMe3)2]-;
- coordinación 10: [Th(CO3-O,O’)5]6-;
- coordinación 9 (prismática trigonal con tres topes): [ThCl2(H2O)7]2+;
- coordinación 8 (dodecaédrica): [ThCl4(OSPh2)4], α-[Th(acac)4], [ThCl4(THF)4];
- coordinación 7 (antiprismática cuadrada): β-[Th(acac)4];
- coordinación 8 (cúbica): [Th(NCS-N)8]4-;
- coordinación 7: [ThCl4(NMe3)3].
19
Los números de coordinación más bajos pueden estabilizarse utilizando ligandos amida
o ariloxi. En la Reacción 24.34, los ligandos bis(silil)amida son demasiado voluminosos
para permitir la sustitución del último grupo cloro. Las Reacciones 24.35 y 24.36 ponen
de manifiesto que el control estérico establece si Th(OR) se establiza con o sin otros
ligandos en la esfera de coordinación
ThCl4 + 3LiN(SiMe3)2
TLC{N(SiMe3)2}3 (tetraédrico) + 3LiCl
(24.34)
piridina/THF
ThI4 + 4KOtBu
cis-Th(py)2(OtBu)4 (octaédrico) + 4KCl
(24.35)
t
t
ThI4 + 4KOC6H3-2,6 Bu2
Th(O C6H3-2,6 Bu2)4 (tetraédrico) + 4KI (24.36)
Uranio
El uranio presenta estados de oxidación de +3 a +6, aunque los más comunes son U(IV)
y U(VI). El punto de partida clave para la preparación de muchos compuestos de uranio
es el UO2 y el Esquema 24.37 muestra la síntesis de fluoruros y cloruros. El Fluoruro
UF5 se preprara por reducción controlada de UF6 pero se desproporciona rápidamente a
UF4 y UF6.
El hexafluoruro de uranio es un sólido incoloro, volátil, con una presión de vapor de 1
bar a 329 K; es de gran importancia en la separación de los isótopos de uranio (véase
Sección 2.5). El sólido y el vapor consisten en moléculas UF6 octaédricas (U-F= 199
pm). El hexafluoruro se hidroliza inmediatamente en H2O (Ecuación 24.38) y es un
20
agente de fluoración potente. El tratamiento de UF6 con BCl3 da UCl6 molecular,
inestable.
UF6 + H2O
UOF4 + 2HF
(24.38)
El UF4 verde, moderadamente soluble, es un sólido inerte (pf 1309 K) con una
estructura de red que contiene U(IV) de coordinación 8. El UCl4 sólido contiene U de
coordinación 8, pero UCl5 es un dímero (24.9); este último se desproporciona al
calentar. Los haluros aceptan X- para dar complejos como NaUF7, Cs2UCl6 y
[NH4]UF8; las sales de los metales alcalinos adoptan estructuras de red con
interacciones U-F-U que dan U en entornos de coordinación elevados.
El óxido UO3 es polimórfico y todas las formas se descomponen en el estado de
oxidación mixto U3O8 al calentar. La mayor parte de los ácidos disuelven el UO3 para
dar soluciones amarillas que contienen el ión uranilo (24.10), en forma de complejo; por
ejemplo en disolución acuosa 24.20 existe como acuoión y se ha asilado la sal de
perclorato [UO2(H2O)5]2+, bipiramidal pentagonal. El ión [UO2]2+ también está presente
en muchos compuestos sólidos, entre ellos uranatos alcalinotérreos (por ejemplo
BaUO4) que están mejor descritos como óxidos metálicos mixtos. Las sales de uranilo
de
los
óxoácidos
incluyen
[UO2][NO3]2.6H2O
(véase
Cuadro
6.3);
[UO2][MeCO3]2.2H2O y [UO2][CF3SO3]2.3H2O y la coordinación de los oxoaniones y
el agua colocan normalmente el centro de U(IV) en un ambiente de coordinación 7 u 8,
como en 24.11 y 24.12. En disolución acuosa, el ión [UO2]2+ se hidroliza parcialmente a
especies como [U2O5]2+ u [U3O8]2+. En disolución acuosa alcalina, las especies
presentes dependen de la concentración de [UO2]2+ y [OH]-. La investigación de los
complejos formados entre [UO2]2+ y [OH]- es difícil por la precipitación de U(VI) en
forma de sales como Na2UO4 y Na2U2O7. Sin embargo, si se utiliza Me3NOH en lugar
de un hidróxido de metal alcalino, se pueden aislar sales de trans-[UO2(OH)4]2octaédrico. El ión [UO2]2+ es duro y forma un complejo más estable con F- que con los
últimos haluros. La Figura 24.6 da un diagrama de potencial para el uranio a pH= =. La
21
reducción de [UO2]2+ da en primer lugar [UO2]+, que es algo inestable con respecto a la
Reacción de desproporcionación 24.39. Como en esta reacción intervienen los protones,
la posición del equilibrio depende del pH. El uranio(V) puede estabilizarse con respecto
a la desproporción formando un complejo con F-, com [UF6]-.
2[UO2]2+ + 4H+
[UO2]2+
+ U4+ + 2H2O (24.39)
El uranio metal desprende H2 de los ácidos para dar U3+, de color Burdeos, que es un
reductor potante (Figura 24.6). El ión U4+ se oxida rápidamente a [UO2]2+ con Cr(VI),
Ce(IV) o Mn(VII), pero la oxidación con aire es lenta. Los pares redox U4+/U3+ y
[UO2]2+ /[UO2]+ son reversibles, pero el par [UO2]+/U4+ no lo es: los dos primeros
suponen solo tranferencia de electrones, pero el último par implica una reorganización
estructural alrededor del centro metálico.
Mientras que la química de coordinación del torio se ocupa solo del estado de oxidación
+4, la del uranio trata de los estados de oxidación +3 a +6. Para U(IV), en general está
presente la unidad lineal [UO2]2+ en el complejo y son normales los complejos transoctaédrico, bipiramidal trigonales y bipiramidal-hexagonales: para otros estados de
oxidación, el poliedro de coordinación está determinado esencialmente por lo requisitos
espaciales de los ligandos más que por los factores electrónicos y el tamaño grande del
centro de U permite que se alcancen números de coordinación elevados. Los complejos
con diferentes estados de oxidación y números de coordinación incluyen:
- coordinación 14: [U(η3-BH4)(THF)2];
- coordinación 12: [U(NO3-O,O’)6]2-; [U(η3-BH3Me)4];
- coordinación 11: [U(η3-BH4)2(THF)5]+;
- coordinación 9: [UCl3(18-corona-6)]+; [UBr2(H2O)5(MeCN) 2]+, [U(H2O)(ox)4]4-;
22
- coordinación 8: [UCl3(DMF)5]+, [UCl(DMF)7]3+, [UCl2(acac)2(THF)2], [UO2(18corona-6]2+; [UO2(NO3-O,O’)2(NO3-O)2]2+, [UO2(η2-O2)3]4-;
- coordinación7/: UO2Cl2(THF)3, [UO2Cl(THF)4]+, [UO2(OS-Me2)5]2+;
- coordinación 6: trans-[UO2Cl4]2-.
Números de coordinación más bajos se observan en derivados alcoxi con sustituyentes
impedidos estéricamente, por ejemplo U(OC6H3-2,6-tBu2)4 (preparación análoga a la
Reacción 24.36). El complejo de U(III) U(OC6H3-2,6-tBu2)3 es probablemente
monomérico; se oxida a UX(OC6H3-2,6-tBu2)3 (X= Cl, Br, I; oxidabte= PCl5, CBr4, I2,
respectivamente) en el cual se ha confirmado U(IV) tetraédrico para X= I. Los
disolventes de coordinación suelen conducir a un aumento en el número de
coordinación, como en la Reacción 24.40.
Plutonio
Los estados de oxidación de +3 a +7 están disponibles para el plutonio, aunque el estado
+7 se conoce solo para unas pocas sales, por ejemplo Li5PuO6 se ha preprarado por
calentamiento de Li2O y PuO2 en O2. De ahí que el diagrama de potencial de la Figura
24.6 muestre solo estados de oxidación de +3 a +6. En la química del estado de
oxidación +6 predomina [PuO2]2+, si bien éste es menos estable con respecto a la
reducción que [UO2]2+. El óxido más estable es PuO2, formado al calentar en aire los
nitratos o hidróxidos de Pu en cualquier estado de oxidación. Aunque Pu forma PuF6, se
descompone en PuF4 y F2 a diferencia de la relativa estabilidad del UF6. El cloruro
binario más elevado de Pu es PuCl3 aunque puede formarse Cs2[PuIVCl6] a partir de
CsCl, PuCl3 y Cl2 a 320 K.
En disolución acuosa, [PuO2]2+ es termodinámicamente inestable (pero por poco) con
respecto a la reacción de desproporción 24.41.
2[PuO2]+ (aq) + 4H+(aq)
[PuO2]2+ (aq) + Pu4+(aq) + 2H2O
(21.41)
La proximidad de los tres primeros potenciales de reducción en la reducción de [Pu
O2]2+ (Figura 24.6) es importante. Si se disuelve PuO2 en un exceso de HClO4 (un
ácido que contiene un anión de coordinación muy débil) a 298 K, la disolución en el
equlibrio contienen Pu(III), Pu(IV) y Pu(VI). En los sistemas redox en los que
interviene Pu, sin embargo, el equilibrio no siempre se alcanza rápidamente, Como el
uranio, los pares que implican solo transferencia de electrones (por ejemplo, [PuO2]2+
/[PuO2]+) son rápidamente reversibles, pero los que suponen también transferencia de
oxígeno (por ejemplo, [PuO2]+/Pu4+) son más lentos. Ya que la hidrólisis y la formación
de complejos (cuya extensión aumenta al aumentar la extensión de la carga iónica, es
decir, [PuO2]+ < [PuO2]2+ < Pu3+ < Pu4+) pueden complicar también la situación, el
23
estudio de los equilibrios y de la cinética en disolución de los compuestos de plutonio es
difícil.
El método clásico de acceder a la química del plutonio es disolver el metal en HCl,
HClO4 o HNO3 acuoso. Esto genera una disolución que contiene Pu(III). Sin embargo,
los iones cloruro y nitrato tiene potencial para coordinarse al centro metálico y mientras
que [ClO4]- se coordina solo débilmente (véase más arriba), las sales de perclorato
tienen el inconveniente de ser potencialmente explosivas. Un enfoque reciente es
disolver Pu metal en ácido trifílico (ácido trifluorosulfónico, CF3SO3H) para dar Pu(III)
como la sal cristalina y aislable [Pu(H2O)9][CF3SO3]3. En estado sólido, [Pu(H2O)9]3+
tiene una estructura prismática trigonal con tres topes, con distancias de enlace Pu-O de
247.6 (prisma) y 257.4 pm (tope).
11.- Complejos organometálicos de torio y uranio
Aunque los complejos organometálicos se conocen para todos los primeros actínidos,
los compuestos de Th y U superan ampliamente los de los otros metales. Además de las
propiedades radiactivas, los organoactínidos son sensibles al aire y se requiere
manejarlos en atmósfera inerte.
Complejos con enlace σ
Al principio hubo alguna dificultad en preparar complejos homolépticos de alquilo o
arilo con enlace σ de los actínidos, pero (como para los lantánidos, Sección 24.8) el uso
del quelato TMED (Me2NCH2CH2NMe2) fue la clave para estabilizar la sal de Li+ de
[ThMe7]3- (Ecuación 24.42 y Figura 24.7a). De manera análoga se han aislado
hexaalquilos del tipo Li2UR6.7TMED.
Et2O, TMED
ThCl4 + exceso MeLi
[Li(TMED)]3[ThMe7]
(24.42)
24
Los grupos alquilo voluminosos son también una influencia estabilizadora como pone
de manifiesto el aislamineto de U{CH(Si-Me3)2}3 (Reacción 24.13) aunque la
desviación de la planaridad puede ser debida a efectos de empaquetamiento cristalino.
U(OC6H3-2,6tBu2)3 + 3LiCH(SiMe3)2
U{CH(Si-Me3)2}3 + 3LiO C6H3-2,6tBu2
(24.43)
Los derivados alquilo son más estables si el metal actínido está unido a ligandos
ciclopentadienilo y las reacciones 24.44-24.46 muestran métodos generales de síntesis
donde M= Th o U.
Et2O
5
(η5-Cp)3MR + LiCl
(η -Cp)3MCl + RLi
(24.44)
THF
(η5-Cp)3MCl + RMgX
(η5-Cp)3MR + MgClX
(η5-C5Me5)2MCl2 + 2RLi
(24.45)
Et2O
(η5-C5Me5)2MR2 + 2LiCl (24.46)
Derivados de ciclopentadienilo
Los derivados de ciclopentadienilo son abundantes entre los complejos organometálicos
de Th(IV), Th(III) y U(III) y las Reacciones 24.47-24.50 dan métodos de síntesis para
las principales familias de compuestos (M= Th, U).
C6H6
(η5-Cp)4M + 4KCl
MCl4 + 4KCp
(24.47
THF
MX4 + 3NaCp
(η5-Cp)3MX + 3NaX X= Cl, Br, I
(24.48)
THF
MX4 + TlCp
(η5-Cp)MX3(THF)2 + TlX
X= Cl, Br
(24.49)
THF
(η5-Cp)3MCl + NaC10H8
(η5-Cp)3M(THF) + NaCl + C10H8
(NaC10H8= naftaleno de sodio)
(24.59)
Los compuestos del tipo (η5-Cp)2MX2 son normalmente susceptibles a una reacción de
redistribución como la 24.51 a no ser que estén impedidos estéricamente como en (η5C5Me5)2ThCl2 y (η5-C5Me5)2UCl2.
2(η5-Cp) 2UCl2
(η5-Cp)3UCl + (η5-Cp)UCl3(THF)2
(24.51)
(η5-Cp)4Th incoloro y (η5-Cp)4U rojo son monoméricos en estado sólido con
estructuras pseudotetraédricas, 24.14 (Th-C 287 pm, U-C= 281 pm). Se observan
también estructuras tetraédricas para derivados (η5-Cp)3MX y (η5-Cp)3M(THF),
mientras que (η5-Cp)MX3(THF)2 es octaédrico. Cómo describir el enlace metal-ligando
en estos y otros derivados Cp de los actínicos es tema de debate teórico. El panorama
actual sugiere la intervención de los orbítales atómicos 6d del metal, estando los
orbitales 5f prácticamente sin perturbar; los efectos relativistas (véase Cuadro 12.2)
también apoyan el papel en el enlace de los orbitales atómicos 6d y no los 5f. las
contribuciones covalentes al enlace parecen estar presentes en los complejos
ciclopentadienilo de Th(IV) y U(IV), pero para Th(III) y U(III) se propone que el enalce
es fundamentalmente iónico.
25
Pueden prepararse una serie de especies organometálicas partiendo de (η5-Cp)3ThCl y
(η5-Cp)3UCl y la Figura 24.8 muestra reacciones seleccionadas de (η5-Cp)3UCl. El
complejo heterometálico (η5-Cp)3UFe(CO)2(η5-Cp) contiene un enlace U-Fe sin puente.
Complejos que contienen el ligando η8-ciclooctatrienilo
Como hemos visto, los centros grandes U(IV) y Th(IV) acomodan hasta cuatro ligandos
η5-Cp- y no se observan complejos tipo ferroceno. Sin embargo, con el ligando de gran
tamaño [C8H8]2- (Reacción 24.52) se forman complejos sándwich por la Reacción
24.53.
MCl4 + 2K2C2H8
(η8-C8H8)2M + 4KCl
M= Th, U
(24.53)
(η8-C8H8)2U (uranoceno), verde y (η8-C8H8)2Th (toroceno), amarillo, son
isoestructurales (figura 24.7b), promedio Th-C= 270 pm y U-C= 256 pm. El enlace en
26
estos metalocenos es muy estudiado por los teóricos, con argumentos que reflejan los
que se han visto anteriormente para los derivados de ciclopentadienilo. El uranoceno es
inflamable en el aire, pero no reacciona con H2O a 298 K; (η8-C8H8)2Th es sensible al
aire, es atacado por reactivos próticos y explota cuando está al rojo vivo.
La reacción de ThCl4 con (η8-C8H8)2Th en THF da el complejo medio-sandwich (η8C8H8)2ThCl2(THF) 2, 24.15, pero la especie análoga de U(IV) se obtiene por la Reacción
24.54 y el yodo derivado por la reacción 24.55.
THF
UCl4 + C8H8 + 2NaH
(η8-C8H8)UCl2(THF)2 + 2NaCl + H2
(24.54)
THF
(η8-C8H8)2U + I2
(η8-C8H8)UI2(THF) 2 + C8H8
(24.55)
Los haluors son sintones útiles en esta área de la química, por ejemplo Reacciones
24.56 y 24.57.
THF
(η8-C8H8)UCl2(THF)2 + 2NaN(SiMe3)2
(η8-C8H8)U{N(SiMe3)2}2 + 2NaCl
THF
(η8-C8H8)UI2(THF)2 + 3LiCH2SiMe3
[Li(THF)3]+[(η8-C8H8)U{CH2SiMe3}3]-
(24.56)
(24.57)