1 Tema 45.- Traducción del RNA.- Biosíntesis de proteínas. Código
Anuncio

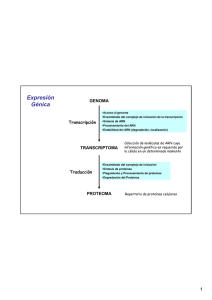
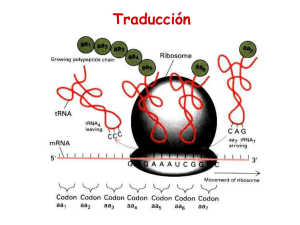
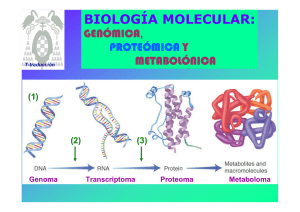
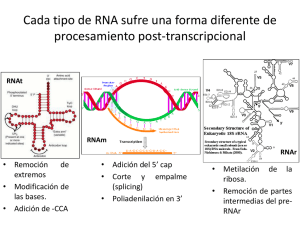
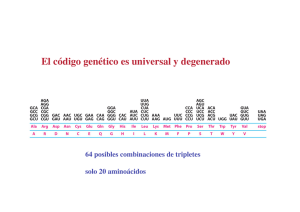
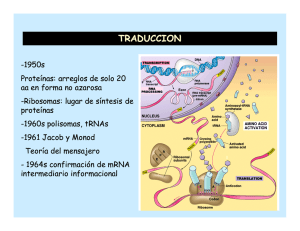
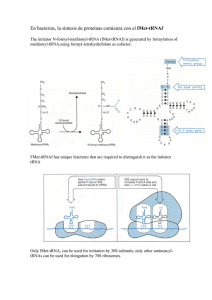
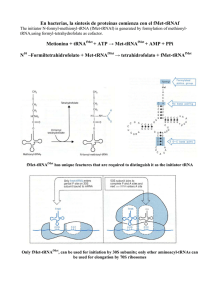
Bioquímica-07 Tema 45.- Traducción del RNA.- Biosíntesis de proteínas. Código genético. Etapas de la traducción. Modificaciones post-traduccionales. Mathews & van Holde.- cap. 27, págs. 1160 y siguientes. Lehninger.- 27, pags. 1034 y siguientes. La biosíntesis de proteínas consiste en la traducción de la información codificada en el RNA mensajero a una secuencia de aminoácidos para sintetizar proteínas y la operación se realiza en un complejo formado por RNA-proteína denominado ribosoma. El alfabeto de cuatro letras de las secuencias nucleotídicas de los Ac. nucleicos se traduce a otro lenguaje distinto, el de los 20 AA en las proteínas. Cada aminoácido viene especificado por unidades de información de tras bases en el mRNA, llamadas codones. La traducción requiere de moléculas adaptadoras, tRNA, que tienen tripletes anticodones, que reconocen los codones complementarios e insertan el AA específico en la posición adecuada en la secuencia polipeptídica. Lectura codón-anticodón Codón: triplete de nucleotidos cuya secuencia es específica para cada AA. Las relaciones de correspondencia entre cada triplete “codón” en el mRNA y cada AA - que se une a su tRNA con el “anticodón” complementario- , constituyen el código genético. Código genético.- Formado por tripletes de nucleotidos (codones) que se relacionan con los AA protéicos. El primer codón que se traduce (codón de inicio, AUG) establece un marco o pauta de lectura, que va a condicionar la secuencia de AA en la proteína. Hay tres codones de terminación o codones sin sentido (UAA, UAG, UGA). El código genético es degenerado, porque un AA puede ser codificado por más de un codón. Cada AA puede tener uno o varios tripletes que lo codifiquen. El balanceo, de la 3ª base, permite que algunos tRNA (anticodón) reconozcan más de un triplete (codón) en el mRNA. Más de 100 macromoléculas intervienen en la traducción, destacan: ribosomas (rRNA y proteínas), t-RNAs, m-RNA, enzimas y factores proteicos. Lugar de la síntesis de proteínas.Hay que estudiar el lugar donde se produce la síntesis de proteínas: los ribosomas. En procariotas los ribosomas tienen un tamaño de 70S y sus dos subunidades son de 30S y 50S. El mRNA se asocia, para ser leido, con la subunidad 30S y después se asocia la subunidad 50S. Cada cadena de mRNA está siendo leída simultáneamente por muchos ribosomas, cada uno sintetizando una copia de la proteina. 1 Bioquímica-07 Etapas de la traducción. 0.- Activación de AA. Consiste en la preparación de los AAs para entrar en la síntesis de proteínas. Se consume 1 ATP por AA. Las aminoacil-tRNA sintetasas catalizan la unión del AA correcto a su tRNA y son específicas para cada AA. Algunos AAs tienen más de un tRNA, pero cada tRNA solo reconoce a un AA. Esta interacción específica entre la aminoacil-tRNa sintetasa y el tRNA constituye un "segundo código genético". Algunas aminoacil-tRNA sintetasas pueden realizar incluso corrección de pruebas. Esquema de un t-RNA + AA____> 1.- Iniciación.- La síntesis de polipéptidos empieza en el extremo amino-terminal y con un AA específico (MET). Complejo de iniciación Este complejo está formado por el mRNA unido a la subunidad ribosómica 30S y al tRNA cargado con dicho MET y asociado por su triplete anticodón con el su triplete de iniciación en el mRNA (AUG). A continuación se une la subunidad 50S que coloca el complejo mRNA(codón)-tRNA(anticodón) cargado en el lugar P del ribosoma. 2.- Elongación.- En el lugar A del ribosoma entra el siguiente tRNA cargado con el AA relativo al triplete siguiente del mRNA; y así situados los dos aminoácidos, en los lugares P y A, se forma el enlace peptídico con la catálisis de la peptidil transferasa. A continuación se produce la translocación, que consiste en el desplazamiento del ribosoma a lo largo del mRNA en sentido 5’ a 3’, de forma que el tRNA 1º quede en el lugar de salida (E), el tRNA 2º quede en el lugar P y el lugar A queda vacio para la entrada de un nuevo tRNA cargado con AA. En el proceso intervienen varias proteínas o factores de elongación (EF-Tu, EF-Ts, EF-G) y también es necesaria la energía en forma de GTP, en varios puntos del proceso (1GTP en iniciación y 2 GTP en elongación). 2 Bioquímica-07 3.- Terminación.- El final de la síntesis de la cadena polipeptídica requiere de una señal especial en los tripletes del mRNA (tripletes sin sentido) y de factores de terminación o liberación (RF). Los tripletes de terminación son: UAA, UAG y UGA Modificaciones post-traducción: plegamiento y maduración de proteínas. Las cadenas polipeptídicas liberadas de los ribosomas se pliegan y sufren modificaciones químicas. Tipos de modificación: - Pérdida de secuencias señal. - Modificaciones amino-terminales y carboxilo-terminales. - Modificaciones en AA concretos. - Unión de cadenas glucídicas. - Modificaciones proteolíticas. - Formación de puentes disulfuro. La fidelidad en la síntesis proteica es energéticamente cara: - Formación de aminoacil-tRNA, 2 ATP - Primer paso de elongación, 1 GTP - Traslocación, 1 GTP La formación de cada enlace peptídico requiere, al menos, 4 ATP . Los polisomas (asociaciones de ribosomas) permiten la traducción múltiple y rápida del mensaje contenido en el m-RNA. puromicina La síntesis de proteinas es inhibida por muchos antibioticos y toxinas. La puromicina es un antibiótico con estructura similar al aminoacil -adenosina del aminoacil-tRNA. Por ello, se acopla en el lugar A de los ribosomas y puede unirse con el grupo carboxilo del péptido en formación, pero la síntesis de la cadena peptídica no puede progresar puesto que la estructura de la puromicina no cuenta con grupo amino terminal para que continúe la síntesis y por tanto la síntesis de la cadena proteica queda interrumpida. 3