Clase 5. Los aminoácidos: Precursores de transmisores. Unidades
Anuncio

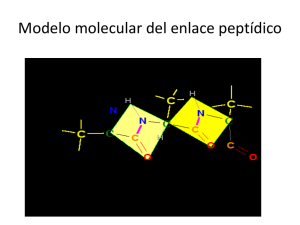
Clase 5. Los aminoácidos: Precursores de transmisores. Unidades de las proteínas. Las enzimas. Los aminoácidos se clasifican en unas pocas categorías diferenciadas, basadas sobre todo en su solubilidad en agua. L os isómeros de una molécula de aminoácido pueden ser representados por dos modelos tridimensionales . Ambos modelos son imágenes espectaculares uno de otro. Los dos isómeros difieren solamente en la dirección en que desvían el plano de la luz polarizada.Un compuesto que hace girar la luz polarizada en el sentido de las agujas del reloj se denomina dextrorrotatorio (+) en oposición al compuesto que es levorrotatorio (-). Los aminoácidos Apolares Polares Básicos Ácidos Los aminoácidos con grupos laterales polares tienden a ubicarse sobre la superficie de las proteínas; al interactuar con el agua posibilitan que las proteínas sean solubles en soluciones acuosas. Por el contrario, los aminoácidos con grupos laterales no polares rechazan el agua y se agrupan para el núcleo insoluble en agua de las proteínas. A pH neutro, arginina y lisina presentan cargas positivas; los ácidos aspártico y glutámico las tienen negativas . Estos cuatro aminoácidos son los principales contribuyentes de la carga global de una proteína. Los enlaces peptídicos conectan los aminoácidos para formar cadenas lineales Las proteínas son las moléculas operadoras de la célula y llevan adelante el programa de actividades codificado por el DNA. Las células contienen una dotación enormemente diversa de moléculas proteicas, cada una de las cuales está constituida por una cadena lineal de aminoácidos unidos entre sí covalentemente Aminoácidos Péptido Polipéptido Proteína Se utilizan muchas denominaciones para designar las cadenas formadas por polímeros de aminoácidos. Los aminoácidos: Por sí solos tienen diversas funciones ejemplo: Precursores de transmisores (hormonas, neurotransmisores). Estructura jerárquica de las proteínas Las proteínas están diseñadas para unirse a cualquier molécula concebible (iones, azúcares, metales…). La configuración espacial de las proteínas, su forma tridimensional, o conformación es fundamental para entender su funcionamiento: la estructura dicta la función. Las proteínas se pliegan en una conformación de menor energía. La estructura plegada final, o conformación, que adopta cualquier cadena polipeptídica es regida por aspectos energéticos: una proteína generalmente se pliega en la forma en la cual la energía libre disminuye. Cada proteína se pliega normalmente en una única conformación estable. Sin embargo, esta conformación a menudo cambia ligeramente cuando la proteína interactúa con otras moléculas en la célula. Ese cambio en la forma es crucial para la función de la proteína. Aunque una cadena proteica puede plegarse en su conformación correcta sin ayuda externa, el plegamiento de una proteína en una célula viva generalmente es asistido por proteínas especiales denominadas moléculas chaperonas. Estas proteínas se unen a cadenas parcialmente plegadas y las ayudan a plegarse a lo largo de la vía energéticamente más favorable. Las Proteínas: Niveles de organización La forma de las proteínas está dada por cuatro niveles estructurales 1. Estructura primaria 2. Estructura secundaria 3. Estructura terciaria 4. Estructura cuaternaria Estructura primaria: Secuencia de los aminoácidos a-b-a-a-c-b-b-c-c-d-d a-a-b-d-d-a-b-b-c-c-c 3a, 3b,3c, 2d Cada tipo de proteína tiene una secuencia determinada de aminoácidos que determina tanto su forma tridimensional como su actividad biológica Estructura secundaria: Puentes de hidrógeno 1. Hoja plegada. Lámina β 1. 2. α-hélice En una proteína promedio, el 60% de la cadena polipeptídica se encuentra como las dos estructuras secundarias regulares: hélice α y lámina β; el resto de la molécula aparece como arrollamiento al azar y giros. Los MOTIVOS son agrupaciones regulares de estructuras secundarias. Ejemplo: Motivo en dedo de zinc (típico de proteínas que se unen ácidos nucleícos) Estructura terciaria : Fuerzas hidrófobas entre las cadenas laterales no polares y, en algunas proteínas, por medio de enlaces disulfuro. Los DOMINIOS estructurales y funcionales son módulos de estructura terciaria Estructura cuaternaria : Formadas por más de una cadena peptídica unidas por enlaces no covalentes. A cada cadena se le llama subunidad y se le da el nombre de una letra griega. Varias subunidades Si una proteína se pliega mal no sólo conduce a una pérdida de su función normal, sino que además es una marca para la degradación proteolítica. La posterior acumulación de fragmentos proteolíticos contribuye a enfermedades degenerativas caracterizadas por la presencia de placas insolubles en distintos órganos. Ejemplo, la enfermedad de Alzheimer y la enfermedad de Huntington. La enfermedad de Alzheimer se caracteriza por la aparición de placas y ovillos en el cerebro en proceso de deterioro. Los filamentos que componen estas estructuras derivan de la proteolísis de abundantes proteínas naturales, como la precursora amiloide, una proteína transmembrana, y Tau, una proteína fijadora de microtúbulos. Actividad 5.1 Representa el tripéptido: Glu-Tyr-Trp (ácido glutámico-tirosina-triptófano) Representa el dipéptido: Cys-Cys (Cisteína-Cysteína) con un enlace disulfuro FUNCIONES GENERALES DE LAS PROTEÍNAS. Las proteínas están diseñadas para unirse a gran cantidad de moléculas o ligandos, con un alto grado de especificidad . Ejemplo las enzimas. Muchas proteínas contienen grupos prostéticos fuertemente unidos. Grupos protético: Pequeña molécula no peptídica o un metal que se une firmemente a la proteína y la mantiene en una conformación fija, mientras participa en la unión con ligandos. Ejemplo, el fe en la hemoglobina Las enzimas son proteínas que primero se unen íntimamente a moléculas determinadas, llamadas sustratos, y luego catalizan en esta moléculas la formación o la rotura de enlaces covalentes. En el lugar activo de la enzima PROTEINAS ESTRUCTURALES. Función: Función proporcionar soporte mecánico a las células y tejidos. Ejemplos: Ejemplos colágeno y elastina. Triple hélice de tropocolágeno PROTEINAS DE TRANSPORTE. Función: Función transportar moléculas pequeñas o iones. Ejemplos: Ejemplos albúmina, hemoglobina, canales iónicos, bombas iónicas... PROTEINAS MOTORAS. Función: generar movimientos en las células y tejidos. Ejemplos: la miosina, actina. PROTEINAS DE DEPOSITO. Función: Función almacenar pequeñas moléculas o iones. Ejemplo: Ejemplo el hierro se almacena en el hígado. PROTEINAS DE SEÑALIZACIÓN. Función: transmitir señales de una célula a la otra. Ejemplo: hormonas y factores de crecimiento, neurotransmisores. Endorfinas, sustancia P… Hormona del crecimiento, Insulina… Factor de crecimiento nervioso… PROTEINAS RECEPTORAS. Función: detectar señales y transmitirlas a la maquinaria de respuesta de la célula. Ejemplo: la rodopsina en la retina detecta la luz. PROTEINAS REGULADORAS GÉNICAS. Función: unirse al DNA para activar o desactivar genes. Ejemplo: el represor de la lactosa en las bacterias silencia a los genes para las enzimas que degradan al azúcar lactosa. La vida media de las proteínas celulares varía desde unos minutos (ejm: ciclinas) hasta toda la vida (ejm: las proteínas del cristalino del ojo)