Problemas sobre fármacos cardiovasculares 1.-
Anuncio
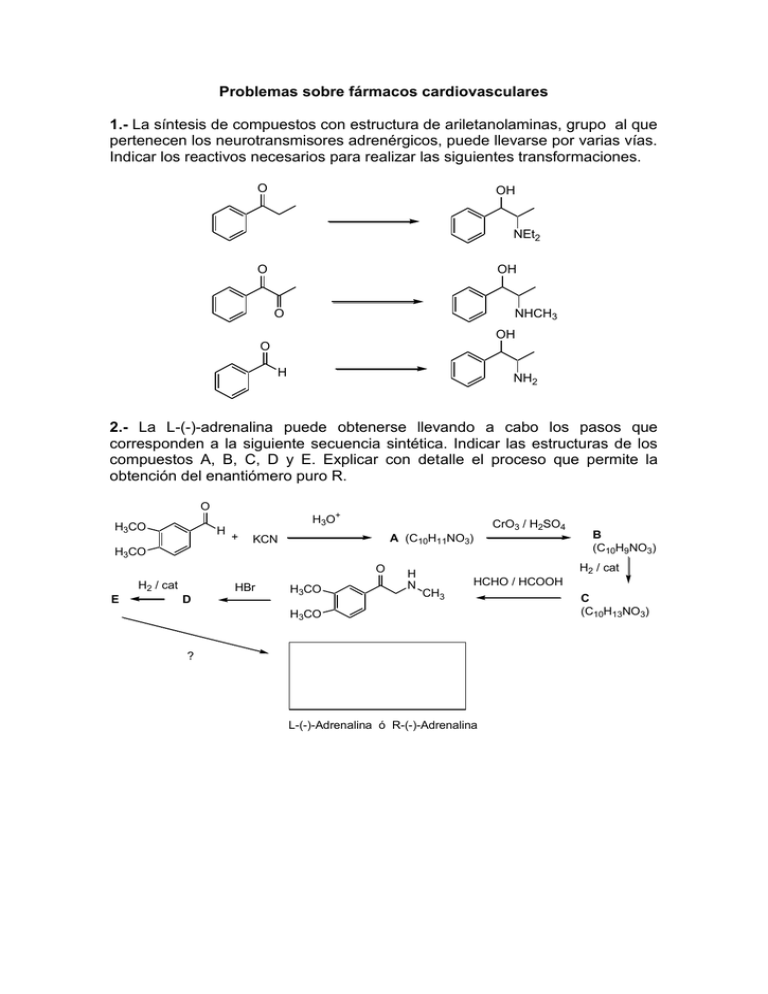
Problemas sobre fármacos cardiovasculares 1.- La síntesis de compuestos con estructura de ariletanolaminas, grupo al que pertenecen los neurotransmisores adrenérgicos, puede llevarse por varias vías. Indicar los reactivos necesarios para realizar las siguientes transformaciones. O OH NEt2 O OH O NHCH3 OH O H NH2 2.- La L-(-)-adrenalina puede obtenerse llevando a cabo los pasos que corresponden a la siguiente secuencia sintética. Indicar las estructuras de los compuestos A, B, C, D y E. Explicar con detalle el proceso que permite la obtención del enantiómero puro R. O H3CO H H3O+ + CrO3 / H2SO4 A (C10H11NO3) KCN H3CO O H2 / cat E HBr D H3CO H N B (C10H9NO3) H2 / cat HCHO / HCOOH CH3 H3CO ? L-(-)-Adrenalina ó R-(-)-Adrenalina C (C10H13NO3) 3.- Completar la siguiente secuencia sintética conducente al fármaco adrenérgico R-(-)-salbutamol con actividad broncodilatadora. O O H3CO2C H3CO2C ? PhCH2Br CH3 CH3 A Base HO PhH2CO (CH3)3CNH2 i) äcido (+)-tartárico ii) cristalización LiAlH4 C R-C B ? OH H N H3CO2C C(CH3)3 HO R-(-)-salbutamol Indicar sobre qué tipo de receptores adrenérgicos actúa el salbutamol. 4.- La prenilamina pertenece al grupo estructural de las 3-arilpropilaminas, posee actividad como vasodilatador coronario y se usa como antianginoso. La síntesis del mismo se lleva a cabo a través de la siguiente secuencia sintética. Indique las estructuras de los compuestos A, B, C, D y E, así como la estructura de la prenilamina. ¿La prenilamina así obtenida, es enantioméricamente pura?. i) PhMgBr Base + + ii) H3O A O H H B C18H17NO2 CN CO2Et i) NaOH, H2O ii) HCl iii) Calor CH3 Prenilamina (C24H27N) H2 / cat O E H2 / cat D C15H17N C C15H13N ¿A qué se debe la acción vasodilatadora de este fármaco?. 5.- El bitartrato de metaraminol que se obtiene mezclando soluciones equimoleculares de ácido (+)-tartárico y (-)-(1R,2S)-metaraminol(1), es un potente vasoconstrictor. En su síntesis se parte de 1-(3-hidroxifenil)-1propanona(2) y mediante las etapas indicadas en el esquema se llega a la obtención de una mezcla de estereoisómeros. Proponer estructuras para los productos intermedios A, B, C y D. Explicar la estrategia a seguir para obtener el isómero (1R,2S) puro. O CH3 HNO2 PhCH2Cl A H2 B (C16H15NO3) Na2CO3 C (C16H17NO2) Ni Raney OH H2 / Ni Raney ? (-)-(1R,2S)-metaraminol D (C9H13NO3) ¿A qué es debida la acción vasoconstrictora? Comente las características estructurales de este grupo de fármacos y su relación con la actividad. 6.- La cinarizina (1) es un bloqueante de los canales de calcio que se usa como vasodilatador. Desarrolle una secuencia sintética para (1) empleando entre otros los siguientes compuestos. H N O Cl N N N H O H cinarizina (1) 7.- El captopril es un peptidomimético inhibidor de ECA con utilidad como antihipertensor. Se sintetiza a partir del aminoácido L-prolina y se requiere de protección del grupo carboxilo y del tiol. O N H + COOH Cl ? OCH2Ph COO C(CH3)3 N bencilcarbamato PhH2CO O ? + Base (S)-captopril i) separación diastereómeros ii) NH3 / CH3OH H3C O COOH N S O CH3 F3CCOOH H3C O COO C(CH3)3 N S O CH3 a) Complete la secuencia de su síntesis y comente los grupos protectores usados y los métodos de desprotección b) Proponga un método de separación de la mezcla de estereoisómeros para la obtención del captopril ópticamente puro. c) ¿Se podría evitar la etapa de separación de la mezcla de estereoisómeros sin renunciar a obtener el estereoisómero puro del captopril?. 8.- La preparación de 1,4-dihidropiridinas sustituidas de forma no simétrica se puede llevar a cabo a través de una modificación de las condiciones originales de Hantzsch. Complete el siguiente esquema correspondiente a la síntesis de la felodipina. Cl Cl + CH3COCH2CO2Et 1 CHO Felodipina 2 CH3COCH2CO2Et + NH3 9.- La actividad como bloqueante -adrenérgico del propranolol está asociada al enantiómero levógiro (S)-4. Dicho compuesto se puede preparar por síntesis asimétrica a partir del alcohol alílico con D-(-)tartrato de diisopropilo según el esquema siguiente: OH TsCl HOO-C(CH3)3 / Ti(O-iPr)4 2 ( R )-1 Et3N D(-)-DIPT HO O i-PrNH3 NaH / DMF 3 1-naftol H2O H NHiPr (S)-(-)-4 a) Indique los productos intermedios de la síntesis del propranolol. Tenga en cuenta que la estereoquímica del producto final se fija en la primera reacción. b) Indique de qué enantiómero del compuesto 1 será necesario partir para obtener el (-)-propranolol con la siguiente secuencia de reacciones. 1 NaH / DMF 1-naftol 5 HBR / HOAc 6 NaOH 7 i-PrNH3 H2O (S)-(-)-4




