Primer Principio de la Termodinámica
Anuncio

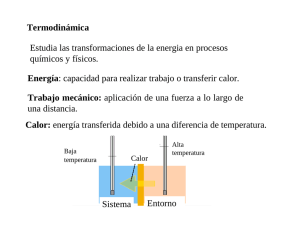
TERMODINÁMICA Y CINÉTICA QUÍMICA TERMODINÁMICA CINÉTICA No depende del tiempo La termodinámica clásica sólo tiene validez en el equilibrio PRIMER PRINCIPIO DE LA TERMODINÁMICA (TEMA 1) SEGUNDO PRINCIPIO DE LA TERMODINÁMICA (TEMA 2) ENERGÍA LIBRE Y EQUILIBRIOS FÍSICOS (TEMA 3) Tema 1 Estudia aquellos procesos que dependen del tiempo Primer Principio de la Termodinámica PROPIEDADES DE TRANSPORTE (TEMA 5) CINÉTICA DE LAS REACCIONES QUÍMICAS (TEMA 6) CINÉTICA ENZIMÁTICA (TEMA 7) ENERGÍA LIBRE Y EQUILIBRIOS QÚIMICOS (TEMA 4) ADSORCIÓN Y CINÉTICA (TEMA 8) SISTEMAS, FRONTERAS Y MEDIOS CIRCUNDANTES TEMA 1 PRIMER PRINCIPIO DE LA TERMODINÁMICA SISTEMAS, FRONTERAS Y MEDIOS FRONTERA MEDIO CIRCUNDANTE VARIABLES TERMODINÁMICAS ECUACIONES DE ESTADO SISTEMA PROCESOS TERMODINÁMICOS PRINCIPIO CERO DE LA TERMODINÁMICA Escalas termométricas Termómetros de gas a V cte Escala Kelvin de temperatura PRIMER PRINCIPIO LA TERMODINÁMICA Trabajo, calor y energía Entalpía Capacidad calorífica TRANSFORMACIONES TERMODINÁMICAS SISTEMA Parte de materia o región aislada imaginariamente, sobre la cual centramos nuestra atención. FRONTERA Límites de un sistema. MEDIO CIRCUNDANTE Región que rodea al sistema. Rígidas S I S T E M A S Aislados No aislados Cerrados Abiertos • No intercambian ni materia, ni energía con el exterior. • Paredes rígidas, adiabáticas e impermeables. • No cumplen las condiciones anteriores. • Pueden intercambiar energía, pero no materia • Pueden intercambiar materia y energía F R O N T E R A S Móviles Adiabáticas No dejan pasar el calor Diatermanas Si dejan pasar el calor Permeables Permiten el paso de sustancias Impermeables No permiten el paso de sustancias Semipermeables Sólo permiten el paso de sustancias hacia un lado de la pared 1 MATERIA VARIABLES TERMODINÁMICAS MATERIA Describen el estado de un sistema termodinámico MATERIA E N T O R N O SISTEMA ABIERTO VARIABLES EXTENSIVAS SISTEMA CERRADO ENERGÍA MATERIA VARIABLES INTENSIVAS Dependen del tamaño del sistema (masa, volumen, energía…) NO dependen del tamaño del sistema (presión, temperatura, densidad…) ENERGÍA MATERIA ESTADO DE EQUILIBRIO Las variables de estado no varían en el tiempo MATERIA NO existen flujos de materia y/o energía a través de las fronteras del sistema SISTEMA AISLADO ENERGÍA SISTEMA CALOR ADIABÁTICO ENERGÍA ESTADO ESTACIONARIO CALOR Las variables de estado no varían en el tiempo Existen flujos de materia y/o energía a través de las fronteras del sistema TRABAJO La ecuación de Van der Waals ECUACIONES DE ESTADO Las ecuaciones de estado describen el estado de agregación de la materia en función de las variables de estado ( temperatura, presión y volumen ) P = P (T ,V ) f ( P, V , T ) = 0 Son útiles para describir las propiedades de los fluidos, mezclas, sólidos o incluso del interior de las estrellas, pero su uso más importante es para predecir el estado de gases y líquidos. Predice la formación de una fase líquida Sólo concuerda con los datos experimentales en las condiciones en las que el líquido se forma. ⎛ a ⎞ ⎜⎜ P + 2 ⎟⎟(Vm − b ) = RT Vm ⎠ ⎝ a = 3PcVc2 Vc 3 8P V R= c c 3Tc b= Constantes que dependen cada sustancia Pueden calcularse a partir de las propiedades críticas Ecuación de Estado del Gas Ideal Predice el comportamiento de los gases a bajas presiones y altas temperaturas. PVm = RT Pierde mucha exactitud a altas presiones y bajas temperaturas, y no es capaz de predecir la condensación de gas en líquido. PROCESOS TERMODINÁMICOS Un proceso tiene lugar cuando un sistema cambia de un estado a otro. Todo proceso termodinámico implica un intercambio de materia y/o de energía con el exterior P Existe ecuaciones de estado más precisas para gases y líquidos, pero hasta ahora no se ha encontrado ninguna ecuación de estado que prediga correctamente el comportamiento de todas las sustancias en todas las condiciones. PRINCIPIO CERO DE LA TERMODINÁMICA Permite definir el concepto de TEMPERATURA 1 V1 2 V2 V PRINCIPIO CERO DE LA TERMODINÁMICA Si dos objetos se encuentran en equilibrio térmico con un tercero, entonces están en equilibrio térmico entre sí No demostrable: basado en la experiencia PROCESOS Todos los objetos en equilibrio térmico con uno dado comparten una propiedad común Reversibles e Irreversibles Cíclicos (coinciden los estados inicial y final) TEMPERATURA: es la propiedad que se iguala entre todos los cuerpos que están en equilibrio térmico entre sí Isotermos, isobaros, isocoros, adiabáticos, isoentrópicos, isoentálpicos … Ahora necesitamos una técnica para medir la temperatura (asignarle un valor numérico): termómetros 2 Escalas termométricas Escalas termométricas Propiedad termométrica: propiedad física que varía con la temperatura Escala Celsius de temperatura ( Longitud de una barra de hierro, altura de una columna de mercurio, presión de un gas a volumen constante…) CONVERSIÓN ENTRE AMBAS ESCALAS Para establecer una escala de temperaturas puede usarse cualquier propiedad termométrica 100 ºC equivalen a 180 ºF 1 ºC = 1.8 ºF = 9/5 ºF Construcción de un termómetro Se escoge una propiedad termométrica: termómetro Las temperaturas cero de ambas escalas difieren Escala Farenheit de temperatura Se pone el termómetro en contacto con un foco térmico y se le asigna un valor de temperatura: Calibrado Foco térmico: sistema cuya temperatura no cambia al ponerlo en contacto térmico con otros sistemas Ejemplo: mezcla de agua y hielo a P= 1 atm Termómetro de gas a volumen constante Diferentes termómetros calibrados en los punto de congelación y ebullición ofrecen lecturas diferentes fuera de esos puntos El gas en B1 se pone en contacto térmico con el medio cuya T se quiere medir La construcción de un termómetro no permite definir la temperatura de una forma absoluta B3 se sube o baja de modo que se mantenga el mercurio en la marca “0” en B2 Es preciso disponer de un tipo de termómetro en que las medidas concuerden fuera de los puntos de calibración: termómetro patrón La presión la indica la altura h de la columna de mercurio en B3 mg ⎫ ⎪ S ⎬ P = P0 + ρgh ⎪⎭ m = ρSh Presión atmosférica P = P0 + La presión de un gas en un recipiente a volumen constante es otra propiedad termométrica t (º C ) = tc = Podemos construir un termómetro de gas a volumen constante Escala Kelvin de Temperatura P − P0 100 p100 − P0 Las lecturas de temperatura en un termómetro de gas son casi independientes de la sustancia utilizada, para bajas densidades y presiones (gas ideal). La propiedad que define la temperatura es el cambio de presión con la temperatura. PRIMER PRINCIPIO DE LA TERMODINÁMICA Representamos P frente a T para un termómetro de gas a V=cte con ρ baja ENUNCIADOS GENERALES La energía del universo se conserva Extrapolamos la recta hasta P=0 Es imposible realizar un trabajo sin consumir una energía Para todos los termómetros de gas obtenemos que P=0 para tc=-273.15 ºC Energía = Capacidad para realizar un trabajo FORMULACIÓN MATEMÁTICA ∆U12 = Q12 + W12 Definimos el cero absoluto como 0 K El valor de un grado en la escala kelvin se hace coincidir con 1 grado Celsius P FUNCIÓN DE ESTADO 1 W1a2 ≠ W1b2 a La única diferencia entre estas dos escalas es un desplazamiento del cero Una diferencia de temperaturas ∆T es igual en ambas escalas Q1a2 ≠ Q1b2 b ∆U1a2 = 2 ∆U1b2 Depende del camino seguido. No son función de estado. Depende del estado inicial y final no del camino seguido. v 3 TRABAJO IRREVERSIBLE 1 P TRABAJO • Frente a Pext = P2 constante W = − 2 ∫ V 2 V Pext wembolo = Pext dV Pext Pext Pext Wsistema = −∫ Pext dV Pint Pint Pext = Pint …en dos etapas 1 Pint 2 W = −[ P '1 (V '1 − V1 ) + P2 (V2 − V '1 )] Pext < Pint Pext = Pint V • Expansión reversible (infinitas etapas) Estado Inicial 1 Estado Final 2 P’ dx Pint W = −P2 (V2 − V1 ) < 0 V P dx Pext > Pint Pint Unidades Equilibrio mecánico 1 at.l x Pext dV 1 REVERSIBLE P W 1 = − ∫ V 2 V ∫ V 2 V Pgas dV 1 ∫ nRT dV V W = −nRT • Gas ideal y T constante V = − W =− • Gas Ideal 2 8.314 J/ K.mol =101.4 J 0.082 at.l/ Kmol Pext dV 1 dV ∫V W = −nRT Ln V 2 V 1 CALOR PROCESO REVERSIBLE ∫ El sistema pasa por una sucesiva serie de estados de equilibrio 2 W12 = - PgdV Es la energía que se transfiere de un objeto a otro debido a una diferencia de temperatura Q = C ∆T 1 C=mc=nc PROCESO IRREVERSIBLE ∫ Los estados intermedios, no están en equilibrio termodinámico, debido al desplazamiento rápido del pistón. 2 W12 = - PgdV 1 W>0 Sistema Trabajo realizado sobre el sistema W<0 Capacidad Calorífica Calor específico C = [J/ºK] 1cal=4.184 J Una caloría es el calor necesario para elevar la temperatura de 1g de agua 1ºC Q>0 Trabajo realizado por el sistema UNIDADES Calor específico molar Sistema Q<0 Calor absorbido por el sistema Calor cedido por el sistema El calor y el trabajo son formas equivalentes de variar la energía de un sistema Cambios de fase y Calor latente Calor de fusión Calor necesario para fundir una sustancia sin modificar su temperatura. Q = m Lf Sistema “Fuerza” “Desplazamiento” Fluido presión, P volumen, V dW - P dV γ dA Superficie tensión superficie, A líquido superficial γ calor Calor de evaporación Calor necesario para vaporizar una sustancia sin modificar su temperatura. Trabajo mecánico Pila fuerza carga, q Eléctrica electromotriz E E dq Otros tipos de trabajo Q = m Le El calor y el trabajo ejercen un efecto distinto sobre las moléculas del entorno • Ambas son formas de variar la energía del sistema • El calor es energía “desordenada” y el trabajo energía “ordenada” • NO son funciones de estado • No es “algo” que posea el sistema 4 ENERGÍA La energía es la capacidad para hacer un trabajo E debida a la posición del sistema en un campo de fuerzas (gravitacional, eléctrico, magnético) y a su movimiento en conjunto: Erestante Esistema= U+ Erestante P ∆U = Q + W 1er Principio de la Termodinámica dU = δQ + δW Variaciones infinitesimales A PROCESO CÍCLICO Energía Interna, U característica del sistema (Et, Er, Ev de moléculas) depende del estado de agregación del sistema Unidades: Julio (J) ∆U = U final − U inicial = U A − U A = 0 W = −Q B La energía es una función de estado U ≡ f (T , P ,V ) La energía es una propiedad extensiva P También podemos definir una propiedad intensiva U = U n V A ∆U BA = ∆U BA [ J / mol ] U ≡ función de estado U ≡ f (T , P ,V ) No es posible conocer la energía de un sistema, sólo conocemos su cambio en un proceso ∆U=U2-U1 B ⎛ ∂U ⎞ ⎛ ∂U ⎞ dU = ⎜ ⎟ dT + ⎜ ⎟ dV ⎝ ∂T ⎠V ⎝ ∂V ⎠T V W = −Q ∆U = 0 Proceso cíclico Sólo trabajo mecánico Proceso a V cte V2 = V1 Proceso a P cte ∫ V2 Pext dV = QP − Pext V1 ∆U=U2-U1 • Función de estado H≡f(T,P,V,U) • Propiedad extensiva • Unidades de energía (J) • H H≡ [ J / mol ] n ∫ V2 V1 Entalpía (H) H ≡ U + PV ∆ U = Qv dV=0 Nos da una forma de determinar ∆U ∆U = Q + W = Q − ENTALPÍA ∆U = W Proceso adiabático dV = QP − P(V2 − V1 ) Es imposible realizar trabajo sin consumir energía • Una forma de determinar ∆U = QV • Una forma de determinar ∆H = QP Relación entre ∆H y ∆U P=cte QQP = (U + PV ) − (U + PV ) = ∆H P 2 2 1 H2 1 v H1 Nos da una forma de determinar ∆H ∆H = ∆U + ∆(PV) ∆H ≅ ∆ U ∆H = ∆U + P ∆V proceso sól/líq Si P=cte ∆(PV) = P∆V+V∆P+∆P∆V = P∆V+V∆P+∆P∆V= P2V2-P1V1 CAPACIDAD CALORÍFICA Q = C∆T •Si no hay cambio de fase •ni reacción química Capacidad calorífica de una sustancia: cantidad infinitesimal de calor necesaria para elevar su T en una cantidad dT . [J×K-1] • Depende de la naturaleza de la propia sustancia • Puesto que Q depende de la trayectoria del cambio de estado, para definir C hay que definir la trayectoria En un sistema cerrado, en equilibrio o proceso reversible y sólo con trabajo mecánico es posible definir : Calor específico molar a P cte P. Intensivas f=(T,P,V) Calor específico molar a V cte cCpp = 1 qP 1 ⎛ ∂H ⎞ = ⎜ ⎟ n dT n ⎝ ∂T ⎠ P U,H≡f(T,P,V) q cCvv = 1 v = 1 ⎛⎜ ∂U ⎞⎟ n dT n ⎝ ∂T ⎠V Calor específico de una sustancia: cantidad de calor necesaria para elevar la T de un gramo de dicha sustancia un grado. [J×g-1×K-1] Calor específico molar de una sustancia: cantidad de calor necesaria para elevar la T de un mol de dicha sustancia un grado. [J×mol-1×K-1] C ≡ [ J / K .mol ] 5 Relación entre CP y CV TRANSFORMACIONES TERMODINÁMICAS ⎛ ∂U ⎞ ⎛ ∂V ⎞ ⎛ ∂U ⎞ ⎛ ∂H ⎞ ⎛ ∂U ⎞ C P − CV = ⎜ ⎟ −⎜ ⎟ = ⎜ ∂ T ⎟ + P ⎜ ∂T ⎟ − ⎜ ∂T ⎟ ⎝ ⎠P ⎝ ⎠P ⎝ ⎠V ⎝ ∂T ⎠ P ⎝ ∂T ⎠V ∆U y ∆H en procesos sencillos de sistemas cerrados H ≡ U + PV U ≡ f (T , V ) V ≡ f (T , P ) Gas Ideal PV = nRT ⎛ ∂U ⎞ ⎛ ∂U ⎞ dU = ⎜ ⎟ dT + ⎜ ∂V ⎟ dV ⎝ ∂T ⎠V ⎝ ⎠T De forma general ⎡ ⎛ ∂U ⎞ ⎤ ⎛ ∂V ⎞ C P − CV = ⎢ ⎜ ⎟ + P⎥ ⎜ ⎟ ⎣ ⎝ ∂V ⎠T ⎦ ⎝ ∂T ⎠ P ⎛ ∂V ⎞ ⎛ ∂V ⎞ dV = ⎜ ⎟ dT + ⎜ ∂P ⎟ dP ⎝ ∂T ⎠ P ⎝ ⎠T ⎛ ∂U ⎞ ⎜ ⎟ =0 ⎝ ∂V ⎠ T U ≡ f (T ,V ) ⎛ ∂U ⎞ ⎛ ∂U ⎞ ⎛ ∂U ⎞ dU = ⎜ ⎟ dT + ⎜ ∂V ⎟ dV = CV dT + ⎜ ∂V ⎟ dV ⎝ ∂T ⎠V ⎝ ⎠T ⎝ ⎠T H ≡ f (T , P ) ⎛ ∂H ⎞ ⎛ ∂H ⎞ ⎛ ∂H ⎞ dH = ⎜ ⎟ dT + ⎜ ∂P ⎟ dP = C P dT + ⎜ ∂P ⎟ dP ⎝ ∂T ⎠ P ⎝ ⎠T ⎝ ⎠T Gas Ideal CP-CV = nR nR ⎛ ∂V ⎞ ⎜ ⎟ = P ⎝ ∂T ⎠ P TRANSFORMACIONES TERMODINÁMICAS ∆U y ∆H en procesos sencillos de sistemas cerrados • En un proceso cíclico TRANSFORMACIONES TERMODINÁMICAS ∆U y ∆H en procesos sencillos de sistemas cerrados • Proceso Isobárico (P≡cte) ∆U = U f − U i = 0 ∆T = ∆P = ∆V = 0 ∆H = H f − H i = 0 Q = C p (T2 − T1 ) = ∆H P W = − P (V2 − V1 ) • Cambio de Fase a T y P constante ∆U = Q p − Pext ∫ dV T 100ºC El calor a P cte se emplea en ∆V y en ∆U H2O ∆U = ∆ H − P ∆V 1at ∆ U = Q − P ∆ V = ∆ H − P∆ V V2 V1 V ⎛ ∂H ⎞ ⎛ ∂H ⎞ ⎟ dT + ⎜ ⎟ dP ⎝ ∂T ⎠ P ⎝ ∂P ⎠T dH = ⎜ dU = q + w tiempo W = − ∫ Pext dV TRANSFORMACIONES TERMODINÁMICAS ∆U y ∆H en procesos sencillos de sistemas cerrados P=cte ∆H = ∫ CP (T )dT = CP ∆T Si CP cte ∆U = ∆H − P∆V P=cte TRANSFORMACIONES TERMODINÁMICAS ∆U y ∆H en procesos sencillos de sistemas cerrados : GASES IDEALES • Proceso Isocórico (V≡cte) ∆U = Cv (T2 − T1 ) = Q P W =0 P2 P1 • Cambio de estado de un Gas Ideal 0 ⎛ ∂U ⎞ ⎛ ∂U ⎞ ⎟ dT + ⎜ ⎟ dV ⎝ ∂T ⎠V ⎝ ∂V ⎠ T dU = ⎜ ∆H = ∆ (U + PV ) = ∆U + V∆P ⎛ ∂U ⎞ ⎛ ∂U ⎞ ⎟ dT + ⎜ ⎟ dV ⎝ ∂T ⎠V ⎝ ∂V ⎠ T dU = ⎜ dH = ⎜ V=cte ∆U = ∫ CV (T )dT GI ∆H = ∫ CP (T )dT = CV ∆T Si CV cte 0 ⎛ ∂H ⎞ ⎛ ∂H ⎞ ⎟ dT + ⎜ ⎟ dP ⎝ ∂T ⎠ P ⎝ ∂P ⎠T V GI = C P ∆T Si CP cte ∆U = ∫ CV (T )dT = CV ∆T ∆H = ∆ (U + PV ) = ∆U + V ∆P Si CV cte V=cte 6 TRANSFORMACIONES TERMODINÁMICAS TRANSFORMACIONES TERMODINÁMICAS ∆U y ∆H en procesos sencillos de sistemas cerrados : GASES IDEALES ∆U y ∆H en procesos sencillos de sistemas cerrados : GASES IDEALES • Proceso Isotérmico de un Gas Ideal (T=cte) • Proceso Adiabático de un Gas Ideal (Q=0) Q = −W P W = − nRT ln V1 V2 V2 P = nRT ln 2 V1 P1 ∆U = Q + W ∆H = 0 V1 P cte dT = 0 ∫ ∆U = 0 V ∆U=0 ∆H=0 ∆U = ∫ CV (T )dT = W = − Pext dV P W = − P ∆V V2 rev. o irrev. nRT dV W = − ∫ Pext dV = − ∫ Pgas dV = − ∫ rev. GI V V2 P W = −nRT Ln = nRT Ln 2 V1 P1 ∆H = ∫ CP dT = CP ∆T Q = -W Si CV cte Si CP cte • Proceso Adiabático de un Gas Ideal (Q=0) ∆U = ∫ CV (T )dT = W = − Pext dV ∫ TRANSFORMACIONES TERMODINÁMICAS • Proceso Adiabático (Q=0) Reversible (P cte) de un G.I. (continuación) 0 dU = q + w CV Ln V nRT dU = CV dT = w = − Pgas dV = − dV V dT dV T2 V CV = − nR CV Ln = − nRLn 2 T V T1 V1 ∆H = ∫ CP dT = CP ∆T ∆U = CV ∆T = W GI P T2 V = − nRLn 2 T1 V1 ⎛ T2 ⎞ ⎛ V1 ⎞ ⎜ T ⎟ = ⎜V ⎟ ⎝ 1⎠ ⎝ 2⎠ • Proceso Adiabático (Q=0) Reversible (P cte) de un G.I. V2 ∆U = ∫ CV (T )dT = CV ∆T = − P∆V W = − Pext ∆V T cte ∆U y ∆H en procesos sencillos de sistemas cerrados : GASES IDEALES V1 V • Proceso Adiabático (Q=0) Irreversible (P cte) de un G.I. TRANSFORMACIONES TERMODINÁMICAS P 0 dU = q + w C P − CV = R γ ≡ CP CV Cte de adiabaticidad T=cte nR / CV Q=0 PV = cte PV γ = cte V ⎛ T2 ⎞ ⎛ V1 ⎞ ⎜ T ⎟ = ⎜V ⎟ ⎝ 1⎠ ⎝ 2⎠ γ −1 TV γ −1 ≡ cte PV γ ≡ cte Ecuación de la adiabática Si CP cte 7