Tema 5.b) Solidificación
Anuncio
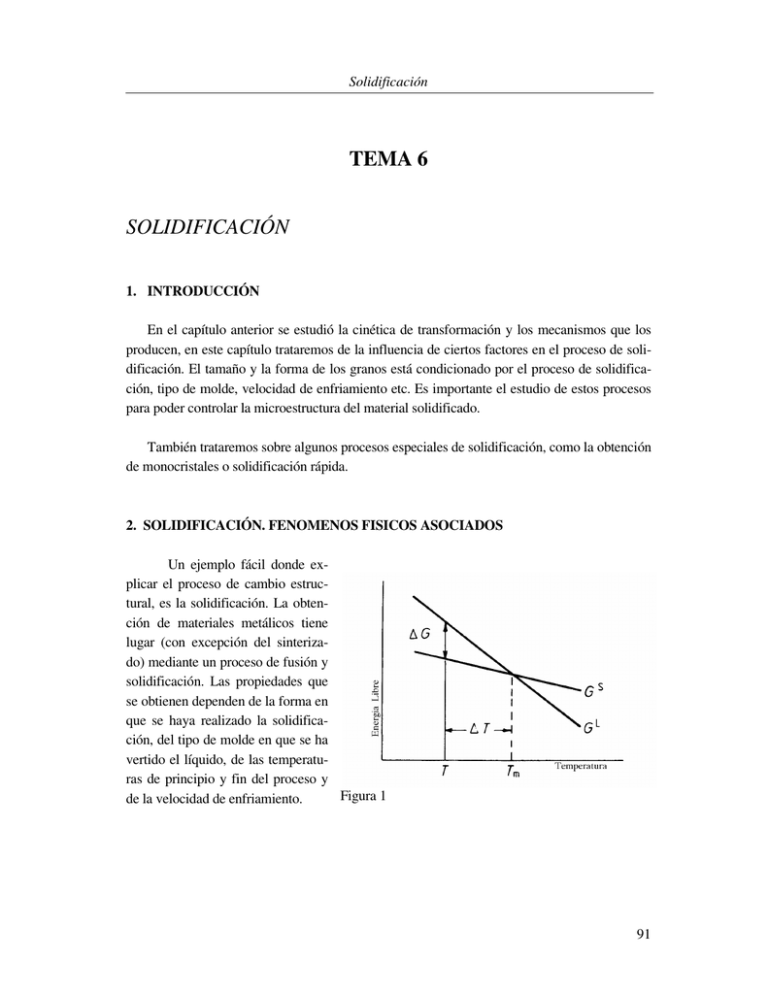
Solidificación TEMA 6 SOLIDIFICACIÓN 1. INTRODUCCIÓN En el capítulo anterior se estudió la cinética de transformación y los mecanismos que los producen, en este capítulo trataremos de la influencia de ciertos factores en el proceso de solidificación. El tamaño y la forma de los granos está condicionado por el proceso de solidificación, tipo de molde, velocidad de enfriamiento etc. Es importante el estudio de estos procesos para poder controlar la microestructura del material solidificado. También trataremos sobre algunos procesos especiales de solidificación, como la obtención de monocristales o solidificación rápida. 2. SOLIDIFICACIÓN. FENOMENOS FISICOS ASOCIADOS Un ejemplo fácil donde explicar el proceso de cambio estructural, es la solidificación. La obtención de materiales metálicos tiene lugar (con excepción del sinterizado) mediante un proceso de fusión y solidificación. Las propiedades que se obtienen dependen de la forma en que se haya realizado la solidificación, del tipo de molde en que se ha vertido el líquido, de las temperaturas de principio y fin del proceso y Figura 1 de la velocidad de enfriamiento. 91 Solidificación Cuando un sólido cristaliza, casi todas las propiedades cambian fuertemente en cantidades finitas. La resistencia cortante es quizá el cambio de propiedad más espectacular. La fluidez del líquido cambia a un estado rígido. En términos de viscosidad este cambio puede llegar a ser de 1020. Las temperaturas a las que ocurren estas transformaciones (temperatura de fusión), es muy variable, dependiendo de la fuerza de unión del enlace, así tenemos metales con temperaturas de fusión de -38°C como el Hg o más de 3000°C como el W. Los calores latentes, indicadores de la energía necesaria para separar los átomos en el proceso de fusión, son también muy variables pudiendo estar entre 2000 J/mol a 20.000 J/mol. La energía libre del líquido es más alta que la del cristal a bajas temperaturas, donde la energía interna es la principal responsable de la energía libre, ésta disminuye más rápidamente que la del cristal sólido cuando se incrementa la temperatura debido al aumento de la entropía del líquido, G = E - TS , cruzándose por tanto, con la curva de energía libre del sólido fig. 1. Los agrupamientos atómicos en los líquido no son aleatorios, sino que muestran un cierto orden a largo alcance, no a distancias cortas. Los átomos en estado líquido aún con gran libertad de movimiento parece que ocupan posiciones ordenadas como si persistieran en algunos momentos cierto tipo de estructura, Fig. 2. A medida que baja la temperatura y disminuye la energía cinética de los átomos, las fuerzas atractivas comienzan a ser suficientemente grandes y por tanto van limitando el movimiento atómico hasta llegar a conseguir la formación del sólido. En general la solidificación de un metal o aleación se puede dividir en dos etapas: a) La formación de agrupaciones estables llamados núcleos, y b) Crecimiento de los núcleos y forFigura 2 mación de la estructura granular. Aún así, habría que distinguir entre la solidificación homogénea y heterogénea y el de un metal puro y una aleación, etc. 92 Solidificación 3. EFECTO DEL FLUJO TÉRMICO EN LA INTERCARA SOLIDO-LIQUIDO. Como se ha visto en el capítulo anterior, para que comience la solidificación es necesario que se produzca un subenfriamiento del líquido, pudiendo comenzar como T consecuencia la nucleación. Después de que ocurra la nucleación la temperatura sube rápidamente debido al calor Tf latente desprendido durante la solidificación. Sien embargo, esta elevación de temperatura se detiene al alcanzar la temperatura de fusión. Si la temperatura siguiera aumentando se produciría Liberación del calor latente un sobrecalentamiento y la fusión del sólido recién formado, obviamente el calor latente por sí solo no es suficiente tiempo para causar esta fusión y como conse- Figura 3 cuencia la temperatura se detiene en el punto de fusión, Figura 3. Al verter un metal fundido en un molde, al estar las paredes del mismo a menor temperatura que la del líquido, se produce una disminución de temperatura en el material próximo a la pared y por tanto un gradiente térmico dentro del líquido y entre éste y la pared. T Esto hace que el líquido en contacto con el molde comience a solidificar, debido al Tm grado de subenfriamiento y favorecido por la nucleación heterogénea que induce la pared del molde. Una vez comenzada la solidificación la temperatura se eleva hasta Tm (como ya se ha dicho), consecuencia del calor latente liberado en el proceso, este calor latente ha de ser extraído a través del molde propio líquido o de las paredes del molde. Según se produzca el flujo térmico princiFigura 4 interior palmente a través del metal fundido o a través del molde, o sólido formado, se presentarán dos procesos de solidificación distintos que producirán tamaños y forma de granos dife- 93 Solidificación rentes. En la figura 4 se muestra el gradiente térmico producido inmediatamente después de verter un metal líquido en un molde (línea de trazos) y el gradiente que se origina una vez comienza la solidificación (línea continua). Una vez comienza la solidificación el crecimiento de los núcleos produce el desprendimiento del calor latente de solidificación. La cinética de evacuación de este calor (además de otras variables) controlará el proceso de solidificación, condicionando la forma orientación y tamaño de los granos. El perfil de temperatura en la interfase sólido-líquido es por tanto un factor importante en el control de la estructura final del grano, por lo que es útil hacer una distinción entre dos tipos de perfiles que se pueden presentar. Consideremos el caso en que el flujo de calor se produce fundamentalmente a través del sólido por estar a menor temperatura que el líquido, cosa que ocurre con bajos valores de subenfriamientos o líquidos muy sobrecalentados. En este caso el calor liberado en el proceso de solidificación, tanto específico como latente, es eliminado hacia el sólido calentándolo, el gradiente térmico, positivo en este caso, es como el de la figura 5 donde la flecha la flecha indica la dirección de la evacuación del calor. El crecimiento de los núcleos hacia el interior del líquido se verá muy dificultado al tener que crecer en zonas de bajo subenfriamiento y hacia el interior de un líquido sobrecalentado. Este proceso permitirá la formación de nuevos núcleos que chocarán con los ya existentes e impedirán su crecimiento. El crecimiento de líquido sólido un frente plano y de granos equiaxiales se T verá favorecido en estas condiciones. Suponiendo que como resultado de un incremento local de la velocidad de crecimiento se produce una protuberancia, el crecimiento de la misma disminuirá al Tf estar rodeada de líquido a alta temperatura y ser mayor la cantidad de calor que tendría que conducir como consecuencia del aumento de superficie, además, puede ser redisuelta por el líquido que la rodea Figura 5 bastante sobrecalentado, esto dificultaría su crecimiento y rápidamente el resto de la interfase alcanzará esta zona y el frente plano continuará su crecimiento estable. 94 Solidificación Por el contrario la situación es muy diferente cuando el sólido crece dentro de un líquido muy subenfriado (gradiente negativo) el calor latente de solidificación tendrá que ser evacuado a través del líquido, este caso ocurre cuando la solidificación se produce con grandes grados de subenfriamiento. Las partículas de sólido crecen dentro del líquido a gran líquido sólido velocidad y el aumento de superficie favoT rece el desprendimiento de calor dentro de un líquido a más baja temperatura. En estas condiciones una protuberancia puede ser estable, siendo más fácil la eliminación de Tf calor del frente de ésta que de los alrededores permitiendo el crecimiento de la misma. El crecimiento en forma dendrítica favorece la eliminación del calor, tanto latente como específico, al aumentar la superficie de evacuación. En este modelo los granos creFigura 6 cen de forma columnar. Figura 6. En este caso el subenfriaminto es un prerrequisito esencial siendo por tanto más probable cuanto mayor sea el grado de subenfriamiento. La forma de los granos durante la transformación refleja un equilibrio entre la necesidad de minimizar la energía asociada a los límites de grano y la necesidad de maximizar la velocidad de transformación. Próximo al equilibrio, cuando la fuerza conductora para la transformación es pequeña, los granos son formados por el control de la energía de los límites de grano. Cuando se está muy lejos del equilibrio, la fuerza conductora es grande y la estructura depende fuertemente del mecanismo de transformación. 4. ORIENTACIÓN PREFERENTE Como se ha dicho en el apartado anterior, cuando se inicia la solidificación a partir de núcleos en la masa del líquido, el crecimiento no es plano, sino que se produce preferencialmente en ciertas direcciones cristalográficas (en la dirección <100> en metales cúbicos y < 1100 > en cristales hexagonales). También se forman ramas secundarias perpendiculares a las anteriores o incluso terciarias, la razón de estas es favorecer la evacuación del calor latente. El crecimiento de estas ramas continúa hasta que el líquido subenfriado que queda atrapado 95 Solidificación entre las ramas se calienta hasta la temperatura de fusión y puede continuar el crecimiento planar. Figura 7. La estructura que se forma en el proceso de crecimiento es arborescente y recibe el nombre de dendrita. Estas se unen como un esqueleto del grano e indican de que manera ha crecido el mismo. 5. ESTRUCTURA DE LINGOTE. Figura. 7 La mayoría de las aleaciones son obtenidas vertiendo el metal fundido en unos moldes denominados lingoteras y dejando que el líquido se enfríe dentro del molde. A partir de los lingotes mediante laminación fundamentalmente, se va conformando la aleación en perfiles y tamaños más utilizables industrialmente. Es importante conocer cual será la macroestructura resultante de solidificación dentro del molde. En el caso más general se pueden distinguir tres zonas en la solidificación de un lingote, una zona en contacto con las paredes del molde de granos pequeños y equiaxiales denominada zona fría, una zona a continuación de grandes granos columnares, y una tercera zona central de granos grandes equiaxiales. Fig.8. A continuación vamos a comentar brevemente cada una de estas zonas. Figura. 8 96 La zona fría es una franja estrecha de granos orientados aleatoriamente formados en la superficie de la fundición. Durante la colada el líquido en contacto con el molde frío es rápidamente subenfriado a temperaturas inferiores a la de fusión, en estas condiciones muchos núcleos son formados sobre las paredes, actuando estas como centros de nucleación heterogénea. Estos núcleos una vez formados comienzan su crecimiento dentro del líquido. Cuando las paredes del molde son calentadas debido a la Solidificación absorción de calor, los cristales formados pueden desprenderse por efecto de las turbulencias del líquido. Si la temperatura de colada es baja, puede ocurrir que todo el líquido disminuya rápidamente su temperatura, encontrándose con grandes cantidades de núcleos repartidos por todo volumen produciéndose una estructura equiaxial en toda la sección del lingote. Asimismo, el uso de moldes con baja conductividad térmica o la presencia de elementos de aleación favorecen este tipo de estructuras. Por el contrario si la temperatura es alta, el líquido en el centro del lingote permanecerá gran cantidad de tiempo a temperatura por encima de la de fusión y consecuentemente los cristales desprendidos se refunden pudiéndose obtener granos columnares. Solamente los cristales que se mantienen próximos a la superficie son capaces de crecer formando la zona fría. La zona columnar contiene granos alargados perpendiculares a las paredes del molde. Muy pronto después de la colada, el gradiente térmico de las paredes disminuye y los cristales de la zona fría crecen dendríticamente en cierta direcciones cristalográficas, como ya se vio anteriormente. Los granos cuya orientación <100> es próxima al flujo de calor, crecen más rápidamente en esta dirección que los no orientados favorablemente,. Cada grano puede tener varias dendritas primarias, a medida que el grano es más ancho aparecen Figura. 9 dendritas adicionales algunas de las cuales a crecido a partir de dendritas terciarias, Fig. 9. Esta zona tienen propiedades anisotrópicas debido a la direccionalidad del grano. La zona equiaxial consiste en una zona central de granos equiaxiales orientados aleatoriamente. Esta puede ser formada por una baja temperatura o por la presencia de afinadores de grano. Cuando la solidificación alcanza esta zona, el grado de subenfriamiento ya es grande y el tamaño crítico de los núcleos ha disminuido, aumentando por tanto la velocidad de nucleación y favoreciendo la formación de granos equiaxiales orientados aleatoriamente. 97 Solidificación 6. SOLIDIFICACIÓN RÁPIDA. En casos de enfriamientos muy rápidos no da tiempo a que aparezca la etapa de nucleación. En estos casos se forma un sólido amorfo metaestable producido al mantener a los átomos en las posiciones que ocupaban en estado líquido y que por disminución de temperatura al perder los átomos su movilidad e impedir la difusión se hace imposible la formación de los cristales. A este estado se le denomina vítreo y es similar a la estructura de los polímeros o de los vidrios. También se considera solidificación rápida, cuando en el proceso se obtiene un producto que no es el obtenido normalmente en procesos de solidificación de fundiciones o en lingotes convencionales. Las velocidades de enfriamiento que se necesitan para que ocurra esto es del orden de 105 ºC/s o mayores. Las técnicas de obtención de vidrios metálicos se pueden resumir en tres tipos. La solidificación sobre una superficie mediante goteo o por chorro continuo sobre una rueda para obtener cintas o hilos. Las dimensiones de los sólidos así obtenidos son muy pequeñas (espesores de micras) para poder conseguir las grandes velocidades de enfriamiento que se necesitan para obtener el material en estado vítreo, hay que tener en cuenta que una gran relación superficie/volumen favorece la extracción de calor del sólido, en la figura 10 se muestra un esquema de cómo sería este proceso. Figura 10 Otro método de obtener sólidos vítreos es mediante la proyección de gotas de líquido muy finas sobre una superficie fría, la formación de gotas se puede conseguir por centrifugación o por proyección bajo un chorro de gas. Al proyectar el metal fundido sobre superficies frías, el metal en gotas muy finas se enfría casi instantáneamente obteniéndose polvo muy fino en estado amorfo o microcristalino. El tercer método consiste en la condensación de vapor sobre una superficie enfriada. Una vez obtenidas estas pequeñas partículas se necesita de algún sistema para la obtención de una pieza de un tamaño de uso industrial. Esto se realiza mediante el sinterizado, técnica que 98 Solidificación consiste en comprimir las partículas a alta temperatura en un molde para producir la unión entre ellas. Las propiedades obtenidas en estas condiciones son muy superiores a las obtenidas por otros métodos convencionales, tanto desde el punto de vista mecánico como eléctrico o magnético. Muchas de las aleaciones de base hierro obtenidas con estas técnicas tienen unas propiedades magnéticas muy interesantes. Al no tener estructura no existen paredes de dominios ferromagnéticos, siendo magníficos materiales ferromagnéticos blandos que tienen uso en núcleos de transformadores y relés. El proceso está todavía en período de experimentación y estudio. 7. FORMACIÓN DE MONOCRISTALES Casi todos los materiales cristalinos de uso industrial están formados por muchos pequeños cristales llamados granos, diciéndose que son policristalinos. Sin embargo, en algunas aplicaciones es necesario la utilización de materiales formados solamente por una única estructura cristalina, estos son los denominados monocristales. Aplicaciones típicas son la industria electrónica donde los dispositivos de semiconductores tales como los transistores y otros elementos están hechos de monocristales. Los álabes de turbinas de vapor aunque por otras causas, se obtienen también algunas veces en forma de monocristal. La solidificación en estas aplicaciones tiene que realizarse a partir de un único núcleo, de manera que no se permita la formación de otro cristal. Para conseguir esto se necesita una velocidad de crecimiento muy lenta, conseguir que la temperatura de la interfase sea ligeramente inferior al punto de fusión y la del líquido superior a la de fusión. Un método utilizado para la obtención de monocristales de silicio, consiste en aproximar a un baño de silicio fundido un germen Figura. 11 monocristalino con la orientación deseada, manteniendo el baño fundido a una temperatura controlada por encima de la de fusión. Al acercarse el germen al baño se funde parte del mismo en el líquido y actúa como un núcleo de cristalización. El cristal está girando constantemente y es extraído lentamente del baño, el calor 99 Solidificación latente de solidificación que se está produciendo en el proceso es extraído a través del sólido. El baño líquido se mantiene en agitación para evitar la formación de otros núcleos. De esta forma se consiguen monocristales de 10 y 15 cm de diámetro. Fig. 11. 8. SOLIDIFICACIÓN DE SÓLIDOS AMORFOS Hay dos mecanismos distintos por los que un líquido puede solidificar al enfriarse; puede cristalizar y formar un sólido policristalino, o puede vitrificarse y formar un vidrio. En la figura 12 se representa la variación del volumen específico frente a la temperatura de un material que se comporta al enfriarse de forma vítrea. A altas temperaturas el material se comporta como un líquido normal, a medida que la temperatura disminuye el volumen se contrae constantemente de forma lineal hasta alcanzar la temperatura de fusión. En este momento, si el material cristalizara, se produciría una extracción de calor a temperatura constante acompañado de una fuerte caída del volumen específico, como consecuencia del reagrupamiento de las moléculas en una estructura periódica. Una vez que se completa el proceso, el volumen específico sigue disminuyendo como consecuencia de la contracción térmica. En el caso de la cristalización el material sigue un proceso de nucleación y crecimiento, en éste proceso las moléculas han de moverse dentro de una masa de una gran viscosidad, lo que dificulta Figura. 11 grandemente su agrupamiento. En el caso de los metales, los átomos esencialmente esféricos y pequeños se mueven con facilidad dentro de un líquido no excesivamente viscoso a la temperatura de fusión (≈ 0,01 poise), cristalizando relativamente bien. Por el contrario los óxidos, boratos, fosfatos, silicatos y otros materiales formadores de vidrios, tienen viscosidades muy elevadas a la temperatura de fusión, del orden de ≈ 1000 poises, lo que dificulta grandemente el movimiento de las moléculas. Cuando la cristalización no se produce al alcanzar la temperatura de fusión, el material continua su enfriamiento normalmente como un líquido subenfriado. El volumen continua 100 Solidificación disminuyendo en la misma relación que lo venía haciendo, aun por debajo de la temperatura de fusión, la viscosidad se incrementa aún más manteniéndose la estructura del líquido a bajas temperaturas. Al alcanzar una cierta temperatura, se produce un cambio de pendiente en la curva, Fig. 12, debido a un gran aumento de la viscosidad a valores del orden de 1013 Poises. A estas viscosidades el flujo de partículas y su reagrupamiento es prácticamente imposible. A partir de esta temperatura, la curva disminuye con una pendiente igual al sólido cristalino, la contracción que experimenta es debida únicamente a la vibración térmica. Las moléculas a partir de este punto han quedado como congeladas en las posiciones que se encontraban, manteniendo el sólido la misma estructura del líquido pero comportándose como un sólido. A esta temperatura se la denomina de transición vítrea y se representa siempre por Tg. La temperatura de transición vítrea no es fija para cada material sino que depende de la velocidad de enfriamiento. A medida que esta velocidad es más alta, aumenta Tg. Cuanto más por debajo de Tg estemos, más se acerca el sólido al estado cristalino. Si se mantiene un vidrio en estado líquido durante mucho tiempo a temperaturas muy próximas a la de fusión, tiende a cristalizar. De esta forma se han obtenido vidrios cristalinos manteniéndolos a temperaturas muy ligeramente por debajo de la fusión durante varios días. A temperatura ambiente, la viscosidad de los vidrios es tan alta que se pueden mantener en estado vítreo de forma indefinida. 9. DEFECTOS DE SOLIDIFICACIÓN En el proceso de solidificación se producen una serie de defectos de tipo químico denominados segregaciones. La segregación consiste en una diferencia de composición química en la aleación. Este hecho se presenta porque la difusión no es capaz durante el tiempo que dura la solidificación de homogeneizar el sólido formado. Como ya se verá, la composición de la primera capa que se forma no es la misma que la de última gota de líquido que solidifica, dando lugar a esta heterogeneidad de tipo químico. Se pueden distinguir dos tipos de segregaciones: - Segregación dendrítica - Segregación principal La segregación dendrítica ocurre a nivel de grano y se pone de manifiesto a través del microscopio mediante la visualización de las dendritas. La segregación principal tiene lugar a 101 Solidificación nivel de lingote y es la diferencia de composición química a nivel macroscópico. La primera zona en solidificar tiene distinta composición (es por tanto otra aleación) que la última que solidifica. Lógicamente este lingote en estas condiciones no puede sufrir ningún proceso, pues las diferentes propiedades de cada zona del mismo lo hacen inutilizable. Para eliminar la segregación es necesario dar un tratamiento al material para favorecer la difusión y conseguir la homogeneización del mismo. Las impurezas son sustancias extrañas que acompañan a los metales y aleaciones en el proceso de solidificación. Las impurezas se pueden clasificar en tres grupos: Metálicas, No metálicas o inclusiones y Gaseosas. Las impurezas metálicas son aquellas que se alean con los metales que forman la aleación pasando a formar parte de la misma, y modificando por tanto sus propiedades. Estas impurezas no tienen porque ser en principio perjudiciales. Las inclusiones son impurezas de tipo no metálico que no se disuelven en el metal base quedando incluidas en la masa metálica de la aleación. Son partículas extrañas ocluidas en la masa del material, las cuales pueden provenir de los propios moldes, como: trozos de ladrillo refractario del recubrimiento de los hornos, o de los contenedores usados para mantener el fundido, pueden también provenir de las escorias o ser productos de reacción en el proceso de obtención etc. Son inclusiones típicas los óxidos y sulfuros en los aceros, fig. 13, o pequeñas partículas incluidas en los vidrios ordinarios, etc. Estas suelen ser perjudiciales disminuyendo generalmente las propiedades mecánicas. Ejemplos de estas son el SMn en los aceros. Las impurezas gaseosas se forman al Figura 13 quedar atrapadas dentro del metal líquido burbujas de aire o gas. Muchos metales en estado líquido disuelven gran cantidad de gases, sin embargo al solidificar, solo mantienen una pequeña cantidad en disolución, el resto forma burbujas que pueden quedar atrapadas en el metal sólido. También se pueden formar por reaccionar el metal caliente con el molde, por arrastrar aire, en el proceso de vertido, o por reacciones en el metal líquido. Estos defectos si son muy grandes, en general son perjudiciales, pudiendo dar lugar a grietas internas y disminuyendo bastante las propiedades mecánicas. También en un 102 Solidificación sólido pueden aparecer los denominados rechupes, siendo estos cavidades producidas al contraerse el material durante la solidificación. Los aceros tienen gran tendencia a disolver oxígeno en el proceso de fabricación. Durante la solidificación el oxígeno se combina con el carbono presente en la aleación formando CO que puede quedar atrapado produciendo pequeñas burbujas. La adición de Al evita la formación de CO formando Al2O3, dado que el Al tiene mayor afinidad por el oxígeno que el carbono. Cuando se desoxida el acero completamente se le denomina calmado. Cuando no está totalmente desoxidado se dice que el acero es efervescente. Este último está formado por una gran cantidad de microporos muy pequeños, en estas condiciones los aceros son muy aptos para embutición de chapas. Otros defectos de tipo volumen son las grietas producidas en los procesos de conformado (fundición, forja, laminación, soldadura ...). Todos estos defectos son de gran importancia en el comportamiento del material reduciendo en general y a veces drásticamente la resistencia mecánica, eléctrica, etc. 103