Bioquímica hepática (VII) Metabolismo hepático de xenobióticos
Anuncio

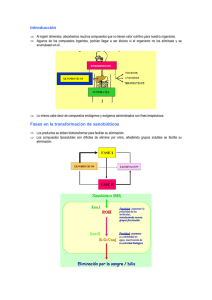
Bioquímica hepática (VII) Metabolismo hepático de xenobióticos. Las reacciones hepáticas de detoxificación Prof. J.V. Castell Al ingerir alimentos, absorbemos muchos compuestos que no tienen valor nutritivo para nuestro organismo... 1 INGREDIENTES: Harina de trigo, Agua, Aceite Vegetal, Levadura, Azúcar, Sal, Suero Lácteo, Emulgentes (E(E-471 y EE-481), Conservantes (E(E-281 y E 202), Vinagre y Estabilizador (E412). (E INGREDIENTES: FLAN:AZUCAR, FECULA, ESTABILIZANTES Y ESPESANTES (E E-410 EE-407), 407 SAL, VAINILLA Y COLORANTES ARTIFICIALES AUTORIZADOS (E(E-102 EE-110). CARAMELO LIQUIDO: GLUCOSA LIQUIDA, AZUCAR Y CONSERVANTE (E(E-211) 2 Algunos de los compuestos ingeridos, podrían llegar a ser tóxicos si el organismo no los eliminase y se acumulasen en él... Lo mismo cabe decir de compuestos endógenos y exógenos administrados con fines terapéuticos... Algunos de los compuestos ingeridos, podrían llegar a ser tóxicos si el organismo no los eliminase y se acumulasen en él... ENDOBIOTICOS TOXICOS ATOXICOS XENOBIOTICOS TERAPEUTICOS NUTRIENTES 3 Biotransformación…por qué RESPIRACIÓ RESPIRACIÓN Volátiles LipoLipo-soluble… soluble…? XENOBIOTICOS BIOTRANSFORMACION Hidro-soluble ORINA HECES SUDOR Cómo se biotransforman los xenobióticos... FASE I XENOBIOTICOS ELIMINACIÓN FASE II 4 El metabolismo de xenobióticos por el hígado... Xenobió Xenobiótico (RH) Fase I ROH Fase II R-O-Conj Finalidad: Finalidad: aumentar la polaridad de las molé moléculas, introduciendo nuevos grupos funcionales Finalidad: Finalidad: aumentar su solubilidad en agua, inactivació inactivación de su actividad bioló biológica Eliminació Eliminación por la sangre / bilis Reacció Reacción de Fase I: I reacciones en las que se introducen nuevos grupos funcionales en la molécula aumentando su polaridad y reactividad Reacció Reacción de Fase II: II Conjugación con moléculas endógenas de la célula, por ej. ácido glucorónico, aumentando notablemente su solubilidad 5 Biotransformació Biotransformación de xenobió xenobióticos Fase I •Hidroxilación •Epoxidación •Desalquilación •Desaminación •S- y N-oxidación Fase II no sti e t In Piel Hígado Pulmones Riñón •Glucuronidación •Glucosidación •Sulfatación •Metilación •Acetilación •Conjug. con GSH •Conjug. con aminoácidos Vías de eliminación de los metabolitos Metabolitos Eliminació Eliminación (detoxificación) • Canalículo biliar • Sinusoide Retí Retículo endoplá endoplásmico Fármaco Por qué enzimas…? 3. Enzimas microsomales extrahepá extrahepáticos (P450, FMN monooxigenasas 1. Enzimas hepá hepáticos microsomales (P450, FMN monooxigenasas) 2. Enzimas hepá hepáticos nono-microsomales: ¾Alcohol/ aldehí aldehído deshidrogenasa hidrolasas, reductasas (Fase (Fase I) I) ¾Acetil transferasas, sulfato transferasas, GSH transferasas, glucoronil transferasas (Fase (Fase II) II) 6 Reacciones de biotransformación de Fase I P450 monooxigenasas Peroxidasas Deshidrogenasas NADPH reductasas Esterasas FMN oxigenasas Tipos de reacciones catalizadas por el citocromo P450 Hidroxilación aromática Hidroxilación alifática N-Dealquilación O-Dealquilación Deaminación N-Oxidación Sulfoxidación 7 El citocromo P450 Hemoproteína. Absorbancia a 450 nm (forma Fe++) Una cadena de 35-45 KDa y grupo prostético heme Asociado a otros componentes en la membrana del retículo endoplásmico Actividad “monooxigenasa” Baja especificidad de substrato Hemoproteínas implicadas en reacciones de oxidación Oxigenasas O2  R + O2 → RO OH + H2 O + D  RH + O2 +DH2 → R-O Dioxigenasas Monooxigenasas Oxidasas  RH2 + O2 → R + H2O2 (2 θ )  2 RH2 + O2 → 2 R + H2O (4 θ ) Peroxidasas  ROOH +2DH2 → R-OH + 2 DH + H2O 8 Estequiometría de la actividad “monooxigenasa” del Citocromo P450 RH + NADPH + H+ + O2 → R-OH + NADP+ + H2O Origen de los electrones en la reacciones de oxidación catalizadas por P450 dadores de θ O2 NAD(P)H Xenobiótico (reducido) P450 Reductasa P450 FADH FMNH Redoxina Fe/S Xenobiótico (oxidado) oxidado) H2O 9 Reacciones catalizadas por el citocromo P450 O2 dadores de θ NAD(P)H Xenobiótico (reducido) P450 Reductasa P450 FADH FMNH Xenobiótico (oxididado) oxididado) H2O Redoxina Fe/S RH + NADPH + H+ + O2 → R-OH + NADP+ + H2O OH Producto H Substrato Fe3+ s OH Substrato P450 n Fe3+ Fe3+ Substrato H P450 P450 e- r H Substrato Mecanismo de la catálisis por el citocromo P450 3+O) (Fe (FeO) P450 P450 CitP450 Reductasa o Substrato Fe2+ H P450 H2O H q H+ Substrato Fe2+OOH Substrato H+ e- P450 H O2 Fe2+ O2 P450 p Cit-b5 10 Componentes del sistema P450 Citoplasma NADPH e- H2O O2 Citocromo P450 reductasa FMN e- Fe2+/Fe3+ FAD Citocromo b5 P450 R Retículo endoplásmico R-OH Citoplasma Nomenclatura del P450 Superfamilia de genes constituida por familias y subfamilias FAMILIA: FAMILIA: homologí homología del 40% aa CYP 1 A 2 NUMERO del gen SUBFAMILIA: SUBFAMILIA: homologí homología del 5555-60 % aa 11 Isoenzimas del Citocromo P450 Familias 1 2 3 5 7 3A3 3A4 3A5 4A9 4B1 4F2 4F3 3A7 4A11 Subfamilias 1A1 4 1B1 1A2 8 11 17 19 21 24 27 21A2 11A1 11B1 11B2 2A6 2B6 2C8 2D6 2E1 2F1 2A7 2C9 2C10 2C18 2C19 Abundancia relativa y variabilidad de los CYPs implicados en el metabolismo humanos de fármacos y xenobióticos CYP 1A2 1B1 2A6 2B6 2C 2D6 2E1 3A4 Abundancia Grado de variabilidad (% total) ~ 13 <1 ~4 <1 ~18 Hasta 2.5 Hasta 7 Hasta 28 ~40-x ~30 - 100-x ~50-x 25-100-x >1000-x ~20-x ~20-x 2E S. Rendic & F.J. DiCarlo, Drug Metab Rev 29:413-80, 1997 12 Los CYPs también se expresan en tejido extrahepático… CYP 1A1 Tejido Pulmón, riñón, intestino, piel, placenta… 1B1 2A6 2B6 2C 2D6 2E1 3A Piel, riñón, próstata, glándula mamaria… Pulmón, epitelio nasal Intestino, pulmón Intestino delgado, laringe, pulmón Intestino Pulmón, placenta… Intestino, pulmón, placenta, feto, utero, riñón S. Rendic & F.J. DiCarlo, Drug Metab Rev 29:413-80, 1997 Enzimas de Conjugación • Glucoronidación (UDP-GT) – 1-naphtol – morphine • Conjugación con GSH (GSH-T) – GSH-Tα (subunidades 1 and 2) – GSH-Tμ (subunidades 3 and 4) – GSH-Tπ (subunidad 7) • Sulfotransferasas – Phenol ST (ST1A1) – N-hydroxy acetaminofluorene (ST1C1), estrogen sulfotransferase (ST1E2) – hydroxyesteroid sulfotransferases (ST 20-21, ST 40-41, ST 60) 13 Reacciones de formació formación y conjugació conjugación del ácido glucoró glucorónico G1P + UTP → UDP-G UDP-G → UDP-GA COOH Enzima: UGT 1A1 R-OH OH + UDP-GA →R-O O-GA R-COOH COOH + UDP-GA →R-CO-O O-GA COOH COOH -R -COCO-R Conjugació Conjugación con GSH y formació formación de derivados del ácido mercaptú mercaptúrico 1. Glutation S-transferasa 2. γ-glutamiltranspeptidasa 3. cisteinil glicinase: 4. N-acetil transferasa 14 Conjugación con sulfato Fosfoadenosil fosfosulfato (PAPS) Diferencias en la expresión de genes CYP no polimórficos CYP2B6 22 20 18 19 21 16 11 7 17 1 5 12 8 3 4 13 6 10 9 2 14 BROD ACTIVITY (pmol/mg x min) MROD ACTIVITY (pmol/mg x min) CYP1A2 70 60 50 40 30 20 10 0 25 20 15 10 5 0 4 3 1 17 7 12 16 14 2 11 8 TEST ACTIVITY (pmol/mg x min) CLZX ACTIVITY (pmol/mg x min) 40000 30000 20000 10000 0 2 13 3 14 1 8 17 7 Liver Nº 9 19 13 18 5 10 22 20 21 CYP3A4 CYP2E1 4 10 11 9 6 Liver Nº Patient Nº 6 16 5 19 20 18 21 22 5000 4000 3000 2000 1000 0 1 17 8 7 11 5 10 6 4 9 2 12 16 21 22 19 18 3 20 14 Liver Nº La variabilidad es mas bien la norma, antes que la excepció excepción...! 15 Variabilidad del Citocromo P450 GENOTIPO + Factores ambientales = FENOTIPO Polimorfismos gené genéticos  Variabilidad en • Edad los niveles de enzimas • Sexo • Raza  Diferencias en el • Dieta, estado nutricional metabolismo  Diferencias en la • Estados patológicos farmacociné farmacocinética • Inductores enzimáticos Un ejemplo: el polimorfismo del CYP2D6 Metabolismo de la debrisoquina - El 7% de la población muestra una metabolización deficiente - Herencia autosomal recesiva - Afecta al metabolismo de 25 fármacos de uso común % Población Debrisoquina CYP2D6 4-Hydroxydebrisoquina Metabolizadores Rápidos Metabolizadores Lentos Significantes diferencias en el metabolismo del fármaco Debrisoquina 4-hidroxylasa 16 Polimorfismos del P450 Causa del polimorfismo Consecuencia No se expresa el gen Defecto parcial Alteración funcional Varias copias del gen Ausencia de metabolización Descenso de la metabolización Alteración de la especificidad Aumento de la metabolización Otros polimorfismos frecuentes Isoenzima P450 Frecuencia de la mutació mutación CYP2A6 5% CYP2C9 20% CYP2C19 10% CYP2D6 23% CYP2E1 2% (*) Enzimas de Fase II NAT-1/2 35% GST(M1/T1/M3/P1/A2) 5-50% UDP-GT ? Factores ambientales que influencian la actividad de los CYPs Nutrición 1A1;1A2;2E1; 3A3; 3A4,5 Tabaco 1A1;1A2 Alcohol 2E1 1A1,1A2; 2A6; 2B6; 2C; 2D6; 3A3, 3A4,5 1A1,1A2; 2A6; 1B; 2E1; Medioambientales 3A3, 3A4,5 Fármacos Rojo enzimas relevantes en el metabolismo de fármacos S. Rendic & F. J. Di Carlo Drug Metab Rev 29: 413-580, 1997 17 Las diferencias en el fenotipo de los enzimas metabolizantes de fármacos y sus consecuencias Toxicidad debida a una dosis excesiva CYP Metabolizador lento Eficacia terapé terapéutica CYP Normal Ineficacia terapé terapéutica CYP Metabolizador rá rápido Consecuencias del polimorfismo del CYP 1. Diferencias en la farmacocinética: biodisponibilidad, vida media 2. Farmacodinámicas: respuesta exagerada, ineficacia terapéutica 3. Interacciones medicamentosas 4. Producción anormal de metabolitos tóxicos 18 Interacción fármaco-fármaco ?+ A B A1 + A2 Fármaco B Fármaco A El metabolismo de uno de los fá fármacos puede verse sensiblemente afectado por la presencia de otro que comparta el mimo enzima o grupo de enzimas para su metabolizació metabolización B1 + B2 B B1 + B2 A A1 + A2 B B1 + B2 A A1 + A2 CONCENTRACIÓN de “A” Interacción fármaco-fármaco A+B Toxicidad A Ventana terapé terapéutica Ineficacia TIEMPO La concentración plasmática del fármaco A puede elevarse en presencia del fármaco B causando efectos tóxicos 19 Efecto de flavonoides presentes en el zumo de pomelo sobre el metabolismo de fármacos 5mg + zumo control Cl H CH 3 O 2 C CH 3 N H Cl Cl CO 2 CH 3 3A4 Cl CO 2 CH 3 CH 3 O 2 C CH 3 CH 3 N CH 3 D.G. Bailey, et al.; Br J Clin Pharmacol 1998, 46:101-110 Inhibidores de CYP3A4 HN H N S N H N Cim etidine N N N Cl N Clotrim azole Cl Cl O O O N O N N Ketoconazole H N 20 El fenómeno de la inducción enzimática ¿Qué es...? ¿Qué trascendencia tiene...? 20 18 16 14 12 10 8 6 4 2 0 M C 2uM P b 2m M 5 3A 3A 4 1 2 E 6 2D 19 2C 9 2C 6 2A 2 1A on tr ol R if 5 0 u M C Times Induction over control Induction of MC, Pb, Rif (Human hepatocytes; incubation 48h) 21 x B (Cyp 4A) x x PXR x x AhR PPAR CAR x Hsp90 AhR x Sp1 C/EBPα Arnt RXR PXR RXR CAR RXR PPAR PPAR - x (Cyp 1A) x x CAR D AhR - C (Cyp 3A) Hsp90 A (Cyp 2B) Cytosol HNF-1 C/EBPβ Nucleus TATAA HNF-3 C/EBPβ (LAP) CYP-promoter SXR=PXR=PAR=PRR El fenómeno de la inducción enzimática: ¿por qué es relevante?  Si un compuesto actúa como inductor enzimático, la expresión de ciertos enzimas de biotransformación aumentará tras la administración repetida del compuesto.  Cambios en la expresión de enzimas de biotransformación influyen la farmacocinética de los fármacos  Un fármaco cuya farmacocinética cambia el el curso de su administración a un paciente es un fármaco de más dificil manejo clínico 22 Inducción del P450 - Importancia Fármacos que inducen su propio metabolismo ó la biotransformación de otros fármacos en el hombre Grupo farmacoló farmacológico Ejemplos Analgésicos, antipiréticos y antiinflamatorios Antibióticos Anticonvulsivantes Antifúngicos Antilipidémicos Antimaláricos Diuréticos Psicotropos Sedantes e hipnóticos Esteroides Vitaminas Antipirina Fenilbutazona Rifampicina Carbamazepina, Fenitoina Griseofulvina Halofenato Quinina Espironolactona Clorimipramina Barbitúricos Testosterona Vitamina C Biotransformación = Detoxificación? 23 Toxicidad como consecuencia del metabolismo... Xenobió Xenobiótico (RH) Phase I Radicales & ROS Metabolitos electrofí electrofílicos ROH Metabolitos tó tóxicos Cell toxicity Phase II Conjugados reactivos R-O-Conj Metabolitos tó tóxicos Toxicidad para las cé células proximales Xenobiótico Bioactivación Detoxificación Biotransformació Biotransformación Metabolito nono-reactivo, menos tó tóxico Conjugació Conjugación Lípidos Metabolito reactivo Proteí Proteínas DNA Eliminació Eliminación Peroxidació Peroxidación de lí lípidos Desnaturalizació Desnaturalización Genotoxicidad Unió Mutaciones Unión covalente 24 Paracetamol NHCOCH3 NHCOCH3 1. Conjugació Conjugación sulfato 2. Conjugació Conjugación Glucoró Glucorónico NHCOCH3 OH 3. Citocromo P450 OSO3H NCOCH3 OC6H9O6 NHCOCH3 GSH δ+ NHCOCH3 Unió Unión Covalente a proteí proteínas hepá hepáticas SCH2 CHCOOH O OH Acido Mercaptú Mercaptúrico N-Acetil-p-benzoquinona imina Necrosis Toxicidad hepá hepática del paracetamol • El paracetamol (acetaminofeno) es una analgésico muy bien tolerado, y de toxicidad baja, que sin embargo puede ser fatal tras una sobredosis • El metabolismo del paracetamol es primariamente a través de su conjugación con sulfato (1), pero dado que la capacidad del organismo es limitada, si se aumenta la dosis de fármaco (1-2 g) se formarán también conjugados glucurónicos (2) • Si hay una sobredosis (>6g), cabe la posibilidad de que el fármaco de oxide (3) por el CYP2E1, formándose el intermedio reactivo N-Acetil-p-benzoquinona imina • Este intermedio, más reactivo y tóxico es conjugado con GSH y posteriormente eliminado como un derivado del ácido mercaptúrico • En el caso de una sobredosis mayor (>10g), y dado que la capacidad de producción y conjugación con GSH es limitada, el intermedio reactivo puede reaccionar con grupos SH de proteínas críticas, modificándolas (inactivándolas) y formando aductos covalentes • Ello lleva a una necrosis del hepatocito que se manifiesta como una insuficiencia hepática fatal • La administración de precursores de GSH (N-acetilcisteína) previene la toxicidad 25