constante de anarmonicidad
Anuncio

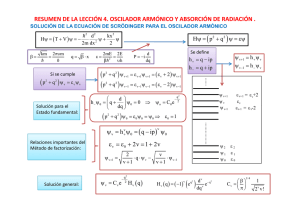
ANARMONICIDAD Y RESONANCIA EN VIBRACIONES DE MOLÉCULAS Jiménez Bárcenas Nadia Rosalina López Salazar Fátima Mendoza Pérez Bernardo Monzón González César Raúl Equipo 3: Principios de estructura de la materia Introducción Al interactuar con las partículas cargadas (núcleos y electrones), los campos eléctricos y magnéticos de la radiación electromagnética provocan una perturbación dependiente del tiempo que puede inducir transiciones entre los estados cuánticos de un sistema. Las transiciones ocurren entre los niveles energéticos disponibles: Rotacionales Vibracionales Traslacionales Electrónicos Probabilidad de transición El Hamiltoniano de un determinado átomo o molécula, en general, no depende del tiempo, de tal manera que la ecuación de valores propios asociada a éste se encuentra dada por: La radiación electromagnética provoca una perturbación dependiente del tiempo Oscilador armónico Ley de Hooke * Energía potencial * Energía cinética Tratamiento mecanocuántico Reglas de selección Anarmonicidad Desviación de un sistema oscilante del movimiento armónico simple. Sucede cuando un oscilador vibra a frecuencias distintas a su frecuencia fundamental. Oscilador armónico: Pequeñas amplitudes de vibración. El espaciado entre los niveles se va haciendo más pequeño hasta formar un continuo en el límite de disociación. Potencial anarmónico (rojo) y potencial armónico (amarillo) Una corrección al modelo del oscilador armónico: 1 2 𝑉 = 𝑘 𝑟 − 𝑟𝑒 2 1 3 − 𝑘 ′ 𝑟 − 𝑟𝑒 3 donde k>>k’. La solución de la ecuación de Schrödinger da los niveles de oscilador anarmónico iguales a: 𝐸𝑣 = 𝑣𝑒 1 1 2 𝑣+ − 𝑣𝑒 𝑥𝑒 (𝑣 + ) 2 2 xe es la constante de anarmonicidad y ve es la separación uniforme entre niveles que corresponden a la parábola con centro en re . Regla de selección: ∆𝑣 = ±1, ±2, ±3 Banda fundamental (∆v=+1) Sobretonos (∆v= +2, +3) La intensidad de estas bandas de sobretonos decrece rápidamente, ya que la probabilidad del tránsito disminuye rápidamente a medida que v aumenta. Potencial de Morse V = ℎ𝑐𝐷𝑒 1 − 𝑒 −𝑎 𝑟−𝑟𝑒 2 𝑎= 𝑚𝑒𝑓 𝜔2 2ℎ𝑐𝐷𝑒 De es la profundidad del mínimo de energía potencial (Energía de disociación). 1/2 Los niveles de energía permitidos son: 1 1 𝐸 𝑣 = 𝑣+ ṽ− 𝑣+ 2 2 2 𝑎2 ℏ ṽ 𝑥𝑒 ṽ 𝑥𝑒 = = 2𝑚𝑒𝑓 𝜔 4𝐷𝑒 xe es la constante de anarmonicidad. El número de niveles vibracionales de un oscilador de Morse es finito, y v= 0, 1, 2,…, vmáx. Expresión más general 𝐸 𝑣 = 𝑣+ 1 2 ṽ− 𝑣+ 1 2 𝑥𝑒 ṽ + 2 𝑣+ 1 3 𝑦𝑒 ṽ 2 +⋯ donde xe, ye… con constantes empíricas adimensionales características de la molécula y para hallar la energía de disociación de la molécula. Frecuencia de radiación absorbida o emitida por un sistema Depende de la separación entre los niveles de energía Electrónica Nuclear Sistema molecular Diferentes tipos de energías Orientación de espines Rotación Vibración Espectroscopia de rotación pura Ocurre en el IR lejano y microondas Las transiciones se producen entre estados con el mismo número cuántico vibracional y diferente numero cuántico rotacional Los números de onda de las líneas espectrales Usando aproximación de rotor rígido El espectro de rotación consiste en una serie de líneas espectrales que aparecen en los números de onda 2𝐵𝑒 , 4𝐵𝑒 , 6𝐵𝑒 , … , Están equiespaciadas Espectroscopia vibracional-rotacional Moléculas reales Vibración Rotación Se producen al mismo tiempo Reglas de selección Combinación de rotacional y vibracional ∆𝑣 = ±1 ∆𝐽 = ±1 Estudio de las transiciones en 2 grupos: ∆𝑣 = 1 , ∆𝐽 = 1 Tomando a 𝑣 = 0 como el nivel más bajo 𝜔𝑣𝑅 3 1 ´´ ´´ = 𝜔𝑣 + 𝐵 𝐽 + 1 𝐽 + 2 − 𝜔𝑣 − 𝐵𝐽´´ 𝐽´´ + 1 2 2 = 𝜔𝑣 + 2𝐵 𝐽´´ + 1 ∆𝑣 = 1 , ∆𝐽 = −1 Tomando a 𝑣 = 0 como el nivel más bajo = 𝜔𝑣 + 2𝐵𝐽´´ (𝐽´´ = 1,2,3) Rama P del espectro (𝐽´´ = 0,1,2,3) Rama R del espectro Aproximación del rotor rígido oscilador armónico 2 series de líneas con un espaciamiento igual a 2B con un hueco entre ambos conjuntos, que representa la frecuencia de vibración fundamental 𝜔0 Rama Q Frecuencia de radiación absorbida Teoría más exacta 3 modificaciones del esquema de movimiento vibración-rotación moléculas diatómicas para adecuarlo a moléculas reales Corrección Efectos de alargamiento centrifugo Corrección No de movimiento rotacional de movimiento vibracional armonicidad de la vibración Corrección Cambios rotación) de constante de rotación en el momento de inercia (acoplamiento vibración- Alargamiento centrifugo para molécula diatómica Rota rápidamente (excitada a estados rotacionales más altos) Incrementa el momento de inercia Decrece la constante de rotación B Es contrarrestado por la cte. De fuerza del enlace 4𝐵3 2 𝐸𝐽 = 𝐵𝐽 𝐽 + 1 − 2 𝐽 (𝐽 + 1)2 𝜔𝑣 = BJ J + 1 − D𝐽2 𝐽 + 1 2 EFECTO Las líneas del espectro rotacional puro no estarán igualmente espaciadas No armonicidad del sistema Los efectos son más importantes a mayor numero Constante de no armonicidad cuántico vibracional 𝑣 1 1 𝜔𝑣 = 𝑣 + 𝜔𝑒 − 𝜔𝑒 𝑥𝑒 𝑣 + 2 2 2 Energía vibracional de la molécula en ausencia de cualquier no armonicidad EFECTO Niveles de energía con espaciado diferente Modifica funciones de onda vibracionales y por lo tanto las reglas de selección ∆𝑣 = ±2,3 (armonicos) ∆𝑣 = ±1 (fundamental) Acoplamiento rotación-vibración La contante rotacional B observada debe ser considerada como función del número cuantico vibracional 𝑣 1 𝐵𝑣 = 𝐵𝑒 − 𝛼 𝑣 + 2 Cte. Rotacional (hipotética) en ausencia de vibraciones Constante de acoplamiento rotaciónvibración EFECTO Líneas de la rama R se junten y las de la rama P se separen a medida que 𝐽´´ crece Rama R 𝜔𝑣.𝑅 = 𝜔𝑣 + 2𝐵´ + 3𝐵´ − 𝐵´´ 𝐽´´ + 𝐵´ − 𝐵´´ 𝐽´´ 2 (𝐽´´ = 0,1, … ) Rama P 𝜔𝑣.𝑅 = 𝜔𝑣 − 𝐵´ + 𝐵´´ 𝐽´´ + 𝐵´ − 𝐵´´ 𝐽´´ 2 (𝐽´´ = 1,2, … ) Espectroscopía infrarroja Espectroscopía Es la interacción entre la radiación y la materia como función de la longitud de onda (λ). Espectroscopía infrarroja Es un tipo de espectroscopía de absorción, que utiliza la región infrarroja del espectro electromagnético con la finalidad de identificar un compuesto o investigar la composición de una muestra. Esta técnica se basa en el hecho de que los enlaces químicos de las sustancias tienen frecuencias de vibración específicas, que corresponden a los niveles de energía de la molécula. Estas frecuencias dependen: forma de la superficie de energía potencial de la molécula, la geometría molecular, las masas atómicas y, el acoplamiento vibracional. Espectroscopía de Raman Es una técnica espectroscópica utilizada en química para el estudio de los modos vibracionales, rotacionales y otros de baja frecuencia en un sistema Espectro Raman Contiene una serie de líneas cuya frecuencia está desplazada de la frecuencia original de excitación Estas líneas son caracterísiticas de la sustancia dispersante. Se basa en la dispersión inelástica, o dispersión Raman, de la luz monocromática. La luz láser interactúa con fonones u otras excitaciones en el sistema, por lo que la energía de los fotones láser se desplaza hacia arriba o hacia abajo. Resonancia de Fermi Resulta del acoplamiento de una banda de absorción fundamental con un sobretono o una banda de combinación. Fermi observó este fenómeno en el espectro Raman del CO2. En el espectro de Raman de CO2, se espera una única banda fundamental ν1 debida a la vibración de tensión simétrica Σ+g. En su lugar, se observan dos bandas intensas a 1285 y 1388 cm-1. Bibliografía Díaz, P. M.; Roig M. A. Química Física. Volumen I. Ed. Alhambra. España, 1985, pp. 430-433. Engel, T.; Reid, Philip; et al. Química Física. Ed. Pearson Addison Wesley. España, 2006, pp. 407-409. Atkins, P.; De Paula, J. Química Física. Ed. Médica Panamericana. Argentina, 2008. pp. 455-456. Levine, I. N. Química Cuántica. 5ta. Edición. Prentice Hall. España, 2001. pp. 61-88. W. F. Pickering. Química analítica moderna. Ed. Reverté, España, 1980. http://www.espectrometria.com (Consultada el 22 de marzo) Hanna, M.W.; Mecánica cuántica para químicos. Ed. Fondo Educativo Interamericano.1985. pp.106-123 Murillo; espectroscopia y estructuras atómicas. Ed Alhambra. pp. 6-10 http://biblioteca.ucm.es/tesis/19911996/X/0/X0021601.pdf (Consultada el 21 de marzo)