terapia de combinacion para canceres avanzados que
Anuncio

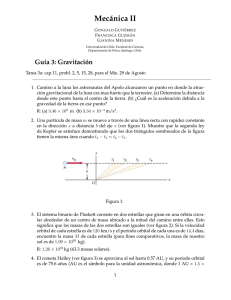
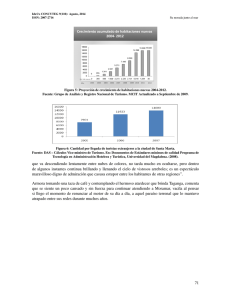
k OFICINA ESPAÑOLA DE PATENTES Y MARCAS 19 k kInt. Cl. : A61K 31/53 11 Número de publicación: 2 162 092 7 51 ESPAÑA A61K 33/24 //(A61K 33/24 A61K 31:53) k TRADUCCION DE PATENTE EUROPEA 12 kNúmero de solicitud europea: 96930553.1 kFecha de presentación: 26.08.1996 kNúmero de publicación de la solicitud: 0 858 341 kFecha de publicación de la solicitud: 19.08.1998 T3 86 86 87 87 k 54 Tı́tulo: Terapia de combinación para cánceres avanzados que comprende temozolomida y cisplatino. k 30 Prioridad: 28.08.1995 US 2877 P 27.03.1996 US 624795 2000 Galloping Hill Road Kenilworth, New Jersey 07033-0530, US k 72 Inventor/es: Dugan, Margaret H. k 74 Agente: Elzaburu Márquez, Alberto 45 Fecha de la publicación de la mención BOPI: 16.12.2001 45 Fecha de la publicación del folleto de patente: 16.12.2001 ES 2 162 092 T3 k 73 Titular/es: SCHERING CORPORATION Aviso: k k En el plazo de nueve meses a contar desde la fecha de publicación en el Boletı́n europeo de patentes, de la mención de concesión de la patente europea, cualquier persona podrá oponerse ante la Oficina Europea de Patentes a la patente concedida. La oposición deberá formularse por escrito y estar motivada; sólo se considerará como formulada una vez que se haya realizado el pago de la tasa de oposición (art. 99.1 del Convenio sobre concesión de Patentes Europeas). Venta de fascı́culos: Oficina Española de Patentes y Marcas. C/Panamá, 1 – 28036 Madrid ES 2 162 092 T3 DESCRIPCION Terapia de combinación para cánceres avanzados que comprende temozolomida y cisplatino. 5 10 15 20 25 A pesar de los numerosos avances en el tratamiento del cáncer, los cambios bien conocidos del estilo de vida que pueden reducir enormemente el riesgo de cáncer, y los signos de advertencia tempranos que proporcionan algunos cánceres, muchos pacientes desarrollan no obstante cáncer avanzado para el cual no existen terapias convencionales que ofrezcan ninguna esperanza de curación razonable o paliación significativa. Esta invención consiste en el uso de dos agentes anti-tumorales conocidos en terapia combinada para proporcionar un efecto positivo sobre dichos cánceres avanzados. Se espera asimismo que la terapia combinada permita la administración de los dos agentes antitumorales en cantidades que no originen efectos secundarios inadmisibles. La temozolomida se conoce por sus efectos anti-tumorales. Por ejemplo, en un estudio se lograron respuestas clı́nicas en 17 % de los pacientes con melanoma avanzado (Newlands ES, et al. Br J Cancer 65 (2) 287-1981, 1992). En otro estudio se logró respuesta clı́nica en 21 % de los pacientes con melanoma avanzado (Journal of Clinical Oncology, Vol 13, No. 4 (Abril), 1995, pp 910-913). Sin embargo, la temozolomida presenta efectos secundarios limitativos de la dosis, como toxicidad hematológica, mielosupresión, anemia, leucopenia, etc. Se sabe que el cisplatino tiene propiedades antitumorales (véase, por ejemplo B. Rosenberg et al. Nature 205, 698 (1965) y 222, 385 (1972). Sin embargo, tiene también efectos secundarios limitativos de la dosis como nefrotoxicidad y ototoxicidad. El uso combinado de cisplatino y temozolomida in vitro se menciona en J. Chemother., 7(3), pp. 224-229, 1995. Es necesario un método pra tratar cánceres avanzados con mayores tasas de respuesta o efectos secundarios reducidos, o ambos. 30 35 Sumario de la invención Esta invención se puede resumir como un método para tratar el cáncer avanzado en pacientes que necesitan dicho tratamiento, que comprende administrar temozolomida y cisplatino en cantidades suficientes para lograr una respuesta clı́nica. La temozolomida se administra al paciente en combinación con el cisplatino, es decir, la dosis de temozolomida y cisplatino se administran durante el mismo perı́odo de tiempo. Los programas de administración preferidos se enumeran más abajo. Descripción detallada 40 El término “temozolomida” se refiere a un compuesto de fórmula. 45 50 55 60 Un nombre quı́mico para la temozolomida es 3,4-dihidro-3-metil-4-oxoimidazo-[5,1-d]1,2,3,4-tetrazin8-carboximida. La sı́ntesis de temozolomida es bien conocida. Véase, por ejemplo, Stevens et al., J. Med. Chem., 1984, 27, 196-201 y Wang et al. J. Chem. Soc., Chem. Commun., 1994, pp 1687-1688. 2 ES 2 162 092 T3 La fórmula del cisplatino (cis-diaminadicloroplatino, The Merc. Index compuesto N◦ 2319, 11th edition) es: QQ NH PtQQ Cl NH Cl 5 3 3 10 15 Los cánceres avanzados tratables mediante esta invención incluyen melanoma maligno, melanoma metastático maligno, cáncer de pulmón, cáncer de mama, cáncer cerebral, cáncer ovárico, cáncer de cabeza y/o de cuello, sarcoma, cáncer de próstata y otros cánceres que se sabe que son al menos parcialmente sensibles al tratamiento con cisplatino, los cuales han avanzado hasta una etapa en la que es improbable que la terapia convencional proporcione una cura. Una persona que padece de cáncer avanzado puede presentar uno o más de los siguientes signos o sı́ntomas: (a) presencia de tumor canceroso, 20 (b) fatiga, (c) dolor, (d) estado de rendimiento reducido procedente de la carga tumoral, y 25 (e) los bien conocidos sı́ntomas asociados con cada cáncer especı́fico. Para poner en práctica la invención, se administran temozolomida y cisplatino al paciente que presenta uno o más de los signos o sı́ntomas anteriores, en cantidades suficientes para eliminar o al menos aliviar uno o más de dichos signos o sı́ntomas. 30 35 La dosis preferida de temozolomida para poner en práctica la terapia combinada de esta invención es 50 a 400 mg por m2 de la superficie corporal del paciente por dı́a, con mayor preferencia 75 a 300 mg/m2 y con la máxima preferencia 100 a 200 mg/m2 /dı́a. Preferiblemente la dosis diaria de temozolomida se administra una vez al dı́a durante un perı́odo de 2 a 10 dı́as, con mayor preferencia durante un perı́odo de 3 a 8 dı́as y con la máxima preferencia durante un perı́odo de 5 dı́as. Alternativamente, la temozolomida se puede administrar durante un perı́odo mucho más largo a una dosis reducida. Por ejemplo, la temozolomida podrı́a administrarse diariamente durante 6 dı́as a seis semanas, a una dosis de 50 a 150 mg/m2/dı́a. 40 La temozolomida se puede administrar por vı́a oral en forma de cápsula, en la que se mezcla con vehı́culos farmacéuticos convencionales. Las formulaciones de cápsulas de temozolomida preferidas son: Ingrediente 45 Temozolomida Lactosa anhidra NF Glicolato de almidón sódico NF Dióxido de silicio coloidal NF Ácido tartárico NF Ácido estéarico NF Tamaño de la cápsula∗ 50 55 ∗ 60 mg/Cápsula 5 132,8 20 182,2 100 175,7 250 154,3 7,5 11,0 15,0 22,5 0,2 1,5 3,0 3 0,2 2,2 4,4 2 0,3 3,0 6,0 1 0,7 9,0 13,5 0 cápsulas de gelatina dura con dos piezas, exentas de conservantes, blancas opacas. Se prefiere especialmente que el paciente se abstenga de tomar cualquier comida o bebida, excepto agua, durante cuatro horas antes de la administración de temozolomida y durante dos horas después. 3 ES 2 162 092 T3 5 10 15 20 25 30 35 40 45 50 55 60 El cisplatino se administra preferiblemente con una única perfusión intravenosa en el dı́a uno del perı́odo de administración de la temozolomida, aproximadamente cuatro horas después de la administración de temozolomida del primer dı́a. Para mantener una hidratación suficiente se administra antes y después de la infusión de cisplatino, un litro de suero salino normal con 20 meq KCI/L y 1 g de sulfato de magnesio, a una velocidad de aproximadamente 250 ml/hora. La cantidad de cisplatino en la perfusión es preferiblemente 25 a 300 mg por m2 de superficie corporal del paciente, con mayor preferencia 50 a 150 mg/m2 y con la máxima preferencia 75 a 100 mg/m2. Se puede suministrar fluido adicional para mantener una producción adecuada de orina. El cisplatino se administra preferiblemente con 500 ml de suero salino normal que contiene 12,5 g de manitol, durante un perı́odo de una hora. Alternativamente, la dosis de cisplatino listada en el párrafo anterior se podrı́a administrar durante un perı́odo de 2 a 5 dı́as. Se podrı́an administrar hasta 100 mg/dı́a/m2 de la superficie corporal del paciente, diariamente durante 5 dı́as consecutivos. Tras un perı́odo de aproximadamente 28 a 42 dı́as, preferiblemente 28 dı́as, desde el primer dı́a del perı́odo de administración de temozolomida, se puede efectuar otro ciclo de administración, siendo administrada la temozolomida en el dı́a uno y en cada dı́a sucesivo del perı́odo de administración y siendo administrado el cisplatino en el dı́a uno o, con menor preferencia durante un perı́odo de 2 a 5 dı́as. Por ejemplo, para un perı́odo de administración de temozolomida de cinco dı́as, un perı́odo de administración de cisplatino de un dı́a, y un ciclo de tratamiento de 28 dı́as, el tratamiento llevará cinco dı́as (tratamiento con temozolomida en los dı́as 1 a 5 y tratamiento con cisplatino en el dı́a 1), seguido por 28-5 = 23 dı́as durante los cuales no se aplica ningún tratamiento, seguido por cinco dı́as más de tratamiento como al comienzo del segundo ciclo. Los ciclos de tratamiento se pueden continuar hasta que se logre una respuesta clı́nica o hasta que aparezcan efectos secundarios inadmisibles. Las dosis de temozolomida y/o cisplatino se pueden incrementar en cada nuevo ciclo de tratamiento, con la condición de que no aparezcan efectos secundarios inadmisibles. Las dosis pueden asimismo reducirse, si se encuentran efectos secundarios inadmisibles. Actualmente se prefiere adaptar gradualmente la dosis de temozolomida, mientras que se mantiene constante la dosis de cisplatino. Un efecto secundario común, pero admisible tanto de la temozolomida como del cisplatino son náuseas y vómito. Éstos se pueden aliviar administrando un antiemético conjuntamente con la temozolomida. Preferiblemente, el antiemético Ondansetron se administra por vı́a oral en una dosis de aproximadamente 8 mg, aproximadamente 30 minutos antes de la administración de temozolomida. Igualmente, es preferible administrar Ondansetron 32 mg IV o Granisetron 1 mg IV y Decadron 10 mg IV, aproximadamente 30 minutos antes de la perfusión de cisplatino. Por supuesto se pueden utilizar otros antieméticos como Haldol, Benadryl y Ativan según las necesidades. Por supuesto, se consideran otras formas de administración de ambos ingredientes activos, cuando éstas estén disponibles, como mediante pulverizador nasal, transdérmicamente, mediante supositorio, mediante una forma de dosificación de liberación prolongada, mediante inyección IV, etc. Cualquier forma de administración funcionará, siempre que se suministren las dosis adecuadas sin destruir el ingrediente activo. La efectividad del tratamiento se puede determinar mediante ensayos clı́nicos controlados. Se incluirán en el estudio pacientes que tengan cáncer avanzado con tumores mensurables o evaluables. Un tumor mensurable es aquél que se puede medir en al menos dos dimensiones, como un tumor de pulmón rodeado por pulmón ventilado, un nódulo cutáneo o un ganglio linfático superficial. Un tumor evaluable es aquél que se puede medir en una dimensión, como un tumor de pulmón no completamente rodeado por pulmón ventilado o una masa de tejido blando o abdominal palpable que se puede medir en una dimensión. Los marcadores tumorales, los cuales se ha determinado que están altamente correlacionados con la extensión de la enfermedad, se tendrán en cuenta asimismo para aportar un indicio de enfermedad evaluable, como el PSA para el cáncer de próstata, el CA-125 para el cáncer ovárico, el CA-15-3 para el cáncer de mama, etc. El tumor se medirá o evaluará antes y después del tratamiento mediante cualesquiera que sean los medios que proporcionen la medición más precisa, como tomografı́a axial computerizada, resonancia magnética nuclear, ultrasonografı́a, etc. Los nuevos tumores o la falta de los mismos en campos previamente irradiados se puede utilizar para valorar la respuesta anti-tumoral. Los criterios para evaluar la respuesta serán similares a los del WHO Handbook of Reporting Results of Cancer Treatment, WHO Offset Publication 1979, 49-World Health Organization, Geneva. Se determinan los siguientes resultados para tumores mensurables unidimensional y bidimensionalmente. 4 ES 2 162 092 T3 Respuesta completa: Desaparición completa de toda enfermedad maligna clı́nicamente detectable, determinada mediante dos observaciones separadas por no menos de cuatro semanas. 5 Respuesta parcial: (a) Para tumores mensurables bidimensionalmente, una reducción de al menos 50 % en la suma de los productos de los diámetros perpendiculares mayores de todos los tumores mensurables, tal y como se determina según dos observaciones separadas por no menos de cuatro semanas. En casos en los que el paciente tiene múltiples tumores, no es necesario que todos los tumores hayan sufrido una regresión para lograr una respuesta parcial tal y como aqui se define, pero ningún tumor debe haber progresado y no debe haber aparecido ningún nuevo tumor. 10 15 Enfermedad estable: (a) Para tumores mensurables bidimensionalmente, menos de un 50 % de reducción a menos de un 25 % de incremento en la suma de los productos de los diámetros perpendiculares mayores de todos los tumores mensurables. (b) Para tumores mensurables unidimensionalmente, menos de 50 % de reducción a menos de 25 % en la suma de los diámetros de todos los tumores. Para (a) y (b) no deben aparecer nuevos tumores. 20 Ninguna respuesta clı́nica, es decir enfermedad progresiva, definida aquı́ como un incremento de más del 50 % en el producto de los diámetros perpendiculares mayores para al menos un tumor mensurable bidimensionalmente, o un incremento de más del 25 % en la dimensión mensurable de al menos un tumor mensurable unidimensionalmente. Para pacientes que tienen tumores mensurables tanto unidimensionalmente como bidimensionalmente, la respuesta total se determinará de acuerdo con la siguiente tabla. 25 30 35 40 Respuesta en enfermedad mensurable Respuesta en enfermedad mensurable bidimensionalmente unidimensionalmente Respuesta global PD cualquiera SD SD PR CR CR cualquiera PD SD o PR CR SD o PR o CR SD o PR CR PD PD SD PR PR PR CR Abreviaturas: 45 50 55 60 PD: CR: PR: S.D.: Enfermedad progresiva Respuesta completa Respuesta parcial Enfermedad estable Por supuesto, se puede utilizar asimismo para evaluar la efectividad de la invención la eliminación o alivio de otros signos o sı́ntomas conocidos del cáncer avanzado, especialmente los enumerados anteriormente. Los cánceres avanzados deben evaluarse, es decir los tumores medirse, etc., no más de 14 dı́as antes del inicio del tratamiento. Dichos cánceres deben volverse a evaluar aproximadamente 28 dı́as después del dı́a 1 de administración de la primera dosis de temozolomida y cisplatino. Veintiocho dı́as después de su administración inicial se puede efectuar otro perı́odo de administración, y efectuar las evaluaciones 28 dı́as después del comienzo de este segundo ciclo. Los ciclos de tratamiento se pueden continuar hasta que se logre una respuesta clı́nica o hasta que aparezca una toxicidad inaceptable. Otro aspecto de esta invención es el tratamiento del cáncer avanzado con efectos secundarios reducidos, asociados normalmente con temozolomida y cisplatino. Se cree que este objetivo se puede lograr mediante la administración de dosis inferiores de los dos ingredientes activos o mediante una duración reducida de la administración, provocada por el efecto sinérgico de la combinación. 5 ES 2 162 092 T3 El efecto secundario más grave de la temozolomida es la toxicidad hemotológica. La toxicidad limitativa de dosis para la temozolomida se define aquı́ como 5 Neutropenia CTC de grado 4 (recuento absoluto de neutrófilos, incluyendo bandas, inferior a 0,5 x 103 /mm3) que no se resuelva en cinco dı́as o Anemia CTC de grado 4 (hemoglobina inferior a 6,5 g/dl), o Trombocitopenia CTC de grado 3 (recuento de plaquetas inferior a 50 x 103 /mm3), o 10 15 Trombocitopenia CTC de grado 4 (recuento de plaquetas inferior a 25 x 10 3 /mm3). El efecto secundario más común de cisplatino es la nefrotoxicidad. La toxicidad limitativa de dosis provocarı́a una persistencia de creatinina sérica superior a 2,2 mg/dL durante más de 2 semanas desde el momento de la administración. 20 25 30 35 40 45 50 55 60 6 ES 2 162 092 T3 REIVINDICACIONES 5 10 15 20 25 30 35 1. Uso de temozolomida en la fabricación de una composición farmacéutica para tratar el cáncer avanzado en pacientes mediante un régimen de tratamiento que comprende administrar temozolomida y cisplatino, en el que la cantidad de temozolomida administrada es de 50 a 400 mg por m2 de la superficie corporal del paciente por dı́a, durante un perı́odo de 2 a 10 dı́as y la cantidad de cisplatino administrada es de 25 a 300 mg por m2 de la superficie corporal del paciente como dosis única en el primer dı́a de administración de la temozolomida. 2. Uso de cisplatino en la fabricación de una composición farmacéutica para tratar el cáncer avanzado en pacientes mediante un régimen de tratamiento que comprende administrar temozolomida y cisplatino, en el que la cantidad de temozolomida administrada es de 50 a 400 mg por m2 de la superficie corporal del paciente por dı́a, durante un perı́odo de 2 a 10 dı́as y la cantidad de cisplatino administrada es de 25 a 300 mg por m2 de la superficie corporal del paciente como dosis única en el primer dı́a de administración de temozolomida. 3. Uso de tanto temozolomida como de cisplatino en la fabricación de una composición farmacéutica para tratar el cáncer avanzado en pacientes mediante un régimen de tratamiento que comprende administrar temozolomida y cisplatino, en el que la cantidad de temozolomida administrada es de 50 a 400 mg por m2 de la superficie corporal del paciente por dı́a, durante un perı́odo de 2 a 10 dı́as y la cantidad de cisplatino administrada es de 25 a 300 mg por m2 de la superficie corporal del paciente como dosis única en el primer dı́a de administración de la temozolomida. 4. Uso según cualquiera de las reivindicaciones precedentes, en el que se repiten las administraciones de temozolomida y cisplatina empezando de 28 a 42 dı́as después del primer dı́a del perı́odo de administración de temozolomida. 5. Uso según cualquiera de las reivindicaciones precedentes, en el que la cantidad de temozolomida administrada es de 75 a 300 mg por m2 de la superficie corporal del paciente, durante un perı́odo de 3 a 8 dı́as, y la cantidad de cisplatino administrada en de 50 a 150 mg por m2 de la superficie del cuerpo del paciente como dosis única en el primer dı́a de administración de temozolomida. 6. Uso de la reivindicación 5, en el que la cantidad de temozolomida administrada es de 100 a 200 mg por m2 de la superficie del cuerpo del paciente por dı́a, durante un perı́odo de 5 dı́as, y la cantidad de cisplatina administrada es de 75 a 100 mg por m2 de la superficie corporal del paciente como dosis única en el primer dı́a de administración de temozolomida. 40 7. Uso según cualquiera de las reivindicaciones precedentes, en el que se repiten las administraciones de temozolomida y cisplatino empezando 28 dı́as después del primer dı́a del perı́odo de administración de temozolomida. 45 8. Uso según cualquiera de las reivindicaciones precedentes, en el que la temozolomida se administra por vı́a oral después de que el paciente se haya abstenido de tomar comida o lı́quidos distintos de agua durante 4 horas antes de la administración de temozolomida, y durante 2 horas después de la administración de temozolomida, y el cisplatino se administra por perfusión intravenosa. 9. Uso de la reivindicación 1, en el que la temozolomida se administra por vı́a oral durante un perı́odo de 6 dı́as a 6 semanas. 50 55 60 NOTA INFORMATIVA: Conforme a la reserva del art. 167.2 del Convenio de Patentes Europeas (CPE) y a la Disposición Transitoria del RD 2424/1986, de 10 de octubre, relativo a la aplicación del Convenio de Patente Europea, las patentes europeas que designen a España y solicitadas antes del 7-10-1992, no producirán ningún efecto en España en la medida en que confieran protección a productos quı́micos y farmacéuticos como tales. Esta información no prejuzga que la patente esté o no incluı́da en la mencionada reserva. 7



![[Prac06-Práctica]](http://s2.studylib.es/store/data/003990529_1-28dd385af0e25f48e807d3d91fd5c4f2-300x300.png)


