Código Genético y Traducción
Anuncio

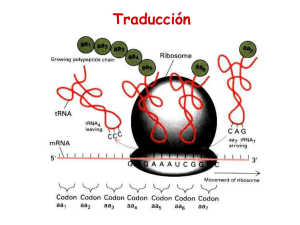
Facultad de Química, UNAM 1630 Genética y Biología Molecular Código Genético y Traducción Unidad 7 Dogma Central de la Biología Molecular. Flujo de la Información Genética Replicación Transcripción. Síntesis de RNA Traducción Síntesis de Proteínas 1 Comparación de la expresión génica entre eucariontes y procariontes Eucariontes Procariontes Núcleo Transcripción Traducción Transcripción Traducción Código genético: DNA -------Æ Bases RNAm -------Æ Bases Proteína -------Æ Aminoácidos En DNA y RNA hay 4 bases pero en proteínas: 20 aminoácidos Combinaciones de bases para determinar un aminoácido: Combinaciones de 2 bases: 42 = 16 (no alcanzan!!) Combinaciones de 3 bases: 43 = 64 !! (ahora sobran!!) Codón: Secuencia de tres bases en el RNAm que especifica un aminoácido en la secuencia de la proteína o causa la terminación de la traducción. 2 Nirenberg y Matthaei descifraron el código genético usando un lisado de E. coli para sintetizar proteínas in vitro al cual le agregaban RNAm sintético poli-U, poli-A, poli-CA..... RNA Proteína Solamente 61 de las 64 combinaciones posibles codifican para aminoácidos Código Genético 61 codones determinan aminoácidos 3 codones son “non-sense” y funcionan como señales de término (stop) de la traducción Segunda posición Primera posición 18 de los 20 aminoácidos están determinados por más de un codón. El código genético es redundante. 3 Solamente Met y Trp están determinados por un codón. Codones sinónimos: Para muchos aminoácidos determinados por mas de un codón, las 2 primeras bases no varían y solamente hay cambio en la 3a posición. ¿Qué característica común tiene esa 3a base en los aminoácidos determinados por dos codones? Esta propiedad minimiza los efectos de alguna mutación. Sustitución por transición en el que hay un cambio de una purina por otra purina. AAG -Æ AAA El código genético está altamente conservado filogenéticamente. De hecho, por muchos años, se consideró que era UNIVERSAL, hasta que se encontraron las excepciones que son mínimas. La mayor parte de estas excepciones se identificaron en los genomas mitocondriales y en algunos protozuarios. Codón Código genético Excepción Genoma AGA/ AGG Arg Ser Mitocondria animal CGG Arg Trp Mitocondria plantas UAA/ UAG Término Glu Nuclear protozuarios UGA Término Trp Micoplasma 4 Para los aminoácidos determinados por mas de un codón, estos no son usados con la misma frecuencia. Para los aminoácidos determinados por mas de un codón, estos no son usados con la misma frecuencia. 5 En el proceso de traducción participan los RNAt, RNAr y RNAm. Estructura de un RNAm maduro. UAA UAG AUG Codones de término UGA Región codificante Cola de Poli-A CAP Región 5’ no traducida Región 3’ no traducida 5’-UTR 3’-UTR Marco de lectura abierto (Open Reading Frame) Marco de Lectura 1 La misma secuencia de RNAm. Marco de Lectura 2 Tres secuencias de polipéptidos distintas!!! Marco de Lectura 3 Solamente uno de los marcos de lectura es el correcto para la traducción. ¿Cómo es reconocido este marco por el aparáto traduccional? 6 Los RNAt son las moléculas adaptadoras (traductoras) que decodifican la información en el RNAm acarreando al aminoácido correspondiente. Estructura y Función del RNAt Los RNAt son las moléculas adaptadoras (traductoras) que decodifican la información en el RNAm acarreando al aminoácido correspondiente. Los RNAt se sintetizan como precursores que son procesados para generar moléculas de 75 a 80 nts de longitud. Generalmente tienen bases modificadas como: Ribotimidina Dihidrouridina Pseudouridina Inosina Inosina 7 Estructura Secundaria del RNAt Asa D – Brazo D * El brazo variable (3- 21 nts) puede formar un tallo de hasta 7 pb. Brazo T. Tallo de 4-5 pb * Función de los RNAt RNAt + Aminoácido --Æ Aminoacil RNAt La reacción ocurre en dos etapas: 1. Activación del aminoácido: Formación del aminoacil adenilato Aminoácido + ATP Æ Aminoácido-AMP + PPi R Se forma el aminoacil adenilato que tiene un enlace de alta energía. La hidrólisis del pirofosfato inorgánico que se produce genera energía para la reacción. 8 2. Formación del aminoacil-RNAt Aminoacil adenilato + RNAt Æ Aminoacil-RNAt + AMP El aminoácido se une al extremo 3’-OH del RNAt. En el brazo aceptor. Aminoacil RNAt sintetasas A pesar de que catalizan la misma reacción, estas enzimas pueden ser muy diferentes. Algunas son monómeros, dímeros y tetrámeros. La misma enzima realiza los dos pasos de la reacción. Tiene sitios de unión para: • el aminoácido • ATP • RNAt 9 Aminoacil RNAt sintetasas. Reconocen secuencias en la región interna del RNAt. Tienen muy alta especificidad pues distinguen entre 40 RNAt que tienen una estructura similar, solamente con algunos cambios en la secuencia de bases. Reconocen elementos de identidad en el RNAt que incluyen: • Región anticodón • Pares de bases en el tallo aceptor. El codón del RNAm es reconocido por la secuencia anticodón del RNAt 5’ C G C 3’ RNAm La interacción ocurre por apareamiento de bases complementarias. Las dos moléculas de RNA son antiparalelas. 10 Hipótesis del “bamboleo” (wobble) Debido a que el código genético es redundante: • Algunos aminoácidos están determinados por 6 codones • Algunos aminoácidos están determinados por 4 codones • Algunos aminoácidos están determinados por 3 codones • Algunos aminoácidos están determinados por 2 codones Algunos codones que determinan al mismo aminoácido son reconocidos por el mismo RNAt Esto implica que hay apareamientos de bases tipo Watson-Crick para las dos primeras posiciones del codón, pero no para la tercera. Hipótesis del “bamboleo” (wobble) La inosina es una purina que forma interacciones débiles con C, U, A 5’ C G I/U C 3’ RNAm Muchos RNAt tienen inosina en la posición 5’ del anticodón 11 La síntesis de proteínas se lleva a cabo en los ribosomas 2.76 x 106 Da El ribosoma procarionte se puede disociar en dos subunidades. Cada una de éstas se compone de RNAr y muchas proteínas Estructura de los Ribosomas Subunidad Pequeña 30S Lectura de los codones 21 proteínas + RNAr 16S Subunidad Grande 50S Polimerización de Aminoácidos 31 proteínas + RNAr 23S y 5S 12 Sitio de unión al ribosoma En los RNAm procariontes hay una secuencia altamente conservada que está entre 8 y 13 nts del codón de inicio. Esta secuencia es rica en purinas y el consenso es: 5’-AGGAGGU-3’ Esta secuencia se aparea por interacciones de puentes de hidrógeno con la secuencia 3’-UCCUCCA-5’ que se encuentra en el RNAr 16S de la subunidad pequeña del ribosoma. Se llama Secuencia de Shine-Dalgarno o sitio de unión al ribosoma. Sirve para posicionar de manera correcta al RNAm en el ribosoma con respecto al codón de incio. El codón que marca el inicio de la traducción es AUG que codifica para el aminoácido metionina 5’- UTR 5’ En procariontes, el codón de inicio AUG codifica para formil metionina: En eucariontes, el codón de inicio AUG codifica para metionina: 13 Formación del complejo de iniciación • Ensamblaje del ribosoma en el RNAm • Se requiere de: – – – – – Subunidad pequeña del ribosoma Subunidad grande del ribosoma RNAm Aminoacil-RNAt (formil-Met) Factores de iniciación (IF) • IF1 e IF3 => se unen a la subunidad 30S y previenen la unión de 50S en ausencia de RNAm • IF2-GTP ayudan a la unión del aminoacil-RNAt de iniciación Formación del complejo de Iniciación. Los factores IF1 e IF3 se unen a la subunidad 30S del ribosoma y previenen la unión de la subunidad 50S En procariontes, el codón de inicio es reconocido por un aminoacil-RNAt que acarrea formil-Met RNAt El grupo formilo se añade después de la carga del RNAt, por una enzima (transformilasa) que usa formiltetrahidrofolato. Solamente el RNAtf-Met se usa para formar el complejo de iniciación. Todos los demás aminoacil-RNAt requieren que el ribosoma esté completamente ensamblado. 14 Formación del complejo de Iniciación. La unión de AA-RNAt(fMet) al codón de inicio es un proceso dependiente de la hidrólisis de GTP. El IF2 se une a GTP acompaña al AA-RNAtf-Met Al disociarse IF1, se une la subunidad 50S del ribosoma. Queda formado el complejo de iniciación. Fase de elongación • Factores de elongación EF – EF-Tu / EF-Ts/ EF-G • Aminoacil-RNAt del resto de los aminoácidos. • GTP • Complejo de Iniciación La fase de elongación se divide en tres etapas ¾ Ocupación del sitio aminoacil ¾ Formación del enlace peptídico ¾ Translocación 15 En el ribosoma se pueden distinguir tres sitios E, P y A, de los cuales el sitio P y A pueden ser ocupados por AA-RNAt Sitio P (Peptidil) del ribosoma Sitio A (Aminoacil) del ribosoma El AA-RNAtf-Met ocupa el sitio Peptidil en el ribosoma. FASE DE ELONGACION Ocupación del sitio Aminoacil por el siguiente AA-RNAt EF-Tu GTP GDP 5' 3' P Sitio P (Peptidil) A Sitio A (Aminoacil) EF-Ts EF-Ts regenera el GTP 16 FASE DE ELONGACION Formación del enlace peptídico El grupo amino del AA-RNAt del sitio A está bien posicionado para atacar el enlace éster entre el RNAt que ocupa el sitio P y el aminoácido. 5' 3' P A Mecanismo de Formación del Enlace Peptídico El grupo amino del AA-RNAt del sitio A está bien posicionado para atacar el enlace éster entre el RNAt que ocupa el sitio P el aminoácido que acarrea. 17 Mecanismo de Formación del Enlace Peptídico Se forma un intermediario tetraédrico que es estabilizado por la peptidil transferasa. Intermediario tetraédrico Mecanismo de Formación del Enlace Peptídico El intermediario se cierra para formar el enlace peptídico y liberar al RNAt que está ocupando el sitio P 18 5' 3' P A El sitio P queda vacío. La actividad de peptidil transferasa se encuentra en el RNA ribosomal 23S con participación de algunas proteínas de la subunidad grande del ribosoma. El centro catalítico responsable de la actividad de la peptidil transferasa se encuentra altamente conservado filogenéticamente. 19 Elongación Translocación EF-G 5' 3' A P La translocación es mediada por el factor EF-G, guíado por la hidrólisis de GTP Elongación Translocación EF-G 5' 3' P A El RNAt que acarrea a la cadena polipeptídica creciente ahora ocupa el sitio P. El sitio A queda desocupado para el siguiente AA-RNAt según el codón que está posicionado en el sitio A. 20 Terminación. El ribosoma llega al codón de término del marco de lectura del RNAm Ruptura del enlace éster Los codones UAA, UAG y UGA no son reconocidos por ningún RNAt Factor de liberación o de terminación (RF) UAA (codón de término) “STOP” RF1=> UAA y UAG / RF2 => UAA y UGA El mecanismo que se ha propuesto para la liberación se basa en la semejanza estructural entre un AA-RNAt y los factores de liberación. El factor de liberación se une al sitio A del ribosoma y acarrea una molécula de agua a la región de elongación de la cadena polipeptídica. H O La actividad de peptidil transferasa emplea esa molécula de agua para romper el enlace éster y liberar al polipéptido. H 21 Polisomas. Un solo RNAm puede ser traducido por varios ribosomas de manera simultánea. Varios inhibidores de la síntesis de proteínas se han usado como antibióticos: ANTIBIÓTICO ACCIÓN Estreptomicina Inhibe la iniciación y causa una lectura incorrecta del RNAm (Procariontes) Tetraciclina Se une a la subunidad 30S del ribosoma e inhibe la unión del aminoacil-RNAt (Procariontes) Cloramfenicol Inhibe a la peptidil transferasa (Procariontes) Eritromicina Se une a la subunidad 50S e inhibe la translocación (Procariontes) Puromicina Causa terminación prematura de la traducción. Actúa como análogo estructural del aminoacilRNAt Cicloheximida Inhibe a la peptidil transferasa (Eucariontes) 22 Traducción en Eucariontes. Los ribosomas en eucariontes son más grandes y están formados por un número mayor de proteínas que los ribosomas procariontes. La principal diferencia en la traducción entre procariontes y eucariontes radica en la fase de iniciación. Los RNAm eucariontes carecen de una secuencia consenso de unión al ribosoma (Shine-Dalgarno). Hipótesis del “scanning” o barrido. La subunidad 40S del ribosoma se une al extremo 5’ del RNAm y hace un barrido hasta encontrar el codón AUG. La subunidad 40S Este codón se debe encontrar en el contexto correcto que es: 5’-CCRCCAUGG-3’ 23 En eucariontes hay varios factores de iniciación que se pueden clasificar por su función: eIF6, eIF3, eIF4C que se unen a las subunidades del ribosoma. eIF4(A,B,E,F) que se unen a la estructura del cap en el extremo 5’ del RNAm eIF2, eIF2B que acarrean al AA-RNAt iniciador El proceso de elongación es similar a los procariontes y la actividad de peptidil transferasa se encuentra en.... El proceso de terminación es similar al de los procariontes y se reconocen los mismos codones de término: UAA UAG UGA 24 Transporte de las proteínas en la célula. La localización final de una proteína en la célula frecuentemente está determinada por alguna secuencia corta de aminoácidos presente en la proteína. En procariontes, los destinos posibles de una proteína: • Secretada hacia el exterior de la célula • Membrana plasmática • Citosol Las bacterias Gramtienen varios sistemas de secrección. Secreción de proteínas en bacterias. La proteína que se va a secretar tiene una secuencia de varios aminoácidos en N-terminal que funciona como señal. La proteína SecB se une a la proteína recien sintetizada y previene que se pliegue y adquiera su estructura terciaria. Las proteínas SecY y SecE son proteínas transmembranales que forman un poro mediante el cual es transportada la proteína que es secretada. Es un proceso dependiente de la hidrólisis de ATP La proteína se pliega y el péptido señal es procesado por una proteasa. 25 En eucariontes, las proteínas pueden tener varios destinos: Núcleo, mitocondria, peroxisomas, cloroplastos, retículo endoplásmico, aparato de Golgi, lisosomas. Las proteínas contienen ciertas secuencias de aminoácidos que son reconocidas por receptores en el organelo blanco o por otras proteínas que las transportan. Hay dos mecanismos generales: Direccionamiento post-traduccional: núcleo, mitocondria, cloroplasto peroxisoma. Direccionamiento co-traduccional: retículo endoplásmico, aparato de Golgi, lisosomas, membrana plasmática, secreción. Transporte de proteínas al núcleo. Proteínas del metabolismo del DNA y RNA requieren estar en el núcleo. También las histonas y otras proteínas que se unen a la cromatina. El transporte de proteínas hacia adentro del núcleo ocurre por los poros nucleares donde hay proteínas que reconocen la secuencia de localización nuclear (NLS) en la proteína que se va a internalizar. Esta NLS es una secuencia rica en aminoácidos básicos. -PKKKRLVHay proteínas que carecen del NLS pero son cotransportadas al núcleo junto con otra proteína. 26 Direccionamiento cotraduccional. La vía secretora. 1. La proteína entra al RE conforme es sintetizada en el ribosoma. 2. Las proteína sale del RE en una vesícula 3. Las proteína viaja a través de la cisterna del aparato de Golgi 4. La proteína entra en una vesícula secretora que se fusiona a la membrana plasmática. 5. Las proteína es secretada. Degradación y reciclaje de proteínas. Las proteínas tienen una vida media determinada por lo que son hidrolizadas por varias vías. Proteínas oxidadas Proteínas mal plegadas Proteínas que forman agregados Proteínas de señalización o regulatorias Degradación de proteínas por vía lisosomal que contienen muchas proteasas. 27 Degradación y reciclaje de proteínas. Ubiquitinación. La ubiquitina es una proteína de 76 a.a. que se une a proteínas que van a ser degradadas. 1. Una enzima activadora se une al extremo C-terminal de la ubiquitina (ATP) 2. La ubiquitina activada es transferida a una segunda enzima que reconoce a la proteína blanco 3. La ubiquitina activada se une covalentemente a residuos de Lys de la proteína blanco. 4. La proteína “marcada” con ubiquitina es reconocida por proteasas en el citosol que la degradan. 5. Estas proteasas forman un complejo de unas 28 subunidades que tiene un alto P.M. (proteasoma). Degradación y reciclaje de proteínas. Ubiquitinación. La proteína “marcada” con ubiquitina es reconocida por proteasas en el citosol que la degradan. La ubiquitinaactivada se une covalentemente a residuos de Lys de la proteína blanco. Una enzima activadora se une al extremo C-terminal de la ubiquitina (ATP) La ubiquitina activada es transferida a una segunda enzima que reconoce a la proteína blanco 28 Estas proteasas forman un complejo de unas 28 subunidades que tiene un alto P.M. (proteasoma) 29