Unidad 3: BIOELEMENTOS Y BIOMOLÉCULAS INORGÁNICAS. 1
Anuncio

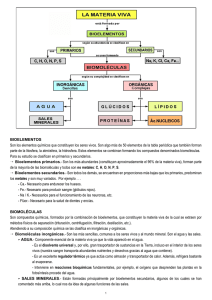
Bioelementos y biomoléculas inorgánicas 2º Bach Unidad 3: BIOELEMENTOS Y BIOMOLÉCULAS INORGÁNICAS. 1.- LOS BIOELEMENTOS. No son exclusivos de los seres vivos. También se encuentran en la materia mineral. Los bioelementos que se encuentran en mayor proporción en los seres vivos son el C, H, O, N, P y S. La razón de esta proporción está en: - Todos tienen capas electrónicas externas incompletas. Pueden formar enlaces covalentes. - Poseen números atómicos bajos. Pueden formar moléculas estables. - El O y el N son electronegativos y por tanto polares y solubles en agua. Pueden intervenir en reacciones biológicas. - Estos bioelementos son accesibles y se pueden incorporar fácilmente a partir de moléculas inorgánicas como el H2O, CO2, nitratos, etc. - El más importante de ellos es el C, que al poseer 4 electrones desapareados en su última capa, es capaz de formar largas cadenas hidrocarbonadas. Clasificación de los bioelementos Primarios o mayoritarios C, H, O, N, P, S Secundarios Na, K, Ca, Mg, Cl Oligoelementos Fe, Cu, I, F, etc. 2.- BIOMOLÉCULAS. Agua Inorgánicas Biomoléculas o Principios inmediatos Orgánicas Sales minerales Precipitadas Disueltas Glúcidos Lípidos Proteínas Ácidos nucleicos 2.1.- EL AGUA. - Principal componente de los seres vivos. Su % depende de la especie, la edad del organismo y la actividad bioquímica del órgano o tejido. Estructura química del agua: Dos átomos de H unido a uno de O mediante enlaces covalentes. Como la electronegatividad del O es mayor que la del H, se crea una asimetría eléctrica adquiriendo un carácter dipolar. (Negativo en el extremo del O y positivo en el extremo de los átomos de H). 1 Bioelementos y biomoléculas inorgánicas 2º Bach Esta polaridad permite la formación de hasta 4 puentes de hidrógeno, lo que confiera a la molécula una gran estabilidad, elevado grado de cohesión e incompresibilidad. Propiedades y funciones del agua: - Debido a su polaridad presenta un gran poder disolvente. Disolvente universal. - Medio ideal para transportar sustancias por el interior del organismo. - Lubricante de estructuras de movimiento. - Su incompresibilidad le permite ejercer funciones de esqueleto hidrostático en las células vegetales. - El elevado grado de cohesión permite el ascenso del agua por capilaridad y una elevada tensión superficial. - El elevado calor específico (1 cal/g °C) y el elevado calor de vaporización hacen del agua un buen amortiguador térmico. - Al ser el hielo menos denso que el agua líquida, permite a este flotar sobre ella y formar una capa helada, que aísla a la capa líquida de abajo, permitiendo la vida durante el invierno a los organismos acuáticos. - El agua es capaz de ionizarse y formar H+ y electrones, necesarios para la cadena transportadora de electrones de la fase lumínica de la fotosíntesis 2 H2O → H3O+ + HO2.3.- LAS SALES MINERALES. - En forma insoluble o precipitadas como los fosfatos, carbonatos, etc. Forman estructuras duras de sostén o protección (caparazones, huesos, dientes, etc.) En forma soluble, en forma de iones (cationes y aniones). Intervienen en muchos procesos biológicos: o la transmisión del impulso nervioso (Na+) o la contracción cardiaca y muscular (K+) o la contracción muscular y coagulación de la sangre (Ca2+) o activador y cofactor de algunas enzimas (Mg2+). o procesos osmóticos. o mantenimiento del pH. Sistemas tampón, buffer o amortiguadores. 2