I.E.D. ALFONSO LÓPEZ PUMAREJO EVALUACION GENERAL DE
Anuncio

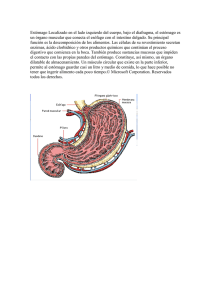
I.E.D. ALFONSO LÓPEZ PUMAREJO EVALUACION GENERAL DE QUIMICA. PRIMER PERIODO GRADO DECIMO Profesor: NELSON BARACALDO AÑO LECTIVO 2010 HIPERTEXTO QUÍMICA 1 Nombre: ______________________________________________ Curso: ____________Fecha:_____________ ¿Por qué se produce la úlcera estomacal? La acidez gástrica está definida regularmente como una sensación subjetiva, no placentera de ardor y calor en el epigastrio, es decir, en la región abdominal situada entre el ombligo y el extremo distal del esternón. Es causada por múltiples factores, entre los cuales el estrés, los malos hábitos alimenticios y el consumo de sustancias irritantes como el alcohol y el cigarrillo son los más comunes. Para comprender mejor la situación, miraremos con mayor detalle el funcionamiento del estómago. El estómago de un adulto produce en promedio 2 a 3 litros de jugo gástrico, el cuál es secretado por algunas glándulas de la capa mucosa que recubre el estómago. La sustancia más común es el ácido clorhídrico, el mismo que has usado en el laboratorio para disolver metales como el zinc. Por esta razón el pH del jugo gástrico es aproximadamente 1,5, que corresponde a una concentración de 0,03 M. Pero ¿cómo se produce este ácido en el estómago?, ¿de donde provienen los iones H+ y Cl- necesarios para formarlo? Por transporte activo las células parietales de la cubierta interior del estómago permiten el paso de agua y moléculas neutras hacia fuera y hacia adentro del estómago pero impiden el movimiento de iones como H+, Na+, K+ y Cl-. El ión hidrónio es el resultado del ácido carbónico que se produce a partir de la hidratación del dióxido de carbono, producido en el metabolismo celular: CO2(g) + H2O(l) H2CO3(ac) H2CO3(ac) H+ (ac) + HCO3(ac) Estas reacciones ocurren en el plasma sanguíneo que irriga las células de la mucosa, en donde, con la ayuda de las enzimas específicas, el H+ pasa al estómago. Para mantener el equilibrio eléctrico del plasma sanguíneo, una cantidad igual de iones Cl _ se mueve hacia el estómago, en donde las membranas de las células parietales impiden su retorno. El ácido clorhídrico que se produce en el estómago tiene el propósito fundamental de ayudar a la digestión de los alimentos y activar el funcionamiento de ciertas enzimas digestivas. Cuando comemos, se estimula la secreción de iones H+, algunos de los cuales pueden provocar pequeñísimas hemorragias que son reabsorbidos por las mucosas. Por ello nuestro cuerpo renueva las células epiteliales en su totalidad cada tres días, manteniendo sano el estómago. Sin embargo, si el contenido de ácido en el estómago es alto, este efecto de los iones H+ puede producir acidez gástrica generando dolor, hinchazón, inflamación y hemorragia. Marca con una X la opción correcta. 1. Los iones H+ y Cl- provienen de: a. El estómago b. El plasma sanguíneo c. Las células parietales d. Del ácido carbónico 2. El pH equivalente a 1,5, significa que: a. es muy ácido b. es muy básico c. neutro d. poco ácido 3. Las fórmulas químicas de los ácidos clorhídrico y carbónico son: a. HCl y HCO3 b. HClO y H2CO3 c. HCl y H2CO3 d. HCl2 y HCO3 4. Los números de oxidación con que trabajan el cloro y el carbono para formar los ácidos correspondientes son: a. +1 y +2 b. +1 y +2 c. -1 y +4 d. -1 y -4 5. Al aumentar el contenido de iones hidronio, en el estómago se produce la acidez estomacal. Explica de donde provienen estos iones: 1 6. ¿Qué ocurrirá, desde el punto de vista químico, si por el contrario se produce poca cantidad de jugo gástrico en el estómago? El pH determina la acidez o basicidad de las sustancias, se puede reconocer cualitativamente por el cambio de coloración de algunos indicadores y también es útil para hallar la concentración de hidrogeniones o hidroxilo de las sustancias 7. Explica ¿por qué las gaseosas afectan el pH de nuestro estómago? 8. Plantea una dieta alimenticia adecuada para evitar la acidez gástrica: 10 113 Hoy en día en las farmacias conseguimos una amplia gama de medicamentos para combatir el problema de la acidez estomacal. 9. ¿Qué opinas acerca del consumo de los mismos sin prescripción médica? 10. ¿Qué peligros acarrea el consumo de estos medicamentos? 11. Cuál es el número de oxidación correspondiente al elemento Cr en la molécula de H2CrO4 a. +2 b. +4 c. +6 d. +7 Relaciona la función con el compuesto que le corresponda, asignando la letra correspondiente en el recuadro. Función Compuesto 12. Óxido básico a. HI 13. Óxido ácido b. Al2O3 14. Hidróxido o base c. K2SO4 15. Ácido oxácido d. HClO4 16. Ácido hidrácido e. SO3 17. Sal oxácida f. Ca(OH)2 18. Sal hidrácida g. Na2S 1 2 El oxígeno se combina con Ca para formar un compuesto A. Se le adiciona H2O y forma un compuesto B. Luego, se adiciona H2SO4 y forma el compuesto C, que corresponde a una sal neutra. Identifica los compuestos A, B y C. 19. A:____________________________________________________________________________________ 20. B:____________________________________________________________________________________ 21. C:____________________________________________________________________________________ Escribe las fórmulas correspondientes a los siguientes compuestos. No olvide el procedimiento: 22. Clorito de sodio __________________________________________ 23. Óxido de fósforo (V) __________________________________________ 3 4 24. Oxido niqueloso __________________________________________ 25. Ácido nítrico __________________________________________ 26. Cloruro de calcio __________________________________________ Escribe 1 ejemplo de los siguientes tipos de reacciones químicas e indica los productos obtenidos. Usa la parte de atrás de la hoja. 27. 28. 29. 30. Óxido ácido + Agua Óxido básico + Agua Hidróxido + Ácido hidrácido Metal + Ácido oxácido