TP 24 Electroquímica 2 (Pilas)
Anuncio

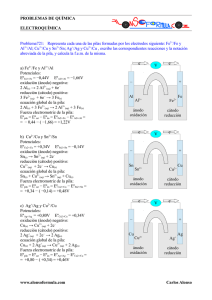
TEMA 24 Cátedra de Introducción a la Química para Ciencias Naturales - UNLP ELECTROQUÍMICA II FUERZA ELECTROMOTRIZ Y CAMBIO DE ENERGÍA LIBRE Tanto la fuerza electromotriz (fem) de una pila como el cambio de energía libre de Gibbs ΔG (tema tratado en el seminario de termodinámica) son una medida de la espontaneidad de toda reacción que se realice en condiciones de P y T constante. Existe, por lo tanto, una relación que las vincula: ΔG = -n F ΔE (1) donde, n es el número de electrones transferidos en la reacción y ΔE la fem de la pila en voltios. F es la constante de Faraday que, como sabemos, es la cantidad de carga eléctrica transportada por un mol de electrones: 1F = 96.500 C/mol = 96.500J/V.mol. De la ecuación es claro que cuando ΔE es > 0, ΔG será negativo y por lo tanto la reacción considerada será espontánea, en caso contrario la reacción será no espontánea. Cuando se trabaja con reactivos y productos en condiciones estándar debemos emplear la siguiente expresión: ΔG0 = -n F ΔE0 (2) EFECTO DE LA CONCENTRACION EN LA FEM DE LA PILA - ECUACIÓN DE NERNST En el seminario anterior se aprendió a trabajar con la tabla de potenciales normales y a calcular el potencial de una celda en condiciones estándar. Asimismo, se vio que el valor de la fem de una pila no es constante sino que depende de las concentraciones de los reactivos y productos de la reacción, así como de la temperatura. Cuando se trabaja en condiciones no estándar se debe calcular el valor de la fem mediante una ecuación, conocida como ecuación de Nernst, en honor al químico alemán que la dedujo. Para llegar a esta ecuación debemos tener en cuenta la dependencia del cambio de energía libre con la concentración, tema tratado anteriormente en el seminario de termodinámica. Para ello, consideremos la ecuación química general: a A + bB ⇔ c C + dD el cambio de energía libre que acompaña a esta reacción está dado por la siguiente expresión: ΔG = ΔG 0 + RT ln Q ΔG = ΔG 0 + RT ln . c [C] .[D] d [ A ] a .[B]b donde Q = cociente de reacción y R es la constante de los gases en unidades apropiadas. Reemplazando en la expresión anterior ∆G y ∆Gº por las ecuaciones (1) y (2) obtenemos: − nFΔE = −nFΔE 0 + RT ln dividiendo ambos miembros por (-nF): Transformando ln en log mediante: ΔE = ΔE 0 − [C] c .[D] d [ A ] a .[B] b RT [C] c .[D] d ln nF [ A ] a .[B] b ln = 2,303 log , se obtiene la ecuación de Nernst: ΔE = ΔE 0 − 2,303 RT [C] c .[D] d log nF [ A ] a .[B]b donde R = 8,3145J/ K.mol y F = 96.500J/ V.mol. Esta ecuación relaciona la variación del potencial de una pila con la variación de la concentración de las especies redox involucradas, a T=constante: 131 TEMA 24 A T = 298 K, el término: Cátedra de Introducción a la Química para Ciencias Naturales - UNLP 2,303 RT 8,314J / K.mol.298K = 2,303 = 0,059 V , nF 96.500J / V.mol Reemplazando en la expresión anterior, la ecuación queda: ΔE = ΔE 0 − [C] c .[D] d 0,059 V × log n [ A ] a .[B] b Debe notarse que el valor 0,059V sólo es válido cuando trabajamos con la función log y a T= 298K. Ejemplo: consideremos una pila constituida por una semicelda Zn2+/Zn, y otra semicelda Cu2+/Cu, en donde la concentración de iones Zn2+ es 1M y la concentración de iones Cu2+ es 0,01M, a T = 298K. La ecuación global que representa este proceso de transferencia de dos electrones (n =2) será: Zn0 + Cu2+ ⎯⎯→ Cu0 + Zn 2+ Debido a que las condiciones estipuladas no son condiciones estándar el potencial de la pila debe calcularse a partir de la ecuación de Nernst: ΔE = ΔE 0 − 0,059 [ Zn 2+ ] log n [Cu 2+ ] Reemplazando: ΔE0 = 1,1V (valor determinado en el práctico anterior), n = 2 y las respectivas concentraciones, se obtiene: 0,059 1 ΔE = 1,1 − log = 1,041V 2 0,01 El valor de ΔE calculado es menor que el valor de ΔE0 ya que la concentración de reactivo es menor. Si por el contrario la concentración de Zn2+ fuera 0,01M y la de Cu2+, 1M, tendríamos que ΔE es mayor que ΔE0 ya que ahora la concentración de producto es menor: 0,059 0,01 ΔE = 1,1 − log = 1,159 V 2 1 Lo anterior demuestra que se puede modificar el valor del potencial de una pila cambiando la concentración de las especies redox involucradas. Esto es así por que al cambiar la concentración se modifica el potencial de cada hemi-reacción. Como ejemplo determinemos como cambia, a T = 298 K, el potencial del electrodo de Cu Cu 2+ + 2e − ⎯⎯→ Cu 0 E 0Cu2 + /Cu0 = 0,34V Planteamos la ecuación de Nernst: E = E0 − 0,059 1 log 2 [Cu 2+ ] si la concentración de Cu2+ es la estándar (1M), entonces el segundo término de la ecuación se anula y E = E0 pero, si la concentración fuese, por ejemplo,0,01M el potencial de la celda sería menor que el valor estándar : E = E0 − 0,059 1 log = 0,291V 2 [0,01] Esto nos indica que para describir correctamente una pila no sólo deben especificarse las sustancias reaccionantes sino también sus concentraciones. 132 TEMA 24 Cátedra de Introducción a la Química para Ciencias Naturales - UNLP Diagrama de una pila: por convención siempre se escribe el ánodo a la izquierda y el cátodo a la derecha. Media celda de oxidación Ánodo Fase en menor estado de oxidación Media celda de reducción Cátodo Fase en mayor estado de oxidación Límite entre fases Fase en mayor estado de oxidación Fase en menor estado de oxidación Puente salino A / An+(C1) // Bn+(C2) / B Por ejemplo, la representación de la pila de Daniell sería: Zn / Zn2+(ac,1M) // Cu2+(ac,1M) / Cu Pila de concentración: están constituidas por dos semiceldas con idénticos electrodos sumergidos en soluciones de concentraciones iónicas diferentes. Como ejemplo consideremos una pila constituida por dos electrodos de Cu cada uno de ellos sumergido en soluciones de concentración 0,01M y 0,1M: Cu / Cu+2(0,01M) // Cu+2(0,1M) / Cu las hemi-reacciones que representan las reacciones anódicas y catódicas son: Ánodo Cátodo Cu 0 ⎯⎯→ Cu 2+ + 2e − E 0 = 0,34 V Cu 2+ + 2e − ⎯⎯→ Cu 0 E 0 = 0,34 V Cu0 + Cu12+ ⎯⎯→ Cu0 + Cu 22+ ΔE 0 = 0,00 V Como los dos electrodos son idénticos, el valor de ∆Eº = Ec - Ea, es cero en condiciones estándar. Sin embargo, como las concentraciones iónicas son diferentes se establece una diferencia de potencial entre las semiceldas la que puede calcularse mediante la ecuación de Nernst: ΔE = ΔE 0 − ΔE = 0,00 V − [Cu 22+ ] 0,059 log n [Cu12+ ] 0,059 [0,01] log = 0,0295 V 2 [0,1] El proceso espontáneo de esta celda tiene como efecto neto diluir la solución más concentrada y concentrar la más diluida ya que, de acuerdo al principio de Le Chatelier, la tendencia para la reducción aumenta con el incremento de la concentración de los iones Cu2. Por este motivo, la reducción ocurrirá siempre en el compartimiento más concentrado y la oxidación ocurrirá en el más diluido. Cálculo de la constante de equilibrio: Resulta posible medir la diferencia de potencial que se establece entre las semiceldas o calcularla mediante la ecuación de Nernst cuando la reacción no se encuentra en equilibrio: 0,059 ΔE = ΔE 0 − log Q n A medida que la reacción transcurre aumenta la concentración de producto con respecto a la inicial y disminuye la de reactivos por lo que el sistema tiende al equilibrio. De esta manera, el término en la ecuación de Nernst que contiene las concentraciones irá aumentando paulatinamente en valor absoluto. Cuando la reacción alcanza el equilibrio este término se hace numéricamente igual a ΔE0. En ese momento ΔE=0, no circula más corriente por el sistema y la ecuación anterior puede expresarse ahora como: 133 TEMA 24 Cátedra de Introducción a la Química para Ciencias Naturales - UNLP ΔE = 0 = ΔE 0 − 0,059 log K n En el equilibrio Q = K; K = cte de equilibrio 0,059 log K n n.ΔE 0 log K = 0,059 ΔE 0 = K = 10 n.ΔE0 0,059 Sabemos que cuanto mayor es el valor de ΔE0, mayor es la tendencia de la reacción a proceder de izquierda a derecha. Además, de la expresión anterior, podemos deducir que cuanto mayor es el valor de ΔE0 mayor es el valor de la constante de equilibrio. Problemas de aplicación: 1.- Calcular el potencial de reducción del par Fe3+ / Fe2+ si: a) la concentración de ión ferroso es cinco veces mayor que la de ión férrico ( [Fe2+/[Fe3+] = 5 ). b) la concentración de ión férrico es cinco veces mayor que la de ión ferroso ( [Fe3+/[Fe2+] = 5 ). c) ambas concentraciones son iguales. De acuerdo con los resultados obtenidos establezca sus conclusiones. 2.- Calcular la fem de las pilas cuyos diagramas se especifican a continuación: a) Zn / Zn2+ (0,005M) // Cu2+ (0,5M) / Cu b) Pt / Fe3+(0,15M) , Fe2+(0,02M) // Ag+ (0,9M) / Ag 3.- Calcular el potencial en medio ácido, [H+] = 1.10-3 M, de la siguiente pila: Pt / Fe3+(0,1M), Fe2+(1M) // MnO4-(0,01M) , Mn2+(0,01M) /Pt 4- Determine como variará el poder reductor del par MnO4-/Mn+2 si se reduce la concentración de H+ desde 1M a 10-4M. 5.- Determine qué concentración de Pb2+ debe tener una solución para que el potencial de un electrodo de Pb tome el valor de -0,18 V. 6.- Calcule la fem de la siguiente pila de concentración: Cu/Cu2+(0,0002M) // Cu2+(0,1M) /Cu 7.-Establezca para los pares dados a continuación cuál será la reacción espontánea en condiciones estándar. Calcule, además, la constante de equilibrio a T = 25°C para cada una de ellas: a) Br2 / Br- y Fe3+ / Fe2+. b) I2 /I- y Mg2+ / Mg c) Fe3+ / Fe2+ y MnO4- / Mn2+ 134 TEMA 24 Cátedra de Introducción a la Química para Ciencias Naturales - UNLP PARTE PRÁCTICA 1.- DETERMINACION DE LA SERIE ELECTROQUÍMICA Material a utilizar: Electrodos de cobre, cinc, aluminio y plomo. Soluciones 0,1M de los sulfatos de dichos metales. Puentes salinos de KCl. Vasos de precipitado. Voltímetro. Procedimiento: a) Limpie de grasa y óxido los electrodos a usar. Para tal fin se aconseja utilizar papel de lija y luego enjuagar con acetona. b) Llene 3/4 partes de un vaso de precipitados con cada una de las soluciones anteriores. Coloque cada uno de los electrodos mencionados en contacto con la solución correspondiente (por ejemplo electrodo de Cu con solución de CuSO4). c) Tome dos medias celdas y conecte los terminales del voltímetro a cada uno de los electrodos. Cierre el circuito por medio del puente salino y determine con el voltímetro la diferencia de potencial entre los dos electrodos. Sobre la base de su observación indique cuales son las reacciones que ocurren. d) Mantenga el Cu como electrodo fijo y mida la diferencia de potencial con cada uno de los restantes pares. e) Ordene los metales de acuerdo a su poder reductor creciente y compare con una tabla de potenciales. 2.- VERIFICACION DE LA FEM DE LA PILA DE DANIELL. Para armar la pila se sigue el siguiente procedimiento: a) se pulen los electrodos metálicos (Cu y Zn) con papel de lija, se los enjuaga con agua destilada y se los deja escurrir, b) cada uno de ellos se introduce en un vaso de precipitado previamente llenado hasta 2/3 de su capacidad con soluciones 0,1M del sulfato correspondiente (sulfato de cinc o sulfato de cobre), c) se coloca el puente salino, se conectan los electrodos a un potenciómetro y se mide la diferencia de potencial. 3.- VERIFICACION DE LA ECUACION DE NERNST. Se efectuará a través de la medida de la FEM de las siguientes pilas. Zn / Zn2+(0,1M) // Cu2+(0,1M) / Cu Zn / Zn2+(0,1M) // Cu2+(0,01M) / Cu Zn / Zn2+(0,1M) // Cu2+(0,001M) / Cu 4.- DETERMINACION DE LA FEM DE PILAS DE CONCENTRACION. Para ello se construirán las siguientes pilas: Cu / Cu2+(0,1M) // Cu2+(0,01M) / Cu Cu / Cu2+(0,1M) // Cu2+(0,001M) / Cu 5.- CORROSION La corrosión es el proceso por el cual los metales son oxidados por el oxígeno del aire en presencia de humedad. Se pierde anualmente muchísimo dinero en productos metálicos a consecuencia de los problemas generados por procesos de corrosión sobre piezas y estructuras metálicas que se deterioran, por lo que el estudio de estos procesos y su prevención tienen gran importancia teórico-práctica. El mecanismo de la corrosión ha sido ampliamente estudiado y se sabe que la oxidación se produce con mayor facilidad en puntos de tensión o esfuerzo, en los que los metales son más activos. Por lo tanto, un clavo de acero, constituido por hierro en su mayor parte, se corroerá en la punta y en la cabeza y un clavo doblado puede corroerse, además, en la zona de la curvatura. 135 TEMA 24 Cátedra de Introducción a la Química para Ciencias Naturales - UNLP La punta de un clavo de acero actuará como ánodo, en el cual el hierro se oxida a Fe2+: Fe ⎯⎯→ Fe 2+ + 2e − (ánodo) Los electrones fluyen a través del clavo hacia las zonas que contengan impurezas o zonas de tensión (puntos débiles), las que actúan como cátodos. Allí, el oxigeno se reduce a iones OH-, según la siguiente ecuación O 2 + 2 H2 O + 4e − ⎯⎯→ 4 OH− la ecuación global de este proceso será, entonces: 2 ( Fe ⎯⎯→ Fe 2 + + 2e − ) O 2 + 2H2 O + 4e − ⎯⎯→ 4OH − 2 Fe + O 2 + 2 H2 O ⎯⎯→ 2 Fe 2 + + 4 OH − Parte experimental: Se utilizará el indicador de corrosión denominado ferroxil, el cual está constituido por una gelatina vegetal (agar-agar) en la cual se hallan disueltos ferrocianuro de potasio, K3[Fe(CN)6], y el indicador fenolftaleina. Se coloca una capa de ferroxil en una caja de Petri y luego un clavo de hierro nuevo desengrasado y se cubre con otra capa de ferroxil. Azul Rosa Azul Azul Rosa Azul Vista de perfil Vista de planta. Las reacciones que se producen son: Zona anódica: Fe ⎯⎯→ Fe 2+ + 2e − el Fe2+ reacciona con el K3[Fe(CN)6] de la siguiente forma: 3Fe 2+ + [Fe(CN) 6 ] 3 − ⎯⎯→ Fe 3 [Fe(CN) 6 ] 2 generando el compuesto hexacianoferrato(III) de hierro(II) o Azul de Prusia, Fe3[Fe(CN)6]2, el que posee color azul intenso. Zona catódica 2 H 2 O + O 2 + 4e − ⎯⎯→ 4 OH − Como consecuencia de la generación de grupos OH-, el medio se alcaliniza y la fenolftaleina, que es un indicador ácido base, se torna de color rosa intenso o fucsia 136