to get the file
Anuncio

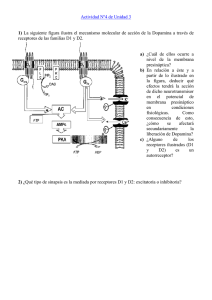
Tema 7 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas y receptores de membrana 4. Ácidos nucleicos 5. Interacciones enlazantes con la biofase 2 1. Concepto y naturaleza química de la biofase 3 BIOFASE O DIANA BIOLÓGICA Lugar del organismo en el que un fármaco ejerce su acción El fármaco para alcanzar el lugar de acción: – Atraviesa una serie de compartimentos – Equilibrios termodinámicos entre regiones • de naturaleza lipídica (membranas) • acuosas (fluidos intra e intercelulares) 4 5 Conocimiento de los procesos químicos entre el fármaco y su diana biológica ESTUDIO DEL MECANISMO DE ACCIÓN DEL FÁRMACO Diana Biológica • Lugar de acción: muy variado o Biofase • Naturaleza química - LÍPIDOS - PROTEÍNAS - A. NUCLEICOS BIOMOLÉCULAS susceptibles de actuar como biofase 6 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas y receptores de membrana 4. Ácidos nucleicos 5. Interacciones enlazantes con la biofase 7 2. Lípidos: acciones inespecíficas 8 2. LÍPIDOS: ACCIONES INESPECÍFICAS Fármacos que actúan directamente sobre los lípidos de membrana Número de fármacos relativamente pequeño Alteración de las propiedades físico-químicas de la membrana Antisépticos detergentes aniónicos y catiónicos Carácter tensioactivo muerte de la célula bacteriana por lisis9 Antibióticos Región hidrofílica Región hidrófoba Formación de canales a través de la membrana Compleja iones K+ Transportador de iones K+ a través de la membrana alteración de la permeabilidad celular Salida del contenido plasmático 10 Tunnel HO2C OH HO Sugar Sugar OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH HO OH CO2H HO CO2H Sugar Sugar CO2H 11 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas y receptores de membrana 4. Ácidos nucleicos 5. Interacciones enlazantes con la biofase 12 3. Proteínas: enzimas y receptores de membrana 13 PROTEÍNAS Amplia familia de macromoléculas fundamentales en la estructura y funcionamiento de la célula ENZIMAS RECEPTORES DE MEMBRANA ENZIMAS Responsables de los procesos catalíticos a nivel biológico CATALIZADOR la energía de activación de una reacción química de la velocidad de la reacción 14 Diagrama comparativo del perfil de energía de una reacción química en ausencia y presencia de catalizador 15 MECANISMOS POR LOS CUALES UN CATALIZADOR DISMINUYE LA ENERGÍA DE ACTIVACIÓN - Capacidad de proporcionar un entorno adecuado para que la reacción tenga lugar - Facilitar que los reactivos alcancen el estado de transición - Debilitar enlaces de los reactivos - Formación de enlaces transitorios entre el sustrato y el catalizador NATURALEZA DE LOS MECANISMOS ENZIMÁTICOS - Reversible - Especificidad respecto del tridimensional del centro activo) sustrato (naturaleza 16 Ejemplo de una enzima ENZIMA LACTATO-DESHIDROGENASA 17 Ejemplo de un fármaco inhibidor enzimático Penicilinas Interfieren en el proceso de biosíntesis de la PC bacteriana Selectividad: células eucariotas carecen de PC Son reconocidas erróneamente por la enzima transpeptidasa Transpeptidasa Enzima que cataliza la formación del enlace entre un resto de glicina y uno de D-Alanina, esencial para el entramado de la pared bacteriana 18 PROTEÍNAS ENZIMAS RECEPTORES DE MEMBRANA 19 RECEPTORES DE MEMBRANA Proteínas especializadas que intervienen en los procesos de comunicación intercelular Componentes de la membrana celular Se orientan hacia el exterior de la membrana Capacidad de interaccionar “selectivamente” con ciertos ligandos o mensajeros químicos formando enlaces 20 EJEMPLO: receptores postsinápticos de la NA 21 INTERACCIÓN LIGANDO-RECEPTOR Formación de enlaces en una zona de unión conceptualmente equivalente al centro activo de un enzima DIFERENCIA ENTRE UNIÓN E-S Y F-R El ligando o mensajero que se enlaza al centro de unión no experimenta modificación química La unión desencadena una respuesta química que depende de la naturaleza del receptor 22 PROCESOS MEDIADOS POR RECEPTORES Tipos de receptores 1. Receptor de membrana asociado a un canal iónico 2. Receptor de membrana ligado a una proteína G 3. Receptor de membrana asociado a un sistema enzimático 4. Receptores intracelulares 23 1. Receptor de membrana asociado a un canal iónico Mecanismo de acción de un mensajero (ligando endógeno o fármaco) sobre un canal iónico asociado a un receptor de membrana 24 Ejemplo de receptor asociado a un canal iónico Modelo propuesto para el receptor nicotínico Unión de la AcH (ligando endógeno) con el receptor Cambio conformacional del receptor apertura de un canal específico para el ión sodio Monómero 5 subunidades 4 fragmentos 2 2. Receptor de membrana ligado a una proteína G Proteína G: Proteína asociada a un nucleótido de guanidina GDP formada por tres subunidades Formación de un mensajero secundario por activación de una proteína G 26 Interacción de la proteína G con el complejo ligando-receptor Cambio conformacionales: intercambio de GDP por GTP 1. 2. Disociación del complejo -GTP Interacción del complejo con un efector intracelular Hidrólisis de una subunidad fosfato 3. Formación del AMPc 27 EJEMPLO: receptores postsinápticos de la NA 28 3. Receptor de membrana asociado a un sistema enzimático Mecanismo de activación de un sistema enzimático asociado a un receptor de membrana 29 4. Receptores intracelulares Propios de: • Hormonas esteroideas • Hormonas tiroideas • Inductores del metabolismo Ejemplo. Modo de acción de las hormonas esteroideas 30 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas y receptores de membrana 4. Ácidos nucleicos 5. Interacciones enlazantes con la biofase 31 4. Ácidos nucleicos 32 Otra de las dianas terapéuticas son los ácidos nucleicos 33 Fármacos que ejercen su acción sobre los ácidos nucleicos Alteración de la estructura de doble hélice del ADN (estructura secundaria) Intercalación entre los pares de bases Corte de cadenas Alquilación de las bases nitrogenadas Mayoría de fármacos que ejercen su acción sobre los ácidos nucleicos Alteración de la estructura terciaria del ADN 34 Ejemplos de fármacos ALTERACIÓN DE LA ESTRUCTURA SECUNDARIA Antineoplásicos Aminoacridinas Bis-2-cloroetilaminas Antibacterianos Actinomicina D Adriamicina ALTERACIÓN DE LA ESTRUCTURA TERCIARIA Antibacterianos Quinolonas antibacterianas 35 Antineoplásicos Aminoacridinas Intercalantes 36 Antineoplásicos Bis(2-cloroetil) aminas 37 Antibacterianos Antibióticos Actinomicina D y Adriamicina 38 Antibacterianos Quinolonas antibacterianas 39 LA BIOFASE: NATURALEZA QUIMICA Y REACTIVIDAD 1. Concepto y naturaleza química de la biofase 2. Lípidos: acciones inespecíficas 3. Proteínas: enzimas y receptores de membrana 4. Ácidos nucleicos 5. Interacciones enlazantes con la biofase 40 5. Interacciones enlazantes con la biofase 41 Interacciones entre dos moléculas orgánicas Tipo de enlace Energía (kJ/mol) Covalente 150-400 Ionico 20-25 Ion-dipolo Dipolo-Dipolo Enlace de hidrógeno 5-30 Tranferencia de carga 5-30 Hidrofobo y Van der Waals 5-30 2-4 42 1. ENLACE COVALENTE Enlace más fuerte Prácticamente irreversible Poco frecuente Unión de un fármaco con enzimas o con ADN Ejemplo clásico: unión de penicilinas a la enzima bacteriana transpeptidasa acilación de un grupo amino en la transpeptidasa 43 2. ENLACE IONICO Interacción de carácter reversible Enlace entre iones del fármaco y los de carga contraria de la zona receptora 44 Enlace más frecuente Receptor proteína Grupos con carga Aniones derivados de las cadenas laterales de aminoácidos como el a. glutámico o el aspártico NH NH COO COO O O aspartato glutamato Cationes protonación de restos amino de las cadenas laterales de ciertos aminoácidos (arginina, lisina o histidina) NH NH NH3 O NH2 NH2 O lisina H N arginina 45 3. INTERACCIÓN ION-DIPOLO Y DIPOLO-DIPOLO Enlace entre átomos de distinta electronegatividad ENLACE POLARIZADO DIPOLO Distribución no homogénea de la densidad electrónica en un enlace dos extremos de carga contraria - Alcoholes y fenoles (C-OH, O-H) - Cetonas, aldehídos, ácidos carboxílicos y derivados (C=O) - Aminas y heterociclos nitrogenados (C-N) - Sulfóxidos, sulfonas, ácidos sulfónicos y derivados (S=O) - Oximas y nitroderivados (N-O) 46 ENLACE DIPOLO-DIPOLO Atracción electrostática entre un extremo de un dipolo y un dipolo inverso C O C N ENLACE ION-DIPOLO Atracción electrostática entre un extremo de un dipolo y una carga iónica C O N 47 4. ENLACE POR PUENTE DE HIDRÓGENO Tipo particular de unión dipolar Se establece a través de: Un átomo de hidrógeno unido a un átomo electronegativo mediante un enlace covalente Dadores de electrones 48 Átomos de hidrógeno adecuados -OH, -NH, SH Dadores de electrones Aniones Carboxilato, fosfato, sulfato Cualquier grupo con un par de electrones no compartido RNH2 ROH, ROR C=O 49 5. ENLACE POR TRANSFERENCIA DE CARGA Atracción electrostática derivada del recubrimiento de orbitales entre una molécula dadora de electrones y otra aceptora Ejemplo: Forma en que la NA se encuentra almacenada en las neuronas presinápticas antes de su liberación en el espacio sináptico Complejo de transferencia de carga entre la porción de la adenina (anillo aromático pobre en electrones) del ATP y el anillo del catecol de la NA, un buen dador de electrones 50 6. ENLACE DE VAN DER WAALS Y ENLACE HIDROFOBO Enlace de Van der Waals Propio de las cadenas hidrocarbonadas Enlace más débil dentro de los enlaces intermoleculares La fuerza del enlace decae rápidamente con la distancia Sólo será efectivo cuando el fármaco se ha aproximado mucho al receptor por otros tipos de enlaces 51 Polarización transitoria de la nube electrónica que rodea la molécula al acercarse dos cadenas hidrocarbonadas Se establece temporalmente una polarización mutua que determina una pequeña atracción 52 Enlace Hidrofobo Medio acuoso Desolvatación por el acercamiento de dos moléculas orgánicas por su parte lipófila 53 54