Requisitos 1. . 2.
Anuncio

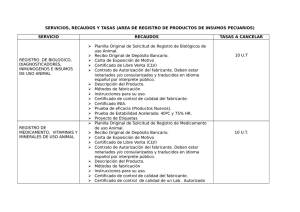
Requisitos REQUISITOS PARA EL REGISTRO DE BIOLOGICOS, DIAGNOSTICADORES, INMUNOGENOS E INMUNOS DE USO ANIMAL. 1. Planilla Original de Solicitud de Servicio de Registro de Productos . 2. Recibo Original de Depósito Bancario por producto. (10 UT). 3. Carta con exposición de motivos dirigida a la Presidencia del INSAI por parte del Asesor Técnico de la Empresa. (Original debidamente firmada y sellada). (imprimirla del Sistema una vez efectuado el Registro) 4. Productos Importados: Certificado de Libre Venta (CLV) y Contrato de Autorización del fabricante. Deben estar notariados, consularizados y traducidos en idioma español por interprete público. (Original). 5. Descripción del producto: Nombre del producto, Empresa fabricante, Composición cuali-cuantitativa, Especie(s) de destino, Indicación(es), Vías de administración, Dosis/Vías de administración, Presentaciones y características de los envases. Diluente (si lo posee). a. Especificar las características físico-químicas del diluente; b. Cuando el producto emplee en su elaboración virus o microorganismos, indicar: nombre de las cepa(s) y grado de virulencia . 6. Del origen: se entiende por origen de la(s) cepa(s), a la organización proveedora de la misma. a. Indicar si los organismos son: activos, vivos, modificados, atenuados, inactivados (anexar métodos de inactivación); b. Si el producto fue elaborado en cultivos celulares indicar: - Especie animal de donde proceden las células, - Cultivo primario o tipo celular, - Evaluación realizada para demostrar la ausencia de virus o microorganismos propios de la especie de donde se origino el cultivo y la presencia de patógenos para la especie que se va a utilizar, - Evaluación para demostrar ausencia de gérmenes diferentes a los empleados específicamente para la elaboración del producto. - Si el producto se obtiene de órganos, tejidos o productos de animales, indicar: Especie animal, Sexo, Raza, Edad y Peso. - Cuando se obtenga de extractos naturales señalar: Naturaleza y fuente de principio e Indicar y describir los pasos activos llevados a cabo en la elaboración del producto (incluyendo generalidades acerca de estabilizadores y/o adyuvantes empleados así como la naturaleza del diluente) 7. Métodos de Fabricación: Descripción del Proceso Productivo. 8. Literatura científica actualizada del producto, apoyar la solicitud e incluir las pruebas de campo realizadas por la propia empresa, previamente autorizadas por el INSAI. 9. Métodos de análisis del principio activo (incluyendo los excipientes de la formulación) y del producto terminado. 10. Métodos utilizados en la comprobación de: Esterilidad, Pureza, Inocuidad, Potencia, Titulación, Viabilidad, Estabilidad, Ausencia de Pirógenos. DESCARGUE AQUI LOS LINEAMIENTOS DE ENSAYOS DE ESTABILIDAD ACELERADA 11. Prueba de Eficacia. (Sólo para productos nuevos). DESCARGUE AQUI LOS LINEAMIENTOS DE ENSAYOS DE EFICACIA. 12. Certificado Original de Control de Calidad del Fabricante (Sellado y firmado). 13. Certificado Original de Control de Calidad del INIA (Sellado y firmado). 14. Proyecto de etiqueta y de los empaques: Nombre comercial, Composición, Indicación(es) para su uso, Vías de administración, dosis y frecuencia, Animal(es) de destino, Fecha de elaboración, Fecha de vencimiento, Nro. de Registro Oficial, Número de lote(s), Nombre del Asesor técnico, Fabricante, Importador/Distribuidor, Indicaciones para su conservación y reconstitución, Peso neto, “Uso Veterinario”, “Manténgase fuera del alcance de los niños”, “Venta bajo prescripción del Médico Veterinario”. NOTA: - La solicitud del registro se puede hacer grupal, no obstante, el recibo de depósito correspondiente a la tasa debe realizarse por producto. - El Asesor Técnico debe ser Médico Veterinario y/o Farmacéutico. - Identificar el cargo dentro de la Empresa y el nombre del responsable de los Controles de Calidad. - Para los Registros de Productos Nuevos, es OBLIGATORIA la presentación de la Copia Certificada del Registro otorgado por el SAPI.