Get cached
Anuncio

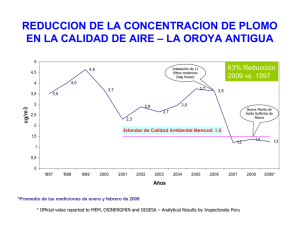
UNIVERSIDAD V E R A C R U Z A N A FACULTAD DE BIOANALISIS XALAPA VER. " M E C A N I S M O S DE A C C I O N Y EFECTOS DEL P L O M O EN LA A G R E G A C I O N PLAQUETARIA." MONOGRAFIA QUE PARA OBTENER EL TITULO DE: L I C E N C I A D O EN Q U I M I C A C L I N I C A PRESENTA: ADRIANA C H A V A R JONGUITUD ASESOR: M . C . ISELA SANTIAGO ROQUE Xalapa, Equez., Ver 2006 Universidad Veracruzana Facultad de Bioanalisis Facultad de Bioandlisi* Xatapa. Ver. Autorizacion de Impresion ( 6 ) C. Q. C. JORGE SIGFRIDO GONZALEZ HERNANDEZ DIRECTOR (A) DE LA FACULTAD DE BIOANALISIS UNIDAD DE CIENCIAS DE LA SALUD PRESENTE Despues de haber revisado el Proyecto de Trabajo de: intitulado: Recepcional, en la modalidad MnNOGRAFTA "MECANISMOS DE ACCION Y EFECTOS DEL PLOMO EN LA AGREGACION PLAQUETARIA" Realizado por: ADRIANA CHAVAR JONGUITUD Hago de su conocimiento que estoy de acuerdo en su contenido cientifico, por lo cual NO TENGO INCONVENIENTE EN AUTORIZAR SU IMPRESION. ATENTAMENTE "Lis de Veracruz, Arte, Ciencia, Luz" Xalapa, Ver, a 10 de enero de 2006. Q. C. JORGE SIGFRIDO GONZALEZ HERNANDEZ Presidente M. C. MARIi / Vocal 1 /mbr. HERNANDEZ En este apartado lo quiero aprovechar para dedicar y agradecer a todas aquellas personas que han sido parte fundamental tanto en mi vida como en la realization de este trabajo. A DIOS: Gracias por ser mi guia dia a dia, por todas las grandes bendiciones que me haz otorgado y sobre todo por ponerme el dia y con las personas correctas, por esta gran oportunidad. MIL GRACIAS... A MIS DOS GRANDES ANGELES: Mis abuelitos, por todas las grandes ensenanzas que me dieron, porque mejor herencia no me pudieron haber dejado y por todos los bellos momentos que me regalaron. Muchas gracias... A MIS PADRES: A ustedes porque mejores padres no me pudieron haber tocado, porque gracias a su amor y apoyo incondicional que siempre me han brindado soy lo que soy. Los amo. A Ml HERMANA: A ti Candy por todo tu invaluable apoyo y compresion. Te quiero mucho hermanita. A TODA Ml FAMILIA: A todos ustedes por ser simplemente mi familia, muchas gracias, porque cada uno de ustedes forma parte importante en mi vida y han sido el motor en muchos momentos de ella. A Ml NOVIO MARIO E. A ti mi amor por todo tu enorme apoyo desinteresado, por todas tus palabras de aliento, por estar siempre corwnigo en los buenos y en los malos momentos de mi vida y por ser parte fundamental en este trabajo. Muchisimas gracias por todo. A LA SENORA ZEILA LUNA: A usted mi querida senora que siempre esta con nosotros incondicionalmente, porque el apoyo que usted nos brinda no se paga con nada. Sinceramente muchas gracias. A LA Dra. ADELA L. RENDON R. Gracias a usted porque simplemente sin usted este trabajo no se hubiera llevado a cabo, por toda su ensenanza y tiempo que desinteresadamente me brindo. Muchas gracias. A Ml JURADO: Q.C. JORGE SIGFRIDO GONZALEZ HERNANDEZ M.C. MARIA LOPEZ HERNANDEZ Q.C. MARIA DOLORES HERNANDEZ PARRA M.C. ISELA SANTIAGO ROQUE Gracias en especial al Quimico Jorge, a la Quimica Mari Lopez y a la Quimica Lolis por su confianza, paciencia y ensenanza para la realization de este trabajo. A TODOS USTEDES DIPS LOS BENDIGA.. INDICE Introduction 1 Objetivo general Objetivos particulars 2 Justification 3 1.1 Hemostasia 4 1.2 Hemostasia primaria 5 1.3Plaquetas 6 1.3.1 Membrana plasmatica 7 1.3.2 Citoesqueleto : 8 1.3.3 Granulos 8 1.3.4 Sistema canalicular abierto 9 1.3.5 Sistema tubular denso 9 1.4 Activation plaquetaria 10 1.4.1 Agonistas plaquetarios y sus receptores 11 1.5 Mecanismo de serialization 11 1.5.1 Proteinas G 11 1.5.2 Activation por adenosin difosfato 14 1.5.3 Activation por adrenalina ; 15 1.5.4 Activation por trombina 16 1.5.5 Activation por tromboxano A2 y endoperoxidos : 16 1.5.6 Activation por el factor activador de plaquetas 17 1.6 Adhesion 18 1.7 Agregacion y liberation 19 1.8 Inhibition plaquetaria 21 1.9 Plomo 1.9.1 Propiedades fisicas y quimicas 1.9.2 Epidemiologia 1.9.3 Exposition, absorcion, distribution y elimination 1.9.4 Efectos del plomo a nivel sistemico 1.9.5 Efectos del plomo a nivel molecular 1.10 Plomo y Agregacion plaquetaria Conclusiones Bibliografia ABREVIATURAS a alfa P beta y gamma P-TG p-tromboglobulina 8-ALA-D 5-aminolevulinico deshidratasa AA acido araquidonico AC adenil ciclasa ADP adenosin-difosfato AMPc adenosin monofosfato ciclico ATP adenosin-trifosfato COOH grupo carboxilo DG diacilglicerol FP4 factor plaquetario 4 GDP guanisin-difosfato GP glucoproteinas GTP guanosin-trifosfato IP3 inositol-1,4,5-trifosfato de inositol NOM norma oficial mexicana PAF factor activador de plaquetas Pb plomo PDGF factor de crecimiento derivado de la plaqueta PG proteina G PGI2 prostaciclina PKC proteina cinasa C PLC fosfolipasa C PLA2 fosfolipasa A2 PRP plasma rico en plaquetas SCA sistema canicular abierto SH grupo sulfhidrilo SSA secretaria de salud y asistencia publica STD sistema tubular denso TXA 2 tromboxano A2 INTRODUCCION Las plaquetas, aunque pequenas en tamano, han dejado de ser un componente menor de los elementos formes de la sangre. Esto se debe al sinnumero de funciones importantes que desempenan en nuestro organismo, juegan un papel preponderante en la hemostasia y en las diferentes fases de la coagulacion sanguinea. El plomo por su parte es un metal pesado, ampliamente distribuido en el medio ambiente. No tiene ningun papel fisiologico dentro de los organismos, sin embargo, el ion Pb2+ puede mimetizar o interferir en funciones biologicas en los que participan otros iones tales como el calcio, reaccionar quimicamente con grupos sulfhidrilo, inhibir potencialmente un gran numero de funciones celulares, principalmente por bloqueo de los sitios activos en los receptores. Es de pensar que teniendo la plaqueta dentro de su estructura varios receptores y necesitando al ion calcio para varias funciones, pueda el plomo interferir en el funcionamiento adecuado de la hemostasia. Sabiendo la importancia que tienen las plaquetas en el organismo humano y la capacidad que tiene el plomo de interferir en ciertas reacciones bioquimicas, se ha realizado en este trabajo una recopilacion bibliografica tratando de saber cual es la participation que tiene el plomo en la agregacion plaquetaria. OBJETIVO GENERAL Identificar el mecanismo de accion del plomo y su efecto en la agregacion plaquetaria. OBJETIVOS PARTICULARES • Profundizar en el conocimiento de senalizacion via Proteinas G que participa en la agregacion plaquetaria. • Identificar la participacion del cation divalente Ca++ en la agregacion plaquetaria. • Identificar la participacion del plomo en la senalizacion via proteinas G y el cation divalente Ca++. \ JUSTIFICACION Puesto que la contaminacion por metales pesados ha llegado a ser motivo de preocupacion en muchas poblaciones, es importante estudiar su efecto sobre sistemas biologicos y evaluar los posibles riesgos involucrados. El efecto toxico de la exposition cronica al plomo se ha conocido por siglos y, al presente, es la causa mas comun de los problemas asociados a contaminacion ambiental. Estudios realizados por Quintanilla B y cols., 2000, en celulas germinales reportaron el posible efecto del plomo en la via de senalizacion dependiente de proteinas G. Por ello resulta interesante revisar monograficamente el efecto que tiene el plomo sobre la agregacion plaquetaria a fin de utilizar a las plaquetas como modelo de dano a las vias de senalizacion durante la intoxicacion con plomo. 1.1 HEMOSTASIA La hemostasia se define como parte del sistema de coagulation. Este se encarga de formar un coagulo para sellar cualquier defecto en la vasculatura que permita la perdida hematica (Ruiz-Arguelles, 2004). Desde el punto de vista practico la hemostasia se divide en dos fases: hemostasia primaria (interaction vaso sanguineo-plaquetas) y hemostasia secundaria (proteinas plasmaticas de la coagulation) (Martinez M., y cols, 1996). La hemostasia se produce practicamente de manera simultanea por varios mecanismos: a) Vascular: es la contraction del vaso lesionado (vasoconstriction). La vasoconstriction es importante para controlar inmediatamente la hemorragia y se debe a que las arterias y venas tienen una capa de musculo liso que se contrae al danarse el vaso. Como la capa muscular es mayor en las arterias, la vasoconstriction arterial es mas importante que la venosa. La adrenalina puede producir vasoconstriction, vasodilatation, o ambas cosas, la vasoconstriction reduce el flujo sanguineo a la zona danada y facilita las fases hemostaticas siguientes (Ruiz-Arguelles, 2004). b) Plaquetario: es la adhesion y posterior agregacion de las plaquetas. El contacto de las plaquetas con la estructura subendotelial del vaso lesionado, es favorecido por la vasoconstriction, este las activa y es el principio de un proceso biologico que culmina con la agregacion de todas las plaquetas en un coagulo hemostatico que llamamos trombo bianco. c) Liberacion: despues de la adhesion, cambio de forma y agregacion primaria, las plaquetas comienzan a descargar en el area circundante los contenidos de los granulos (Mckenzie B., 2000). d) Plasmatico: es la production de una molecula (fibrina) capaz de formar un coagulo firme que asegura el cese de la hemorragia (Cordova A. y cols, 1996). 1.2 HEMOSTASIA PRIMARIA En condiciones fisiologicas la hemostasia primaria funciona equilibradamente, entre elementos celulares y proteicos. Esto se lleva a cabo gracias a las funciones que desempena la celula endotelial, su funcion especifica es la tromborregulacion y las plaquetas estan capacitadas para reaccionar ante una lesion del vaso sanguineo y formar rapidamente un tapon plaquetario, mediante los procesos de adhesion y agregacion plaquetaria (Quintana G., 2002). Cuando ocurre una lesion de un vaso sanguineo se ponen en juego una serie de mecanismos que funcionan equilibradamente con la finalidad de hacer cesar una hemorragia. En primer lugar existe una vasoconstriction seguido por la exposition al subendotelio que esta constituido por colagena y elastina, exponiendo cargas positivas que incrementan la atraccion plaquetaria, ademas de la atraccion producida por la enzima glucosiltransferasa. Por otra parte la production y liberation de prostaciclinas (PGI2) disminuye drasticamente, por lo que favorecen los mecanismos de activation plaquetaria. Las glucoproteinas (GP) de la membrana actuan como receptores, mediando diferentes procesos de la hemostasia primaria. En este proceso, la interaction entre plaquetas y celulas endoteliales es fundamental para el adecuado y equilibrado funcionamiento de la hemostasia (Martinez M., y cols, 1996) (Figura 1). Plaquetas Contacto Lesion Adhesion FuW ^ colagena ADP Liberacion Ca++ Serotooina. Agregacion Fosfolipidos Coagulacion Figura 1. Mecanismos principales en la hemostasia, desde la lesion vascular hasta la formacion del coagulo hemostatico. 1.3 PLAQUETAS Las plaquetas quiescentes circulantes son celulas en forma de disco con superficies lisas. A diferencia de las superficies exteriores de los eritrocitos y leucocitos, las plaquetas tienen varias aberturas semejantes a los orificios de una esponja, los cuales son conductos membranosos que se extienden profundamente al interior de la celula. Despues de una lesion se producen varios cambios que afectan la morfologia y la bioquimica de las plaquetas, y hacen que las plaquetas se vuelvan "activadas". 1.3.1 Membrana plasmatica La membrana plasmatica de la plaqueta esta recubierta en el exterior por una capa superficial laxa, y en el interior por una region submembranosa delgada. La cubierta superficial, llamada tambien glucocalix, consiste en varias GP, proteinas, mucopolisacaridos y fosfolipidos que muy probablemente se absorben del plasma. Algunas de las proteinas de la superficie pueden ser receptores para las sustancias que causan la activation de la plaqueta (Mckenzie B., 2000). Los fosfolipidos se distribuyen asimetricamente en la bicapa y los que poseen carga negativa, tales como el fosfatidilinositol, fosfatidiserina y fosfatidiletanolamina se localizan preferentemente en la capa interna. Esta distribution tiene, tambien, un signifigado funcional ya que sirven como sustratos para enzimas intracelulares (fosfolipasas) durante la activation plaquetaria (Monteiro M.C. y cols, 2001). Las GP median un amplio numero de interacciones de adhesividad celular. Estas funcionan como receptores que reciben senales del exterior de las plaquetas, facilitando la interaction celula a celula y uniendose a ligandos especificos en sus receptores, desencadenan la respuesta plaquetaria a diferentes estimulos Tabla 1(Camacho J.A., 2000). GLICOPROTEINA GPIIb/llla ( aifa2bbeta3CD41/CD61) GPIa/lia(VLA-2-alfa2beta1-CD49b/CD29) GPIc-lia(alfa5beta1-CD49e/CD29) GPIc-lla(VLA-6;alfa6beta1; CD49f/CD29) Alfav-beta3 (CD51/CD61) GPIb-IX (CD42) GPV Selectina P (GMP-140; PADGEM) PECAM-1 FUNCION PROPUESTA Receptor Receptor Receptor Receptor Receptor Receptor de fibrinogeno y factor FvW de colageno de fibronectina de laminina de vitronectina, FvW, fibrinogeno de FvW y trombina Sustrato de trombina Interaction de plaquetas y leucocitos Interaction celula a celula TABLA 1: Caracterfsticas de las glicoproteinas de la membrana plaquetaria. J.A., 2000 Fuente: Camacho 1.3.2 Citoesqueleto Esta constituido por microtubulos y una red de proteinas. Las funciones de este consiste en dar soporte a la membrana plasmatica, en mantener la forma discoide de la plaqueta en reposo y en proporcionar un medio para el cambio de forma cuando la plaqueta se activa. Cuando las plaquetas son activadas, una cantidad adicional de actina polimeriza y se asocia a otras proteinas, lo que determina la organization de estos filamentos en una red tridimensional periferica y la formation de haces, originando los pseudopodos. Estas transformaciones de la actina son responsables del cambio de forma de las plaquetas, el cual caracteriza su activation en el aspecto morfologico. La contraction de los filamentos perifericos hace que los granulos dispersos en el citoplasma ocupen una position central, y simultaneamente liberen sus contenidos (Monteiro M.C. y cols, 2001). 1.3.3 Granulos La plaqueta contiene, distribuidos por su citoplasma, una gran cantidad de granulos: granulos a, granulos densos y lisosomas. Al ser activada la plaqueta estos granulos son centralizados, a lo que sigue la secretion se sus contenidos. Los granulos densos recibe ese nombre debido a que se presentan mas densos en los preparados de microscopia electronica que los otros tipos de granulos. Estos cuerpos contienen mediadores de la funcion de las plaquetas y de la hemostasia que no son proteinas: ADP, ATP y otros nucleotidos, asi como compuestos de fosfatos, iones de calcio y serotonina. Los granulos alfa son los mas abundantes de los tres tipos de granulos. Contienen dos grupos principales de proteinas, un grupo consiste en proteinas similares a las proteinas hemostaticas que se encuentran en el plasma, como el Factor de Von Willebrand (FvW) y el factor V. Otras como el fibrinogeno, se absorben del plasma y se empacan en los granulos alfa. El segundo grupo incluye proteinas con una diversidad de funciones, algunas se encuentran exclusivamente en las plaquetas como: el factor plaquetario 4 (FP4), la (-tromboglobulina (/?-TG) y el factor de crecimiento derivado de la plaqueta (PDGF). Los lisosomas se caracterizan por su contenido rico en enzimas hidroliticas, principalmente hidrolasas acidas. La exteriorization del contenido de estos granulos puede ser observada durante la activation plaquetaria con agonistas fuertes, por ejemplo a traves de la exposition en la superficie celular de glucoproteinas, unicamente presentes en la membrana de los lisosomas de la plaqueta en reposo (Monteiro M.C. y cols, 2001). 1.3.4 Sistema canalicular abierto El SCA se presenta como una red de vesiculas y canales, interconectados, que se ramifican a traves de todo el citoplasma y se comunican con la superficie. Tiene v una localization preferential bajo la membrana celular y estan aparentemente desprovistos de contenido. El SCA consiste en invaginaciones de la membrana citoplasmatica de la cual deriva su estructura, este sistema constituye una via de acceso de sustancias plasmaticas a lugares mas internos de la celula, y durante la activation plaquetaria constituye una reserva de membrana plasmatica que permite el cambio de forma y la emision de pseudopodos (Figura 2). 1.3.5 Sistema tubular denso El STD se presenta como un conjunto de tubos apretados y cortos, que se distinguen del SCA por su opacidad, estos tubos forman una red continua por todo el citoplasma, siendo mas apretado en la periferia que en el centra de celula. El STD constituye el principal lugar de almacenamiento del calcio intraplaquetario, siendo por eso comparable al reticulo sarcoplasmic de las celulas del musculo estriado, este acumula calcio debido a la presencia de un transportador de Ca+2 ATPasa, en sus membranas, citoplasmatico libre (Figura 2). que regula.n la concentration de calcio Glucocalix Microtubulos j Granulos alfa Glucogeno Granulos densos ^ s & a z * ^ ^ S i s t . Tubular denso Sist. Canicular abierto FIGURA 2. Diagrama de las caracteristicas estructurales primarias de la plaqueta en reposo. Fuente: www.hhmi.org/askascientist/ images/platelet2.gif Innumerables fenomenos de la fisiologia plaquetaria dependen de la concentracion citoplasmatica de este ion, por ejemplo, para mantener los microtubulos en la forma polimerizada y, consecuentemente, la forma discoide de la plaqueta, que requiere una baja concentracion citoplasmatica de Ca+2 (Monteiro M.C. y cols, 2001). 1.4 ACTIVACION PLAQUETARIA La activacion se inicia con la union del agonista a receptores de la membrana plasmatica de la plaqueta. Este agonista puede ser cualquier agente que induzca la activacion de las plaquetas. Se ha visto que varias sustancias estimulan a las plaquetas y causan los cambios metabolicos. Algunas son generadas por las propias plaquetas y otras por diversas celulas en el tejido lesionado. Otras estan presentes normalmente dentro de las celulas, pero se generan cuando las celulas se lesionan. Cada agonista se enlaza a un receptor de plaquetas especifico y causa una serie de reacciones en el interior de la plaqueta (Mckenzie B., 2000). Cuando un agonista se une a un receptor este adquiere una conformation que le permite interactuar con una determinada proteina G, la cual se encuentra en un estado inactivo produciendo un complejo transitorio. El acoplamiento del receptor activado con la region amino terminal de la proteina G induce a su vez cambios conformacionales que conllevan a la liberation de GDP. 1.4.1 AGONISTAS PLAQUETARIOS Y SUS RECEPTORES Los agonistas fisiologicos que pueden activar las plaquetas son muy variados e incluyen trombina, TXA 2 , PAF, ADP y epinefrina. Hasta hace poco se conocia mas de las respuestas plaquetarias a diversos agonistas que sobre la estructura de sus receptores. Sin embargo, en los ultimos anos se han hecho progresos en esta area, habiendose clonado con exito los receptores de la trombina, TXA2, PAF y ADP. Todos los receptores de agonistas que interactuan con proteinas G, identificados hasta el momento, consisten tipicamente en una cadena polipeptidica con una portion N-terminal extracelular, una portion C-terminal intracelular y siete dominios transmembrana. 1.5 MECANISMOS DE SENALIZACION Ante el estimulo de los agonistas, las plaquetas inician una serie de eventos bioquimicos que les permiten responder en caso necesario. Uno de ellos es la transduction de la senal al interior de esta celula, la cual se realiza a traves de la proteina G (PG) (Martinez M., y cols, 1996), dando initio a la cascada de senalizacion. 1.5.1 PROTEINAS G Son un grupo de proteinas que tienen especial afinidad por los nucleotidos de guanina. Estas desempenan un papel muy importante en la transduction de senates en las celulas eucariotes. Estas proteinas acoplan a mas de 100 receptores distintos para diversas proteinas como la adenilato ciclasa (AC), la guanilato ciclasa, y algunos tipos de canales ionicos. Los estudios estructurales indican que las proteinas G tienen estructura de trimeros que pueden adoptar una conformation "abierta" o "cerrada". Estas proteinas pueden ser consideradas como nanomaquinas moleculares. La proteina G heterotrimerica consta de una subunidad alfa de 45-47 kDa, una subunidad beta de 35 kDa y una subunidad gamma de 7-9 kDa. Se han identificado tambien isoformas de cada una de las tres subunidades, lo cual permite que exista una amplia variedad de proteinas G diferentes (Khan N. y cols, 2001). Las subunidades de la proteina G en su forma inactiva se encuentran unidas. Cuando estan activas, la subunidad a se une al GTP y las subunidades p y y se encargan del anclaje de la PG quienes regulan las enzimas intraplaquetarias como son: AC y fosfolipasa A 2 (PLA 2 ) y fosfolipasa C (PLC) Existen varias proteinas G con funciones diferentes: • Gp: Activan las interacciones ligando-receptor a traves de la Fosfolipasa C (PLC). • Gs: ("s" por stimulation = estimulacion) activa la AC.al unirse el ligando con el Receptor. • Gi: ("i" por inhibition) tiene algunas interacciones inhibitorias sobre el agonista-receptor de la adenilato ciclasa (Martinez M., y cols, 1996). Los receptores para muchos agonistas de las plaquetas interactuan con las proteinas G para activar fosfolipasas, tales como la fosfolipasa C (PLC) y fosfolipasa A 2 (PLA2), tirosina cinasas y tambien suprimiendo la formation de AMPc (segundo mensajero) por inhibition de la adenil ciclasa. Como el AMPc tiene un papel inhibidor en la plaqueta, ambos efectos favorecen la activacion plaquetaria. La formation de segundos mensajeros activadores de vias bioquimicas intracelulares comunes, son generados como consecuencia de la hidrolisis enzimatica de fosfolipidos especificos de la membrana. La cual se Neva a cabo por dos vias, una mediada por PLC y otra por PLA2. La PLC inicia el metabolismo de los fosfoinositidos y los productos de su reaction incluyen inositol-1,4,5-trifosfato de inositol (IP3) y diacilglicerol (DG). El IP3 promueve la liberation de calcio del sistema tubular denso, contribuyendo al incremento de la concentration intracelular de este ion. Un aumento de calcio citoplasmatico, tiene un papel central en la activation de la plaqueta estimulando la respuesta de sistemas dependientes, tanto de calcio libre, como del complejo calcio-calmodulina. El DG activa la proteina cinasa C, llevando a la fosforilacion de proteinas, secretion de los granulos y expresion del receptor para el fibrinogeno. La activation de la PKC requiere calcio y fosfolipidos, siendo la fosfotidilserina un cofactor esencial. Esta proteina cataliza la fosforilacion de residuos de serina y treonina en diversas proteinas implicadas en la secretion de los granulos y en la exposition del sitio receptor para el fibrinogeno en el complejo Gp llb/llla. El principal substrato de la PKC es la proteina P47 o pleckstrina, cuya fosforilacion ocurre de modo simultaneo a la liberation de serotonina de los granulos densos. La PLA2 media la formation de endoperoxidos de prostaglandinas y de tromboxano A2, liberando gran cantidad de acido araquidonico (AA) a partir de fosfolipidos de la membrana, durante la activation plaquetaria (Monteiro M.C. y cols, 2001). La cadena de miosina es el sustrato principal dependiente de calcio-calmodulina y de la protein Cinasa C en las plaquetas. La fosforilacion de la cadena de miosina es relacionada casualmente con el cambio de forma de la plaqueta, la contraction y la secretion. El calcio induce la union de la calmodulina con la proteina Cinasa C, con consecuente activacion enzimatica que tiene como resultado la fosforilacion de la cadena ligera de miosina. Esta cadena permite que el hexamero de miosina pueda ser activado por la actina, y esta activacion genera las fuerzas requeridas para la funcion contractil. Una proteasa dependiente de calcio se adhiere a una proteina de union-activacion y a un polipeptido que permite la reorganization del citoesqueleto de la plaqueta durante la agregacion plaquetaria (Kroll H.M. y cols, 1989). 1.5.2 Activacion por Adenosin difosfato El ADP como ya se menciono se encuentra almacenado en los granulos densos de las plaquetas, de los cuales se liberan tras la activacion plaquetaria. La exposition de las plaquetas al ADP produce un incremento de calcio. El ADP causa cambio de forma, activacion del receptor del fibrinogeno, agregacion y secretion. Las respuestas plaquetarias inducidas por ADP fueron inicialmente atribuidas a un unico receptor del tipo purinergico P2T. Sin embargo, estudios mas recientes pusieron de manifiesto la posibilidad de que los efectos de ADP en las plaquetas sean mediados por 3 subtipos de receptores P 2 . Segun Kunapuli y Daniel., un receptor esta acoplado por Gi a la inhibition de la adenil ciclasa (P2tac), otro acoplado por Gq a la activacion de la PLC (P2yi) y el tercero, es un receptor ionotropico P 2 xi mediador de influjo rapido de calcio. El receptor receptor P 2 yi P2jac media en el cambio de forma inducido por ADP, mientras que el es esencial para la agregacion, aunque esta respuesta resulte de la serialization a traves de P2tac y P2Y1. 1.5.6 Activacion por el Factor Activador de Plaquetas El factor activador de plaquetas (PAF) es una molecula generada por diversas celulas circulantes activadas, incluyendo las plaquetas y los leucocitos. Es un lipido complejo formado, a partir de fosfolipido membranar, por la accion consecutiva de la PLA2 y una acil transferasa. Esta molecula es un potente activador de cambio de forma, agregacion y secrecion de las plaquetas. El PAF actua mediante receptores especificos acoplados a la PLC, induciendo por eso el metabolismo de fosfoinositidos y movilizacion de calcio. Tal como el TXA2, PAF no inhibe la adenilato ciclasa (Monteiro M.C. y cols, 2001) (Figura 3). Figura 3. Fisiologia plaquetaria y principales www.strokecenter.org/.../ platelet_activation.jpg vias metabolicas. Fuente: 1.6 ADHESION El evento inicial de activacion de las plaquetas en la hemostasia, se conoce como adhesion plaquetaria y consiste en el contacto de las plaquetas con el subendotelio rico en colagena (Bobadilla L., 1985). Cuando el endotelio se lesiona se produce hemorragia y las plaquetas se escapan de los vasos sanguineos y fluyen al interior de los tejidos subendoteliales. Inmediatamente se pegan a los componentes del subendotelio, de los cuales el elemento mas importante son las fibras de colagena (Mackenzie B. 2000). El proceso de adhesion comprende el transporte por difusion de las plaquetas hacia la superficie reactiva y la interaction de los receptores de la membrana plaquetaria con sus ligandos en las estructuras de la pared lesionada. Entre las proteinas adhesivas de la matriz se incluyen la colagena, la fibronectina, el FvW, la laminina, la vitronectina y la trombospodina. En los segundos siguientes a la lesion, las plaquetas se adhieren a las fibrillas de colagena del subendotelio vascular a traves de un receptor de la colagena especifico para las plaquetas y presente en su estructura terciaria. Dicho receptor es la Gp la/I la. Esta interaction esta estabilizada por el FvW, una glucoproteina adhesiva que permite a las plaquetas permanecer unidas a la pared del vaso a pesar de las elevadas fuerzas tangenciales que se generan en el interior de la luz vascular como consecuencia de altas velocidades de cizalladura. El FvW realiza esta funcion formando un enlace entre el receptor plaquetario situado en la Gplb/IX y las fibrillas de colagena subendoteliales. Por otro lado, el receptor plaquetario Gp llb/llla tambien participa en la adhesion plaquetaria, sobre todo en condiciones de alta velocidad de cizalladura local, ligandose al FvW. Una vez adheridas al subendotelio, las plaquetas se extienden sobre la superficie y plaquetas adicionales aportadas por el flujo sanguineo se unen a las plaquetas ya adheridas (Herrero L., y cols, 2000) Fig 4. Figura 4. Fase de Adhesion de la Hemostasia Primaria 1.7 AGREGACION Y LIBERACION Despues que las plaquetas adherentes se activan, el tapon hemostatico primario continua en una fase conocida como agregacion. La agregacion de las plaquetas es la adhesion de las plaquetas entre si. Las plaquetas nuevas que fluyen al interior del tejido hemorragico se activan por contacto con agonistas como ADP los cuales se liberan por el tejido y las celulas endoteliales (Mackenzie B. 2000). La adhesion y agregacion implica secrecion la cual, a su vez, recluta mas plaquetas. En este punto, el coagulo es una masa de plaquetas degranuladas, empacadas estrechamente y rodeadas de muy poca fibrina. Hay otros agonistas incluyendo epinefrina, colagena, trombina y Factor activador de plaquetas (PAF) pero, aparentemente, existe una via agonista comun que hace aumentar el calcio citoplasmatico, fenomeno clave en la activacion plaquetaria (Ruiz-Arguelles G.J., 2004). La agregacion se produce en dos fases llamadas primaria y secundaria. Durante la agregacion primaria las plaquetas se adhieren laxamente entre si; si el estimulo por los agonistas es debil la agregacion es reversible. La agregacion secundaria tarda mas tiempo y empieza cuando las plaquetas comienzan a liberar su propio ADP y otros contenidos de los granulos. Presuntamente, las sustancias liberadas se vuelven agonistas que continuan con el proceso de estimulacion. Se necesita fibrinogeno y calcio extracelular para que se produzca la agregacion. Ambos son elementos constitutivos del plasma. Tambien, ambos son liberados por las plaquetas de los granulos internos de almacenamiento para proporcionar altas concentraciones en el area lesionada (Mackenzie B. 2000). La reaction de liberacion es un proceso de secretion de las sustancias que se encuentran almacenadas en los granulos plaquetarios, ADP, adrenalina, tejido conectivo subendotelial y trombina son los agentes fisiologicos mas importantes para producir esta reaction de liberacion ( Figura 5). Finalmente, viene la fusion de sus membranas. Este fenomeno es conocido como agregacion secundaria, la cual tiene caracter irreversible. La agregacion y la liberacion plaquetaria requieren la presencia de calcio extracelular (Martinez M., y cols, 1996). Figura 5. Fase de Liberacion y Agregacion de la Hemostasia Primaria. 1.8 INHIBICION PLAQUETARIA Cada una de estas proteinas G son un complejo heterotrimerico (subunidades alfa, beta, y gamma), que tiene GDP unido estrechamente a la subunidad alfa en estado basal. Despues de que ocurre la union del receptor-ligando, GDP se disocia del complejo. En reposo citoplasmaticos, y presencia de GTP y Mg+2, se lleva a cabo la disociacion de GTP, permitiendo la interaccion con una enzima "amplificadora de la senal". La cual se encuentra dentro de la matriz de la membrana convirtiendose en moleculas fosforiladas liamadas segundos mensajeros. El GTP estimula la adenilato ciclasa para la produccion de AMPc llevando la inhibicion plaquetaria y por actividad de la GTPasa convierte el GTP en GDP liberando fosforo inorganico regresando asi a su estado basal. La subunidad p y y son importantes ya que participan en la regulation de la AC (Figura 6). Las PG juegan un papel importante en los mecanismos de activation, al modificar positivamente (activar) o negativamente (inhibir) a diferentes enzimas, por lo tanto se les considera el "switch" del sistema de activation (Martinez M, y cols, 1996). Inhibicion Plaquetaria 6TP, Mg FIGURA 6. Modelo Teorico de la PG. El modelo teorico general por el cual las proteinas G transmiten senales extracelulares en respuestas intracelulares: 1) En estado basal, GDP esta ligada al heterotrimero de la proteina G (en este .caso Gs) a traves de un sitio de union de la subunidad a; 2) un ligando extracelular une a una proteina G receptor (PGI2 o PGD2) causa la hidrolisis de GDP de la subunidad a; 3) en presencia de Mg2+, GTP ocupa el sitio abierto de union con el nucleotido guanina, teniendo como resultado la disociacion de la subunidad a del complejo de la proteina G. Ga GTP activan la adenilato ciclasa, resultando en la elevation de los niveles de cAMP en el citosol. La actividad intrinseca de la GTPasa de la proteina G convierte el GTP en GDP, resultando en la reasociacion del heterotrimero y restauracion ciclica del estado basal FUENTE: (Kroll H.M. y cols, 1989). 1.9 PLOMO 1.9.1 PROPIEDADES FISICAS Y QUIMICAS El plomo (Pb) es un metal pesado de color gris plateado, maleable y dificil de corroer. Tiene un numero atomico de 82, un peso atomico de 207.19, con una gravedad especifica de 11.34 y con cuatro electrones de Valencia en su ultimo orbital, pero solo dos se ionizan facilmente por lo cual el estado habitual de oxidation de sus compuestos inorganicos es de +2 y +4 (Lopez-Miranda A. 1994). En algunas de sus propiedades quimicas el plomo tiene mas parecido con los metales alcalinoterreos (grupo IIA) que con los miembros de su grupo. Lo cual explica por que el plomo puede competir con el calcio, el zinc y el hierro. El plomo forma complejos con moleculas organicas como los acidos grasos, los lipidos, las proteinas y los acidos nucleicos. El plomo metalico es resistente a la corrosion (resiste la action del aire o del agua). Cuando el metal se expone al aire, una capa fina de compuestos de plomo cubre al metal y lo protege de ataque adicional. Se encuentra en las minas de yacimientos ricos en zinc o en cobre. La abundancia del plomo en la tierra y su bajo punto de fusion ha hecho que sea uno de los metales mas utilizados por el hombre (Rendon-Ramirez AL. 2005). En alguna epoca de su historia el hombre ha utilizado extensivamente el plomo y sus compuestos; por ello se ha hecho patentes sus efectos toxicos (Cervantes C. y cols, 1999). La ingestion de plomo fue probablemente difundida a traves de las costumbres de los romanos, debido a que muchos utensilios contenian pigmentos a base de plomo y se utilizaban tanto para la elaboration como el transporte de la comida. Se ha sugerido que una de las causas de la caida del imperio romano fue la toxicidad causada por el plomo. Mas adelante; en los anos 40's se reconocieron los efectos nocivos del plomo, especialmente en las personas laboralmente expuestas. Es hasta la decada de los 70's" cuando se comienzan a estudiar los efectos a niveles de exposition menores. Entre 1950 y 1990 se tuvieron grandes avances en epidemiologia y politicas publicas respecto al plomo mundialmente (Vazquez-Ballesteros y cols., 2002). 1.9.2 EPIDEMIOLOGIA En nuestro pais, el plomo es uno de los contaminantes mas ampliamente distribuidos en la corteza terrestre. Se emite por combustion de la gasolina en los vehiculos y en las fabricas de fundicion. Anualmente se deposita en el ambiente una gran cantidad de plomo que ahi permanece por largo tiempo debido a que este elemento no es biodegradable y su solubilidad es limitada (Navarro-Moreno LG, 2004). Mexico es el tercer exportador de plomo despues de Australia y Canada. Las pinturas y los pigmentos que contenian cromato de plomo fueron de uso comun en Mexico. Estos cromatos se utilizaron en la production de lapices de colores, juguetes y tinta para envoltura de algunos dulces. Esto genero la intoxication con plomo en personas que tienen la costumbre de masticarlos. Otra fuente de exposition a este toxico lo es la elaboration de piezas artesanales de barro, que utilizan el oxido de plomo para la fase de esmaltado. El Instituto Mexicano del Seguro Social, por medio de la Coordination de Salud en el Trabajo, en el periodo de 1985-1994, senalaba a la intoxication con plomo (saturnismo) como una de las diez primeras causas de enfermedades del trabajo (Rendon-Ramirez AL. 2005). De acuerdo a la Norma Oficial Mexicana (NOM), el minimo tolerable de plomo en sangre es de 25 pg/dl en personas ocupacionalmente expuestas, pese a que las normas de Estados Unidos senalan estandares menores que indican atencion medica ante solo 10 pg/dl, sin embargo este limite en nuestro pais es aplicable a la poblacion abierta (Navarro-Moreno LG, 2004). En 1995 la Secretaria de Salud y Asistencia Publica (SSA) realizo un estudio en 49 industrias de seis estados del pais, en una poblacion de 4,022 trabajadores, este estudio mostro que el 1.7% de los trabajadores presentaron niveles de plomo en sangre de 40 pg/dl. El dato es sobresaliente debido a que estas industrias no involucran procesos de exposition a plomo y sus trabajadores presentaron una concentracion de plomo en sangre cuatro veces por arriba de los limites establecidos por la SSA (menor a 10pg/dl). Lo que sugiere que se requiere una mayor protection laboral en las industrias mexicanas (Rendon-Ramirez AL. 2005). En el estado de Veracruz en la localidad de Chavarrillo en el municipio de Emiliano Zapata, se realizo, un estudio para conocer los niveles de plomo en sangre en mujeres y ninos de familias que se dedican a la alfareria. Encontrando como resultado que el 100% del grupo de estudio presento concentraciones de plomo superiores a los 10pg/dl, no presentando ninguna sintomatologia asociada a la intoxication por plomo (Chantiri Perez JN y cols, 2004). 1.9.3 EXPOSICION, ABSORCION, DISTRIBUCION Y ELIMINACION Se conocen tres formas de exposition al plomO: ocupacional, paraocupacional y ambiental. • La exposition ocupacional se da entre trabajadores que tienen actividades de riesgo tales como: las industrias procesadoras de plomo entre las que se encuentran: la mineria, la refinacion de metales, las generadoras y recicladotas de baterias automotrices, en la production de vitrales, en la production artesanal de barro vidriado. • La exposition paraocupacional se presenta cuando ios trabajadores de las actividades antes mencionadas llevan sus ropas, zapatos o utensilios de trabajo a casa o cuando tienen deficiencia en sus habitos higienicos. Estas conductas llevan el contaminante a otros ambitos con lo cual se extiende la exposition a otros miembros de la familia, principalmente a los ninos debido a sus habitos y a su mayor susceptibilidad. La exposition ambiental es factible para las personas que viven en las cercanias de las industrias en donde se procesa, se utiliza, se acumula o se desecha el plomo, y que no cuentan con las medidas de control sanitario adecuadas Fig. 7. (Rendon-Ramirez AL. 2005). FIGURA 7.Distribution del plomo en el organismo humano. Fuente: Rendon-Ramirez AL. 2005 El plomo ingresa al organismo basicamente por las vias digestivas y respiratorias aunque, eventualmente y bajo ciertas condiciones, tambien puede ser absorbido por la piel. Una vez en el organismo se distribuye por medio de la sangre al resto de los tejidos, preferencialmente hacia el hueso, que es muy resistente al plomo. El tejido oseo en realidad constituye un organo de almacenamiento, ya que retiene una buena parte y por lo tanto la cantidad de plomo disponible es mucho menor. El resto del plomo se distribuye a otros organos, tales como el cerebro, el rinon, la medula osea y el higado, algunos de los cuales se danan aun con bajos niveles de plomo, lo que los convierte en organos bianco (Calderon S., 1997). Una vez que el plomo es absorbido por las distintas vias se distribuye y redistribuye a todos los tejidos a traves de la sangre causando alteraciones en los sistemas nervioso, hepatico, renal y hematopoyetico. En la sangre el plomo se concentra principalmente en los eritrocitos (94%) y el restante en el plasma. La union del plomo a los eritrocitos no se limita a la membrana plasmatica, sino que el 80% penetra al citoplasma y solo el 20% se une a los constituyentes membranales, en particular a la fraction proteica. El metal se absorbe en el tracto gastrointestinal a traves de los transportadores del calcio. La absorcion intestinal del plomo tiene una relation inversa con el contenido de calcio en la dieta, a mayor contenido de calcio en la dieta hay una menor absorcion de plomo. Las proteinas transportadoras del calcio en el intestino son inducidas por la hormona calcitriol 1,25-dihidroxicolecalciferol favoreciendo la absorcion de plomo en el organismo durante la intoxication (Rendon-Ramirez AL. 2005). El plomo puede formar sales inorganicas y organicas. Las sales inorganicas se forman cuando el plomo tiene una Valencia de +2, mientras que en las sales organicas su Valencia puede ser ademas de +4. Una vez en el organismo, las sales son transformadas a plomo +2 y en esta forma el plomo es capaz de competir con el calcio y con otros cationes divalentes de importancia fisiologica. Solamente una proportion del plomo circulante puede ser excretado; la principal via de excretion es la urinaria, mientras que una proportion mas pequena puede desecharse por los fluidos de secretion gastrointestinal, de manera que la mayor parte del plomo que se encuentra en las heces es plomo que no fue absorbido por la via digestiva. Tambien es posible eliminar una pequena cantidad de plomo por las celulas que se descaman en la piel, en elpelo y las unas, y existen algunas condiciones fisiologicas que permiten que el plomo pueda ser excretado por otros fluidos, como la leche materna. A pesar de que una parte importante de la permanencia del plomo en el organismo podria atribuirse a la diferencia entre la absorcion y la excretion, tambien podria explicarse por la gran afinidad que muestra el plomo por las celulas y por los tejidos, como resultado de su interaction con macromoleculas. Aun cuando existen diferentes vias de excretion, la relation absorcion/excrecion siempre es mayor a la unidad; esto se traduce en acumulacion de plomo en el organismo. Se estima que el tiempo necesario para que una persona expuesta a bajas dosis de plomo elimine completamente ese metal de sus tejidos es de 20 anos a partir de que cesa la exposition (Calderon S., 1997). 1.9.4 EFECTOS DEL PLOMO A NIVEL SISTEMICO El plomo metalico no representa ningun problema ambiental o de salud, estos comienzan cuando se disuelve y pasa a su forma ionica. El mecanismo de action del metal se debe principalmente a su efecto sobre el organismo cuando se acumula en el, por carecer de una funcion fisiologica y repercutir en una diversidad de procesos bioquimicos esenciales ocasionando dano. El plomo tiene la caracteristica de intoxicar no solo a quien lo maneja, sino tambien a quienes habitan en la periferia de los sitios en donde se efectuan manipulaciones con el (Albert, 2004). Se han detectado efectos hematologicos, cardiovasculares y evidencia de deterioro de la funcion renal en sujetos con cifras de plomo plasmatico elevado. Asimismo, los danos al sistema respiratorio se reflejan en el incremento de neumonias asociadas a niveles elevados de plomo en aire. Se ha detectado la inhibition de fagocitos y distintos efectos sobre la inmunidad pulmonar. A niveles de bajas dosis, existen evidencias de dano neurologico y neurocomportamental, que podrian expresarse en trastornos del aprendizaje y deficit atencional. Tambien existen asociaciones en trabajadores expuestos a plomo, con mayor mortalidad portumores en general. • Sistema Hematopoyetico: en la sangre el plomo se concentra principalmente en los eritrocitos (94%) y el restante en el plasma. La union del plomo a los eritrocitos no se limita a la membrana plasmatica, sino que el 80% penetra al citoplasma y solo el 20% se une a los constituyentes membranales, en particular a la fraction proteica. La 5-ALA-D es una enzima citosolica que se inhibe con rapidez por el plomo tanto in vivo como in vitro. La base molecular radica, en parte, en la alta afinidad del plomo para unirse a los grupos sulfhidrilos de las cisteinas, con las cuales forma complejos llamados mercaptidos. O por la generation de radicales libres provocando dano oxidativo (entorno de la proteina) u oxidando la enzima directamente (Rendon-Ramirez AL. 2005). Otra enzima inhibida es la hem-sintetasa o ferroquelatasa. Enzima intramitocondrial que cataliza el paso de protoporfirina IX a hemo, incorporando el hierro a su molecula (figura 5). La consecuencia de esta inhibition es triple: se produce una acumulacion de protoporfirina IX en el eritroblasto; el hierro no utilizado se acumula en el eritroblasto ocasionando su intoxication y probable muerte, con la consecuente eritropoyesis ineficaz y el incremento serico de este metal (ligera hipersideremia), y la protoporfirina IX quela al zinc, formando una nueva molecula Zn-protoporfirina (Zn-PP), que, por su tamano, no puede salir del eritrocito, incrementando la concentracion de dicha metaloporfirina y disminuyendo la de la hemoglobina. Todo esto se traduce clinicamente en diversos tipos y grados de anemia, cuando se alcanzan niveles de plomo en sangre alrededor de 50 pg/dl. Durante la intoxication cronica por plomo se ha reportado disminucion de la coagulation sanguinea. El principal mecanismo es la suplantacion de cationes polivalentes (esencialmente calcio) en el organismo, lo cual es posible gracias a una estructura ionica que le permite establecer interacciones muy favorables con los grupos que coordinan los cationes polivalentes en las proteinas, en ocasiones con mas afinidad que la del propio ion suplantado (Garza A. y cols, 2005). • Renal: uno de los organos afectados por la intoxication con plomo es el rinon, en donde el plomo se concentra una hora despues de su absorcion por el intestino. El plomo puede ser excretado dependiendo de la cantidad y duration de la exposition. En la exposition aguda el plomo se excreta via filtration glomerular y secretion tubular. En casos de exposition cronica se ha observado que el plomo se encuentra en las celulas de los tubulos proximales. Se ha observado que pueden existir dos formas de dano renal. La primera de elas la constituye el dano a tubulos proximales, que se caracteriza por sintomas similares a los del Sindrome de Fanconi (caracterizado por glucosuria, aminoaciduria, fosfaturia, etc) y por cambios morfologicos caracterizados por la degeneration de las celulas epiteliales. La segunda es la falla renal, caracterizada por filtration glomerular disminuida, fibrosis intersticial y alteraciones vasculares severas. Algunos estudios han revelado que cerca del 1% de los casos de nefropatia en estado final que requieren de dialisis o transplante son originadas por la intoxication con plomo, sin embargo, el hecho de que no existan indicadores tempranos de nefropatia ocasionada por intoxication con plomo hace que sea dificil conocer la incidencia de problemas nefrologicos inducidos por la intoxication con plomo (Navarro-Moreno LG, 2004). • Sistema nervioso: el sistema nervioso es especialmente susceptible a la action del plomo, en particular durante la etapa de maduracion, lo que hace que los ninos sean unos de los grupos poblacionales mas vulnerables a una exposition a este metal. Los estragos ocasionados ocurren aun en niveles reducidos de plomo y, aunque son irreversibles pueden pasar inadvertidos (Garza A. y cols, 2005). Entre estos se encuentran cambios neuropsicologicos como alteraciones en el aprendizaje, reduction del cociente intelectual, cambios de comportamiento con hiperactividad, vocabulario escaso, reduction de crecimiento y perdida de la agudeza auditiva (Ferrer A. 2003). • Cardiovascular: La intoxication cronica tambien se ha vinculado con la gota y la hipertension. Los niveles de plomo sanguineo se han asociado directamente con la presion arterial en adultos, inclusive cuando dichos niveles llegan a ser de 5 a 10 pg/dl. Los estudios de seguimiento de largo plazo en personas con intoxication por plomo apoyan la posibilidad de un riesgo incrementado de hipertension y enfermedad cardiovascular (Matte TD, 2003). Estudios realizados por Kaji y cols, en 1992 proponen al plomo como un factor de riesgo que puede provocar lesiones vasculares. El metal induce aterosclerosis e hipertension in vivo y causa vasoconstriction in vitro, datos epidemiologicos sostienen que existe una relation significativa entre los niveles de plomo en sangre y la presion sanguinea (Kaji, T. y cols. 1992). • Hueso: el sitio primario de almacenamiento de plomo en el organismo es el hueso. Los individuos que han estado expuestos al plomo por largo tiempo alcanzan una mayor acumulacion de este metal en el hueso compacto que en el hueso trabecular el plomo tiene un recambio de minutos a horas, posiblemente por la mayor vascularidad y a que sufre una remodelacion constante. Por el contrario el plomo del hueso compacto tiene un menor intercambio (dias a anos) (Maldonado V. 1997). Las acciones toxicas del plomo se atribuyen a su afinidad por los sitios de action molecular del calcio; el metal actua como sustituto del calcio en varios eventos regulatorios intracelulares, ya que es capaz de activar las fosfodiesterasas dependientes de calmodulina y las proteinas cinasas independientes de la misma, teniendo efectos, ademas, sobre los canales de calcio (Gonzalez C. y cols 1998). En estudios realizados en ratas durante el embarazo y la lactancia se ha demostrado que en estados fisiologicos donde la absorcion y la cinetica distributiva del calcio se ven aumentada, la absorcion y la movilizacion del plomo tambien se ve estimulada. Cuando los animales intoxicados cronicamente con plomo y cursando el embarazo y lactancia se les administro un exceso de calcio en la dieta se observo un aumento en la resorcion osea de plomo, lo que condujo a un aumento de plomo en la sangre y la redistribution del toxico a los tejidos blandos, fenomeno denominado como autointoxication (Cortina-Ramirez GE, 1999). El deposito de plomo en hueso esta influido por practicamente todos los procesos que afectan el deposito o la movilizacion del calcio en el mismo. En etapas como la gestation, la lactancia y en estados nutricionales como la descalcificacion en las mujeres con exposition cronica a plomo se presentan incrementos de la concentration del plomo en la sangre, lo cual hace suponer que el plomo previamente acumulado en el hueso se moviliza de este tejido siguiendo una redistribution semejante a la de calcio. Cuando los niveles de calcio en la dieta son adecuados no se presentan descalcificaciones debido a que el calcio que sale del hueso es restituido por el que ingresa en la dieta, dando lugar a un fenomeno de recambio; asi, el calcio sale y entra al hueso en periodos muy cortos, dando la impresion de permanencia (Gonzalez C.y cols 1998). 1.9.5 EFECTOS DEL PLOMO A NIVEL MOLECULAR El plomo es un elemento que no tiene ninguna funcion fisiologica conocida en el organismo humano, pero cuyos efectos adversos inciden sobre una diversidad de procesos bioquimicos esenciales. El plomo se une a las proteinas por medios de cuatro mecanismos: 1) la interaction con sitios estereoespecificos que constituyen los sitios de union natural de los metales divalentes de importancia biologica como el Ca, Zn y Fe; 2) la interaction electrostatica, en dominios con alta densidad de carga negativa; 3) la interaction covalente con grupos sulfhidrilo vecinales, con los cuales forma mercaptidos y 4) por oxidation de lo.s grupos disponibles en las proteinas (grupos SH yCOOH) Fig 8 (Calderon S„ 1997). Otro tipo de macromoleculas que pueden sufrir danos estructurales y funcionales a consecuencia de la union del plomo son los acidos nucleicos. En concentraciones elevadas el plomo puede ser mutageno; sin embargo, si estas concentraciones se presentaran en un organismo antes de ocurrir la mutagenicidad, el organismo moriria por los danos renales, hepaticos y de sistema nervioso. No obstante, hasta el momento no se ha demostrado que el plomo pueda ser carcinogenico a las concentraciones que causan intoxication cronica y existen dudas sobre su capacidad teratogenica. El plomo puede ademas interaccionar con los lipidos, basicamente con los fosfolipidos de las membranas y particularmente con aquellos que poseen carga negativa; pero el problema principal no resulta de la interaction entre ellos, sino de la posibilidad de inducir lipoperoxidacion. Solamente a concentraciones elevadas, el plomo es capaz de inducir por si mismo lipoperoxidacion; sin embargo, en dosis bajas puede producirla si estan presentes grupos hemo libres o hierro. Debido a que la intoxication cronica con plomo induce el incremento de la concentracion de acido delta:aminolevulinico, de protoporfirinas eritrocitarias libres, de grupos hemo libres y de hierro libre, aun a bajas concentraciones del plomo puede tener un efecto oxidativo (Calderon S., 1997). La naturaleza de las manifestaciones de toxicidad depende no solo de la magnitud de la exposition sino tambien de las caracteristicas de la persona expuesta; la neurotoxicidad del plomo es mas critica para el feto en desarrollo y el nino en crecimiento que para los adultos (Gonzalez C. y cols 1998) (Figura 8). POSIBLES FORMAS DE DANO A MACROMOLECULAS DURANTE LA INTOXICACION POR PLOMO OXIDACIOII 1 INTERACCIOI1ES ELECTROSTATICAS y MACROMOLECULAS MERCAPTIDOS COPETEHCIA CON CATIONES D1VALEIITES Figura 8. Representacion del posible dano del plomo a macromoleculas. Fuente: Adela Rendon Ramirez, 2005. 1.10 PLOMO Y AGREGACION PLAQUETARIA Trabajos realizados por Sharp y cols., en 1991 reportaron una asociacion entre el retrazo en la agregacion plaquetaria in vitro y la presencia de altas concentraciones de plomo en sangre. De igual manera en 1992 la Dra. Banos de Mac Carthy y cols, del instituto nacional de cardiologia de la ciudad de Mexico, al investigar el efecto del plomo y el cadmio sobre la agregacion plaquetaria, descubrio que a altas concentraciones de plomo (2-4 mM) se inhibida la agregacion plaquetaria, por ello, en su trabajo concluye que otros organos o sistemas mas sensibles podrian sufrir mayores alteraciones debido a la presencia de este metal en etapas tempranas, y a menores concentraciones. Es importante recordar que el plomo tiene la capacidad de oxidar proteinas, generar indirectamente oxidation de lipidos, sustituyendo o antagonizando al calcio, o formando mercaptidos. v En el caso de los lipidos membranales la oxidation de estos en presencia de plomo puede inducir la lipoperoxidacion (Rendon-Ramirez A, 2005). Esto generaria una modification en el entorno de las proteinas que se encuentran vinculadas con la membrana, tal es el caso de los receptores, las proteinas G, la adenilato ciclasa y la protein cinasa C. la actividad de las proteinas antes mencionadas y su efecto seria analogo al del plomo. Olivares-Reyes J.A., en el 2000 propuso que todos los receptores acoplados a proteinas G tienen una estructura terciaria comun, la cual consistente en siete dominios transmembranales unidos por alternantes dominios extracelulares e intracelulares, con el extremo amino terminal extracelular y el extremo carboxilo terminal intracelular. Dada la capacidad del plomo para oxidar a grupos carboxilo, hace pensar que el plomo puede afectar a los receptores para diferentes agonistas presentes en la membrana plaquetaria. En el mismo estudio de la Dra. Banos de Mac Carthy y cols se observo que cuando se empleo como agente agregante el ADP en un plasma rico en plaquetas (PRP), en presencia de plomo, observo que existe una disminucion en la agregacion plaquetaria, esto nos conduce a suponer que el receptor de ADP y cualquier otro receptor que contenga grupos sulfhidrilos disponibles para la formation de mercaptidos los podra formar en presencia de plomo. Estos grupos de receptores deben estar libres para que se produzca una respuesta adecuada de la agregacion. El plomo como se ha menciona anteriormente puede interaccionar con las proteinas por uniones estereoespecificas, compitiendo con otros cationes de importancia biologica por ejemplo los que se encuentran en el sitio activo de algunas proteinas. Un ejemplo de esto es la calmodulina, la cual forma un complejo con el calcio para ser activada. Se sabe que esta proteina no cuenta con grupos sulfhidrilos, por lo que se ha propuesto que el plomo se puede unir en forma estereoespecifica formando un complejo Pb-calmodulina capaz de funcionar de forma semejante al complejo formado con el calcio (Figura 9). Lopez-Miranda A., en 1994 propuso que el plomo se puede a unir de manera estereoespecifica con la calmodulina, teniendo mayor afinidad que el calcio con la calmodulina observando asi una mayor actividad en el complejo Pb-calmodulina. Figura 9. Agregacion plaquetaria inducida por los agonistas ADP y Adrenalina ® Sitios posibles de accion del plomo durante la intoxicacion Los canales ionicos de la membrana celular representan uno de los blancos moleculares de mayor importancia para el plomo, ya que de ellos depende el funcionamiento celular coordinado y podrian ser el origen de varios de los trastornos celulares presentes en las intoxicaciones por plomo. Este metal afecta la activacion, conductancia y regulacion de distintos canales ionicos de manera directa o indirecta, siendo los canales de calcio y potasio dos de los mas afectados (Garza A. y cols, 2005). CONCLUSIONES Despues de haber estudiado las diferentes bibliografias consultadas y comparado la information obtenida, se llego a las siguientes conclusiones: 1) El plomo puede interferir en la plaqueta por varios mecanismos, ya sea bloqueando los receptores, compitiendo con el calcio u oxidando grupos carboxilo, ya que la plaqueta posee en su estructura sitios especificos donde puede actuar este metal. 2) El calcio juega un papel importante en la activation de la plaqueta pues regula las respuestas celulares a traves de vias efectoras, incluyendo la activation de cinasas dependientes de Ca2+/calmodulina, PLA2, PLC y Proteina cinasa C. 3) Si bien a bajas dosis de plomo (1 mM) existe cierto riesgo de provocar lesiones cardiovasculares, aterosclerosis e hipertension in vivo y vasoconstriction in vitro, de igual manera, a concentraciones mas altas (2-4 mM) inhibe la agregacion plaquetaria, teniendo como consecuencia desordenes en el proceso de la hemostasia. B1BLIOGRAFIA - Albert L. 2004. Plomo en: Toxicologia ambiental. Ed Universidad Autonoma Ciudad Juarez. Ciudad Juarez Chihuahua, Mexico. 217-239 - Alonso A., Flores J., Garza T., Halffter G. 1996. Receptores, proteinas y segundos mensajeros. Mexico D. F. Segunda Edition. - Banos de M., Lopez P., De la Pena A. 1992. Efecto del plomo y cadmio sobre la agregacion plaquetaria. Instituto National de Cardiologia "Ignacio Chavez" Mexico, D.F. 62:317-324 - Berridge M.1987. Inositol triphosphate and diacylglycerol: Two interacting second messengers. Annu Rev Biochem 56: 159-162 - Bobadilla L. 1985.Papel de las plaquetas y de la cascada de la coagulacion en los cambios Hemodinamicos producidos durante la embolia pulmonar- experimental en conejos. Tesis para obtener el titulo de maestro en ciencias en la especialidad de Farmacologia. CINVESTAV I.P.N. Mexico, D.F. - Calderon S. 1997. Efectos del plomo sobre la salud: el plomo y la lactancia. CINVESTAV Mexico, D.F. 16: 181-188 - Cervantes C., Moreno S.1999. Contamination Ambiental por metales pesados: Impacto en los seres vivos. Mexico, D. F. primera edition. - Cordova A., Ferrer R., Munoz M.E., Villaverde C.1996 Compendio de fisiologia para ciencias de la salud. Mexico, D. F. segunda edition. - Cortez L., Tellez R., Gomez D., Hernandez A., 2003. Tendencia de los niveles de plomo en la atmosfera de la zona metropolitana de la Ciudad de Mexico. 1988-1998 en: Salud Publica de Mexico. 45 supl 2:S196-S202 - Cortina R. 1999. Efecto de la administration de Calcitriol y del incremento de calcio y de fosfato en la dieta sobre la distribution de plomo durante el crecimiento. Tesis para obtener Maestra en ciencias en la especialidad de Bioquimica. CINVESTAV. I.PN. - Chantiri P., Azamar A., Galvan R., Lozada H. 2004. Niveles de plomo en mujeres y ninos alfareros. Servicios de Salud de Veracruz - Ferrer A. 2003. Intoxication por metales pesados. Unidad de Toxicologia Clinica. Hospital Clinico Universitario. Zaragoza. http://www.cfnavarra.es/salud/anales/textos/vol26/sup1/suple8a.html - Garcia M., Coma A. 2000. Caracteristicas funcionales y estructurales de las plaquetas. Revista Cubana. 1: 132-140 .- Garza A., Chavez H., Vega R., Soto E. 2005. Mecanismos celulares y moleculares de la Neurotoxicidad por plomo. Salud Mental, Mex. 28: 48-58 - Gonzalez C., Sanin L., Romieu I., Hernandez A. 1998. Acumulacion de plomo en hueso y sus efectos en la salud. Salud Publica Mexico, D. F. 40: 359-368 - Herrero L., Silgado G., Carrizosa C. 2000. Inhibidores de la funcion plaquetaria: Fisiologia de la hemostasia. Mexico D.F. - Kroll H., Schafer 1.1989. Biochemical Mechanisms of platelet Activation. The journal of The American Society of Hematology. 74: 1181-1195 - Lopez M. 1994. Posible participacion de la calmodulina en la fisiopatologia de la intoxication por plomo. Tesis para obtener el grado de maestro en ciencias. CINVESTAV. I.P.N. - Maldonado V. 1997. Efectos de diferentes concentraciones de Calcio en la Dieta durante la lactancia sobre la distribution del calcio y plomo en ratas expuestas cronicamente a plomo. Tesis para obtener el grado de Doctorado en ciencias en la especialidad en Toxicologia. Mex. CINVESTAV. I.P.N. - Martinez M., Quintana G. 1996. Bases fisiopatologicas y clinicas de las enfermedades hemorragicas y tromboticas. Mex. Primera edition - Matte T.2003. Efectos del plomo en la salud de la ninez en: Salud Publica de Mexico.45 supl 2:S220-S224 - Monteiro M., O'Connor J., Martinez M. 2001. La citometria de flujo en el analisis de las plaquetas: Aspectos estructurales y funcionales de las plaquetas. Revista de diagnostico biologico, Madrid. 50:111-136 - Mckenzie B.2000. Hematologia Clinica, Manual moderno, segunda edition - Morante A. 2001. el plomo y la salud humana, Mexico D.F. - Navarro M. 2004, Proteinas de los cuerpos de inclusion y la susceptibilidad renal hacia la intoxication con plomo. Tesis para obtener el grado de Doctora en ciencias en la especialidad de Bioquimica. CINVESTAV. I.P.N. - Needleman H. 2004. Lead Poisoning. Annu Rev Med. 55: 209-222 - Neocoechea continua A.,Escalante A., Navarro R. 1998. Programa de actualization para cardiologia biologia molecular en enfermedades cardiovasculares. Mexico,D.F. - Perez R., Castillo H„ Gortazar G., Allvarez F„ Douglas P., Diaz R.1997. Participation plaquetaria en la Hemostasia primaria. Revista Cubana de Investigation Biomedicas; 16: 180-187 - Quintanar E.1996. Mecanismos de incorporation de plomo en eritrocitos Humanos. Tesis para obtener el grado de maestra en ciencias en la especialidad en Bioquimica. CINVESTAV I.P.N. - Quintana G. 2002. Actualidades en Hemostasia: Nuevos conceptos en fisiologia de la Coagulacion. Gaceta Medica Mex. 138: 47-51 - Raisman S., Gonzalez A. 2004. Receptores: Proteinas G. Universidad nacional del Noreste. Republica de Argentina. http://fai.unne.edu.ar/biologia/celulamit/gp.htm - Rendon R. 1998. Protection de la enzima deshidratasa del acido 5aminolevulinico por la vitamina E durante el estres oxidativo inducido por el plomo en el eritrocito de rata. Tesis de Maestria. CINVESTAV-IPN. Mexico - Rendon R. 2005. El dano oxidativo y la respuesta antioxidante durante la intoxication con plomo en una poblacion expuesta y los efectos del tratamiento' con antioxidantes. Tesis para obtener el grado de Doctora en ciencias en la especialidad de Bioquimica. CINVESTAV. I.P.N. - Ruiz-Arguelles G.J. 2004. Fundamentos de Hematologia. Mexico; tercera edition. - Vazquez B., E., Maldonado M., Videgaray O., Moreno S., 2002. Intoxication por plomo. Reporte de un caso y revision de la literatura en: Anales Medicos de la Asociacion Medica del Hospital ABC. 47 (1):33-37.