HER2/CEN 17 Dual CISH detection kit* Kit HER2/CEN 17 Dual CISH
Anuncio

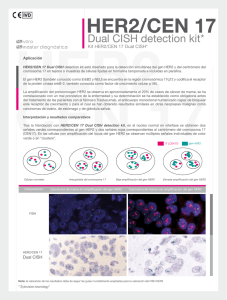
–– Avda. Conocimiento, 100 P.T. Ciencias de la Salud 18016 Granada Fax: 958.27.14.34 Telf.: 958.27.14.49 www.masterdiagnostica.com HER2/CEN 17 Dual CISH detection kit* Kit HER2/CEN 17 Dual CISH* Kit completo para la determinación del estado de amplificación del gen HER2 mediante hibridación in situ cromogénica *(Zytovision technology) DESCRIPCIÓN: Este kit contiene reactivos para llevar a cabo de forma manual o semiautomática, la técnica de hibridación in situ cromogénica (CISH) sobre secciones de tejidos humanos fijados en formalina tamponada e incluidos en parafina para determinar el estado del gen HER2 en relación con el centrómero del cromosoma 17. Este kit contiene reactivos suficientes para la realización de 5 o 20 determinaciones siguiendo estrictamente el protocolo recomendado. Presentación : La referencia/presentación general para este Kit es: MAD-001896QK-MP-A semiautomatizado 5 test MAD-001896QK-A semiautomatizado 20 test MAD-001896QK-MP manual 5 test MAD-001896QK manual 20 test Esta referencia es para presentación en envases de Polietileno de Baja Densidad (LDPE) con gotero. En caso de que el usuario desee otro tipo de presentaciones (referencias/volúmenes diferentes) deberá contactar con el proveedor. Uso Previsto : Diagnóstico in vitro en la especie humana Condiciones de almacenamiento : Frigorífico entre 2 y 8º C. Periodo de validez : El envase una vez abierto puede conservarse hasta la fecha de caducidad del reactivo señalada en la etiqueta. Si el reactivo ha sido almacenado en otras condiciones a las señaladas en este documento el usuario deberá chequear previamente su correcto funcionamiento teniendo en cuenta que la garantía del producto ya no es válida. Instrucciones especiales de manipulación: Estos reactivos están especialmente diseñados para su manejo en los inmunoteñidores LabVision Autostainer 480 y 780. Advertencias y precauciones: 1) El producto solo debe ser manejado por usuarios entrenados y en laboratorios autorizados. Para su manejo en investigación existen otras presentaciones más idóneas. 2) Téngase en cuenta que la última responsabilidad en la optimización e interpretación de las hibridaciones cromogénicas practicadas corresponde al facultativo responsable y los técnicos que emplean el kit y que, asimismo, este conjunto de reactivos no es más que una herramienta útil para la interpretación de los hallazgos morfológicos de cada caso en conjunción con otros tests diagnósticos y los pertinentes datos clínicos del paciente. 3) El reactivo contiene azida sódica (NaN3) como conservante. Aunque este producto es altamente tóxico y si se mezcla con agua o ácidos, principalmente en presencia de metales, existe peligro de explosión, estos riesgos están minimizados al máximo cuando se emplea a concentraciones inferiores al 0,05% como ocurre en este caso. No obstante para el manejo de este reactivo deben tomarse las siguientes precauciones: a) Uso de guantes y del equipo de protección establecido para las técnicas de hibridación e inmunohistoquímicas del laboratorio así como estricto respeto de las prácticas generales de seguridad existentes en el mismo; b) No almacenar los reactivos en envases metálicos ni emplear utillaje de esta naturaleza para su manejo; c) Almacenar los residuos para su eliminación reglada en contenedores apropiados según la normativa vigente en cada laboratorio. Nunca arrojarlos por el desagüe. Página 1 de 7 MAD-001896QK ESPECIFICIDAD El HER2 también conocido como receptor del factor de crecimiento epidérmico humano 2, neu, ERBB2 o CD340, es un protooncogén localizado en el cromosoma humano 17, banda 21, que codifica una glicoproteína transmembrana (p185) con actividad tirosin-cinasa. Por su interacción y semejanza con el EGFR y otros miembros de la familia de receptores de los factores de crecimiento epidérmicos, HER2 interviene en la diferenciación de algunas líneas celulares durante la embriogénesis tras la interacción entre mesénquima-epitelio-neuroectodermo y además influye en la migración, diferenciación e interacción entre numerosas células. La sobreexpresión de HER2 ha sido demostrada en más del 20% de adenocarcinomas de diferentes localizaciones, incluyendo pulmón, útero, tracto gastrointestinal y urinario, mama y anejos cutáneos en diferentes estudios. En el caso de los cánceres de mama y estómago la sobreexpresión de esta oncoproteína, que está asociada a peor pronóstico, se relaciona con la amplificación génica y es subsidiaria de respuesta al tratamiento anti HER2 con Trastuzumab (Herceptin), el anticuerpo monoclonal humanizado capaz de bloquear este receptor de crecimiento y para cuyo efecto se han obtenido resultados similares en otras neoplasias malignas como carcinomas de ovario, de estómago y de glándula salivar. La sonda suministrada contiene polinucleótidos marcados con digoxigenina dirigidos hacia las secuencias diana del gen HER2 y polinucleótidos marcados con DNP para los satélites alfa del centrómero del cromosoma 17. La reacción puede ser visualizada utilizando anticuerpos primarios (no marcados), que son detectados mediante anticuerpos secundarios conjugados con polímeros que portan enzimas. De este modo, las reacciones enzimáticas con sus correspondientes sustratos conducen a la formación de potentes señales rojas y verdes permanentes que pueden ser visualizadas mediante microscopía de luz empleando una lente seca de 40 o 60x. APLICACIONES DIAGNÓSTICAS Y VENTAJAS: Los estudios con matrices de ADN sobre la base de la presencia de receptores hormonales y la sobreexpresión o no del gen HER2 han dividido los carcinomas de mama en 5 subtipos moleculares: luminal A (RE+, HER2-), luminal B (RE+, HER2+), HER2 positivo (RE-, HER2+), de tipo mama normal (RE+, RP+, HER2-) y de tipo basal (RE-, HER2-, EGFR+ o queratina 5/6+). Por estas razones la evaluación de HER2 se ha trasformado en una prueba imprescindible para el tratamiento de los carcinomas de mama. La mayoría de los laboratorios de América del Norte y Europa utilizan técnicas de inmunohistoquímica para determinar el estado de HER2 y en las cuales los resultados equívocos (2+) deben ser confirmados por hibridación in situ fluorescente (FISH). La inmunohistoquímica identifica la expresión de la proteína HER2 en la superficie celular mientras que el FISH determina el grado real de amplificación del gen HER2. Sin embargo tanto la inmunohistoquímica como el FISH tienen algunas limitaciones. De este modo, mientras que la inmunohistoquímica se encuentra fácilmente disponible en la mayoría de laboratorios sus resultados son susceptibles de variaciones en la metodología de obtención y la interpretación entre laboratorios. El procedimiento de FISH es un método altamente sensible y específico para la determinación de la amplificación del gen HER2 aunque, sin embargo, este método es más costoso que la inmunohistoquímica y requiere habilidades interpretativas especiales y equipos costosos de observación que no están ampliamente disponibles en los laboratorios de diagnóstico. Además, la evaluación de la morfología del tumor en FISH no es óptima, por lo que es difícil distinguir entre carcinoma invasivo y carcinoma in situ. El método de FISH también está limitado por el hecho de que la señal fluorescente se desvanece rápidamente a temperatura ambiente, por lo que es difícil conservar las preparaciones para futuras referencias. La hibridación in situ cromogénica (CISH) es un método alternativo para evaluar el estado de amplificación del gen HER2 utilizando una reacción cromogénica basado en la peroxidasa, que puede ser observado con un microscopio óptico de campo claro convencional. Como el FISH, el procedimiento CISH determina el grado real de amplificación del gen HER2. Sin embargo, y a diferencia del primero, las señales positivas pueden ser identificadas empleando el equipo estándar de cualquier laboratorio. Adicionalmente, la histopatología de la muestra puede ser evaluada al mismo tiempo y la señal no se desvanece y sigue siendo estable durante un largo período de tiempo, lo que permite el almacenamiento de las muestras a temperatura ambiente. Por todos los motivos expuestos el método de CISH tiene mayor potencial para su integración rutinaria en los laboratorios de diagnóstico que el FISH. Los pacientes con tumores que presentan una tinción 3+ en inmunohistoquímica o son FISH positivos se consideran HER2 positivos y por lo tanto son elegibles para el tratamiento con Trastuzumab, mientras que los pacientes con tumores 2+ en inmunohistoquímica deben ser evaluados para chequear la amplificación del gen HER2 por FISH o CISH a fin de determinar su elegibilidad para la terapia. También, según las últimas recomendaciones de la Sociedad Americana de Oncología Clínica y del Colegio Americano de Patólogos, el método de CISH está indicado en casos de carcinomas de mama de grado 1 de tipo ductal y lobulillar con receptores hormonales positivos, carcinomas tubulares, mucinosos, cribriformes, adenoide quísticos y triple negativos con resultados iníciales positivos 3+ en la tinción inmunohistoquímica. Si la inmunotinción ha resultado negativa en una biopsia tumoral el procedimiento de CISH puede también ser recomendado en la pieza de resección tumoral en casos de carcinoma invasivo grado 3, carcinomas invasivos con muy poca representación en la biopsia, en piezas de resección con carcinomas de alto grado distintos a los diagnosticados en la biopsia o en casos con artefactos técnicos preanalíticos. Página 2 de 7 MAD-001896QK INTERPRETACIÓN La señal de hibridación CISH para una sola copia del gen HER2 aparece como una señal distintiva en forma de punto oscuro de color verde mientras que la señal de la región centromérica del cromosoma 17 lo hace como una señal puntiforme de color rojo brillante, que puede distinguirse claramente del fondo de contraste con hematoxilina. La visualización de las señales debe realizarse con al menos un objetivo de 40x, donde se muestran como señales fácilmente visibles. No deben usarse lentes de filtro para mejorar el contraste ya que se podría distorsionar la señal de color. Para obtener señales de colores brillantes es muy conveniente aumentar la apertura del diafragma. Asegúrese además de enfocar arriba y abajo cuando hace la evaluación de un núcleo ya que las señales rojas y verdes pueden estar situados en planos diferentes. Antes de proceder a cuantificar la señal, la sección de tejido/extendido celular debe ser escaneada con un objetivo de 10x o 20x para detectar cualquier posible heterogeneidad intratumoral. En caso de heterogeneidad para la evaluación debe elegirse un área representativa del estado de amplificación. Para cuantificar numéricamente la señal deben evitarse las áreas de necrosis, la de superposición de los núcleos y los núcleos con una intensidad débil de señal. En los núcleos diploides normales sin amplificación del gen, incluso en las células del parénquima normal u otras células acompañantes, en cada núcleo serán visibles 2 señales verdes y 2 señales rojas puntiformes de contorno liso (véase la fig. 1). Debido a la mitosis, pueden ser visibles señales adicionales incluso en un pequeño porcentaje de células no neoplásicas. Ocasionalmente y debido a estar situadas por encima o por debajo del plano de corte pueden observarse núcleos con ausencia de señales en las secciones de tejido incluidas en parafina. En caso de aneuploidía del cromosoma 17 (ver fig. 2) serán visibles como múltiples puntos diversas señales rojas suplementarias específicas del centrómero del cromosoma 17. En caso de amplificación del gen HER2 (ver fig. 3) las señales verdes específicas del gen HER2 serán visibles como múltiples puntos o pequeños grupos de forma irregular. Como referencia debe utilizarse el único punto verde de las células normales presentes en la misma preparación. Además, las señales rojas de los centrómeros serán claramente visibles. En caso de alta amplificación génica un gran número de puntos verdes o grupos grandes de los mismos serán visibles en los núcleos (véase la fig.4). Como referencia debe utilizarse el único punto verde de las células normales presentes en la misma preparación. Las señales rojas centroméricas pueden estar superpuestas y podrían no ser aparentes o visibles. Fig.2. Aneuploidia del cromosoma 17 Fig.1. Células normales Fig.3. Amplificación baja del gen Fig.4. Amplificación alta del gen No obstante para la interpretación correcta de los resultados se recomienda atenerse a las últimas guías de valoración en vigor para cada tipo de tejido analizado publicadas en la literatura. Página 3 de 7 MAD-001896QK LIMITACIONES DEL REACTIVO El uso sobre tejido congelado no ha sido evaluado. TIPOS DE MUESTRA Secciones de 3 micras de espesor montadas sobre portaobjetos especiales para inmunohistoquímica y obtenidas de tejidos incluidos en parafina, preferiblemente fijados en formalina tamponada. PRINCIPIO DEL MÉTODO ANALÍTICO (hibridación in situ) La hibridación in situ (ISH) permite la detección de secuencias especificas de DNA o RNA en muestras histológicas y citológicas, sin perder los detalles morfológicos. El fundamento de la ISH está basado en la hibridación entre una secuencia de DNA o RNA marcado específicamente (sonda) y una secuencia de DNA o RNA presente en la muestra. En caso de existir complementariedad entre las secuencias se produce la hibridación, que tiene como resultado un producto híbrido. Los híbridos pueden ser fácilmente visualizados por un procedimiento de tinción inmunohistoquímica cromogénica (CISH) dirigida hacia el marcador específico de la sonda empleada. La técnica ISH es altamente sensible, específica y fácil de realizar; además, no contiene productos radioactivos. Los reactivos suministrados en este kit están perfectamente adaptados entre sí y por lo tanto, el kit constituye una herramienta de fácil uso para la realización de CISH. COMPONENTES Y REACTIVOS SUBMINISTRADOS EN EL KIT: EDTA Buffer pH8 Pepsina lista para uso Sonda HER2/CEN17 Solución de Lavado Post-Hibridación Mix de Anticuerpos Secundarios Mix de Polímeros Cromógeno Rojo Cromógeno Verde Hematoxilina de Contraste 5/20 test 5/20 test 5/20 test 5/20 test 5/20 test 5/20 test 5/20 test 5/20 test 5/20 test EQUIPAMIENTO Y MATERIAL NECESARIO PERO NO SUMINISTRADO EN EL KIT Cámara húmeda de incubación Portaobjetos tratados con silano o cargados eléctricamente Cubreobjetos Fixogum u otro producto similar Placa térmica o estufa (37ºC) Batería de desparafinado-hidratación (Xileno, etanol absoluto y a concentraciones del 80% y 70%) Tampón TBS - Tween 20 Micropipetas Microscopio óptico Página 4 de 7 MAD-001896QK PROTOCOLO TÉCNICO PARA CISH C-erb-B2 SOBRE TEJIDOS INCLUIDOS EN PARAFINA UTILIZANDO EL KIT DE DETECCIÓN DE MASTER DIAGNÓSTICA Este protocolo está recomendado para la realización de CISH sobre secciones de tejido fijado en formalina tamponada e incluido en parafina. 1. Desparafinado a. b. Incubar los portaobjetos con las secciones de tejido parafinado en la estufa a 60ºC toda la noche. Desparafinar: - Xilol 2x 10 min - Etanol absoluto 2x 5 min - Etanol 80% 5 min - Etanol 70% 5 min - Agua destilada (10 min) 2. Pretratamiento por Calor a. Colocar las preparaciones en el módulo PT en solución Tampón EDTA pH8 durante 20 min a 95ºC o sumergir las preparaciones en una jarra coplin con Tampón EDTA pH8 en un Baño de agua, 20 min a 95ºC. b. Lavar 3 veces con Tampón TBS a TA. 3. Digestión enzimática a. b. c. Aplicar 100ul de pepsina lista para uso sobre el tejido e incubar 5 min a temperatura ambiente (TA). Lavar 3 veces con Tampón TBS - Tween 20 a TA. Deshidratar las preparaciones en alcoholes crecientes: - Etanol 70 % 3 min - Etanol 80% 3 min - Etanol absoluto 3 min - Dejar secar al aire 4. Hibridación a. b. c. Aplicar 10 µl de sonda sobre el tejido. Colocar un cubreobjetos sobre la sección y sellarlos con Fixogum. Desnaturalizar la preparación en placa térmica 5 min a 80º C e incubar en cámara húmeda, 16 horas a 37º C. 5. Lavados Post – Hibridación a. Retirar el cubreobjetos sumergiendo las portas en solución de lavado post-hibridación 5min a temperatura ambiente. b. Lavar los portaobjetos en la solución de lavado precalentada, 5 min a 75º C. (Se recomienda no lavar simultáneamente más de 5-6 portas). c. Mantener los portaobjetos en TBS hasta iniciar el revelado. 6. Detección y revelado (manual o automático) a. Aplicar sobre el tejido 200 µl del bloqueante de la Peroxidasa e incubar 10 min a TA b. Lavar 3 veces en tampón TBS – Tween 20. c. Aplicar sobre el tejido 200 µl del Mix de Anticuerpos Secundarios e incubar 20 min a TA. d. Lavar 3 veces en tampón TBS – Tween 20. e. Aplicar sobre el tejido 200 µl del Mix de Polímeros e incubar 20 min a TA. f. Lavar 3 veces en tampón TBS – Tween 20. g. Aplicar sobre el tejido 200 µl del Cromógeno Rojo e incubar 10 min a TA.(se prepara mezclando 1ml de substrato con una gota de cromógeno o 200 ul de substrato con 5 ul de cromógeno) h. Lavar 3 veces en Agua Destilada Página 5 de 7 i. Aplicar sobre el tejido 200 µl del Cromógeno Verde e incubar 10 min a TA (se prepara mezclando 1ml de substrato con una gota de cromógeno o 200 ul de substrato con 5 ul de cromógeno) j. Lavar 3 veces en Agua Destilada 7. Tinción de Contraste y montaje a. b. c. d. Teñir con Hematoxilina de Contraste durante 30 seg. Azular en agua corriente 5 min. Deshidratar y aclarar 30 segundos en alcohol absoluto y 30 segundos en xileno. Montar e interpretar los resultados al microscopio. INCIDENCIAS Y RECLAMACIONES Se recomienda seguir exhaustivamente todas las indicaciones contenidas en estas instrucciones técnicas. En la tabla se exponen posibles problemas y medidas correctoras para tomar. De todas maneras, en caso de que se produzcan resultados atípicos o no esperados, incluso después de repasar todas las recomendaciones sobre el protocolo de trabajo, se ruega contacten con el delegado comercial de la zona representante de Vitro S.A. En su defecto, pueden dirigirse a Master Diagnóstica en la dirección comercial, telefónica o electrónica arriba indicada. INCIDENCIAS CAUSAS MEDIDAS A ADOPTAR Morfología pobre Tejido con exceso de digestión Reducir el tiempo de incubación en pepsina Fijación inadecuada Optimizar el tiempo de fijación; chequear la calidad del fijador y su compatibilidad con el técnicas de ISH Exceso de digestión o digestión insuficiente Optimizar el tiempo de tratamiento enzimático Temperatura inadecuada de desnaturalización y/o hibridización, de la solución de lavado post hibridización o de la sonda Chequear y ajustar la temperatura si fuese necesario Tiempo de hibridización muy corto Hibridar un mínimo de 12 horas y prolongar el tiempo si fuese necesario Incubación corta con el cromógeno Prolongar el tiempo de incubación Solución del cromógeno preparada muy temprano Preparar la solución del cromógeno inmediatamente antes de su uso Contratinción muy oscura Reducir el tiempo de incubación con la hematoxilina Soluciones de cromógenos incorrectamente preparadas Revisar detenidamente las cantidades empleadas y las recomendadas La solución del cromógeno fue expuesta a la luz directa No preparar la solución del cromógeno y ni realizar la tinción bajo luz intensa Tiempos de lavados post-tinción demasiado largos Respetar los tiempos de lavados recomendados Tiempo de contratinción muy largo Reducir el tiempo de contratinción Medio de montaje no adecuado Utilizar solo medio de montaje a base de xileno Ausencia o debilidad de las señales Señales rojas débiles Señales verdes débiles Señales verdes poco definidas o fusionadas Página 6 de 7 Tinción débil focal Tinción de fondo intensa Las secciones no fueron correctamente deshidratadas Utilizar soluciones frescas de alcohol etílico y xileno Desparafinado incompleto Utilizar soluciones frescas y verificar los tiempos de desparafinado Volumen bajo de la solución de desparafinado Asegurarse de que el volumen es suficiente para cubrir el corte entero Burbujas de aire atrapadas antes de la hibridización o durante el montaje Evitar generar burbujas Lavado insuficiente Utilizar soluciones frescas de buffers o agua desionizada o destilada cuantas veces sea necesario Las secciones se secaron durante la hibridización Utilizar cámaras de incubación húmedas y sellar bien los cubreobjetos Temperatura de lavado post hibridización muy baja Chequear y ajustar la temperatura si fuese necesario LIMITACIONES DEL REACTIVO Si se han cumplido todas las condiciones de almacenamiento y manejo en el laboratorio, este reactivo está garantizado todo el tiempo hasta su fecha de caducidad. Master Diagnóstica no es responsable de los daños, lesiones personales o pérdidas económicas en los que este reactivo pueda encontrarse implicado. BIBLIOGRAFÍA: 1. Penault-Llorca F, Bilous M, Dowsett M, Hanna W, Osamura RY, Rüschoff J, van de Vijver M. Emerging technologies for assessing HER2 amplification. Am J Clin Pathol. 2009 Oct;132(4):539-48 2. Dandachi N, Dietze O, Hauser-Kronberger C. Chromogenic in situ hybridization: a novel approach to a practical and sensitive method for the detection of HER2 oncogene in archival human breast carcinoma. Lab Invest. 2002 Aug;82(8):1007-14 3. Hanna WM, Kwok K. Chromogenic in-situ hybridization: a viable alternative to fluorescence in-situ hybridization in the HER2 testing algorithm. Mod Pathol. 2006 Apr;19(4):481-7 4. Hwang CC, Pintye M, Chang LC, Chen HY, Yeh KY, Chein HP, Lee N, Chen JR. Dual-colour chromogenic in-situ hybridization is a potential alternative to fluorescence in-situ hybridization in HER2 testing. Histopathology. 2011 Nov;59 (5):984-92 5. Lehmann-Che J, Amira-Bouhidel F, Turpin E, Antoine M, Soliman H, Legres L, Bocquet C, Bernoud R, Flandre E, Varna M, de Roquancourt A, Plassa LF, Giacchetti S, Espié M, de Bazelaire C, Cahen-Doidy L, Bourstyn E, Janin A, de Thé H, Bertheau P. Immunohistochemical and molecular analyses of HER2 status in breast cancers are highly concordant and complementary approaches. Br J Cancer. 2011 May 24;104(11):1739-46 6. Mayr D, Heim S, Weyrauch K, Zeindl-Eberhart E, Kunz A, Engel J, Kirchner T. Chromogenic in situ hybridization for Her-2/neu-oncogene in breast cancer: comparison of a new dual-colour chromogenic in situ hybridization with immunohistochemistry and fluorescence in situ hybridization. Histopathology. 2009 Dec;55(6):716-23 7. Moelans CB, de Weger RA, Van der Wall E, van Diest PJ. Current technologies for HER2 testing in breast cancer. Crit Rev Oncol Hematol. 2011 Dec;80(3):380-92 8. Schiavon BN, Jasani B, de Brot L, Vassallo J, Damascena A, Cirullo-Neto J, Ivanildo Neves J, Augusto Soares F, Gobbi H, Malagoli Rocha R. Evaluation of reliability of FISH versus brightfield dual-probe in situ hybridization (BDISH) for frontline assessment of HER2 status in breast cancer samples in a community setting: influence of poor tissue preservation. Am J Surg Pathol. 2012 Oct;36(10):1489-96 Página 7 de 7