Módulo de Instrumentación Médica
Anuncio

UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica INSTRUMENTACION MÉDICA Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 1 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica UNIDAD 1. INSTRUMENTACION DIAGNOSTICA JUSTIFICACION: Los equipos de medida y registro de bioseñales tales como electrocardiógrafos, electroencefalógrafos, electromiógrafos, tensiometros, cardiotacómetros, pulsioxímetros, termómetros, etc., se encuentran ampliamente en el ambiente hospitalario y son el soporte tecnológico para que a través de sus medidas, el especialista medico pueda emitir el diagnostico del funcionamiento de un sistema o de un órgano del cuerpo humano, para entrar a implementar un determinado tratamiento o terapia. En vista de lo anterior el ingeniero electrónico debe estar en capacidad de: • Entender el funcionamiento de tales equipos, para poder diseñarlos y calibrarlos, como también hacerles mantenimiento preventivo, correctivo y predictivo. • Diseñar y construir cualquier otro sistema de bioinstrumentación que le permita al medico e investigador biomédico tomar medidas significativas y exactas de variables biológicas no tradicionales para lograr el avance de la ciencia medica y por lo tanto el mejoramiento de la salud humana. OBJETIVO GENERAL: Estudiar las técnicas de ingeniería para el diseño de sistemas y/o equipos de instrumentación electrónica que permitan adquirir, registrar, medir, analizar y hacer procesamiento análogo o digital a cualquier bioseñal procedente del cuerpo humano. OBJETIVOS ESPECIFICOS: • Utilizar amplificadores de instrumentación y filtros activos de circuitos integrados para el procesamiento análogo de las bioseñales. • Diseñar instrumentos analogos. • Diseñar instrumentos digitales con lógica programada. • Aplicar los conceptos de instrumentación para hacer medición, registro, análisis y procesamiento de bioseñales procedentes del sistema cardiovascular: ECG (Electrocardiografía), FCG (Fonocardiografía), RC (Ritmo cardiaco). Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 2 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica BIBLIOGRAFIA: • Medical Instrumentation. Applications and Desing. Jhon G Webster. • Biomedical Transducer and Instruments. Tatsuo Togawa • Biomedical Instrumentation and Measurement. Leslie Cromwell • Introduction to Biomedical Engineering. Jhon D Enderle • Handbook Biomedical Engineering. Vol. 1. • Bioingenieria Tomo IV.Mauricio Wilches. • Sensores y Acondicionadores de señal. Ramón Pallas. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 3 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica CAPITULO 1. INTRODUCCION A LA INGENIERÍA BIOMÉDICA 1.1 QUE ES LA INGENIERÍA BIOMÉDICA La Instrumentacion Medica es una disciplina propia de la Ingeniería Biomédica. Por lo tanto, es importante que el ingeniero electrónico que incursione en esta área del conocimiento, al participar en grupos de Investigación y Desarrollo de tecnologías medicas o trabaje instalando y manteniendo estos equipos, tenga una visión general de esta área tan importante del conocimiento. Se puede entonces definir la Ingeniería Biomédica como la aplicación de las Ciencias Exactas (Física y Matemáticas) a la preservación y mejoramiento de la salud del SER HUMANO. Su propósito es contribuir al progreso de la Medicina y al mejoramiento de la salud por medio de la tecnología. Trabaja en estrecho contacto con la profesión médica y al mismo nivel jerárquico. La figura 1 muestra algunas tecnologías médicas utilizadas en el área de cirugía. Figura 1. Tecnologías médicas del área quirúrgica Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 4 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1.2 HITOS MODERNOS EN DESARROLLO DE TECNOLOGÍAS MEDICAS A continuación se mostrará cronológicamente los principales desarrollos de tecnologías biomédicas: 1895: W.K. Roentgen descubre los Rayos X (RX). Inicialmente los RX se usaron para diagnosticar fracturas y dislocaciones de huesos. Para 1930 con RX se podían visualizar prácticamente todos los órganos del cuerpo gracias al uso de sales de bario y a una gran cantidad de materiales radiopacos o de contraste. 1903: W. Einthoven, desarrolló el primer electrocardiógrafo para medir la actividad eléctrica del corazón. Aplicando descubrimientos hechos en las ciencias aplicadas (química, física, ingeniería, fisiología, microbilogía, farmacología, etc) al análisis de procesos biológicos, se inició una nueva era en las técnicas de medicina cardiovascular y mediciones eléctricas. La figura 2, muestra una estampilla alusiva al centenario del inicio de la electrocardiografía. Figura 2. Estampilla del centenario de la ECG 1927: Se introduce el primer respirador artificial en procedimientos quirúrgicos. 1939: Se desarrolló el primer bypass corazón -pulmón. 1935-1939: Se desarrolló la sulfanilamida y la penicilina disminuyéndose el principal peligro de la hospitalización en la época: infecciones. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 5 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1940: Los procedimientos médicos de alto riesgo dependen mucho más de la tecnología médica. Se desarrolló la cateterización cardiaca y la angiografía, que consiste en la introducción de una cánula a través de la vena de un brazo hasta llegar al corazón inyectando un tinte radiopaco para la visualización del pulmón y los vasos y válvulas del corazón. La figura 3 muestra el equipo para efectuar cateterismo cardiaco. Figura 3. Tecnología para efectuar cateterismo cardiaco (www.cmcv.com) 1945 adelante: Después de la II Guerra Mundial. Los avances tecnológicos fueron impulsados por la investigación en el campo militar y el objetivo de establecer habitats en el espacio y en el suelo oceánico. Como un producto de esos esfuerzos, la profesión médica se benefició pues se han estado desarrollando todos los días nuevos dispositivos, equipos y sistemas puestos al servicio de la salud. La figura 4 muestra diferentes tecnologías electrónicas aplicadas al campo medico. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 6 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 4. Tecnologías electrónicas de aplicación médica (Union Medical. USA) Los avances en la electrónica de estado sólido, han hecho posible estudiar el comportamiento de la neurona, la unidad central del sistema nervioso, así como monitorear parámetros fisiológicos, como el ECG, de pacientes en la unidad de cuidados intensivos. Nuevos desarrollos de prótesis se ha convertido en la meta de los ingenieros biomédicos para mejorar la calidad de vida del hombre. La Medicina Nuclear una consecuencia de la era atómica, surge como una poderosa solución en la detección y tratamiento de anormalidades fisiológicas tales como el cáncer. El diagnostico de ultrasonido basado en la tecnología del sonar, se ha vuelto tan aceptado ampliamente que los estudios de ultrasonido son ahora parte de la rutina de diagnóstico de muchas de las especialidades médicas. Las “partes de repuesto” para cirugía se han vuelto muy comunes. Por ejemplo, dispositivos de asistencia cardiaca, como el corazón artificial, válvulas y vasos Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 7 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica sanguíneos artificiales están disponibles para reemplazar a corazones humanos enfermos. Los adelantos en nuevos materiales han permitido el desarrollo de dispositivos médicos, como agujas, termómetros, así como los sistemas implantables de suministro de drogas. Las computadoras, se emplean para almacenar, procesar y chequear registros médicos, para monitorear el estado del paciente en la unidad de cuidados intensivos y para entregar estadísticas sofisticadas de diagnóstico de enfermedades potenciales correlacionándolas con juegos específicos de síntomas en pacientes. Al desarrollarse las aplicaciones médicas del computador, se llegó a la escanografía de Tomografía Computada (TC), que revolucionó los procedimientos de diagnostico no invasivo mediante imágenes médicas, que incluyen ahora las Imágenes de Resonancia Magnética Nuclear (RMN) y la Tomografía por Emisión de Positrones. La figura 5 muestra un equipo de tomografía computada. Figura 5. Equipo de Tomografía Computada (www.imaxe.com.ar) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 8 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1.3 OPORTUNIDADES DE INVESTIGACION Y DESARROLLO DE TECNOLOGÍAS BIOMÉDICAS Se presenta a continuación diferentes áreas de investigación y desarrollo de tecnologías biomédicas, en donde el ingeniero electrónico desarrolla un papel importante al formar parte de los equipos multidisciplinarios que se conforman para tal fin. 1.3.1 INSTRUMENTACION DE MEDIDA Es la encargada de medir, registrar y almacenar cualquier variable fisiológica de origen mecánico, hidráulico, neumático, térmico, eléctrico empleando la más depurada técnica de tratamiento de señales por procedimientos analógicos digitales (A/D). El monitor de signos vitales es el equipo más representativo dentro del campo de la instrumentacion de medida. La figura 6, muestra un monitor de signos vitales de última generación. Figura 6. Monitor de signos vitales (www.ultramedica.com.co) 1.3.2 INSTRUMENTACION DIAGNOSTICA Clasificación automática de electrocardiogramas y electroencefalogramas. El computador se emplea como un sistema que procesa las señales, las clasifica y en base a pautas preseleccionadas es capaz de suministrar un primer Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 9 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica diagnóstico, que el especialista analizará adecuadamente. La figura 7 muestra un sistema de electrocardiografía automatizada. Figura 7. Sistema de electrocardiografia automatizada (www.dremed.com) 1.3.3 INSTRUMENTACION TERAPÉUTICA Es el campo de aplicación donde más se requiere la cooperación médicoingeniero. El médico posee la idea del porqué, mientras que el ingeniero puede aportar la solución al problema. Los desarrollos van desde el tratamiento de dolores incurables mediante estimulación eléctrica y de ultrasonido, hasta las técnicas de electrocirugía, desfibrilación, láserterapia y litotricia. La figura 8 muestra un bisturí electrónico. Figura 8. Bisturí electronico (www.valleylab.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 10 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1.3.4 INSTRUMENTACION DE IMAGENES MEDICAS Tecnologías de punta en equipos de diagnóstico no invasivo de imágenes médicas, como Tomografía Computada (TC), por Emisión de Positrones (PET) y por emisión de Fotones (SPECT), Resonancia Magnética Nuclear (RMN), Ecografía. La figura 9 muestra un equipo portátil de ecografía. Figura 9. Equipo portátil de ecografía (www.sonosite.com) 1.3.5 INSTRUMENTACION PARA AYUDAS FUNCIONALES Denominada también Ingeniería de Rehabilitación, consiste en todos los desarrollos que contribuyen a suplir una función defectuosa del organismo. Desde prótesis controladas por la actividad eléctrica de los músculos hasta prótesis visuales implantadas en el cerebro, que permiten la percepción de puntos de luz y sombras para los invidentes. Esta disciplina especializada recibe el nombre de Robótica Médica. La figura 10 muestra a un discapacitado por amputacion de sus brazos con prótesis mioeléctricas de brazo. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 11 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 10. Prótesis mioeléctricas de brazos (http://weblog.mendoza.edu.ar/robotica) 1.3.6 TELEMEDICINA Es el empleo de las telecomunicaciones y de la informática (Telemática) para el diagnóstico, tratamiento y la atención médica de los pacientes. Implica el uso de la tecnología de las comunicaciones como un medio para llevar servicios médicos a lugares remotos. La figura 11 muestra la infraestructura necesaria para desarrollar telecirugías. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 12 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 11. Sistema de telecirugía de última generación (www.nextgenmd.org) 1.4 LA INGENIERÍA DEL CUERPO HUMANO Los médicos inician el estudio del cuerpo humano desde la anatomía (estudio de la estructura o las partes que lo componen), la fisiología (estudio de cómo funciona cada una de las partes) y la patología (conocimiento de las enfermedades y como afectan a cada una de las partes). En el caso de los ingenieros, es importante tener un buen conocimiento de estas materias para entrar a desarrollar tecnología para la salud. Es necesario mencionar que el cuerpo humano esta conformado por sistemas (por ejemplo, el sistema cardiovascular), que a su vez los componen órganos (por ejemplo, el corazón), que están compuestos de tejidos (por ejemplo, tejido muscular) y que los componen células (por ejemplo, neuronas, células nerviosas). Se presenta a continuación un esbozo muy general de cuales son los sistemas que componen el cuerpo humano y como están interrelacionados desde la óptica de la ingeniería. La figura 12, muestra el diagrama de bloques del cuerpo humano. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 13 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica SISTEMA SISTEMA NERVIOSO ENDOCRINO SNC SEN SALIDAS COORDINACION E INTEGRACION SISTEMA RESPIRATORIO INGESTA VENTILACION SRO I2 SISTEMA SISTEMA SISTEMA I3 GASTROINTESTINAL SGI CARDIOVASCULAR I4 RENAL SRN SCV I1 EXCRECION EXCRECION TEJIDOS SISTEMA SISTEMA LOCOMOTOR REPRODUCTOR SLM SRP Figura 12. Diagrama de bloques del cuerpo humano 1.4.1 RELACION SISTEMA CARDIOVASCULAR - TEJIDOS A través del intercambiador I1 (capilares sistémicos), el SCV suministra O2 y nutrientes a los tejidos y estos le entregan CO2 y otros productos de desecho. La figura 13 muestra el la anatomía del corazón. Figura 13. Anatomia del corazón (www.nlm.nih.gov/medlineplus/spanish) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 14 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 14, muestra el sistema cardiovascular. Las arterias están coloreadas en rojo y las venas en azul. Figura 14. Sistema cardiovascular (www.educa.aragob.es) 1.4.2 RELACION ENTRE EL SISTEMA CARDIOVASCULAR Y EL RESPIRATORIO El SCV, elimina el exceso de CO2 a través del intercambiador I2 (capilares pulmonares) y a través de I2 se recarga de O2. La figura 15 muestra la anatomía de los pulmones. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 15 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 15. Anatomia del pulmon (www.nlm.nih.gov/medlineplus/spanish) La figura 16, muestra la anatomia del sistema respiratorio. Figura 16. Anatomía del sistema respiratorio (www.nlm.nih.gov/medlineplus/spanish) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 16 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1.4.3 RELACION ENTRE EL SISTEMA CARDIOVASCULAR Y EL GASTROINTESTINAL La sangre del SCV, se abastece de nutrientes y elimina desperdicios como la bilirrubina a través del intercambiador I3 (capilares mesentéricos), que lo relacionan con el SGI, el cual posee una entrada (ingesta) y una salida (excreción). El hígado forma parte de I3. La figura 17, muestra la anatomia del sistema gastrointestinal. Figura 17. Anatomía del sistema gastrointestinal (www.nlm.nih.gov/medlineplus/spanish) 1.4.3 RELACION ENTRE EL SISTEMA CARDIOVASCULAR Y EL RENAL La sangre del SCV pasa por el intercambiador I4, compleja estructura del sistema renal (SRN), donde se regula la relación ácido-base, de regulación osmolar, de retención de ciertas sustancias y de excreción de otras. La figura 18, muestra la anatomía del riñón. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 17 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 18. Anatomia del rinon (www.nlm.nih.gov/medlineplus/spanish) 1.4.5 RELACION ENTRE EL SISTEMA CARDIOVASCULAR Y EL DE COORDINACION E INTEGRACION (SISTEMA DE CONTROL) Todos los sistemas del cuerpo son controlados en su funcionamiento por el sistema nervioso central (SNC) y por el sistema endocrino (SEN), que reciben y procesan toda la información enviada por las distintas partes para generar señales eléctricas (EEG) u hormonales que efectúan control (adrenalina) y regulación (insulina). La figura 19, muestra la anatomía del sistema nervioso. Figura 19. Anatomia del sistema nervioso (www.nlm.nih.gov/medlineplus/spanish) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 18 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 20, muestra la anatomia del sistema endocrino (glandular). Figura 20. Anatomia del sistema endocrino (www.educa.aragob.es) 1.4.6 SISTEMA REPRODUCTOR El sistema reproductor (SRP) cumple la función del mantenimiento de la especie, secundaria con respecto al mantenimiento del organismo. 1.4.7 SISTEMA LOCOMOTOR El sistema locomotor (SLM), fundamental en las funciones de búsqueda de alimento, de pareja, huida y defensa. 1.4.7 FUNCIÓN PRINCIPAL DE LA MAQUINA HUMANA Mantener vivos los tejidos, por medio de suministrarles O2, nutrientes, como también disponer los desechos sólidos, líquidos y gaseosos. 1.4.8. NIVELES DE LA ORGANIZACIÓN ESTRUCTUAL DEL CUERPO HUMANO La figura 21, muestra los niveles de organización estructural del cuerpo humano, comenzando desde el nivel químico (átomos) hasta finalizar en el nivel orgánico Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 19 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica como tal, es decir, el cuerpo humano, visto como una compleja maquina biológica. Figura 21. Niveles estructurales del cuerpo humano (www.saludmed.com/AnaFisio/OrgCuerp/OrgCuNiv.html) Como se ha visto brevemente, el cuerpo humano está diseñado con elementos de ingeniería avanzada. ¿Quién es el Gran Bioingeniero?, ¿Con que propósito nos creó?, ¿Cuidamos y valoramos nuestro cuerpo? Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 20 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 2. PRINCIPIOS DE BIOINSTRUMENTACIÓN Se denomina bioinstrumentación a la rama de la ingeniería electrónica que se dedica a medir y registrar señales de origen biológico. Cuando se diseñan sistemas de instrumentación biomédica se aplican los mismos principios y limitaciones de la instrumentación industrial. Adicionalmente, se debe tener en cuenta la anatomía y la fisiología del cuerpo humano. Así mismo, la seguridad para el paciente y el operador del equipo es el parámetro más importante a tener en cuenta, aun más que su propio funcionamiento, para ello la COMISION ELECTROTÉCNICA INTERNACIONAL (IEC), es quien regula a nivel internacional las normas que deben cumplir todos los equipos biomédicos. (Normas IEC 601.1 - 601.2) 2.1 OBJETIVOS DE LA BIOINSTRUMENTACIÓN DIAGNOSTICA Ayudar al médico y al investigador a idear formas de obtener medidas de bioseñales provenientes del ser humano vivo que sean confiables y significativas. Confiables en el sentido que la medida sea lo mas exacta posible. Por ejemplo la temperatura corporal externa, medida debajo de la axila, se considera normal cuando su nivel es de 37.5 °C. Un aumento de un grado en la temperatura se diagnostica como fiebre y en el caso de un neonato (recién nacido) esta es una condición critica, por lo tanto, si el termómetro clínico digital presenta un error de exactitud de – 1.0 °C una temperatura de 38.5 °C la mostraría como normal, cuando en realidad el bebé se encuentra es estado febril. Así mismo, las medidas deben ser significativas, para que aporten información importante al especialista medico. Por ejemplo, diseñar un sistema de bioinstrumentación para medir la permitividad eléctrica de las uñas no tiene mayor relevancia clínica. 2.2 CONDICIONES EN LA TOMA DE MEDICIONES FISIOLOGICAS Al tomar medidas de parámetros importantes del cuerpo humano, se deben tener en cuenta las siguientes condiciones: • No poner en peligro la vida del paciente: ya que se perdería la razón de ser de la bioinstrumentación, contribuir al mejoramiento de la salud. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 21 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • No someter al individuo a extremo dolor e incomodidad: Este es un principio de naturaleza bioética, por lo tanto, muchas técnicas de la instrumentación industrial no se pueden aplicar a las personas. Por las razones expuestas anteriormente, la mayoría de la medicina diagnostica ha dejado de ser invasiva, no solo para disminuir las molestias causadas al paciente, sino para conseguir mayores niveles de precisión que garanticen la certeza del diagnostico. La figura 22 muestra a un medico tomando la presión arterial no invasiva con el método tradicional de auscultación (método manual) Figura 22. Medición manual de la presión arterial La figura 23, muestra un monitor de presión arterial automático, en donde la intervención del medico en la medida es mínimo (solo colocar el brazalete). Figura 23. Monitor de presión arterial automático (www.omron.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 22 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 2.3 DIFICULTADES EN LA TOMA DE MEDICIONES FISIOLOGICAS El cuerpo humano presenta una considerable variabilidad en la medida de sus parámetros importantes debido a su gran complejidad y elevado grado de interacción entre los sistemas que lo componen. A continuación se presentan las mayores dificultades encontradas al tomar medidas fisiológicas: • Las relaciones entrada/salida no son deterministicas. Existe una relación deterministica siempre que un mismo valor de entrada produce siempre el mismo valor de salida. Por ejemplo, en un sistema físico, como un amplificador con ganancia 10, siempre que la señal de entrada sea de 100 mV, la salida será de 1 V. Esto no sucede con un paciente, mantenido en condiciones ambientales constantes al cual se le toma la presión arterial en 10 instantes diferentes, separados entre ellos en 10 minutos pues las mediciones serán diferentes en todos los casos. Entonces se requiere aplicar técnicas bioestadísticas para determinar la presión arterial. • Muchas variables fisiológicas importantes no son de fácil acceso a los instrumentos de medida. Por ejemplo medir el gasto cardiaco, definido como la cantidad de sangre que bombea el corazón hacia la arteria aorta cada minuto (lts/min), requiere de una medición invasiva mediante la introducción de un catéter en cuya punta se ubica un sensor para tal fin, lo cual implica un procedimiento de riesgo. • El elevado grado de interacción entre las variables, debido a que todos los sistemas del cuerpo se encuentran interrelacionados, hace prácticamente imposible mantener constante una variable mientras se mide la relación entre otras dos. Por ejemplo tratar de medir la presión arterial manteniendo el consumo de O2 en cero durante una hora, es imposible de llevarse a cabo, debido a que el paciente moriría. • Algunas veces es difícil identificar quienes son las variables de salida y quienes las de entrada, debido a la presencia de uno o más lazos de realimentación. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 23 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • El instrumento de medida afecta las medidas hasta el punto que no se puede representar fielmente las condiciones normales, principalmente en mediciones invasivas. 2.4 DIAGRAMA DE BLOQUES DE UN BIOINSTRUMENTO ANALOGO 2.4.1 BIOINSTRUMENTO ANALOGO Se considera que un bioinstrumento es análogo, cuando presenta la medida empleando un voltímetro o amperímetro DC, debidamente calibrado en las unidades de la bioseñal bajo estudio. La figura 23 muestra el diagrama de bloques de este tipo de tecnología biomédica. X(t) SENSOR / ADECUA DOR DE SENAL AMPLIFICADOR DE INSTRUMEN TACION FILTRADO ACTIVO PROCESAMIENTO ANALOGO ADICIONAL INDICADOR Y(t) ANALOGO Figura 23. Diagrama de bloques de un bioinstrumento analogo A continuación se describirá la función de cada uno de los componentes del bioinstrumento: • X(t): bioseñal a medir y registrar. • Sensor: dispositivo que convierte un tipo de energía en otra. Presión (mmHg) en diferencia de potencial (mV). En instrumentación electrónica la salida es una señal eléctrica (v,i,R,C,L) • Adecuador de Señal: Es necesario únicamente cuando la salida del sensor es el cambio en su R, C o L. Convierte estos cambios en diferencia de potencial proporcional. • Amplificador de Instrumentación: es un circuito integrado especializado en amplificar señales diferenciales y con unas características técnicas para rechazar el ruido de tipo eléctrico. • Filtrado Activo: se utiliza para seleccionar un determinado espectro de frecuencia de la señal y para eliminar ruidos de 60/120 Hz. • Procesamiento Análogo Adicional: Tal como derivar, para obtener la rapidez de cambio con respecto al tiempo, o integrar la señal, para obtener otra señal a partir de la original, por ejemplo a partir de la variación de un desplazamiento obtener la velocidad o viceversa. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 24 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Indicador Análogo: Convierte la información electrónica en algo inteligible para el ser humano, que pueda ser percibido por uno de sus sentidos (vista u oído). Por ejemplo si se esta midiendo temperatura la diferencia de potencial a la entrada del indicador análogo se convierte en una lectura en ºC presentada por medio de un voltímetro de aguja. Si se estudian señales de fonocardiografía, la salida debe ser audible a través de parlantes o auriculares. La figura 24 muestra un modelo comercial de un termómetro análogo, cuyo diagrama de bloques se acaba de explicar. Figura 24. Termómetro Análogo (www.autosale.es) 2.4.2 BIOINSTRUMENTO DIGITAL CON LOGICA CABLEADA Se considera que un bioinstrumento es digital con lógica cableada cuando no utiliza microcontroladores, ni microprocesadores, que son circuitos integrados programables y se presenta la información en un display de siete segmentos o en una pantalla de cristal liquido (LCD). La figura 25 muestra el diagrama de bloques de este tipo de bioinstrumentos electrónicos. Y(t) CAD DECODIFICADOR DRIVER DE DISPLAY INDICADOR DIGITAL Figura 25. Diagrama de bloques de un bioinstrumento digital con lógica cableada • Y(t): Señal análoga eléctrica debidamente tratada y que es proporcional a la señal a medir X(t). (Véase la ubicación de Y(t) en la figura 23) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 25 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • CAD: Convertidor Análogo/Digital. Convierte la información análoga a formato binario codificado, por ejemplo BCD. • Decodificador: Convierte la información binaria a formato decimal, fácil de entender para el ser humano, por ejemplo decodificador BCD. • Driver de Display: Amplifica la corriente a la salida del decodificador para manejar display de 7 segmentos LEDs o pantallas LCD. Algunas veces viene incluido en el CI del decodificador. • Indicador Digital: Display a 7 segmentos o pantallas LCD. La figura 26 muestra el plano del modulo digital de un instrumento electrónico, basado en el CAD CA3162E y el decodificador/driver CA3161E. Figura 26. Modulo digital de un instrumento (www.intersil.com) Este tipo de bioinstrumento solo se limita a presentar la lectura correspondiente a los valores de la señal que se encuentra bajo estudio. La figura 27 muestra un modelo comercial de termómetro digital básico. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 26 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 27. Termómetro electrónico digital lógica cableada (www.icespedes.com) 2.4.3 BIOINSTRUMENTO DIGITAL CON LOGICA PROGRAMADA Se considera que un bioinstrumento es digital con lógica programada cuando utiliza microcontroladores o microprocesadores, que son circuitos integrados programables y se presenta la información en un display de siete segmentos o en una pantalla de cristal liquido (LCD). Este tipo de instrumentos es mas “inteligente” que el anterior, pues mediante la programación del microcontrolador el instrumento puede avisar cuando la señal ha sobrepasado un limite superior o cuando ha disminuido por debajo de un limite inferior. Por ejemplo en el caso de termómetros clínicos, cuando la temperatura aumenta un grado centígrado por encima de 37.5 °C, suena una alarma que indica fiebre y cuando disminuye un grado por debajo de lo normal, suena una alarma indicando hipotermia. La figura 28 muestra el diagrama de bloques de este tipo de bioinstrumentos electrónicos. Y(t) CAD MICROCONTROLADOR INDICADOR DIGITAL Figura 28. Diagrama de bloques de un bioisntrumento digital con lógica programada Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 27 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Y(t): Señal análoga eléctrica debidamente tratada y que es proporcional a la señal a medir X(t). (Véase la ubicación de Y(t) en la figura 23) • CAD: Convertidor Análogo/Digital. Convierte la información análoga a formato binario codificado, por ejemplo BCD. En la mayoría de los casos este modulo esta incluido dentro del microcontrolador • Microcontrolador: Circuito Integrado programable que contiene CPU, RAM, ROM, ALU, etc. Es un computador en un chip. Permite no solo presentar la información, sino que mediante programación puede suministrar información adicional sobre el estado de la bioseñal. La figura 29 muestra el modelo de un termómetro clínico comercial. Figura 29. Termómetro clínico con microcontrolador (www.pacienteplus.com) La figura 30, muestra el diagrama de bloques de un monitor de signos vitales, empleado para medir presión arterial, temperatura, registrar la señal electrocardiográfica y a partir de esta medir el ritmo cardiaco. Figura 30. Diagrama de bloques de un monitor de signos vitales (www.ti.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 28 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Observe como se amplifica (amplificadores de instrumentacion) cada una de las señales, se filtran y entran a un Multiplexor análogo (MUX) controlado desde la CPU, para luego hacer la conversión A/D que digitaliza las señales y entran al microprocesador (CPU) o al Procesador Digital de Señales (DSP) en donde se efectúan cálculos y mediciones de las mismas para luego presentar las medidas respectivas y su variación en el tiempo en el display de cristal liquido (LCD). 2.4.4 BIOINSTRUMENTO VIRTUAL Instrumentacion virtual se refiere al uso del computador para efectuar adquisición, análisis y presentación de datos provenientes de señales. El instrumento virtual también involucra la interfaz hombre-máquina, las funciones de análisis y procesamiento de señales, las rutinas de almacenamiento de datos y la comunicación con otros equipos. Se denomina virtual, ya que el computador en si mismo no es un bioinstrumento como lo es el monitor de signos vitales, sino que se puede utilizar para cumplir las mismas funciones. En este caso, el usuario mismo es quién, a través del software, define su funcionalidad y "apariencia" y por ello se dice que "virtualizamos" el instrumento, ya que su funcionalidad puede ser definida una y otra vez por el usuario y no por el fabricante. El instrumento virtual es definido entonces como una capa de software y hardware que se le agrega a un PC en tal forma que permite a los usuarios interactuar con la computadora como si estuviesen utilizando su propio instrumento electrónico "hecho a la medida". En el instrumento virtual, el software es la clave del sistema, a diferencia del instrumento tradicional, donde la clave es el hardware. Con el sistema indicado anteriormente, se puede construir un electrocardiógrafo "personalizado", con la interfaz gráfica que se desee, agregándole inclusive más funcionalidad. Sin embargo, este mismo sistema puede también ser utilizado en la medición de los signos vitales, construyéndose así un monitor de signos vitales virtual. Es allí donde radica uno de los principales beneficios del instrumento virtual, su flexibilidad. Este instrumento virtual no sólo permite visualizar las señales, sino que a la vez permite graficar su espectro de potencia en forma simultánea, algo que no se puede hacer con un instrumento convencional. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 29 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Los tres componentes principales de un bioinstrumento son, la tarjeta de adquisición de datos, el computador mismo y el software. La figura 31 muestra el diagrama de bloques de un bioinstrumento virtual. SOFTWARE COMPUTADOR Y(t) TAD Figura 31. Diagrama de bloques de un bioinstrumento virtual • Y(t): Señal análoga eléctrica debidamente tratada y que es proporcional a la señal a medir X(t). (Véase la ubicación de Y(t) en la figura 23) • TAD: Tarjeta de adquisición de Datos. Se encarga de digitalizar las bioseñales y convertirlas al protocolo que maneja el puerto de comunicación al cual se ha conectado (RS232, USB, ETHERNET) • Computador: Se desempeña como instrumento virtual. • Software: Programa informático encargado de la adquisición, registro, análisis y procesamiento de las bioseñales. La figura 32 muestra un electrocardiograma tomado con el popular sistema de instrumentacion virtual Labview. Figura 32. Electrocardiograma tomado con Labview (www.e-dsp.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 30 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3. SEÑALES BIOMÉDICAS 3.1 DEFINICION DE SEÑAL BIOMÉDICA Una señal es una cantidad que varia en el tiempo y por lo tanto contiene información. En el cuerpo humano cada sistema genera una cantidad de señales que informan sobre el estado del mismo, normal o enfermo. Una enfermedad o defecto en un sistema causa una alteración y por lo tanto genera señales que son diferentes a las señales en estado normal. Para ilustrar, tenemos las señales ElectroCardioGráficas (ECG), que suministran información sobre el estado del sistema eléctrico del corazón. Por ejemplo, la figura 33 muestra la señal de electrocardiografía (ECG) de un paciente sano y la de la figura 34 muestra la de un paciente enfermo con taquicardia supraventricular (aumento de los latidos cardiacos por minuto). Figura 33. Señal ECG paciente sano Figura 34. Señal ECG paciente enfermo de taquicardia supraventicular Comparando la segunda señal con respecto a la primera se puede observar que los picos máximos (correspondientes al latido) se presentan con mayor frecuencia y que la pequeña onda que precede a la onda de mayor amplitud no esta presente. El cardiólogo esta entrenado para percibir estas diferencias con respecto a la señal ECG normal y con base a ello emite su diagnostico. Como las señales provenientes del cuerpo humano son de origen biológico reciben el nombre de bioseñales. Estas diferencias en la forma de las señales, se refleja en el dominio de la frecuencia al aplicar la Transformada Rápida de Fourier (FFT) para determinar su contenido espectral. Las figuras 35 y 36 muestran el espectro de frecuencias del ECG correspondientes a las señales de la figura 33 y 34 respectivamente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 31 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Obsérvese como el espectro de frecuencia de la señal ECG normal tiene un mayor contenido de armónicos que la de señal correspondiente a la taquicardia supraventricular. Figura 35. Espectro de frecuencia de la señal ECG paciente sano Figura 36. Espectro de frecuencia de la señal ECG paciente enfermo de taquicardia supraventicular Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 32 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3.2 TIPOS DE SEÑALES BIOMEDICAS A continuación se mostrará de forma breve los tipos de bioseñales más importantes del cuerpo humano y los equipos electrónicos empleados en su medición y registro. 3.2.1 SEÑALES DE BIOIMPEDANCIA La impedancia eléctrica de los tejidos, Z(t), contiene información importante sobre su composición, volumen y distribución sanguínea, actividad endocrina, actividad del sistema nervioso y mas. Se aplica al cuerpo una fuente de corriente alterna con una frecuencia en el rango de 200 Khz. a 1 Mhz, con el propósito de evitar la estimulación del sistema neuromuscular. Las amplitudes de estas corrientes sinusoidales van desde 20 µA a 20 mA, para lograr bajas densidades de corriente y evitar el recalentamiento de los tejidos, lo que cambiaría el valor de la impedancia de los mismos, ya que en condiciones normales los tejidos se encuentran a una temperatura de 37.5 °C. Se utilizan 4 electrodos, dos conectan la fuente de corriente AC (no de voltaje) e inyectan esta al tejido bajo estudio y los restantes se ubican sobre el tejido en investigación y se utilizan para medir la caída de tensión generada por la corriente y la Z(t) del tejido. La figura 37, muestra la aplicación de los electrodos en la técnica de bioimpedanciometría. Figura 37. Técnica de la bioimpedanciometría torácica (http://butler.cc.tut.fi) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 33 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 38, muestra la grafica de la Z(t) torácica, la variación de la misma con respecto al tiempo dZ(t)/dt y su correlación con la señal de ECG y la de fonocardiografía (PCG). Figura 38. Señal de bioimpedanciometría torácica Z(t) (http://butler.cc.tut.fi) Una de las aplicaciones de la técnica de bioimpedanciometría es la de medir el porcentaje de grasa corporal de un paciente, con el propósito de análisis nutricional y de obesidad. La figura 39, muestra un medidor digital de grasa corporal comercial. Figura 39. Medidor de Grasa Corporal (www.omrom.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 34 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3.2.2 SEÑALES BIOACUSTICAS Muchos fenómenos biomédicos generan señales acústicas. La medición y registro de estas suministran información acerca del fenómeno que lo produce. Por ejemplo, el flujo de sangre en el corazón o a través de las válvulas cardiacas genera sonidos típicos, cuya técnica de estudio se denomina FonoCardioGrafía (FCG). El flujo de aire a través de las vías aéreas superiores e inferiores también produce ruidos acústicos, sonidos como la tos, ronquidos y sonidos pulmonares se utilizan extensamente en medicina. La contracción muscular también produce sonidos (Fonomiografía). Ahora bien, como la energía acústica se propaga a través del medio biológico, la señal bioacústica se puede adquirir en la superficie del cuerpo utilizando transductores acústicos (micrófonos). La figura 40, muestra en la parte inferior, la señal acústica producida por la actividad del corazón correlacionada con la señal ECG, el volumen ventricular y la presión arterial. Se muestran tres sonidos, denominados S1, S2 y S3 respectivamente, producidos durante un ciclo cardiaco. Figura 40. Señal FCG (www.upload.wikimedia.org) La figura 41, muestra un sistema de instrumentacion virtual, para medir, registrar y analizar las señales de FCG. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 35 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 41. Instrumentacion virtual para adquisición y registro de FCG (www.thehealthcarenet.com) 3.2.3 SEÑALES BIOMAGNETICAS Varios órganos, como el cerebro, el corazón y los pulmones generan campos magnéticos extremadamente débiles. La medición y registro de tales campos suministra información no incluida en otras bioseñales. Por ejemplo la técnica para medir los campos magnéticos producidos por el corazón se denomina MagnetoCardioGrafía (MCG), la de los músculos se denomina MagnetoMioGrafía (MMG) y la del cerebro MagnetoEncefaloGrafía (MEG). Debido al bajo nivel de los campos biomagnéticos se deben tomar precauciones extremas en el sistema de instrumentación empleado para medir estas bioseñales, ya que el solo campo magnético terrestre es un ruido de fondo. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 36 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 42, muestra los espectros de frecuencia de las señales MCG, MMG y MEG en comparación con otros campos magnéticos. Figura 42. Señales Biomagnéticas del cuerpo humano (http://butler.cc.tut.fi) El electromagnetismo, se basa en el principio de que toda corriente eléctrica que circula por un conductor produce un campo magnético, cuya intensidad es proporcional a la intensidad de la corriente. En la figura 43, se muestra como las corrientes iónicas que producen el campo eléctrico de la actividad cardiaca (ECG Lead II), es la fuente del campo magnético cardiaco, que induce un potencial eléctrico en el transductor, que en este caso es una bobina. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 37 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 43. Origen de los campos magnéticos del corazón (http://butler.cc.tut.fi) La figura 44, muestra un equipo para adquirir las señales biomagnéticas producidas por la actividad cerebral (MEG). Figura 44. Equipo de MEG (http://biomag.uni-muenster.de) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 38 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3.2.4 SEÑALES BIOMECANICAS Incluyen todas aquellas señales que se originan de una función mecánica del cuerpo humano. Algunas de estas señales son el desplazamiento, velocidad, aceleración, fuerza, presión, flujo. El fenómeno mecánico, no se propaga, como si lo hacen los campos magnéticos, los eléctricos y las ondas acústicas. Por lo general, la medición se hace en el sitio exacto donde se origina la señal biomecánica. La figura 45 muestra la medición de la presión arterial aortica de forma no invasiva mediante el clásico brazalete. El examen de la presión arterial se usa para medir la fuerza con la que la sangre está siendo bombeada por el corazón a través de las arterias y la fuerza de éstas a medida que resisten el flujo sanguíneo. Figura 45. Medición de la presión arterial (http://healthlibrary.epnet.com) La figura 46, muestra la señal de presión ventricular, medida mediante método invasivo. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 39 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 46. Señal de la presión sanguínea ventricular (www.bme.gatech.edu) La figura 47, muestra un modelo comercial empleado para medir la presión arterial de forma no invasiva Figura 47. Monitor de presión arterial (www.somatechnology.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 40 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3.2.5 SEÑALES BIOQUIMICAS Son el resultado de mediciones químicas de los tejidos vivos o de muestras analizadas en el laboratorio químico. Por ejemplo, la medición de concentración de iones dentro y fuera de la célula, por medio de electrodos específicos para cada ion, como también la presión parcial de oxígeno (pO2) y de dióxido de carbono (pCO2) en la sangre o en el sistema respiratorio. La figura 48, muestra un modelo comercial de un glucómetro, que es un instrumento para efectuar el examen de glicemia que consiste en medir la concentración de azúcar en la sangre, para el control de la diabetes. Figura 48. Glucometro (www.sanborns.com.mx) 3.3.6 SEÑALES BIOOPTICAS Son el resultado de funciones ópticas de los sistemas biológicos que ocurren naturalmente o inducidas para medición. La oxigenación sanguínea puede estimarse midiendo la luz transmitida y reflejada por los tejidos a distintas longitudes de onda. Puede obtenerse información importante acerca del feto midiendo la fluorescencia del líquido amniótico. El desarrollo de la tecnología de la fibra óptica ha ampliado el espectro de medición de estas señales. La figura 49, muestra un modelo comercial para medir el porcentaje de glóbulos rojos en las arterias que están transportando oxigeno, a esta variable se le denomina saturación de oxigeno (SpO2) y el equipo se denomina oxímetro de pulso. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 41 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 49. Oxímetro de pulso digital (www.burtons.uk.com) 3.2.7 SEÑALES BIOELECTRICAS Su fuente son los potenciales de transmembrana celular, el cual ante ciertas condiciones puede variar para generar un potencial de acción. En mediciones sobre células aisladas, donde se utilizan microelectrodos como transductores, el potencial de acción es en sí mismo la señal biomédica. En mediciones sobre grandes grupos celulares, donde se utilizan electrodos de superficie como transductores, el campo eléctrico generado por la acción de muchas células distribuidas en las vecindades de los electrodos constituye la señal biomédica. Las más importantes y estudiadas son: • Electrocardiografía (ECG): Actividad eléctrica del corazón • Electroencefalografía (EEG): Actividad eléctrica del cerebro • Electromiografía (EMG): Actividad eléctrica de los músculos El campo eléctrico se propaga a través del medio biológico, y así el potencial puede adquirirse a distancia desde la superficie del sistema en estudio, eliminándose la necesidad de invadirlo. La señal bioeléctrica utiliza electrodos como transductores ya que la conducción eléctrica en el medio biológico es a través de iones, mientras que en el sistema de medición la conducción es Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 42 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica mediante electrones. La figura 50, muestra las señales ECG, tomadas con un electrocardiógrafo. Figura 50. Señales ECG (electronicdesign.com) La figura 51, muestra un modelo de un electrocardiógrafo digital. Figura 51. Electrocardiógrafo digital (www.tmamedica.com) La figura 52, muestra las señales EEG, tomadas con un electroencefalógrafo. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 43 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 52. Señales EEG (http://butler.cc.tut.fi) La figura 53, muestra un modelo comercial de un electroencefalógrafo. Figura 53. Electroencefalógrafo virtual (www.twistermedical.com) La figura 54, muestra una señal de EMG, tomada con un electromiógrafo virtual. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 44 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 54. Señal de EMG (www.dataq.com) La figura 55, muestra un modelo comercial de un electromiógrafo. Figura 55. Electromiógrafo virtual (www. catalogomedico.com.mx) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 45 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 3.3 CARACTERIZACION DE SEÑALES BIOMEDICAS La tabla numero uno, caracteriza las principales señales bioeléctricas del cuerpo humano, en donde se considera su rango de amplitud, el espectro de frecuencia y el sensor utilizado para medirlas. Tabla 1. Caracterización de señales bioeléctricas Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 46 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 4. AMPLIFICADORES DE BIOINSTRUMENTACIÓN Se denominan amplificadores de bioinstrumentación a los amplificadores de instrumentacion que han sido diseñados para aplicaciones médicas, tal como los INA 114, INA 331 e INA 126 fabricados por la Texas Instruments o el AD620 de Analog Device. La figura 56 muestra algunas de las aplicaciones de un amplificador de bioinstrumentación, tales como, amplificación de bioseñales, adquisición de imágenes medicas, ingeniería de rehabilitación (prótesis de mano). Figura 56. Aplicaciones medicas de un amplificador de bioinstrumentación (www.analog.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 47 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 4.1 PARAMETROS DE SELECCIÓN DE UN AMPLIFICADOR DE BIOINSTRUMENTACIÓN Un amplificador de instrumentación es un dispositivo electrónico capaz de lograr amplificaciones importantes señales diferenciales, con muy bajo ruido, con alimentación simple o doble, baja deriva térmica, bajo consumo y variación de la salida hasta los límites de la alimentación, es decir sin caída en la salida. Las bioseñales son enmascaradas por ruidos eléctricos provenientes principalmente de la red eléctrica de 60Hz y por lo tanto se hace indispensable la amplificación con estos dispositivos. Las principales características de los amplificadores de instrumentación que conforman el conjunto de parámetros de selección son las siguientes: 1) Son amplificadores diferenciales con una ganancia diferencial precisa y estable, generalmente en el rango de 1 a 1000. Su ganancia diferencial se controlada mediante un único elemento analógicos (potenciómetro resistivo) o digital (conmutadores) lo que facilita su ajuste. 2) Su ganancia en modo común debe ser muy baja respecto de la ganancia diferencial, esto es, debe ofrecer una CMRR muy alta en todo el rango de frecuencia en que opera. 3) Impedancia de los terminales de entrada muy alta para que su ganancia no se vea afectada por la impedancia de la fuente de entrada. 4) Impedancia de salida muy baja para que su ganancia no se vea afectada por la carga que se conecta a su salida. 5) Bajo nivel de la tensión de offset del amplificador y baja deriva en el tiempo y con la temperatura, a fin de poder trabajar con señales de continua muy pequeñas. 6) Ancho de banda ajustada a la que se necesita en el diseño. 7) Un factor de ruido muy próximo a la unidad, esto es, que no incremente el ruido. 8) Una razón de rechazo al rizado a la fuente de alimentación muy alto. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 48 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 4.2 AMPLIFICADOR DE BIOINSTRUMENTACIÓN INA114 La siguiente información esta tomada de la hoja de especificaciones técnicas del fabricante. (http://focus.ti.com/docs/prod/folders/print/ina114.html) • DESCRIPCION: El INA114 es un amplificador de instrumentacion de propósito general, de bajo costo y alta exactitud. Esta construido con la configuración clásica de 3 amplificadores operacionales. Su ganancia se puede ajustar desde 1 hasta 10.000 con una simple resistencia conectada externamente entre los pines 1 y 8. Cuenta con un circuito de protección de entrada para recortar tensiones mayores a +/- 40V y evitar así danos por sobre tensiones. (Esto es muy importante cuando el INA114 se utiliza en el modulo ECG de un monitor de signos vitales, en donde en la Unidad de Cuidados Intensivos, se puede aplicar al paciente un defibrilador, cuando el paciente se encuentra en paro cardiaco, y este equipo entrega picos de voltaje del orden de 1 a 3 KV que se van por los cables de electrocardiografía hacia el INA114.) • CARACTERISTICAS TECNICAS: - Bajo voltaje offset: 50µV - Baja deriva térmica: 0.25 µV/°C - Baja corriente de polarización de entrada: 2nA - Alta Relación de Rechazo en Modo Común: 115 dB mínima - Protección contra sobre voltaje de entrada: +/- 40V - Amplio rango de alimentación: +/- (2.5 a 18V) - Bajo consumo de corriente en reposo: 3 mA - Impedancia de entrada: 1012 Ω - Ruido térmico de voltaje: 11 nV/(Hz) ½ (f = 1 KHz) - Máximo voltaje de salida: +/- 13.7V Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 49 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica - Ancho de banda: 1 KHz (Ganancia = 1000), suficiente para la . amplificación de la mayoría de bioseñales en instrumentacion medica. • APLICACIONES: - Amplificador de puentes (Wheatstone y AC) - Amplificador de termocuplas - Amplificador de sensores RTD (Resistencias Dependientes de la Temperatura) - Adquisición de datos (Adecuar la señal de entrada al convertidor análogo/digital) - Instrumentacion Medica (Aplicaciones en instrumentacion diagnostica) La figura 57, muestra el circuito interno del INA114: Figura 57. Circuito interno del INA114 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 50 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 4.3 AMPLIFICADOR DE BIOINSTRUMENTACIÓN INA331 La siguiente información esta tomada de la hoja de especificaciones técnicas del fabricante. (http://focus.ti.com/docs/prod/folders/print/ina331.html) • DESCRIPCION: El INA331 es un amplificador de instrumentacion CMOS de baja potencia, de amplio rango de aplicaciones. Es de bajo costo y amplificación de bajo ruido, como también es un circuito integrado de bajo consumo que puede ser alimentado con baterías. Necesita de solo una fuente de alimentación. • CARACTERISTICAS TECNICAS: - Bajo voltaje offset: 250µV - Baja deriva térmica: 5 µV/°C - Baja corriente de polarización de entrada: 0.5pA - Alta Relación de Rechazo en Modo Común: 94 dB mínima - Rango de alimentación: +(2.5 a 5.5V) - Bajo consumo de corriente en reposo: 415 µA - Impedancia de entrada: 1013 Ω - Ruido térmico de voltaje: 46 nV/(Hz) ½ (f = 1 KHz) - Máximo voltaje de salida: +5.5V - Rango de Ganancia: 5 a 1000 - Ancho de banda: 2 MHz (Ganancia = 25) • APLICACIONES: - Amplificador de puentes (Wheatstone y AC) - Amplificador de termocuplas - Amplificador de sensores RTD (Resistencias Dependientes de la Temperatura) - Adquisición de datos (Adecuar la señal de entrada al convertidor análogo/digital) - Audio amplificación - Sistemas de telecomunicación Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 51 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica - Autotrónica - Instrumentacion Medica (Aplicaciones en instrumentacion diagnostica) La figura 57, muestra el circuito interno del INA331: Figura 57. Circuito interno del INA331 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 52 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 4.4 AMPLIFICADOR DE BIOINSTRUMENTACIÓN INA126 La siguiente información esta tomada de la hoja de especificaciones técnicas del fabricante. (http://focus.ti.com/docs/prod/folders/print/ina126.html) • DESCRIPCION: El INA126 es un amplificador de instrumentacion de precisión, bajo ruido, baja corriente de consumo, lo que lo hace ideal para instrumentos portátiles alimentados con baterías. • CARACTERISTICAS TECNICAS: - Bajo voltaje offset: 250µV - Baja deriva térmica: 3 µV/°C - Baja corriente de polarización de entrada: 10nA - Alta Relación de Rechazo en Modo Común: 94 dB mínima - Rango de alimentación: +/-(1.35 a 18V) - Bajo consumo de corriente en reposo: 175 µA - Impedancia de entrada: 109 Ω - Ruido térmico de voltaje: 35 nV/(Hz) ½ (f = 1 KHz) - Máximo voltaje de salida: +/- 17.1V - Rango de Ganancia: 5 a 10000 - Ancho de banda: 1.8 KHz (Ganancia = 500) • APLICACIONES: - Amplificador de puentes (Wheatstone y AC) - Amplificador de termocuplas - Amplificador de sensores RTD (Resistencias Dependientes de la Temperatura) - Adquisición de datos (Adecuar la señal de entrada al convertidor análogo/digital) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 53 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica - Instrumentación portátil - Instrumentacion Medica (Aplicaciones en instrumentacion diagnostica) La figura 58, muestra el circuito interno del INA126: Figura 58. Circuito interno del INA126 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 54 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 5. TERMOMETRIA CLINICA La temperatura es considerada un signo vital, es decir, el valor de esta variable es un indicador medico importante a la hora de determinar el estado de salud del paciente. Por lo tanto, es necesario desarrollar sistemas electrónicos exactos y confiables para medirla y registrarla. 5.1 TERMORREGULACION Es la capacidad del cuerpo para regular su temperatura. Los animales homeotermos tienen capacidad para regular su propia temperatura. La temperatura normal del cuerpo de una persona varía dependiendo de su sexo, su actividad reciente, el consumo de alimentos y líquidos, la hora del día y, en las mujeres, de la fase del ciclo menstrual en la que se encuentren. La temperatura corporal normal, de acuerdo con la Asociación Médica Americana (American Medical Association), puede oscilar entre 36,5 y 37,2°C. En el caso de los humanos, el control de la temperatura es increíble, ya que este no pasa más allá de los 0,6 ºC, aún sometidos a temperaturas altas (60 ºC) o relativamente bajas (12 ºC). Todo lo relacionado con la temperatura animal ha sido medido cada vez con más precisión desde 1592 con la creación del primer termómetro. 5.2 LA FIEBRE Los seres humanos tienen desarrollado mecanismos fisiológicos que les permiten tener una temperatura corporal constante. Sin embargo, el equilibrio Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 55 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica calórico de un organismo se puede perder con gran facilidad y ocasionar alteraciones como la fiebre. La fiebre es una alteración del “termostato" corporal, ubicado en el hipotálamo, que conduce a un aumento de la temperatura corporal sobre el valor normal. Éstos pueden ser causados por: Enfermedades Infecciosas Bacterianas, Lesiones Cerebrales, Golpes de Calor. Enfermedades infecciosas bacterianas: Es el caso de las bacterias que generan toxinas, que afectan al hipotálamo, aumentando la temperatura. Esto afecta a los mecanismos de ganancia de calor, los cuales se activan. Los compuestos químicos que generan aumento de temperatura son los pirógenos Lesiones cerebrales: Al practicar cirugías cerebrales se puede causar daño involuntariamente en el Hipotálamo, el cual controla la temperatura corporal. Esta alteración ocurre también por tumores que crecen en el cerebro, específicamente en el Hipotálamo, de manera que el termostato corporal se daña, desencadenando estados febriles graves. Cualquier lesión a esta importante estructura puede alterar el control de la temperatura corporal ocasionando fiebre permanente. Golpes de calor: El límite de calor que puede aumentar el humano, está relacionado con la humedad ambiental. Así, si el ambiente es seco y con viento, se pueden generar corrientes de convección, que enfrían el cuerpo. Por el contrario, si la humedad ambiental es alta, no se producen corrientes de convección y la sudoración disminuye, el cuerpo comienza a absorber calor y se genera un estado de fiebre. Esta situación se agudiza más aún si el cuerpo está sumergido en agua caliente. En el ser humano se produce una aclimatación a las temperaturas altas, así nuestra temperatura corporal puede llegar a igualar la del medio ambiente sin peligro de muerte. Los cambios físicos que conducen a esta aclimatación son: el aumento de la sudoración, el incremento del volumen plasmático y la disminución de la pérdida de sal a través del sudor. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 56 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 5.3 REACCIONES DEL CUERPO A LOS CAMBIOS TERMICOS 5.3.1 AL CALOR 36 °C: Temperatura normal del cuerpo, ésta puede oscilar entre 36-37,5 ºC 38 °C: Se produce un ligero sudor con sensación desagradable y un mareo leve. 39 °C: Pirexia, existe abundante sudor acompañado de rubor, con taquicardias y disnea. Puede surgir agotamiento. Los epilepticos y los niños pueden sufrir convulsiones llegados a este punto. 40 °C: Mareos, vértigos, deshidratación, debilidad, náuseas, vómitos, cefalea y sudor profundo. 41 °C: Urgencia. Todo lo anterior más acentuado, también puede existir confusión, alucinaciones, delirios y somnolencia. 42 °C: Además de lo anterior, el sujeto puede tener palidez o rubor. Puede llegar al coma, con hiper o hipotensión y una gran taquicardia. 43 °C: Normalmente aquí se sucede la muerte o deja como secuelas diversos daños cerebrales, se acompaña de continuas convulsiones y shock. Puede existir el paro cardiorrespiratorio. 44 °C ó superior: La muerte es casi segura, no obstante, existen personas que han llegado a soportar 46 °C. 5.3.2 AL FRIO 35 °C: Se llama hipotermia cuando es inferior a 35 °C. Se presenta temblor intenso, entumecimiento y coloración azulada/gris de la piel. 34 °C: Temblor severo, pérdida de capacidad de movimiento en los dedos, cianosis y confusión. Puede haber cambios en el comportamiento. 33 °C: Confusión moderada, adormecimiento, arreflexia, progresiva pérdida de temblor, bradicardia, disnea. El sujeto no reacciona a ciertos estímulos. 32 °C: Urgencia. Alucinaciones, delirio, gran confusión, muy adormilado pudiendo llegar incluso al coma. El temblor desaparece, el sujeto incluso puede creer que su temperatura es normal. Hay arreflexia, o los reflejos son muy débiles. 31 °C: Existe coma, es muy extraño que esté conciente. Ausencia de reflejos, bradicardia severa. Hay posibilidad de que surjan graves problemas de corazón. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 57 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 28 °C: Alteraciones graves de corazón, pueden acompañarse de apnea e incluso de aparentar o incluso estar muerto. 26-24 °C ó inferior: Aquí la muerte normalmente ocurre por alteraciones cardiorrespiratorias, no obstante, algunos pacientes han sobrevivido a bajas temperaturas aparentando estar muertos a temperaturas inferiores a 14 °C. 5.4 TERMISTORES CLÍNICOS Un Termistor NTC (Negative Temperature Coefficient) es una resistencia variable cuyo valor va decreciendo a medida que aumenta la temperatura. Son resistencias de coeficiente de temperatura negativo, constituidas por un cuerpo semiconductor cuyo coeficiente de temperatura es elevado, es decir, su conductividad crece muy rápidamente con la temperatura. Se emplean en su fabricación óxidos semiconductores de níquel, zinc, cobalto, etc. La relación entre la resistencia y la temperatura no es lineal sino exponencial, como lo muestra la figura 60. Figura 60. Relacion R Vs. T de un NTC (www.betatherm.com) La ecuación que relaciona la Resistencia con la Temperatura es la siguiente: R(T) = Ro e β (1/T – 1/To) ,(Ecuación 1), donde: • To: Temperatura inicial del rango de medida (°K), • Ro: Resistencia del termistor a la temperatura To (Ω), • β: Constante térmica (°K), Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 58 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • T: Temperatura a medir (°K), • R(T): Resistencia del termistor a la temperatura T (Ω). El sensor mas utilizado en termometría clínica es el termistor (NTC), por las siguientes razones: • Alta exactitud: esto significa errores mínimos en la medición. • Rápida respuesta térmica: Cuando varia la temperatura se obtiene rápidamente el cambio en el valor de la resistencia. • Pequeño tamaño: permite introducirlo en el canal auditivo para medir la temperatura del oído medio. • Alta resolución: pequeños cambios en la temperatura producen cambios detectables en la resistencia del sensor. Es norma en termometría clínica que los sensores tengan una resolución menor de 0.1 °C. • Alta estabilidad: su relación salida entrada es estable. • Larga vida: el paso del tiempo no lo envejecen tan rápidamente conservando los valores de sus parámetros técnicos. La figura 61muestra modelos comerciales de sensores NTC de aplicación clínica. Figura 61. Sensor térmico clínico NTC (www.advindsys.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 59 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Las siguientes son las especificaciones técnicas de sensores NTC del fabricante americano U.S.SENSOR (www.ussensor.com): Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 60 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 5.5 DISEÑO DE UN TERMOMETRO CLINICO La figura 62 muestra el diagrama de bloques del módulo de temperatura de un termómetro clínico. T NTC CIRCUITO MICROCONTROLADO R(T) ADECUADOR DE SEÑAL Vo4(T) Vo1(T) FILTRO PASABAJAS AMPLIFICADOR Vo3(T) Vo2(T) CIRCUITO DE CALIBRACION Figura 62. Modulo de temperatura de un monitor de signos vitales A continuación se describe la función de cada etapa del módulo: 5.5.1 NTC Termistor clínico (Estudiado en el numeral anterior) 5.5.2 ADECUADOR DE SEÑAL Consiste en un amplificador no inversor, en donde la salida, Vo1(T), es proporcional al producto entre la resistencia del NTC y una corriente DC menor a 100 µA. Este valor de la intensidad de la corriente garantiza que el NTC no se autocaliente por ley de Joule. Además, al NTC se le conecta una resistencia en paralelo (Rp), con el propósito de linealizar la relación Resistencia versus Temperatura del sensor. El valor de Rp en la práctica, se toma como el valor de la resistencia del NTC a la mitad del rango de temperatura medido. Por ejemplo, en el caso de termometría clínica, el rango de temperatura a medir va desde 33 °C hasta 43 °C y por lo tanto la mitad de la escala corresponde a 38 °C. Si se utilizara el sensor mencionado en el numeral 6.4 referencia PR222J2, su resistencia a 38°C, sería de 1301.1 Ω. La figura 63, muestra el circuito del adecuador de señal. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 61 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Rp I = 100 µA Figura 63. Adecuador de señal 5.5.3 AMPLIFICADOR Como la salida de la etapa anterior es negativa y está en el orden de los 100 mV, es necesario amplificar esta señal diez veces con otro amplificador inversor cuya salida sea ahora positiva, Vo2(T). La figura 64 muestra esta etapa amplificadora. Figura 64. Etapa amplificadora Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 62 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 5.5.4 CIRCUITO DE CALIBRACIÓN Consiste en un amplificador de instrumentacion (INA 114), a cuya entrada inversora se conecta Vo2(T) y a la no inversora se le conecta un divisor de voltaje basado en un potenciómetro de precisión para calibrar la temperatura mínima (33 °C). Esto se hace, colocando el NTC a 33 °C y ajustando el potenciómetro del de precisión hasta que la salida amplificador de instrumentacion, Vo3(T), sea cero. El ajuste de plena escala se hace colocando el NTC a 43 °C y se ajusta la resistencia de ganancia, Rg, del amplificador de instrumentacion hasta que la salida de este es de 5V, ya que el convertidor análogo digital dentro del microcontrolador, convierte a digital, señales análogas que varíen desde cero a 5V. La figura 65 muestra el circuito de calibración. Figura 65. Etapa de calibración 5.5.5 FILTRO PASABAJAS El espectro de la señal térmica del cuerpo humano, va desde DC hasta 5 Hz. Se emplea el filtro pasabandas con frecuencia de corte a 10 Hz y atenuación de 20 dB/década, para eliminar ruidos de 60 Hz inducidos por la red de potencia eléctrica y ruidos de 120 Hz inducidos por rectificadores de onda completa de las fuentes de alimentación. En la banda pasante del filtro Vo3(T) es igual a Vo4(T). La figura 66 muestra el circuito del filtro pasabajas. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 63 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 66. Filtro pasabajas 5.5.6 CIRCUITO MICROCONTROLADO En un monitor de signos vitales convencional, la salida del filtro pasabajas, se conecta a un convertidor análogo/digital de alta resolución (10 bits o mas) y a su vez la salida de este se conecta a la entrada de un microprocesador. Ahora bien, si el monitor de signos vitales es virtual, es decir, se utiliza un computador externo para visualizar la información y almacenarla, las señales de los signos vitales, una vez han recibido el correspondiente proceso análogo para que sus variaciones sean positivas y oscilen en el rango de 0 a 5V, se conectan a la entrada de un microcontrolador que dispone de convertidores análogo/digitales y mediante múltiplexación en el tiempo, se digitalizan para entregárselas a un puerto de comunicación del computador, que bien pudiera ser el puerto USB (Bus Serial Universal). Esto se hace mediante un circuito que convierte el formato binario puro en protocolo USB. El circuito de la figura 67 muestra la etapa microcontrolada de un termómetro clínico que entrega la información en un display LCD y que emite una alarma acústica, mediante un zumbador, cuando la temperatura del paciente es mayor a 38 °C (hipertermia) o cuando es menor a 35 °C (hipotermia), como también se encienden y apagan los diodos emisores de luz (LED) respectivos. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 64 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica MICROCONTROLADOR Vo4(T) HIPERTERMIA HIPOTERMIA NORMAL Figura 67.Etapa microcontrolada de un termómetro clínico 5.6 TERMOMETRO CLINICO COMERCIAL Con los avances de la microelectrónica, actualmente se construyen termómetros clínicos de pequeño volumen y bajo peso. La figura 68 muestra un modelo comercial. Figura 68. Termómetro clínico (www.globalsources.com) Las siguientes son las especificaciones técnicas: Key Specifications/Special Features: • Display range (Rango de medida) : 32 to 42 degrees Celsius • Accuracy (Exactitud): 0.1 degrees Celsius • Minimum scale (Resolución): 0.1 degrees Celsius • Measures orally (Medición oral) • Beeper function (Función beeper): pita cuando ha establecido la medida • Auto shut-off : Se apaga automáticamente después de 5 minutos • 1.5V battery (LR/SR-41) : Alimentación con batería Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 65 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Size: (tamaño) 122 x 17 x 10mm • LCD: 20 x 7.5mm (Dimensiones de la pantalla LCD) • Net weight (Peso neto): 9.5g 6. GENERACIÓN DE POTENCIALES BIOLECTRICOS Las señales bioeléctricas son las más estudiadas en el campo medico (ECG, EEG, EMG) y por lo tanto es importante entender los principios básicos de cómo se generan los potenciales bioeléctricos a nivel celular y como se manifiestan en el exterior del cuerpo, para adquirirlos y procesarlos electrónicamente. Estos potenciales se producen debido a la actividad electroquímica de las células conocidas como excitables pertenecientes al tejido nervioso, muscular y glandular. Se considera que una célula se encuentra en reposo, cuando no se encuentra excitada, es decir no está estimulada por ningún tipo de energía. En este caso se genera una diferencia de potencial entre el interior y el exterior, denominada potencial de reposo, debido a que no varía en el tiempo. Así mismo, una célula está excitada cuando experimenta una estimulación debido a la aplicación de una energía, que puede ser de naturaleza química, lumínica, eléctrica, magnética, mecánica, calórica, etc. En este caso, se genera una variación dinámica en el tiempo de la diferencia de potencial intercelular, a la que se le denomina potencial de acción. 6.1 GENERACIÓN DEL POTENCIAL DE REPOSO Toda célula, animal o vegetal, se caracteriza por tener una membrana semipermeable y selectiva que demarca el límite de separación entre su estructura interna y el medio que la rodea, siempre líquido. Tanto el interior de la célula, como el medio ambiente que la rodea, son soluciones electrolíticas y el sistema se caracteriza por el hecho de que en el interior de la célula se acumula potasio, mientras en el medio externo, el ion prevaleciente es el sodio. La figura 69 muestra la concentración de iones tanto en el interior como en el exterior de la célula. Ambos medios se encuentran separados por la membrana celular. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 66 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 69. Concentración de iones en las células (http://butler.cc.tut.fi) Si estas concentraciones se igualaran, la diferencia de potencial celular seria cero y esto representaría la muerte de la célula, tal como se puede observar en la figura 70. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 67 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 70. Cero potencial de reposo (http://butler.cc.tut.fi) Ahora bien, esta asimetría iónica da origen a un potencial bioeléctrico, el denominado “Potencial de Membrana” o de reposo. En general, cuando dos soluciones electrolíticas semipermeable se encuentran (membrana, separadas película, restricción, por etc.), una barrera se establece un potencial electroquímico, tal como se muestra en la figura 71. Figura 71. Potencial de reposo diferente de cero (http://butler.cc.tut.fi) La membrana celular es semipermeable, es decir, permite el flujo de algunos iones mientras impide el paso de otros, por lo tanto se considera que es selectiva. A continuación se indican las velocidades de los iones permeables: • Na+: 2 E- 8 cm/s (- permeable) • K+ : 2 E - 6 cm/s • : 4 E - 6 cm/s (+permeable) • Resto sustancias: 0 cm/s En el estudio del potencial eléctrico de una célula solo se toman en cuenta los iones con mayor permeabilidad: Na+, K+, Cl-. Los factores que intervienen en la generación del potencial de reposo son: • Gradientes de difusión • El campo eléctrico opuesto a la difusión Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 68 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • La membrana semipermeable. Como [K+]i > [K+]o se presenta un gradiente de difusión, es decir una fuerza que tiende a que la [K+]i = [K+]o y por lo tanto hace que el ion K+ tienda a desplazarse del interior al exterior de la célula. El mismo fenómeno hará que iones Cl- ingresen a la célula mientras que los de Na+ por su baja permeabilidad en reposo prácticamente no se mueven. En vista de lo anterior, el interior de la célula es mas negativo que el exterior, estableciéndose un campo eléctrico dirigido hacia el interior que tiende a inhibir el flujo de K+ y Cl-. Las fuerzas de difusión y eléctricas se oponen entre si llegándose a un estado de equilibrio entre ambas. El rango del potencial de reposo para varios tipos de células va desde -60mV a -100 mV. Cuando una célula se encuentra en estado de reposo se dice que está polarizada. A continuación se muestra la ecuación de Goldman-Hodgkin-Katz que permite calcular el potencial de reposo: Donde: • Vm = Potencial de reposo a través de la membrana • R = Constante universal de los gases [8.314 J/(mol·K)] • T = Temperatura absoluta [K] • F = Constante de Faraday [9.649 E04 C/mol] • ci,x = Concentración intracelular del ion x • co,x = Concentración extracelular del ion x • Pk, PNa, Pcl: Permeabilidades 6.2 GENERACIÓN DEL POTENCIAL DE ACCION La membrana celular se puede excitar por corrientes iónicas que la atraviesen o por algún tipo de energía aplicada externamente. El efecto en la membrana es el cambio de su permeabilidad, empezando a ser más permeable al Na+. El potencial de membrana empieza a variar, dejando de ser estático (potencial de Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 69 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica reposo), convirtiéndose en dinámico, generándose el potencial de acción, como se observa en la figura 72. Figura 72. Generación del potencial de acción El proceso en la generación del potencial de acción es el siguiente: 1. Se aplica un estímulo a la membrana celular. 2. La membrana se hace muy permeable al Na+, presentándose una avalancha desde el exterior al interior, intentando alcanzar el equilibrio de concentraciones. 3. Al mismo tiempo los iones de K+ salen de la célula, a menor velocidad. El interior llega a ser ligeramente más positivo en el interior (+20mV). 4. La avalancha de Na+ termina cuando las concentraciones han alcanzado el equilibrio 5. La membrana vuelve a ser impermeable al Na+ bloqueando el flujo de este. 6. Mediante un proceso activo denominado la bomba Na-K, los iones Na+ son expulsados rápidamente al exterior y los K+ introducidos hasta que la membrana vuelve a su estado de reposo (-80mV). La figura 73, muestra los canales iónicos y la bomba Na-K, descritos anteriormente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 70 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 73. Proceso de generación del potencial de acción (http://butler.cc.tut.fi) El proceso desde la aplicación del estímulo, cuando la célula se encuentra en reposo (-80 mV), hasta que se llega a los +20 mV se denomina despolarización. Y el proceso desde los +20 mV hasta llegar de nuevo a los -80 mV se denomina repolarización. En las células nerviosas y musculares el tiempo de repolarización es muy pequeño. En el músculo cardiaco está entre 150 y 300 ms. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 71 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El potencial de acción posee una amplitud y duración fijos, independientes de la intensidad y duración del estímulo, siempre que este supere el umbral de excitación, este comportamiento recibe el nombre de ley del todo o nada. La despolarización empieza en una parte determinada de la membrana y las corrientes iónicas que circulan al generarse un potencial de acción excitan áreas adyacentes de la célula, propagándose la excitación (despolarización). Esta excitación puede propagarse a otras células vecinas. La velocidad a la que se mueve un potencial de acción se denomina velocidad de propagación. En los nervios está en el rango de 20 a 140 m/s y en el músculo cardiaco en el rango de 0.2 a 0.4 m/s. Aunque la medida de un potencial de acción es posible, se trata de una medida difícil de tomar, pues requiere la colocación de un electrodo dentro de una célula. En diagnóstico clínico se miden y registran los efectos combinados de un número elevado de potenciales de acción empleando electrodos superficiales o de aguja insertados en un músculo, nervio o alguna parte del cerebro. De esta manera, la medida de un potencial bioeléctrico cualquiera, es el resultado de la sumatoria en el tiempo de los potenciales de acción externos de un elevado número de células: Cardiacas (ECG), Musculares (EMG), Cerebrales (EEG), etc. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 72 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 7. FUNDAMENTOS DE ELECTROCARDIOGRAFIA En este punto, ya se tienen los conceptos básicos de cómo se generan los potenciales de acciona nivel celular, que finalmente son los que producen las señales bioeléctricas, entre ellas las electrocardiográficas (ECG). Los principios de electrocardiografía que se estudian en este capitulo, muestran como se determinan las doce señales ECG, o derivaciones (según los cardiólogos), que son las que se adquieren, registran y analizan con instrumentación electrónica, que son la base de los electrocardiógrafos. 7.1 ANATOMIA DEL CORAZÓN El corazón pesa entre 7 y 15 onzas (200 a 425 gramos) y es un poco más grande que una mano cerrada. Al final de una vida larga, el corazón de una persona puede haber latido (es decir, haberse dilatado y contraído) más de 3.500 millones de veces. Cada día, el corazón medio late 100.000 veces, bombeando aproximadamente 2.000 galones (7.571 litros) de sangre. El corazón se encuentra entre los pulmones en el centro del pecho, detrás y levemente a la izquierda del esternón. Una membrana de dos capas, denominada «pericardio» envuelve el corazón como una bolsa. La capa externa del pericardio rodea el nacimiento de los principales vasos sanguíneos del corazón y está unida a la espina dorsal, al diafragma y a otras partes del cuerpo por medio de ligamentos. La capa interna del pericardio está unida al músculo cardíaco. Una capa de líquido separa las dos capas de la membrana, permitiendo que el corazón se mueva al latir a la vez que permanece unido al cuerpo. El corazón tiene cuatro cavidades. Las cavidades superiores se denominan aurícula izquierda y aurícula derecha y las cavidades inferiores se denominan ventrículo izquierdo y ventrículo derecho. Una pared muscular denominada tabique separa las aurículas izquierda y derecha y los ventrículos izquierdo y derecho. El ventrículo izquierdo es la cavidad más grande y fuerte del corazón. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 73 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Las paredes del ventrículo izquierdo tienen un grosor de sólo media pulgada, pero tienen la fuerza suficiente para impeler la sangre a través de la válvula aórtica hacia el resto del cuerpo. La figura 74, muestra la anatomía del corazón. Figura 74. Anatomía del corazón (www.texasheartinstitute.org) En la figura 74 puede observarse que el corazón posee cuatro válvulas denominadas válvulas cardiacas que controlan el flujo de sangre. Las funciones de estas son: • La válvula tricúspide controla el flujo sanguíneo entre la aurícula derecha y el ventrículo derecho. • La válvula pulmonar controla el flujo sanguíneo del ventrículo derecho a las arterias pulmonares, las cuales transportan la sangre a los pulmones para oxigenarla. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 74 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • La válvula mitral permite que la sangre rica en oxígeno proveniente de los pulmones pase de la aurícula izquierda al ventrículo izquierdo. • La válvula aórtica permite que la sangre rica en oxígeno pase del ventrículo izquierdo a la aorta, la arteria más grande del cuerpo, la cual transporta la sangre al resto del organismo. 7.2 BIOHIDRAULICA DEL CORAZÓN El corazón se puede comparar a una bomba hidráulica de 2 etapas colocadas físicamente en paralelo pero con el torrente sanguíneo circulando en serie por ambas etapas, como se muestra en la figura 75. Figura 75. El corazón desde el punto de vista hidráulico El corazón izquierdo está compuesto por la aurícula izquierda (AI), la válvula mitral (VM), el ventrículo izquierdo (VI) y la válvula aórtica (VA). (F) es el flujo total promedio de sangre (lts/min). La circulación sistémica (CS) recibe sangre que pasa por la (VA) y que ingresa a la aurícula derecha (AD). Los tejidos (T) intercambian sustancias con CS y el sistema linfático (SL) es el reingreso de líquido a la circulación general a través del corazón derecho. El corazón derecho está formado por la aurícula derecha (AD), por la válvula tricúspide (VT), por el ventrículo derecho (VD) y por la válvula pulmonar (VP). La Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 75 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica circulación pulmonar (CP) se conecta con el ambiente externo (AE) recibe la sangre que pasa VP y la devuelve a AI. 7.3 FUNCIONAMIENTO DEL SISTEMA CARDIOVASCULAR El corazón y el aparato circulatorio componen el aparato o sistema cardiovascular. El corazón actúa como una bomba que impulsa la sangre hacia los órganos, tejidos y células del organismo. La sangre suministra oxígeno y nutrientes a cada célula y recoge el dióxido de carbono y las sustancias de desecho producidas por esas células. La sangre es transportada desde el corazón al resto del cuerpo por medio de una red compleja de arterias, arteriolas y capilares y regresa al corazón por las vénulas y venas. Si se unieran todos los vasos de esta extensa red y se colocaran en línea recta, cubrirían una distancia de más de 96.500 kilómetros, lo suficiente como para circundar la tierra más de dos veces. Las arterias transportan sangre rica en oxígeno del corazón y las venas transportan sangre pobre en oxígeno al corazón. En la circulación pulmonar, sin embargo, los papeles se invierten. La arteria pulmonar es la que transporta sangre pobre en oxígeno a los pulmones y la vena pulmonar la que transporta sangre rica en oxígeno al corazón. En la figura 76, los vasos que transportan sangre rica en oxígeno aparecen en rojo y los que transportan sangre pobre en oxígeno aparecen en azul. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 76 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 76. Sistema cardiovascular (www.texasheartinstitute.org) 7.4 SISTEMA DE CONDUCCION ELECTRICO DEL CORAZON La figura 77 muestra el sistema de conducción eléctrico del corazón. Figura 77. Sistema de conducción eléctrico del corazón (www.texasheartinstitute.org) Los impulsos eléctricos generados por el músculo cardíaco (el miocardio) estimulan el latido (contracción) del corazón. Esta señal eléctrica se origina en el nódulo sinoauricular (SA) ubicado en la parte superior de la aurícula derecha. El nódulo SA también se denomina el «marcapasos natural» del corazón. Cuando Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 77 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica este marcapasos natural genera un impulso eléctrico, estimula la contracción de las aurículas. A continuación, la señal pasa por el nódulo auriculoventricular (AV). El nódulo AV detiene la señal un breve instante y la envía por las fibras musculares de los ventrículos, estimulando su contracción. Aunque el nódulo SA envía impulsos eléctricos a una velocidad determinada, la frecuencia cardiaca podría variar según las demandas físicas o el nivel de estrés o debido a factores hormonales. 7.5 GENERACIÓN DE LA SEÑAL ELECTROCARDIOGRAFICA Para que el sistema cardiovascular funcione correctamente, es necesario que las aurículas y los ventrículos funcionen sincronizados temporalmente de forma exacta. Cada potencial de acción en el corazón se origina en el punto denominado marcapasos o nódulo sinoauricular (SA). Este es un grupo de células especializadas que generan espontáneamente potenciales de acción a un ritmo regular (70 potenciales de acción/minuto). Para iniciar el latido cardiaco, el potencial de acción generado por el marcapasos se propaga en todas direcciones a lo largo de las superficies de ambas aurículas. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 78 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 78. Potenciales de acción cardiacos (http://butler.cc.tut.fi) Este frente de onda de activación de potenciales de acción viaja paralelo a la superficie de las aurículas hacia la unión de las aurículas y los ventrículos, terminando la onda en un punto cerca del centro del corazón denominado nódulo auricoventricular (AV) (50 potenciales de acción/minuto). En este punto, unas fibras nerviosas especiales, o sistema de conducción especializado compuesto por el haz de Hiz y las fibras de Purkinje actúan como retardadores (15-30 potenciales de acción/minuto) para lograr una temporización adecuada entre la acción de las aurículas y los ventrículos. Una vez los potenciales de acción atraviesan esta red de retardo, se inician los potenciales de acción en la potente musculatura de los ventrículos. El frente de onda en los ventrículos es ahora perpendicular a su superficie y se mueve desde el interior al exterior de la pared ventricular, terminando en la punta o ápice del corazón, presentándose el latido cardiaco o contracción del ventrículo izquierdo, para bombear la sangre oxigenada a toda la red arterial. Todos los potenciales de acción presentes en la actividad del sistema eléctrico del corazón se propagan por todo el cuerpo, ya que este se puede considerar como un volumen conductor de la electricidad, y con electrodos colocados en la superficie del cuerpo se pueden adquirir y registrar. La figura 79 muestra como se genera la señal ECG a partir de los potenciales de acción cardiacos. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 79 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 79. Generación de la señal ECG (http://butler.cc.tut.fi) La señal ECG esta compuesta básicamente por la onda P, el complejo QRS y la onda T. La onda P representa la despolarización de la musculatura auricular. El complejo QRS es el resultado combinado de la repolarización de las aurículas y la despolarización de los ventrículos que se producen casi simultáneamente. La onda T es la onda de repolarización ventricular, mientras que la onda U, si está presente se considera que son potenciales posteriores de los músculos ventriculares. El intervalo P-Q representa el tiempo durante el que se retrasa la onda de excitación en las fibras cerca del nódulo AV. La figura 80, muestra un electrocardiograma típico de un paciente sano. Para efectuar un diagnóstico el cardiólogo mide con detalle los intervalos de tiempo, las polaridades y las amplitudes. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 80 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 80. Señal ECG de paciente sano Se dan a continuación los valores normales de las amplitudes y tiempos del ECG normal: Amplitudes: • Onda P: 0.25mV • Onda R: 1.60mV • Onda Q: 25% de la onda R • Onda T: 0.1 a 0.5 mV Duraciones: • Intervalo P-R: 0.12 a 0.20 s • Intervalo Q-T: 0.35 a 0.44 s • Segmento S-T: 0.05 a 0.15 s • Onda P: 0.11 s • Intervalo QRS: 0.09 s 7.6 SEÑALES DE UN ELECTROCARDIOGRAMA El electrocardiograma (ECG) es un estudio de rutina que se realiza para observar la actividad eléctrica del corazón. El electrocardiograma puede suministrar mucha información sobre el corazón y su funcionamiento. Con este estudio es posible averiguar más sobre el ritmo cardíaco, el tamaño y Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 81 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica funcionamiento de las cavidades del corazón y el músculo cardíaco. El electrocardiograma de una persona sana presenta un trazado particular. Cuando se producen cambios en ese trazado, el médico puede determinar si existe un problema. Por ejemplo, durante un ataque cardíaco, la actividad eléctrica del corazón cambia y ese cambio se registra en el ECG. La figura 81, muestra el momento en que se le toma un electrocardiograma a un paciente hospitalizado. Un estudio completo de electrocardiografía contiene 12 diferentes señales provenientes de la actividad eléctrica del corazón, como se explicó anteriormente. A estas señales se les conoce en el campo medico como derivaciones ECG. Figura 81. Realización de un electrocardiograma Las corrientes iónicas, debidas a los potenciales de acción asociados a la actividad cardiaca, circulan por el tórax produciendo una distribución de potenciales superficiales, que se pueden aproximar a un dipolo de corriente situado en el hipotético centro eléctrico del corazón. La dirección y magnitud del dipolo va cambiando a lo largo del ciclo cardiaco. Su momento dipolar constituye el denominado vector cardiaco. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 82 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La señal obtenida al medir el ECG depende de la localización de los electrodos y se encuentra normalizada. Cada par de electrodos o combinaciones entre ellos se denomina derivación y el potencial obtenido entre ellos es la proyección del vector cardiaco en la dirección que definen, tal como se puede apreciar en la figura 82. Existen tres clases de derivaciones: tres bipolares, tres unipolares aumentadas y 6 precordiales, para un total de doce. La figura 82, muestra las tres derivaciones bipolares. 7.6.1 DERIVACIONES BIPOLARES Las tres primeras derivaciones que son las denominadas estándar o bipolares VI, VII y VIII, fueron introducidas por Einthoven (El padre de la electrocardiografía) en 1912. La polaridad de los electrodos se refiere a la polaridad de los terminales de entrada del amplificador de instrumentación característicos de los electrocardiógrafos, cuya señal de entrada es diferencial. LA RA VI VII RL LL VIII Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 83 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 82. Adquisición de las derivaciones bipolares En electrocardiografía al brazo derecho se le identifica como RA (Right Arm), al brazo izquierdo LA (Left Arm), a la pierna derecha RL (Rigth Leg) y a la pierna izquierda LL (Left Leg). Sobre estas extremidades se colocan los electrodos, que convierten potencionales iónicos (potenciales de acción) en potenciales electrónicos, que serán amplificados por los amplificadores de instrumentación. La pierna derecha se toma como la referencia de los biopotenciales presentes en las otras extremidades, por ello se ve conectada a tierra. Obsérvese de la figura 82 como se generan las tres derivaciones bipolares: • La derivación I (Lead I): es la diferencia de potencial entre LA y RA. Por ello LA se conecta al terminal de entrada no inversor del amplificador de instrumentacion y RA en el inversor, obteniéndose así una señal diferencial que será amplificada. VI = VLA - VRA • La derivación II (Lead II): es la diferencia de potencial entre LL y RA. Por ello LL se conecta al terminal de entrada no inversor del amplificador de instrumentacion y RA en el inversor, obteniéndose así una señal diferencial que será amplificada. VII = VLL - VRA • La derivación III (Lead III): es la diferencia de potencial entre LL y LA. Por ello LL se conecta al terminal de entrada no inversor del amplificador de instrumentacion y LA en el inversor, obteniéndose así una señal diferencial que será amplificada. VIII = VLL - VLA La figura 83, muestra el famoso triangulo de Einthoven, en donde cada derivación bipolar constituye un vector. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 84 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 83. Triángulo de Einthoven (http://library.med.utah.edu/kw/ecg) En cada una de estas derivaciones el complejo QRS de un corazón normal es positivo. Las diferencias de potencial activas (RA, LA, LL), se miden con respecto a la pierna derecha (RL), que se toma como potencial 0V, de referencia y está conectada a tierra. En cualquier caso, a partir de la relación geométrica de las derivaciones se deduce que los potenciales medidos cumplen la siguiente ecuación: VII = VI + VIII, por lo tanto, se pueden adquirir físicamente dos derivaciones y reconstruir la tercera electrónicamente o con software. De las tres derivaciones la II, produce el mayor potencial de la onda R, de acuerdo con la ecuación anterior. La figura 84, muestra las derivaciones bipolares de un paciente sano tomadas con el sistema de bioinstrumentación virtual BIOPAC RESEARCH. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 85 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 84. Derivaciones bipolares de paciente sano 7.6.2 DERIVACIONES UNIPOLARES AUMENTADAS Consisten en registrar los potenciales de los electrodos activos (RA, LA, LL) con respecto a un punto de referencia denominado terminal central de Wilson (CT). Los tres electrodos activos se conectan al CT a través de resistencias iguales. La diferencia de potencial del CT con respecto a RL es el promedio aritmético de los tres potenciales activos. A estas derivaciones se les denomina como unipolares básicas, tal como se observa en la grafica 85. VR VL F RL VF Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 86 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 85. Adquisición de las derivaciones unipolares básicas Las ecuaciones que definen las derivaciones unipolares básicas son las siguientes: • VCT = (VRA + VLA + VLL) / 3 • VR = VRA – VCT = (2VRA – VLA – VLL)/3 = – (VI + VII) /3 • VL = VLA – VCT = (2VLA – VRA – VLL)/3 = (VI – VIII) /3 • VF = VLL – VCT = (2VLL - VRA - VLA)/3 = (VII + VIII) /3 Las ecuaciones anteriores demuestran que las derivaciones unipolares están en función de las bipolares, por lo tanto, adquiriendo físicamente las derivaciones bipolares I y II, se pueden reconstruir la bipolar III y las tres unipolares. En la práctica no se utilizan en electrocardiografía las unipolares básicas sino las aumentadas que en amplitud son 50% mayores. Las unipolares aumentadas son aVR, aVL, aVF. Para las aumentadas se abre el circuito entre la extremidad que se está midiendo y el CT, como se muestra en la figura 86. + + - - + - Figura 86. Adquisición de las derivaciones unipolares aumentadas Las señales diferenciales mostradas en la figura 86 son las que se amplifican con amplificadores de instrumentacion. Para cada caso, el potencial en CT, es el promedio entre dos potenciales activos únicamente. Por ejemplo en el caso de aVR, equivaldrá a (aVL + aVF) / 2. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 87 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Haciendo los cálculos se obtiene: • VR = VRA – VCT = (2VRA – VLA – VLL)/2 = – (VI + VII) /2 • VL = VLA – VCT = (2VLA – VRA – VLL)/2 = (VI – VIII) /2 • VF = VLL – VCT = (2VLL - VRA - VLA)/2 = (VII + VIII) /2 Comparando las ecuaciones de las unipolares aumentas con respecto a las unipolares básicas, se concluye que las primeras, son mayores a las últimas en un factor de 3/2, lo que equivale a un aumento del 50%, lo que las hace más fáciles de amplificar y por ello son las que finalmente se emplean en electrocardiografía. La figura 87, muestra las derivaciones unipolares aumentadas de un paciente sano tomadas con el sistema de bioinstrumentación virtual BIOPAC RESEARCH. Figura 87. Derivaciones unipolares aumentadas de un paciente sano 7.6.3 DERIVACIONES PRECORDIALES Se obtienen colocando los electrodos en varias posiciones anatómicamente definidas sobre la pared del pecho. El potencial entre los electrodos individuales Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 88 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica y el CT es el ECG para las derivaciones precordiales, tal como se aprecia en la figura 88. CT V1 V2 V3 V4 V5 V6 Figura 88. Adquisición de las derivaciones precordiales La figura 89, muestra la distribución de las derivaciones ECG en los tres planos espaciales empleados en anatomía. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 89 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 89. Distribución espacial de las derivaciones ECG 8. INSTRUMENTACION ELECTRÓNICA PARA ELECTROCARDIOGRAFIA En este punto del estudio de las señales electrocardiográficas, ya se ha analizado cómo las ha generado el corazón y cómo se colocan los electrodos para ser adquiridas. Ahora, es importante conocer los circuitos electrónicos que utilizan los electrocardiógrafos, para adquirirlas, procesarlas, registrarlas y almacenarlas, que se fundamentan principalmente en Amplificadores de Instrumentación (AI) con características especiales, para amplificar la señal ECG de unos pocos mV y atenuar drásticamente los ruidos de 60 Hz (voltajes de modo común) que enmascaran la señal. 8.1 AMPLIFICADOR ELECTROCARDIOGRAFICO DE UNA DERIVACION Es un circuito electrónico, que permite adquirir una derivación bipolar, como se muestra en la figura 90. Figura 90. Amplificador ECG de una sola derivación (www.ti.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 90 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El circuito de la figura fue diseñado por la Texas Instruments, los fabricantes de los amplicadores de instrumentacion INAXXX. Está propuesto para instrumentos portátiles en donde se requiere que todos los elementos del circuito sean de bajo consumo de energía. Una aplicación práctica del circuito se encuentra en los equipos HOLTER ECG, que son instrumentos para monitorear el ritmo cardiaco durante 24 o 48 horas continuas con el propósito de identificación de arritmias cardiacas. A continuación se presenta una explicación detallada de la función de cada uno de los circuitos que componen todo el sistema: • INA326: Amplificador de instrumentacion con ganancia calibrada en 5. Se utiliza esta baja ganancia en la primera etapa, para evitar la saturación del amplificador debida a los potenciales de semicelda que se generan en la interfase electrodo piel, que están en el orden de las décimas de voltio y en magnitud son mayores que las mismas señales ECG. Las resistencias de 390 KΩ, en los terminales de entrada tienen la función de limitar corrientes provenientes de la red eléctrica de 60 Hz, producidas por fallas de otros equipos eléctricos con los cuales el paciente pudiera entrar en contacto. Las dos resistencias de 40 KΩ conectadas en serie, junto con la de 200 KΩ conectada al pin de referencia determinan la ganancia diferencial del amplicador como lo muestra la figura 91. Figura 91. Distribución de pines y ganancia del INA 326 El capacitor C2 elimina el ruido térmico producido por R2. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 91 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Amplificador Operacional A1: Trabaja como un buffer análogo o seguidor de señal. Su función es independizar los circuitos de entrada del INA326 del circuito de pierna derecha basado en el amplificador operacional A2. • Amplificador Operacional A2: Es un amplificador inversor. Tiene básicamente dos funciones. La primera, aislar eléctricamente la pierna derecha (RL) de la tierra electrónica, para evitar que descargas provenientes de la red eléctrica, que se encuentra aterrizada, circulen a través del cuerpo del paciente, pudiendo causarle fibrilación ventricular, ya que tan solo una corriente de 60 µA de 60 Hz, que pase a través del miocardio la puede producir. La segunda función, es realimentar la pierna derecha con el ruido inducido por la red eléctrica de 60 Hz, en las extremidades activas, con el propósito de atenuar drásticamente esta diferencia de potencial entre RA y RL, LA y RL, LL y RL, de tal manera que el voltaje en modo común a la entrada del amplificador de instrumentacion sea mínimo y la relación señal/ruido a la salida de este sea el máximo posible. • Amplificador Operacional A3: Cumple también dos funciones. La primera servir como amplificador inversor con ganancia 200. Tradicionalmente, la ganancia total de un amplificador ECG debe ser de 1000, por ello, la ganancia del INA326 multiplicada por la del amplificador operacional A3, cumple con esta condición. Es inversor, ya que aunque se esta adquiriendo la derivación I, la conexión de los electrodos a los terminales del amplificador de instrumentacion se encuentra invertida. La segunda función, es la de servir como filtro pasabajas, con atenuación de 20 dB/década y frecuencia de corte de 106,1 Hz. • Amplificador Operacional A4: Es un circuito integrador, que trabaja como filtro pasaaltas con atenuación de 20 dB/década y frecuencia de corte de 0,05 Hz. • REF3125 Y A5: Entregan un voltaje de referencia de precisión de 2.5 V, para los amplificadores y el convertidor análogo digital. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 92 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • ADS8321: Convertidor Análogo/Digital tecnología SAR de 16 bits y 100 Kmuestras/segundo. Este circuito entrega la señal ECG debidamente digitalizada para conectársela a un pin de entrada de un microprocesador, microcontrolador o un procesador digital de señales (DSP), para almacenarse, procesarse y obtener información de la señal. 8.2 AMPLIFICADOR ELECTROCARDIOGRAFICO DE TRES DERIVACIONES La figura 92, muestra los circuitos electrónicos para adquirir las tres derivaciones bipolares. VI VIII CT VII D Figura 92. Amplificador ECG de tres derivaciones bipolares (www.analog.com) A continuación se presenta una explicación detallada de la función de cada uno de los circuitos que componen todo el sistema: • Circuito Protección de Paciente: Consiste en resistencias que oscilan entre los 100 y 400 KΩ, conectadas entre los electrodos y los terminales Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 93 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica de entrada de los amplificadores para limitar corrientes de descarga eléctrica de 60 Hz, como se explicó anteriormente. • Circuito de Aislamiento: Son básicamente amplificadores de aislamiento, como el ISO122 de la Texas Instruments, mostrado en la figura 93. Estos amplificadores son de ganancia uno, pero tienen aislada eléctricamente los circuitos de entrada y de salida, por lo tanto brindan seguridad al paciente, ya que no permiten circulación de corrientes de fallo provenientes del equipo electrónico hacia el paciente. Figura 93. Amplificador de aislamiento ISO122 (www.ti.com) • Amplificadores Buffer: Amplificadores seguidores de señal (A,B,C) con ganancia uno para independizar los terminales de entrada de los amplificadores de instrumentacion de los de salida de los amplificadores de aislamiento. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 94 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Circuito Estrella: Compuesto por tres resistencias de 100 KΩ, cuyo punto común es el terminal central de Wilson (CT). La tensión en este punto con respecto a tierra es la señal de entrada del circuito de pierna derecha RL. • Circuito de Pierna Derecha: Basado en el amplificador operacional D, cuya función ya fue explicada en el numeral anterior. • Amplificadores de Instrumentación: (IN-AMP#1, 2, 3), amplifican las derivaciones I, II y III respectivamente, con ganancias que pueden oscilar entre 5 y 50. • Filtros Pasaaltas: Con frecuencias de corte de 0,03 Hz a 0,5 Hz, de acuerdo a la aplicación. Por ejemplo para estudios completos de ECG, se utiliza 0,05 Hz y para solo monitoreo de la señal ECG y medición de ritmo cardiaco se emplea 0,5 Hz. • Filtros Pasabajas: Conectados a la salida de los pasaaltas. Para estudios completos de ECG, se utiliza 100 Hz y para solo monitoreo de la señal ECG y medición de ritmo cardiaco se emplea 40 Hz. 8.3 AMPLIFICADOR ELECTROCARDIOGRAFICO DE SIETE DERIVACIONES La figura 94, muestra el circuito electrónico para adquirir directamente las tres derivaciones bipolares, las tres unipolares aumentadas y una precordial. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 95 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 94. Amplificador ECG de siete derivaciones El propósito de las resistencias de las entradas, los amplificadores buffer y el circuito de pierna derecha ya fueron explicados anteriormente. A continuación se presenta una explicación detallada de la función de los circuitos que componen todo el sistema: • Red de Wilson: Cumple dos funciones. La primera es generar la tensión del terminal central de Wilson, por medio de las tres resistencias conectadas en estrella desde las extremidades activas (RA, LA, LL), para excitar el circuito de pierna derecha y el amplificador de la derivación precordial. La segunda es generar las tensiones promedio para las derivaciones unipolares aumentadas, que alimentaran los terminales inversores de los amplificadores de instrumentación. • Amplificadores Diferenciales: Amplifican las señales diferenciales de cada una de las siete derivaciones propuesta. Pueden reemplazarse también por amplificadores de instrumentacion convencionales. 8.4 AMPLIFICADOR ELECTROCARDIOGRAFICO DE DOCE DERIVACIONES La figura 95 presenta el diagrama de bloques del procesamiento análogo y adquisición digital un electrocardiógrafo digital de última generación. Los bloques marcados en amarillo ya fueron analizados en los numerales inmediatamente anteriores. Las funciones de los demás bloques funcionales son las siguientes: QRS QRS Detector Detec tor CT Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 96 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 95. Etapa análoga y adquisición digital de un electrocardiógrafo • 12 60 Hz Notch Filtres: Consiste en 12 filtros analogos rechaza banda de banda angosta con frecuencia de resonancia de 60 Hz y factor de calidad (Q) igual a 15. Su función es eliminar el ruido inducido en los electrodos por la red eléctrica de potencia. Un filtro por cada derivación. • Program Gain Amplifiers: Consiste en 12 amplificadores de ganancia programable, controlados digitalmente desde el microprocesador, para ajustar automáticamente la ganancia por cada derivación. • Analog Multiplexer: Multiplexor analogo de 12 entradas. Su función es tomar muestras de cada derivación para ser digitalizada. La frecuencia de muestreo debe ser mayor a 200 muestras/segundo, para cumplir con la condición de la frecuencia de muestreo mínima de Nyquist y poder reconstruir fielmente las señales. • Sample/Hold: Consiste en un circuito que toma la muestra entregada por el multiplexor y la mantiene el suficiente tiempo a la entrada del convertidor Análogo/Digital para que este efectúe su función. • 12 bit A/D Convertidor: Convertidor Análogo/Digital de 12 bits con salida serial. Su función es convertir cada muestra de las derivaciones en código digital, para entregarlo a la Unidad Central de Proceso. • Opto or Data Coupler: Circuito de aislamiento alvánico (eléctrico) entre la instrumentacion electrónica conectada al paciente y el sistema que efectuara el procesamiento digital de las señales adquiridas, con el propósito de brindar seguridad electromédica. Las funciones de Simple (Muestreo), Hold (Retención) y conversión A/D, se encuentran disponibles en un solo circuito integrado, tal como el DSP101 de la Texas Instruments. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 97 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 96, muestra la etapa de procesamiento digital de las señales ECG y su etapa de presentación de la información a partir de que las señales se han digitalizado. Figura 96. Etapa de procesamiento digital de un electrocardiógrafo Una vez se han adquirido las derivaciones ECG y se han logrado digitalizar, estas se introducen a un Procesador Digital de Señales (DSP), un microprocesador, un microcontrolador o un computador. A partir del software, se aplican entonces filtros digitales (FIR o IIR), para eliminar el ruido de 60 Hz, y el Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 98 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica ruido producido por los músculos al moverse el paciente, como también, se puede calcular el ritmo cardiaco. Incluso se puede implementar un algoritmo de medición e interpretación automática del ECG, que reemplace el estudio que manualmente hacen los cardiólogos. Las señales una vez se han procesado digitalmente se convierten ahora a formato análogo a través de convertidores D/A, para imprimirlas en una impresora de papel térmico o presentarlas en un display digital LCD. 8.5 ESPECIFICACIONES TECNICAS DE UN ELECTROCARDIOGRAFO La figura 97, muestra a un electrocardiógrafo digital de ultima generación. Figura 97. Electrocardiógrafo comercial (http://www.stelectromedicina.es) Las especificaciones técnicas y su respectiva interpretación son las siguientes: • 12 derivaciones Estándar: DI, DII, DIII, aVR, aVL, aVF, V1, V2, V3, V4, V5, V6 • Rechazo de modo común: > 90 dB. Se refiere a que la relación entre la ganancia diferencial (amplificación de señales ECG) y la ganancia en modo común (amplificación de ruido 60 Hz), multiplicado por 20 de los canales de electrocardiografía. CMRR = 20 log (Gd/Gmc) (dB). • Respuesta en frecuencia: 0,05 - 150 Hz (-3dB) sin filtros. Ancho de banda normalizado para estudios completos de ECG. • Filtros digitales: Para eliminar interferencias de la red, muscular y antidesplazamiento Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 99 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Protección contra desfibrilación Interna: En caso de que el paciente entre en paro cardiaco, se le puede aplicar el desfibrilador sin tener que desconectarle los electrodos del equipo. • Programa de interpretación: Programa de interpretación HES (ECG 531i), desarrollado en Medizinische Hochschule Hannover (Alemania), para diagnostico automatizado. • Sensibilidad del registro: 2,5 - 5 - 10 - 20 mm/mV ± 5% . Indica que se pueden seleccionar 4 tipos diferentes de sensibilidad del instrumento. Por ejemplo 10 mm/mV, indica que 1 mV de la señal de entrada equivale a 10 mm en el papel milimetrado donde se imprimen las derivaciones. La menor sensibilidad es para pacientes con señales ECG de gran amplitud y la mayor es para pacientes con bajas amplitudes de las señales. • Sistema de impresión: Impresora térmica de 8 puntos/mm de resolución. • Canales de impresión: 1 ó 3. Cuando se selecciona un canal de impresión, las doce derivaciones se imprimen una detrás de otra. Cuando se seleccionan 3 canales de impresión, la tira de papel se divide en tres zonas y en cada una se imprimen cuatro derivaciones. • Velocidad del papel: 25 - 50 mm/s ± 5%. Se utiliza la mayor velocidad cuando el paciente presenta taquicardias, es decir que el ritmo cardiaco es muy alto y por lo tanto los complejos QRS se presentan muy rápido y por lo tanto al imprimir a alta velocidad los complejos quedan más espaciados en el papel. • Papel: termosensible en rollo de ancho 60 mm y plegado en Z: 75x60 mm. • Seguridad: Clase II, tipo CF (según EN 60601-1). Se refiere a la normatividad que el equipo electromédico debe cumplir según la Comisión Electrotécnica Internacional (IEC) para garantizar la seguridad eléctrica del paciente y del operador del equipo. • Conformidad: con normas EN 60601-1; EN 60601-1-2; EN 60601-2-25; EN 60601-3-2. Indica que el equipo cumple con la regulación impuesta en la fabricación del equipo por las normas internacionales. • Alimentación: Red y batería interna;100 mA (117 Vac)/50mA (230 Vac) • Autonomía: de la batería interna, 3 horas (1 canal) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 100 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Peso: 1 Kg. • Dimensiones :250 x 50 x 170 mm (LargoxAltoxAncho) 9. MEDICION DEL RITMO CARDIACO El ritmo cardiaco es la medida de la frecuencia cardiaca, es decir, del número de veces que el corazón late por minuto. Cuando el corazón impulsa la sangre a través de las arterias, éstas se expanden y se contraen con el flujo de la sangre. El pulso normal de los adultos sanos oscila entre 60 y 100 latidos por minuto. El pulso podría fluctuar y aumentar con el ejercicio, las enfermedades, las lesiones y las emociones. Las niñas a partir de los 12 años y las mujeres en general suelen tener el pulso más rápido que los niños y los hombres. Los deportistas, como los corredores, que hacen mucho ejercicio cardiovascular, pueden tener ritmos cardiacos de hasta 40 latidos por minuto sin tener ningún problema. El ritmo cardiaco es uno de los signos vitales más importantes del cuerpo humano, de ahí la importancia de medirlo electrónicamente con la mayor exactitud. 9.1 TECNICAS DE MEDICION El corazón es un músculo que siempre está en movimiento, primero se dilata entrando sangre al corazón, a esta fase se le denomina diástole. Luego se contrae enviando sangre a todo el cuerpo, denominándose a esta fase sístole. La circulación sanguínea está acompañada de otros fenómenos fisiológicos de los cuales se puede obtener el ritmo cardiaco: • Fonocardiografía: El corazón en su funcionamiento produce sonidos. Captando los sonidos al latir se puede medir el ritmo cardiaco. • Termometría: Variaciones de Temperatura por la dilatación de los vasos sanguíneos. Cuando el corazón bombea sangre se dilatan todos los vasos sanguíneos. Esto provoca pequeñas variaciones de temperatura Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 101 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica en la superficie de la piel. Detectando estos ∆T se puede detectar el ritmo cardiaco. • Pletismografía: Incluye aquellas técnicas que miden cambios de volumen como consecuencia de variaciones del flujo sanguíneo. No son métodos específicos de un solo vaso arterial sino que miden cambios de volumen en un segmento de la extremidad, cuando el corazón late, se aumenta el volumen periférico de un dedo. Detectando estos cambios de volumen se puede medir el ritmo cardiaco. • Fotopletismografía: Detecta el flujo de sangre cutáneo y traduce sus pulsaciones. Consiste en la emisión de luz infrarroja desde un diodo emisor y un fotodetector adyacente que recibe la luz infrarroja reflejada. A medida que aumenta el flujo de sangre cutáneo aumenta la cantidad de luz reflejada. De esta manera se obtiene una medida cualitativa del flujo sanguíneo cutáneo y se puede medir el ritmo cardiaco. • Electrocardiografía: Cuando se presenta un latido cardiaco, la señal ecg esta generando el complejo QRS. Contando cuantos complejos QRS se presentan en un minuto se obtiene el ritmo cardiaco (pulsaciones por minuto) 9.2 DISEÑO DE UN CARDIOTACOMETRO El instrumento empleado para medir el ritmo cardiaco (pulso), recibe el nombre de cardiotacómetro, debido a que mide pulsaciones por minuto (ppm), asociándolo con el tacómetro convencional que mide revoluciones por minuto (rpm). La figura 98, muestra el diagrama de bloques de un cardiotacometro promediador, es decir, que mide las pulsaciones durante un minuto, tomando la información de la señal ECG, por lo general la derivación DII. DII INA 114 G=10 AMPLIFICADOR NO INVERSOR G=100 V1(t) FILTRO PASABANDA BANDA ANGOSTA V2(t) CIRCUITO V4(t) V3(t) MONOASTABLE CIRCUITO DETECTOR DE MICROCONTROLADO J orge Eduardo Quintero MuñozLM – jo rgequintero@biUMBRAL oingenie(LM311) ros.com 555 102 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 98. Cardiotacometro ECG A continuacion se explica detalladamente la funcion de cada bloque: • INA114: Amplificador de instrumentacion con ganancia 10, para evitar la saturación del mismo debido a los potenciales de semicelda de los electrodos. • Amplificador: No Inversor, con ganancia 100, para completar una ganancia de amplificación de la señal ECG de 1000. La señal a la salida del amplificador V1(t), adquirida con el sistema BIOPAC es la mostrada por la figura 99. Figura 99. Señal a la salida del amplificador no inversor • Filtro: Pasabanda de banda angosta, con frecuencia de resonancia de 17 Hz y factor de calidad de 3.3. La figura 100 muestra el circuito y la figura 101 muestra la señal a la salida de este filtro V2(t). Obsérvese como el filtro elimina las ondas P y T de la señal ECG y deja solo el complejo QRS, el cual es quien genera el latido. V1(t) V2(t) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 103 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 100. Circuito filtro pasabanda de banda angosta Figura 101. Señal a la salida del filtro pasabanda de banda angosta • Detector de Umbral: Circuito basado en el comparador LM311, con histéresis, tal como se muestra en la figura 102. A la salida del comparador se presenta un pulso cada vez que sobrepasa el voltaje umbral. Cada QRS puede generar más de un pulso. V3(t) V2(t) Figura 102. Detector de umbral Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 104 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Monoestable: Basado en el CI 74121, tal como se muestra en la figura 103. El monoestable hace que por cada latido se obtenga un solo pulso. La duración del pulso monoestable se calibra en 250 ms, ya que después de producirse un QRS pasa cierto tiempo en el cual es imposible que se produzca otro. V4(t) V3(t) Figura 103. Monoastable La figura 104, muestra la correlación entre las señales V1(t) y V4(t), que consisten en la señal ECG amplificada y los pulsos digitales a la entrada del microcontrolador respectivamente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 105 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 104. Correlación entre la señal ECG y la señal de pulsos • Circuito microcontrolado: Consiste en un microcontrolador que contiene convertidores A/D, y que se programa para contar los pulsos de entrada durante un minuto. Si las pulsaciones por minuto son mayores a 100, se enciende un led rojo marcado “taquicardia” y se activa un zumbador. Si las pulsaciones son menores a 60 se enciende un led amarillo rotulado “bradicardia” y se activa el zumbador. Si las pulsaciones son mayores a 60 y menores a 100, se enciende el led verde rotulado “normal”. La figura 105 muestra el circuito microcontrolado. Las lecturas y su diagnostico se muestran en el display LCD. MICROCONTROLADOR V4(t) TAQUICARDIA > 100 ppm BRADICARDIA < 60 ppm 61<NORMAL<99 ppm Figura 105. Circuito microcontrolado del cardiotacometro ECG Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 106 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica UNIDAD 2. INSTRUMENTACION TERAPEUTICA JUSTIFICACION: Los equipos terapéuticos aplican diferentes tipos de energía al cuerpo (eléctrica, magnética, electromagnética, mecánica de vibraciones, ultrasonido, fotónica, etc) buscando un electroestimuladores, efecto curativo. electrobisturís, Un ejemplo equipos de de ellos son los magnetoterapia, desfibriladores, marcapasos, equipos de litotricia, equipos de hemodiálisis, etc. En vista de lo anterior el ingeniero electrónico debe estar en capacidad de: • Entender el funcionamiento de tales equipos, para poder diseñarlos y calibrarlos, como también hacerles mantenimiento preventivo, correctivo y predictivo. • Diseñar y construir cualquier otro equipo terapéutico que le permita al medico e investigador biomédico desarrollar nuevos tratamientos para lograr el avance de la ciencia medica y por lo tanto el mejoramiento de la salud humana. OBJETIVO GENERAL: Aprender las técnicas de ingeniería para el diseño de sistemas y/o equipos de instrumentación terapéutica que permitan mediante su aplicación al cuerpo humano el mejoramiento de la salud del paciente. OBJETIVOS ESPECIFICOS: • Diseñar equipos de electroterapia. • Diseñar electrobisturís. BIBLIOGRAFIA: Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 107 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Medical Instrumentation. Applications and Desing. Jhon G Webster. • Introduction to Biomedical Engineering. Jhon D Enderle • Handbook Biomedical Engineering. Vol. 1. • Bioingenieria Tomo IV.Mauricio Wilches. • Electroterapia en Fisioterapia. • Manuales de equipos terapéuticos 10. EQUIPOS DE ELECTROTERAPIA 10.1 COMPORTAMIENTO ELECTRICO DEL CUERPO La Electroterapia, por definición, consiste en la aplicación de energía eléctrica al organismo, con el fin de producir sobre los tejidos enfermos reacciones biológicas y fisiológicas que finalmente los curen. La figura 106, muestra a un fisioterapeuta aplicando un equipo de electroterapia a una paciente. Figura 106. Aplicación de electroterapia (http://www.efmedica.com) Desde el punto de vista eléctrico, el cuerpo humano se considera un conductor de segundo orden, ya que el transporte de la carga eléctrica lo efectúan los iones contenidos en las disoluciones y dispersiones coloidales. La mayor o menor conductividad de los tejidos depende de la cantidad de agua en ellos, Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 108 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica que actúa como disolvente y sus solutos. El agua pura de por si no es buena conductora de la electricidad, pero si se le disuelven solutos, mejora notablemente su conductividad. Los tejidos se clasifican en: • Tejidos poco conductores: hueso, grasa, piel callosa, pelo, uñas. • Tejidos medianamente conductores: piel, tendones, cartílagos. • Tejidos relativamente buenos conductores: sangre, linfa, líquidos intra y extracelulares, tejido muscular, vísceras, hormonas, tejido conjuntivo, tejido nervioso. • Tejidos generadores de electricidad: nódulo sinoauricular (marcapasos) La energía eléctrica se transmite por el cuerpo en forma de electrones asociados a iones que se desplazan por diferencias de potencial aplicadas por los electrodos conectados al equipo de electroterapia y por las cargas eléctricas internas. Dentro del cuerpo se desplazan sustancias y elementos químicos que tienen carga eléctrica presentes en los tejidos, los cuales funcionan bien dependiendo de: • Las distintas concentraciones y proporciones de cada una, • De su facilidad para desplazarse, • De su capacidad para producir reacciones bioquímicas, que desencadenan el trabajo encomendado a cada tejido. Al aplicar una diferencia de potencial externa mediante los electrodos, los iones positivos se concentraran en la vecindad del electrodo negativo y los iones negativos buscaran al positivo, rompiéndose las proporciones y composición de las disoluciones. 10.2 CORRIENTES ELECTROTERAPEUTICAS Las corrientes electroterapéuticas se clasifican según: • Los efectos sobre el cuerpo: - Electroquímicos - Motores sobre nervio y músculo - Sensitivos sobre nervio y músculo Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 109 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • • • Aporte energético para mejora de metabolismo Los modos de aplicación: - Pulsos aislados - Trenes o ráfagas - Aplicación mantenida o frecuencia fija - Corrientes moduladas La frecuencia: - Baja: 0 a 1000 Hz - Media: 1.000 a 500.000 Hz - Alta: mayores a 500.000 Hz Las formas de onda: - Galvánica o DC: La galvánica tiene polaridad, es única en su grupo y se destina a provocar cambios electroquímicos en el organismo. (Véase la figura 107) Figura 107. Corrientes Galvánicas - Galvánicas Interrumpidas: Todas aquellas que están conformadas por pulsos positivos o negativos, pero todos en el mismo sentido, luego, poseen polaridad. Los pulsos pueden ser de diferentes formas y frecuencias, así como agrupados en trenes, impulsos aislados, modulados o frecuencia fija. Son las más características de la baja frecuencia. (Véase la figura 108) Figura 108. Corrientes Galvánicas Interrumpidas Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 110 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica - Alternas: Reciben el nombre de alternas porque su característica fundamental se manifiesta en el constante cambio de polaridad, en consecuencia, no poseen polaridad. La forma más característica es la sinusoidal perfecta de mayor o menor frecuencia, empleada en media y alta frecuencia. Existen otras corrientes cuya forma no es la típica sinusoidal, sino que pueden dibujarse como cuadrangulares, triangulares, etcétera, pero que, aunque siguen manteniendo la alternancia en la polaridad, realmente se les denomina como bifásicas. (Véase la figura 109) Figura 109. Corrientes Alternas o Bifásicas - Alternas Interrumpidas: En este grupo entran un gran conjunto de corrientes no bien definidas y difíciles de clasificar, pero que normalmente consisten en aplicar interrupciones en una alterna para formar pequeñas ráfagas o paquetes denominados pulsos. Es muy Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 111 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica frecuente encontrar estos pequeños paquetes de alterna en magnetoterapia, alta frecuencia, pulsos de láser, equipos de media frecuencia. (Véase la figura 110) Figura 110. Corrientes Alternas Interrumpidas - Moduladas: Las moduladas son corrientes que están sufriendo cambios constantes durante toda la sesión. Pueden pertenecer al grupo de las interrumpidas galvánicas o al de las alternas. Las modulaciones más habituales son las de amplitud, modulaciones en frecuencia y modulaciones en anchura de pulso (Véase las figuras 111 a y b) Figura 111(a). Corriente Modulada en Frecuencia Figura 111(b). Corriente Modulada en Amplitud 10.3 CONDICIONES DE DISEÑO PARA LOS EQUIPOS DE ELECTROTERAPIA Los equipos de última generación en electroterapia cumplen las siguientes condiciones: • Generación de ondas: basada en electrónica programada (software) con base en microcontroladores, no en electrónica cableada (hardware). El Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 112 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica microcontrolador controla la forma de la onda, los tiempos de encendido y apagado, los modos de aplicación (pulsos, trenes, mantenida). • No se usan transformadores para elevar la tensión de aplicación de los pulsos al paciente, ya que estos los deforman debido a la oposición de las bobinas al cambio brusco de corriente, cuando se pasa del estado ON al OFF. • El equipo debe estar en capacidad de entregar picos de corriente de 80 mA, y picos de tensión hasta de 180V, sobre una impedancia de paciente equivalente a 500 Ω. La figura 112, muestra la concepción de diseño de un equipo de electroterapia de baja frecuencia (menor a 1000 Hz). Figura 112. Equipo electroterapéutico de baja frecuencia En el panel frontal del equipo se observan los siguientes conectores: • Interruptor de encendido / apagado. • Conector para cargador de batería (pues la tendencia es evitar las conexiones a la red eléctrica, pero requiere buenas baterías). • Conector para terapias combinadas con equipos de ultrasonidos. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 113 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Conector RS232 para almacenar datos en un computador para manejar el equipo o modificar los programas. • Conector para salida de la corriente galvánica (dadas sus características diferenciadas). • Conector para salida de baja frecuencia. • Conector para pulsador de aplicación intencionada. En cuanto el modo de aplicación el equipo presenta las siguientes opciones, como se muestra en la figura 113: • Impulsos aislados • Trenes de impulsos • Corrientes de aplicación fija Figura 113. Modos de aplicación de la corrientes El equipo ofrece dos tipos de formas de corriente. La forma uno se basa en pulsos rectangulares, tal como se muestra en la figura 114: • Cuadrangular monofásica • Cuadrangular bifásica consecutiva • Cuadrangular bifásica desfasada Figura 114. Formas de aplicación de las corrientes. Pulsos La forma de corriente dos se muestra en la figura 115: • Triangular monofásica • Triangular bifásica desfasada • Diadinámicas Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 114 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 115. Formas de aplicación de las corrientes. Triangulares/Diadinamicas 10.4 EQUIPOS TENS Y TEMS El mercado ofrece a los fisioterapeutas una infinidad de equipos diferentes que cubren todas las necesidades de aplicación terapéutica de estos profesionales. Sin embargo, los equipos más populares en electroterapia son los TENS y los EMS. El TENS (Estimulación Nerviosa Eléctrica Transcutánea) es un pequeño aparato generador de pulsos eléctricos destinado a conseguir analgesia (eliminación del dolor). Se diseña para actuar sobre los nervios sensitivos. El TEMS (Estimulación Motora Eléctrica Transcutánea) es otro pequeño aparato destinado al trabajo muscular en conjuntos neuromúsculo normal. La figura 116, muestra los paneles frontales de un TENS y TEMS comerciales. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 115 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 116. Panel frontal de un TENS y un TEMS A continuación se presentan las diferencias entre un equipo TENS y un TEMS: TENS TEMS Destinado a analgesia. Destinado a trabajo muscular. Suelen tener 2 salidas. Suelen tener 2 salidas. Intensidad hasta 50 mA. Intensidad hasta 80 ó 100 mA. Modos de trabajo en burst, FF frecuencia Modos de trabajo en trenes (algunos fija y modulaciones. ofrecen la posibilidad de frecuencia fija FF). Frecuencia regulable entre 1 a 200 Hz. Frecuencia regulable entre 10 a 100 Hz (algunos ofrecen frecuencia por debajo de 10 Hz). El tiempo de sesión tiende a ser relativamente largo (15, 20, 30 minutos). El tiempo de sesión tiende a ser más corto que en el TENS (10, 15, 20 minutos). En modulaciones pueden modularse la No tiene modulaciones. anchura de pulso PWM, modulaciones en amplitud AM, y modulaciones de frecuencia FM. En las modulaciones de frecuencia, se tiene la opción de ajustar sus límites con FRECUENCIA MENOR y FRECUENCIA MAYOR. No ofrecen trenes Los trenes son regulables entre 1 y 20 segundos. Las pausas entre trenes son regulables desde 1 a 60 segundos. La RAMPA de subida del tren debe Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 116 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica regularse para que se establezca más o menos bruscamente. Unos ajustan el tiempo de subida y otros un porcentaje del tiempo ocupado por el tren. Los BURST son pequeñas ráfagas, 2 por Es muy interesante que los TEMS segundo, que pueden utilizarse para posean frecuencia fija muy baja (entre vibración muscular. 1 y 10 Hz) para aplicar vibraciones musculares. Suelen alimentarse con una pila de 9 Volt. Suelen alimentarse con una o dos pilas de 9 Volt. Algunos ofrecen la opción de que los trenes surjan simultáneamente por ambas salidas o que se alternen para trabajar los antagonistas cuando los agonistas se relajan. Trabajan en voltaje constante (VC). Trabajan en voltaje constante (VC). Las formas de pulso pretenden ser monofásicas cuadrangulares. Las formas de pulso pretenden ser monofásicas cuadrangulares. Algunos poseen ondas cuadrangulares bifásicas digitales. En general los EMS cuidan más las ondas de salida. Los electrodos suelen ser pequeños e iguales. Es importante que el tamaño de electrodos sea variado para combinarlos y adaptarlos a los diferentes músculos y métodos de estimulación. Los TENS suelen ser más baratos. Los EMS suelen ser bastante más costosos. Con el TENS no de debe superar las respuestas motoras salvo cuando se genere alternancia en el trabajo muscular. Con el EMS se supera el umbral motor para tonificar y potenciar musculatura, excepto cuando se aplique frecuencia fija, que solamente debe quedarse en estímulo sensitivo. El TENS se destina al estímulo de fibras nerviosas sensitivas. El EMS se destina al estímulo de fibras nerviosas motoras. Tiempo de pulso regulable entre 0,05 a Tiempo de pulso regulable entre 0,1 a Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 117 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 0,3 ms (pasando por toda la gama). 0,75 ms (dos o tres opciones). 10.5 DISEÑO DE UN EQUIPO DE ELECTROTERAPIA MICROCONTROLADO La figura 117, muestra el diagrama de bloques de un equipo de electroterapia, basado en microcontrolador, que puede funcionar como TENS y TEMS de acuerdo a la manera como lo programe y aplique el usuario. +5V +12 V 120 V 60 Hz +170 V Puente H VG 1-3 VG 1-3 S1 Preamplificador de Corriente Optoacoplador VG 1-3 + VG 2-4 S4 Vo S2 S3 µC VG 2-4 VG 2-4 Control de Intensidad Figura 117. Diagrama de bloques de un electroestimulador A continuación se describirá la función de cada bloque: Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 118 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Fuente de alimentación: Entrega +5V para el microcontrolador, +12V a los circuitos intermedios y +170V para el amplificador de salida. • Microcontrolador: Circuito encargado mediante programación de generar las formas de onda requerida. Tiene dos pines de salida donde genera las tensiones VB1-2 y VB2-3 que controlaran los terminales de puerta de los transistores MOSFET 1-2 y 2-3, respectivamente. Las ondas de salida dependen de las teclas de membrana que se pulsen en el panel frontal del equipo y que se encuentran conectadas a los pines de un puerto configuradas como entradas y la tensión de alimentación de +5V. • Optoacoplador: Separa eléctricamente al microcontrolador del resto del circuito, para protegerlo de posibles cortocircuitos. Se puede utilizar el circuito integrado 4N26. La figura 118, muestra la configuración interna de este circuito integrado, como también el tipo de encapsulado de 6 pines. Figura 118. Circuito integrado 4N26 • Preamplificador de corriente: Por lo general es un circuito Par Darlinton de alta ganancia de corriente que se encarga de entregar la corriente necesaria a los terminales de entrada del circuito de salida, sin cargar la salida del optoacoplador. La figura 118, presenta a la estructura circuital de un par Darlinton. +Vcc = 12V I C1 IB1 β1 I C2 2N2222 I I Jorge Eduardo Quintero MuñoE1z – jorgeqB2 uintero@bioingenieros.com β 2 D325 119 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 119. Par Darlinton El par Darlinton, es un circuito amplificador de corriente con ganancia de tensión aproximadamente igual a uno. La corriente de salida IE2 es igual al producto de las dos ganancias de corriente de los dos transistores (β1 x β2) multiplicado por la corriente de base del primer transistor IB1. • Puente H: Circuito de salida, basado en cuatro transistores MOSFET, conectados en puente, tal como lo muestra la figura 120, en donde los transistores son MOSFET de enriquecimiento, canal P para 1 y 4 y canal N para 2 y 3. Los transistores se activan al mismo tiempo por parejas, 1/3 o 2/4, de acuerdo con las tensiones aplicadas a los terminales de entrada (puertas o Gate) para lograr una determinada onda a la salida. Figura 120. Puente H de circuito integrado Para obtener pulsos aislados positivos en la carga (resistencia del paciente) conectada entre los drenadores D1/D2 y D3/D4, el microcontrolador genera la tensión VG1-3 de pulsos con las condiciones de tiempos TON (desde 0,005 ms a Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 120 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 1 s) y TOFF (desde 1 a 5 s) determinadas para aplicaciones TENS o TEMS, mientras que la tensión VG2-4 será cero todo el tiempo, tal como se muestra en la figura 121. Para obtener pulsos aislados negativos en la carga, el microcontrolador genera la tensión VG2-4 de pulsos con las condiciones de tiempos ON y OFF determinadas para aplicaciones TENS o TEMS, mientras que la tensión VG1-3 será cero todo el tiempo, tal como se muestra en la figura 122. VG1-3 5V TOFF TON t VG2-4 0V t V0 170V TOFF TON t Figura 121. Generación de pulsos aislados positivos VG1-3 0V VG2-4 t 5V TON TOFF Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 121 t UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 122. Generación de pulsos aislados negativos Para generar pulsos monofásicos mantenidos ya sean positivos o negativos se disminuye el TOFF (desde 5 a 20 ms) a valores similares a los de TON (0,1 a 5 ms), con las mismas tensiones de control de puerta de las graficas 121 y 122 respectivamente, tal como se muestra en la gráfica 123. VG1-3 5V t VG2-4 0V t V0 170V t Figura 123. Generación de pulsos mantenidos positivos Para trenes de pulsos se programa el microcontrolador con los tiempos de encendido y apagado de los impulsos descritos por la figura 123 (TON1, TOFF1), Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 122 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica pero adicionalmente se temporiza durante cuanto tiempo se aplican (TON2: 1 a 20 s) y durante cuanto tiempo no se aplican (TOFF2: 1 a 40 s), como se muestra en la figura 124. Para generar pulsos bifásicos las tensiones de control de puerta deben estar negadas, es decir cuando una es +5V, la otra es cero y viceversa, tal como se muestra en la figura 125. VG1-3 TON2 5V TOFF2 t VG2-4 0V t V0 TON2 170V TOFF2 t Figura 124. Generación de trenes de pulsos positivos VG1-3 5V TOFF 0V VG2-4 5V TON t TON TOFF Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 123 0V t V0 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 125. Generación de pulsos bifásicos Obsérvese como con el puente H y las tensiones de control de puerta, generadas por el microcontrolador, se pueden generar una gran cantidad de formas de onda para aplicar al paciente, jugando con los tiempos de encendido (TON) y apagado (TON) de acuerdo con la aplicación terapéutica. Si se requiere analgesia (TENS) para estimular nervios sensitivos y si se necesita estimulación motora (TEMS) para estimulación de nervios y músculos motores. 10.6 ESPECIFICACIONES TECNICAS DE UN EQUIPO DE ELECTROTERAPIA La figura 126, muestra el equipo comercial de electroterapia microcontrolado de última generación Therapic 9400, fabricado por la empresa española QUIRUMED (www.quirumed.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 124 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 126. Equipo de electroterapia Therapic 9400 A continuación se muestran las especificaciones técnicas de este equipo: Tipos de corriente Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 125 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 11. EQUIPOS DE ELECTROCIRUGÍA 11.1 PRINCIPIOS DE ELECTROCIRUGÍA La electrocirugía se define como la aplicación de corrientes de radiofrecuencia (RF) para CORTAR, COAGULAR y QUEMAR tejidos. Se basa en la ley de Joule (I2 x R x t) de producción de calor cuando la corriente atraviesa la resistencia eléctrica de los de los tejidos. Se trabaja con corrientes de RF, debido a que la estimulación nerviosa y muscular debidas al paso de la corriente eléctrica cesa a los 100kHz, por lo tanto, la electrocirugía puede realizarse de forma segura con radio frecuencias mayores a 100kHz, esta frecuencia electroquirúgica puede pasar a través del paciente sin causar la mínima estimulación neuromuscular y ningún peligro de electrocutar al paciente como si lo haría una corriente de 60 Hz. La figura 127, muestra el ancho de banda de las frecuencias empleadas en electrocirugía. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 126 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 127. Ancho de banda de la electrocirugía (www.valleylab.com) La figura 128, muestra la relación entrada salida de un equipo de electrocirugía. Obsérvese como el equipo se alimenta a 120V RMS y entrega al paciente 2400 V pico-pico. Además, la red de alimentación trabaja a 60 Hz y el equipo puede entregar una onda seno oscilando a 500 KHz. En modo de corte, el equipo puede estar entregando al paciente 350 W de potencia, para una resistencia del mismo de 300 Ω y consumir de la red eléctrica 650 W, lo cual implica que en la transformación de la tensión aparecen perdidas de potencia. 120V/60Hz 2400V pp/500 KHz 650W/Cut 350W/300Ω/Cut Figura 128. Relación entrada-salida de un electrobisturí (www.valleylab.com) En electrocirugía se emplean dos técnicas, la monopolar y la bipolar. En la técnica monopolar, el electrodo activo se encuentra en la región a intervenir y el Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 127 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica electrodo de retorno de paciente (electrodo de placa) se encuentra en alguna parte del cuerpo del paciente, por lo tanto, la corriente pasa a través del paciente completando el circuito desde el electrodo activo al electrodo de retorno de paciente, tal como se puede observar en la figura 129. Figura 129. Electrocirugia monopolar (www.valleylab.com) La técnica monopolar es la modalidad electroquirúrgica más usada, debido a su versatilidad y efectividad clínica, ya que con esta técnica se puede cortar, coagular y quemar tejidos. En electrocirugía bipolar, tanto el electrodo activo y el electrodo de retorno están montados en la misma pinza, aunque aislados eléctricamente, tal como se muestra en la figura 130. Figura 130. Electrocirugia bipolar (www.valleylab.com) Las dos puntas de la pinza realizan las funciones del electrodo activo y el electrodo de retorno. Solamente los tejidos asidos están incluidos en el circuito eléctrico. Ya que la función de retorno es realizada por una punta de la pinza, el Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 128 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica electrodo de retorno de paciente no es necesario. Esta técnica se utiliza principalmente para coagular. En electrocirugía se utilizan tres formas de onda, tal como se puede observar en la grafica 131, estas son: onda de corte puro (CUT), onda de corte con mezcla (BLEND) y onda de coagulación (COAG). Figura 131. Ondas electroquirurgicas (www.valleylab.com) Las ondas Blend y Coag, tiene características de encendido (ON) y apagado (OFF). El ciclo de trabajo se define como la relación porcentual entre el tiempo de encendido (Ton) y el periodo (T= Ton+Toff). Para el caso de la onda Cut, su ciclo de trabajo es del 100%, ya que siempre esta presente. En el caso de las ondas Blend, el ciclo de trabajo es del 50%, 40% y 25% respectivamente. Finalmente, para la onda Coag, el ciclo de trabajo es de solo 6%. El ciclo de trabajo determina la capacidad de producir calor en los tejidos de cada onda, por lo tanto la onda Cut, es la de mayor poder de corte y la Coag la de menor y es por ello que esta onda no produce corte, sino coagulación. Las ondas Blend, tienen ambos efectos combinados, es decir corta y coagula a la vez. La única variable que determina si una forma de onda vaporiza el tejido o produce coagulación es la cantidad de calor producido. Un alto calor produce una vaporización rápida. Un bajo calor produce una muy lenta coagulación. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 129 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El corte electroquirúrgico produce una incisión en el tejido por medio de chispas eléctricas que focalizan el intenso calor en el sitio quirúrgico. Al chispear el tejido, el cirujano produce una máxima concentración de corriente. Para crear esta chispa el cirujano debe sostener el electrodo ligeramente lejos del tejido. Esto producirá una gran cantidad de calor en un periodo muy corto de tiempo obteniendo la vaporización de tejido, tal como se muestra en la figura 132. •CUT •Voltaje Medio/Alto •Monopolar Tejido Figura 132. Corte electroquirurgico (www.valleylab.com) La desecación (deshidratación celular) electroquirúrgica ocurre cuando el electrodo está en contacto directo con el tejido. Las células secas forman un coágulo vaporizándose y no explotan. Se puede emplear cualquiera de las tres formas de onda. Cuando se emplea “CUT”, se baja el voltaje de la onda y al tocar el tejido con el electrodo, la concentración de corriente se reduce. Se genera menos calor y no se produce el “corte”, tal como se muestra en la figura 133. •CUT •COAG •Voltaje Bajo •Voltaje Medio •Monopolar •Monopolar •Bipolar Tejido Tejido Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 130 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 133. Desecación electroquirúrgica (www.valleylab.com) Fulguración Electroquirúrgica: Chispas generadas con la forma de onda COAG. Coagula y trabaja el tejido en una área amplia. Su ciclo de trabajo (tiempo real) es del 6%, produciendo poco calor. El resultado será coagular en lugar de la vaporización celular, Para superar la alta impedancia del aire, la forma de onda de coagulación debe tener un voltaje significativamente más alto que la onda de corte, como se muestra en la figura 134. •CUT o COAG •Voltaje Alto •Monopolar Tejido Figura 134. Fulguración electroquirúrgica (www.valleylab.com) 11.2 DISEÑO DE UN EQUIPO DE ELECTROCIRUGÍA La figura 135, muestra el diagrama de bloques funcional de un equipo de electrocirugía de última generación. FASE NEUTRO TIERRA MICROCONTROLADOR OSCILADOR DE COAG. INDICADOR DE AUDIO SELECTOR DE POTENCIA PURE/BLEND/COAG OSCILADOR DE CORTE SELECTOR DE POTENCIA PREAMPLIFICADOR DE CORRIENTE SELECTOR DE OPERACION FUENTES DE ALIMENTACION DC MONITOR ALAMBRE DE TIERRA AMPLIFICADOR DE POTENCIA RF PREAMPLIFICADOR DE POTENCIA RF PREAMPLIFICADOR DE CORRIENTE CONTROL AUTOMATICO DE POTENCIA MONITOR CALIDAD CONTACTO DE PLACA Figura 135. Diagrama de bloques de un equipo de electrocirugía Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 131 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Los bloques azul y amarillo pertenecen al sistema de generación de las ondas electroquirúrgicas en baja tensión. Los bloques verdes pertenecen al sistema de control del equipo. Los bloques rojos pertenecen al sistema de potencia. A continuación se describirá la función de cada bloque: 11.2.1 GENERACIÓN DE ONDAS ELECTROQUIRURGICAS Un microcontrolador se encarga de generar las ondas de corte puro (PURE CUT), corte mezclado (BLEND) y coagulación (COAG), de acuerdo a la selección que ha hecho el cirujano, mediante el accionamiento de pedales (técnica bipolar) o pulsadores que se encuentran en el electrodo activo (técnica monopolar). La figura 136 muestra las cinco ondas generadas por el microcontrolador de un equipo de electrocirugía comercial las cuales se describen a continuación: • Onda 1: PURE CUT. Onda de pulsos cuadrada a 510 KHz. Amplitud, 5V. • Onda 2: BLEND 1. Onda de pulsos cuadrada a 510 KHz., con ciclo de trabajo del 50% y frecuencia de repetición de 31 KHz. • Onda 3: BLEND 2. Onda de pulsos cuadrada a 510 KHz., con ciclo de trabajo del 37.5% y frecuencia de repetición de 31 KHz. • Onda 4: BLEND 3. Onda de pulsos cuadrada a 510 KHz., con ciclo de trabajo del 25% y frecuencia de repetición de 31 KHz. • Onda 5: COAG. Onda de pulsos, con ciclo de trabajo del 6% y frecuencia de repetición de 31 KHz. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 132 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 136. Ondas generadas por el microcontrolador de un equipo de electrocirugía A la salida de los pines del microcontrolador se conectan circuitos integrados optoacopladores, para aislar galvánicamente al microcontrolador del resto del circuito y así protegerlo de posibles cortocircuitos que puedan dañarlo, tal como se observa en la figura 137. +5V +12V OND A 5 AL S EL EC T O R D E P O T EN C IA C O AG P U R E/B LE N D AL SE LE C T O R D E PO T E N C IA O N D AS 1-2-3-4 +12V Figura 137. Circuito generador de ondas por microcontrolador de un equipo de electrocirugía 11.2.2 SELECTOR DE POTENCIA Consiste en un potenciómetro digital de circuito integrado, en donde la potencia requerida por el cirujano se ajusta con las teclas de membrana UP/DOWN, tal como se observa en la figura 138. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 133 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 138. Circuito selector de potencia de un equipo de electrocirugía 11.2.3 PREAMPLIFICADOR DE CORRIENTE +Vcc = 12V IC 1 IB 1 β1 IC 2 2N 2222 IE 1 IB 2 β2 A L S E L E C T O R D E O P E R A C IO N D 325 1K IE 2 1K Figura 139. Circuito preamplificador de corriente de un equipo de electrocirugía Por lo general es un circuito Par Darlinton de alta ganancia de corriente que se encarga de entregar la corriente necesaria a los terminales de entrada del circuito selector de operación, sin cargar la salida del potenciómetro digital que funciona como selector de potencia. La figura 139, mostrada arriba, presenta a la estructura circuital de un par Darlinton. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 134 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 11.2.4 SELECTOR DE OPERACIÓN Consiste en un sistema de control accionado por pedales, uno para corte (color amarillo) y el otro para coagulación (color azul) cuando el cirujano emplea la técnica bipolar. También es accionado por el pulsador de corte (amarillo) ubicado en el lapicero quirúrgico o el de coagulación (azul), cuando el cirujano utiliza la técnica monopolar. Solo una onda electroquirúrgica será seleccionada y se aplica a la entrada del preamplificador de potencia de RF. La figura 140, muestra al circuito selector de operación cuando se emplean pedales. CIRCUITO DE CONTROL CIRCUITO DE ACCIONAMIENTO K1 K2 NO NC COAG. +Vcc = 12V BOBINA RELE CUT K1 PEDAL DE CUT K2 AL PREAMPLIFICADOR DE CORRIENTE DE RF BOBINA RELE COAG PEDAL DE COAG K1 K2 NC NO PURE/BLEND Figura 140. Circuito selector de operación de un equipo de electrocirugía En la figura 140 se observa que los elementos actuadores son dos relevadores, cuyas bobinas se energizan al accionarse los pedales ubicados en el circuito de control. En el circuito de accionamiento se encuentran los contactos normalmente abiertos (N.O) y normalmente cerrados (N.C) de los relevadores. Nótese como si se accionaran al mismo tiempo los pedales de corte y coagulación, ninguna onda será conectada a la entrada del preamplificador de corriente de RF. 11.2.5 PREAMPLIFICADOR DE POTENCIA DE RF Consiste en un par Darlinton pero polarizado a +250V, cuya función principal es entregar la suficiente corriente a la entrada del amplificador de potencia de RF. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 135 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 11.2.6 AMPLIFICADOR DE POTENCIA DE RF Consiste en un amplificador de potencia de RF sintonizado, a base de transistores de potencia BJT o MOSFET, conectados todos en paralelo, para disminuir la potencia disipada por cada uno, tal como se muestra en la figura 141. +Vcc = 250V C1 L1 RP N1 N2 PURE/BLEND COAG. Q2 Q1 2SD200 0.33Ω/10W 2SD200 0.33Ω/10W Q3 2SD200 0.33Ω/10W Q4 2SD200 0.33Ω/10W Q5 2SD200 0.33Ω/10W Q6 2SD200 0.33Ω/10W Figura 141. Circuito amplificador de potencia de RF de un equipo de electrocirugía Este amplificador tiene las siguientes características: • Trabaja en clase B cuando la onda de entrada es PURE CUT, ya que es una onda cuadrada donde el ciclo de trabajo es del 50%. • Trabaja en clase C cuando la onda de entrada es COAG, ya que es una onda con ciclo de trabajo menor al 10%. • Es un amplificador sintonizado, ya que entre la fuente de alimentación y los colectores, existe un circuito tanque RLC paralelo. Este circuito se sintoniza por lo general con la frecuencia del primer armónico de la onda de corte puro. Cuando esto se logra se dice que el circuito entra en resonancia y se genera una onda de voltaje seno pura en el circuito RLC Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 136 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica paralelo, cuya fuente de energía, viene a ser la corriente de colector que oscila a la frecuencia de resonancia ( 1/[2π (L1C)1/2]. Las demás componentes de frecuencia de la corriente de colector son rechazadas por el circuito tanque ya que este se comporta como un filtro rechazabanda de banda angosta. El núcleo del transformador es de ferrita, debido a la alta frecuencia de trabajo. • El numero de espiras secundarias N2, se calcula, de tal manera que se cumpla con el teorema de la máxima transferencia de potencia de Thellegen. En este caso, la resistencia de paciente Rp, se asume como de 300 Ω para técnica monopolar y de 100 Ω para bipolar. 11.2.7 CONTROL AUTOMATICO DE POTENCIA Consiste en un sistema de control digital, que mantiene la potencia de corte aplicada al paciente, prácticamente en el mismo valor seleccionado en el panel frontal del equipo, dentro de un amplio rango de impedancias de tejidos diferentes. La figura 142, muestra el comportamiento del sistema de control automático de potencia para el modelo FORCE FX de Valleylab. Figura 142. Respuesta del control automático de potencia del FORCE FX Obsérvese como para una potencia de corte puro seleccionada de 40W, la potencia entregada al paciente se mantiene muy cerca de este valor desde los 100 hasta los 4000 Ω. Valleylab mide la eficacia de su sistema de control automático, mediante un indicador denominado PER (Power Efficiency Rating), que se calcula hallando el cociente entre la potencia real entregada por el equipo Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 137 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica y la potencia de corte seleccionada, multiplicado por 100. Nótese como el PER del equipo de Valleylab es del 98%, muy superior al de un equipo convencional sin el control automático de potencia que viene a ser solo del 61%. 11.2.7 MONITOR CALIDAD CONTACTO DE PLACA Consiste en un sistema de control que mide constantemente la impedancia de contacto entre el paciente y el electrodo de placa, con el propósito de eliminar el riesgo de quemaduras al paciente por corrientes de fuga de RF, cuando la placa se aísla del paciente. Cuando la impedancia sobre pasa un valor establecido, el equipo automáticamente deja de generar potencia de RF y se dispara una alarma tanto audible como visual que indica esta situación peligrosa para el paciente. La técnica de medición es la de bioimpedanciometría, que consiste en aplicar al paciente una corriente seno de menos de 10 µA RMS con frecuencia de 100 KHz, midiéndose la tensión entre este y la placa, que viene a ser proporcional a la impedancia de contacto. Por lo general el máximo valor permitido es de 135 Ω. 11.2.8 MONITOR ALAMBRE DE TIERRA Consiste en un sistema de control que monitorea la continuidad del alambre de tierra que se encuentra conectado entre el chasis del equipo y el polo a tierra del tomacorriente. Es fundamental el buen estado del alambre de tierra (baja resistencia: menor a 0.5 Ω), ya que las corrientes de fuga de baja frecuencia, generadas por el equipo se van a tierra, protegiendo la seguridad eléctrica del paciente, ya que solo 10 µA de 60 Hz que pasen directamente a través del músculo cardiaco producen fibrilación ventricular, pudiendo causar la muerte. Cuando la diferencia de potencial entre el neutro y la tierra es mayor a un voltio se debe desconectar automáticamente el equipo de la red, disparando una alarma sonora y visual. 11.2.9 INDICADOR DE AUDIO Consiste en circuito de audio, que genera un tono de 800 Hz cuando se selecciona corte y uno de 1200 Hz, cuando se selecciona coagulación. Esto es necesario para realimentar al cirujano que ha seleccionado, especialmente cuando utiliza los pedales en modo bipolar. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 138 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 11.2.10 FUENTES DE ALIMENTACION DC Se encarga de generar las tensiones DC de 5V para los circuitos digitales, 12V para los circuitos de preamplificación de corriente y de 250V para alimentar el amplificador de potencia. 11.3 ESPECIFICACIONES TECNICAS DE UN EQUIPO DE ELECTROCIRUGIA La figura 143, muestra el equipo comercial de electrocirugía microcontrolado de última generación FORCE FX, fabricado por la empresa americana Valleylab Inc. (www.valleylab.com) Figura 143. Equipo de electrocirugía FORCE FX (www.valleylab.com) A continuación se presentan sus especificaciones técnicas, tal como aparecen en su datasheet: Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 139 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 11.4 ACCESORIOS PARA ELECTROCIRUGÍA Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 140 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 144, muestra lapiceros quirúrgicos, electrodos de paciente y pedaleras. Figura 144. Accesorios básicos de electrocirugía (www.geister.com) La figura 154, muestra una gran variedad de electrodos quirúrgicos en técnica monopolar. Figura 144. Electrodos monopolares (www.geister.com) La figura 145, muestra las pinzas bipolares. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 141 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 145. Pinzas bipolares (www.geister.com) La figura 146, muestra estructuras porta equipos. Figura 146. Estructuras porta electrobisturís (www.geister.com) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 142 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica UNIDAD 3. INSTRUMENTACION DE IMÁGENES MÉDICAS JUSTIFICACION: Los equipos de imágenes medicas se utilizan para “ver” dentro del cuerpo sin invadirlo. Las imágenes médicas se utilizan cada vez mas en los protocolos para hacer diagnostico especializado. Ejemplos de tales equipos son los de Rayos X (RX), Tomografía Computada (TC), Resonancia Magnética Nuclear (RMN), Ultra Sonido (US). En vista de lo anterior el ingeniero biomédico debe estar en capacidad de entender el funcionamiento de tales equipos, para poder efectuar mantenimiento preventivo, correctivo y predictivo. OBJETIVO GENERAL: Aplicar los conceptos básicos de física moderna, matemáticas avanzadas y electrónica que se utilizan en la construcción de equipos de imágenes medicas. OBJETIVOS ESPECIFICOS: • Estudiar los equipos de RX convencionales. • Estudiar los equipos de TC. BIBLIOGRAFIA: • Medical Instrumentation. Applications and Design. Jhon G Webster. • Introduction to Biomedical Engineering. John D Enderle • Handbook Biomedical Engineering. Vol. 1. • Introducción a la Bioingeniería. Mundo Electrónico. • Tecnología Radiológica. Rayos X. Javier González Rico • Tomografía Computada. Javier González Rico Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 143 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica CAPITULO 12. INTRODUCCIÓN A LAS IMÁGENES MÉDICAS 12.1 DEFINICION DE RADIOLOGIA La radiología es el estudio de la interacción de una determinada radiación energética cuando atraviesa un tejido humano y la obtención de información clínica de interés a partir de la observación de esta interacción. La figura 147, muestra una imagen de cráneo tomada con un equipo de resonancia magnética nuclear, en donde los tejidos interactúan con un campo magnético. Se ha hecho un corte con técnicas de procesamiento digital de imágenes para ver el interior del mismo. Figura 147. Resultado de la interacción de campos magnéticos con tejidos Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 144 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 12.2 DEFINICION DE IMÁGEN MÉDICA Es la representación espacial en forma de imagen de la distribución de una o más propiedades físicas dentro del cuerpo humano. Al igual que una señal, la imagen contiene información, la diferencia estriba en que la cantidad bajo estudio de la señal varia en el tiempo, mientras la cantidad de la imagen varía en el espacio. Esta cantidad es un parámetro físico asociado a los tejidos. Por ejemplo en la figura 148, se muestra la variación del parámetro de atenuación (µ) en función de las coordenadas espaciales X, Y cuando los tejidos del abdomen son atravesados por RX en un imagen tomada con un equipo de TC. Y (mm) X (mm) µ = f ( X,Y ) Figura 148. Variación espacial del coeficiente de atenuación, µ Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 145 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La imagen de la figura 148, esta representada en la escala de grises, que va desde el blanco hasta el negro. En RX y TC, al mayor coeficiente de atenuación, µ, se le asigna el color blanco, mientras que al menor se le asigna el negro y a los valores intermedios, se le asignan los diferentes grises de la escala. Obsérvese como la variación de tonalidades grises, permite crear la imagen, pues una imagen compuesta de un solo color no contiene información. 12.3 CLASIFICACION DE LAS IMÁGENES MÉDICAS Las imágenes médicas se pueden clasificar de dos maneras: • Según la energía de radiación empleada • Según la forma de obtención de la imagen. Que a su vez se puede clasificar en: - Imágenes obtenidas por proyección - Imágenes obtenidas por reconstrucción 12.3.1 SEGÚN LA ENERGIA DE RADIACION EMPLEADA Actualmente hay cuatro tipos de energía que se emplea para radiar a los tejidos del cuerpo y a partir de la interacción de estos con la energía obtener las imágenes médicas: • Rayos X: Se aplican en radiología convencional, radiología digital, angiografía digital por sustracción y tomografía computada. • Medicina Nuclear: Se emplea radiaciones procedentes de isótopos radioactivos. Las aplicaciones de esta radiación son la tomografía por emisión de fotones simples (SPECT) y tomografía por emisión de positrones (PET). • Ultrasonidos: Se aplican en ecografía convencional (gineco-obstetricia) y ecodoopler (ecocardiografía). • Electromagnéticas: Se aplican en Imágenes por resonancia magnética nuclear (MRI), magnetoencefalografía (MEG) y electroencefalografía por potenciales evocados (EEF). La figura 149, muestra un collage de las energías de radiación descritas anteriormente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 146 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica RAYOS X MEDICINA NUCLEAR ULTRASONIDOS ELECTROMAGNETI CAS Figura 149. Radiaciones empleadas en radiología 12.3.2 SEGÚN LA FORMA DE OBTENCION DE LA IMAGEN 12.3.2.1 IMÁGENES OBTENIDAS POR PROYECCION Consiste en la manifestación directa de la interacción de alguna forma de radiación con un tejido: • Radiología convencional: Proyección de un haz de RX, a través del cuerpo humano, sobre una película sensible a esta radiación. La imagen médica obtenida es una medida de la atenuación de los RX en el tejido, tal como puede apreciarse en la figura 150. Figura 150. Placa de RX del tórax Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 147 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Radiología Digital: Los mismos principios de la radiología convencional, pero las imágenes se obtienen en formato digital. La Angiografía Digital por Sustracción (DSA), pertenece a esta clasificación y se emplea regularmente en medicina vascular para ver el estado de las arterias y las venas en tiempo real, empleando medios de contraste. La figura 151, muestra una imagen de este tipo. Figura 151. Angiografía Digital por Sustracción • Medicina nuclear: Es una medida de la localización y concentración de un isótopo radiactivo. Suministra información morfológica de un órgano, como también del funcionamiento de un proceso biológico. La figura152 presenta una imagen típica de medicina nuclear. Figura 152. Imagen de Medicina Nuclear Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 148 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Ultrasonido: Es un mapa de intensidades eco (reflejadas) como resultado de la interacción del pulso de ultrasonido con los tejidos. La figura 153, presenta imágenes de ecografía. Figura 153. Imágenes de ecografía 12.3.2.2 IMÁGENES OBTENIDAS POR RECONSTRUCCION Imagen indirecta obtenida en dos etapas: 1. Creación de las secciones o proyecciones de la imagen. 2. Generación de la imagen a partir de sus proyecciones. Las imágenes por reconstrucción son las siguientes: • Tomografía Computada: Las imágenes se generan con fuentes de RX. Se reconstruye la imagen a partir de los valores de atenuación de los distintos haces de RX medidos desde múltiples ángulos. La figura 154, muestra una imagen típica de TC. Figura 154. Imagen de TC Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 149 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • SPECT/PET: Tomografía por Emisión de Fotones Simples/Tomografía por Emisión de Positrones. Imágenes de medicina nuclear tomadas con la técnica de la tomografía computada. En el caso de SPECT, se introducen al cuerpo elementos radiactivos con desintegración Gamma (Rayos de fotones). En el caso de PET se introducen al cuerpo elementos radiactivos con desintegración Beta+ (Positrones). La figura 155, muestra este tipo de imágenes. Cerebros Normales Cerebros con Alzeimer Figura 155. Imágenes SPECT/PET • Imágenes por Resonancia Magnética Nuclear: Se fundamenta en la propiedad de los núcleos atómicos del cuerpo humano, que presentan un momento magnético que les hace actuar como imanes. Al colocar al paciente dentro de un campo magnético fuerte, los núcleos de Hidrogeno se alinean en la dirección éste, girando alrededor de esta dirección con una frecuencia proporcional al tipo de núcleo y a la magnitud del campo. Si se aplica un pulso de radio frecuencia con un ángulo determinado con respecto al campo estacionario, los núcleos con frecuencia de rotación igual a la del pulso de RF resonarán absorbiendo energía. Si a Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 150 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica continuación se elimina el pulso, los núcleos volverán a su estado original de alineación con el campo estático, emitiendo una señal de RF cuya intensidad y duración depende de la densidad y tipo de núcleo. La medición de estos parámetros puede procesarse posteriormente y utilizarse para generar imágenes que representan diferencias biológicas entre los tejidos. La figura 156, muestra una imagen obtenida con RMN. Figura 156. Imagen de RMN Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 151 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 13. EQUIPOS DE RAYOS X Los equipos de rayos X se utilizan para tomar radiografías. Una radiografía es una imagen registrada en una placa o película fotográfica. La imagen se obtiene al exponer dicha placa o película a una fuente de radiación de alta energía, comúnmente rayos X o radiación gamma procedente de isótopos radiactivos (Iridio 192, Cobalto 60, Cesio 137). Al interponer un objeto entre la fuente de radiación y la placa o película las partes más densas aparecen con un tono más o menos gris en función inversa a la densidad del objeto, como es el caso de los huesos en el cuerpo humano. Si la radiación incide directamente sobre la placa o película, se registra un tono negro, por la baja densidad, tal como sucede con los pulmones. Sus usos pueden ser tanto médicos, para detectar fisuras en huesos, como industriales en la detección de defectos en materiales y soldaduras tales como grietas y poros. La figura 157, muestra un equipo de RX utilizado para tomar una radiografía de tórax y la imagen resultante. Figura 157. Radiografía de tórax tomada con equipo de rayos X Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 152 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 13.1 PRINCIPIOS FÍSICOS DE LA GENERACIÓN DE LOS RX Los RX son ondas electromagnéticas ionizantes de origen no nuclear en el rango de 3 X 1017 hasta 5 X 1019 Hz, a los cuales se les considera fotones. Ionizantes significa que son capaces de arrancar electrones de sus orbitas y por lo tanto rompen enlaces y de origen no nuclear significa que esta radiación no proviene del núcleo de los átomos. La figura 158 muestra una comparación de la longitud de onda de los RX comparado con otros tipos de energía, tal como RF, microondas, luz infrarroja, luz visible, luz ultravioleta y rayos gamma. Figura 158. Longitud de onda de los RX comparada con otras energías Los RX se obtienen haciendo incidir un haz de electrones (e-) acelerados con alta velocidad sobre una estructura metálica que por lo general es una placa de tungsteno. La figura 159, muestra como se generan los RX. Los electrones incidentes se generan a partir del efecto termoiónico, que consiste en calentar un filamento de tungsteno, por medio de hacerle pasar una corriente eléctrica, produciéndose el efecto Joule. Al calentarse el filamento, los electrones de valencia de los átomos en la superficie de éste, abandonan esta órbita atómica y quedan libres, no perteneciendo entonces a ningún átomo del filamento, formándose una nube electrónica alrededor del filamento. Al perder electrones estos átomos se convierten en iones positivos, de ahí el nombre de efecto termiónico. Si a este filamento caliente se le conecta un alto voltaje DC negativo, por razones de la ley de cargas de Coulomb, los electrones que fueron excitados por el efecto termoiónico son repelidos con una gran fuerza. Al filamento negativo se le denomina Cátodo. El potencial positivo de la fuente DC Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com se 153 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica conecta a la placa del ánodo para atraer a los electrones expulsados del cátodo y así cerrar el circuito. Alto voltaje (-) Bobinas de aceleración Cátodo Rejillas de enfoque caliente Alto voltaje (+) Ánodo Haz electrónico incidente Fuente DC Alta Tensión (KV) Rayos X (Fotones) Figura 159. Generación de los RX Como los electrones repelidos se dispersan en el espacio en todas las direcciones es necesario dirigirlos hacia el blanco (Ánodo), por medio de unas rejillas polarizadas negativamente denominadas placas de enfoque. Una vez enfocados correctamente, los electrones incidentes se deben acelerar a alta velocidad para aumentar su energía cinética (1/2 m v2) y para ello se emplean unas bobinas cuyo campo magnético aumentan la velocidad. Al “chocar” los interacción de los electrones incidentes con los electrones y núcleos de los átomos del ánodo. 13.1.1 INTERACCION ELECTRONES INCIDENTES – ELECTRONES ANODO La grafica 160 ilustra lo que sucede cuando se presenta la interacción entre un electrón incidente proveniente de la nube electrónica del cátodo y un electrón perteneciente a un átomo de la placa del ánodo. Cuando el electrón incidente (1), entra dentro del campo eléctrico del electrón anódico de la orbita K (2), se presenta una enorme fuerza de repulsión que hace que el incidente rebote y el anódico salga expulsado de su orbita. En ese momento, un electrón anódico de Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 154 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica la orbita L (3) salta a llenar el vacío dejado por el electrón 2 y como en la orbita L posee un mayor nivel de energía que en la K, se libera entonces el excedente energético generándose una radiación en forma de fotón que constituye un rayo X. Electrón del ánodo expulsado Átomo del Ánodo Electrón incidente Electrón incidente rebotado Electrón del ánodo que abandona su orbita Fotón de RX característico Figura 160. Interacción electrón incidente con electrón anódico Este fenómeno que se acaba de explicar sucede en el mismo instante con millones de electrones incidentes y produce lo que se denomina la radiación característica de RX, que depende principalmente del tipo de material de la placa del ánodo. La energía del fotón de RX (EF), su frecuencia y longitud de onda se determinan así: • EF = EL - EK = h x f; (electrón-voltio, eV), donde h es la constante de Plank y f es la frecuencia de radiación del fotón. • h = 4.135 X 10-15 ; (eV x s), • f = EF / h, (Hz), • λ = c / f, (m); donde c, es la velocidad de la luz, • c = 3 X 108 , (m/s). Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 155 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 161, muestra la relación entre la intensidad relativa de la radiación y la longitud de onda de los RX generados por la interacción electrón-electrón, que como se puede observar solo tiene dos frecuencias o longitudes de onda, por eso esta radiación también recibe el nombre de espectro discreto o discontinuo. I n t e n s i d a d Rayos X característico para un ánodo de molibdeno a 35 KV r e l a ti v a Longitud de onda (nm) Figura 161. Espectro discreto de RX. 13.1.2 INTERACCION ELECTRONES INCIDENTES – NUCLEOS ANODO La grafica 162 ilustra lo que sucede cuando se presenta la interacción entre un electrón incidente proveniente de la nube electrónica del cátodo y un núcleo perteneciente a un átomo de la placa del ánodo. Cuando el electrón incidente (1, 2, 3), entra dentro del campo eléctrico del núcleo anódico, se presenta una enorme fuerza de atracción que hace que el incidente cambie su trayectoria y sufra un frenado. Como la velocidad es una cantidad vectorial, al cambiar la dirección del vector de los electrones incidentes, la energía cinética final (1/2 m v22) es menor a la inicial, antes de interactuar (1/2 m v12). En ese momento, se libera entonces el excedente energético del electrón incidente generándose una radiación en forma de fotón que constituye un rayo X. A esta radiación se le conoce como radiación de frenado. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 156 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Átomo del Ánodo Electrones incidentes Impacto con el núcleo. Máxima energía del fotón Interacción mediana con el núcleo. Moderada energía del Interacción fotón lejana con el núcleo. Mínima energía del fotón Figura 162. Interacción electrón incidente con núcleo anódico La figura 162 muestra las tres posibilidades de interacción entre los electrones incidentes y el núcleo de un átomo del ánodo: • Posibilidad uno: Impacto frontal. Máximo frenado. Esto le sucede al electrón incidente (1). La energía del fotón es: EF = 1/2 m v12 - 1/2 m v22 ; como v2 es cero en este caso, la energía del fotón es máxima, por lo tanto también lo será la frecuencia de radiación y mínima la longitud de onda. • Posibilidad dos: Interacción lejana. Mínimo frenado. Esto le sucede al electrón incidente (3). La energía del fotón es: EF = 1/2 m v12 - 1/2 m v22 ; como v2 es muy cercana a v1 en este caso, la energía del fotón es mínima, por lo tanto también lo será la frecuencia de radiación y máxima la longitud de onda. • Posibilidad tres: Interacción mediana. Frenado moderado. Esto le sucede al electrón incidente (2). En este caso, la energía del fotón es mediana, Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 157 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica por lo tanto también lo será la frecuencia de radiación y la longitud de onda. La figura 163, muestra la relación entre la intensidad relativa de la radiación y la longitud de onda de los RX generados por la interacción electrón-núcleo, que como se puede observar esta compuesto de infinitas frecuencias o longitudes de onda, por eso esta radiación también recibe el nombre de espectro continuo. Obsérvese como a mayor tensión aplicada en KV al ánodo, mayor en la intensidad energética de los fotones de RX generados. I n t e n s i d a d r e l a ti v a Longitud de onda (nm) Figura 163. Espectro continuo de RX. La figura 164, muestra los dos tipos de radiaciones que se generan en un tubo de RX, para un ánodo de tungsteno con tensión de 100 KV y un ángulo de inclinación de 13°. Con las técnicas actuales de diagnostico medico, en donde se trabajan con tensiones entre 30 KV y 150 KV, el espectro predominante es el continuo. Para el tungsteno, el espectro característico se presenta a los 69.5 KV únicamente. Es decir, para tensiones elevadas predomina el espectro continuo y para las bajas el característico. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 158 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica N u m e r o R e l a t i v o Radiación de frenado Radiación característica F o t o n e s Energía de los fotones (KeV) Figura 164. Radiación completa de un tubo de RX con placa de tungsteno. La siguiente tabla relaciona la energía de cada fotón con su frecuencia y longitud de onda asociada, como también el máximo espesor que es capaz de atravesar para el concreto, lead, tejido humano y aluminio. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 159 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 13.2 EL TUBO DE RAYOS X La figura 165, muestra el esquema de un tubo de RX comercial. FUENTE DC TUBO DE VACIO IB VF IF ......N......... E FOCO ACEITE CARCAZA RAYOS X Figura 165. Esquema de un tubo de RX comercial A continuación se describe cada una de las partes que componen al tubo de RX: • Cátodo (C): Filamento de tungsteno de 0.2 a 0.3 mm de diámetro, que al calentarse produce una nube de electrones por efecto termoiónico. Tiene una resistencia RF. • Fuente de Filamento: Produce la tensión VF, necesaria para calentar el filamento, por ley de Joule ([VF2 / RF] x t). Esta tensión es regulable entre 0 y 15 V. La corriente de filamento IF, varia entre 3 y 8 amperios. • Nube de electrones: NE, es la cantidad de electrones producidos por la tensión de filamento. • Ánodo (A): Construido de material de tungsteno, para soportar temperaturas elevadas. Tiene una superficie inclinada para direccionar mejor los RX y es giratorio para distribuir la temperatura en su superficie. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 160 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica En la practica, el ánodo en el rotor de un motor de inducción jaula de ardilla. • Fuente de DC: Fuente de alta tensión regulable entre 25 y 200 KV que dispara los electrones de la nube hacia el ánodo. • Corriente del tubo (IB): Solo el 1% de los electrones incidentes que llegan al ánodo chocan o interactúan con los átomos para producir RX. El 99% restante generan la corriente IB que circula por el circuito de alta tensión, determinando los mA del tubo. • Tubo de vacío: El Cátodo y el Ánodo están encerrados dentro de un tubo de vacío perfecto, para evitar la combustión por el calentamiento del filamento. • Aceite: El tubo se encuentra refrigerado en un baño de aceite debido a la gran disipación calórica. • Carcaza: Envoltura de plomo que forma una pantalla de protección frente a los RX no deseados, que se dispersan dentro del mismo y no fueron direccionados. • Filtro (F): Absorbe la radiación menos energética, es decir los fotones de mayor longitud de onda que pudieran causar radiaciones innecesarias dentro del paciente, ya que no lo atravesarían. Se utiliza aluminio cuando la tensión es menor a 150 KV y cobre cuando es mayor. • Diafragma (D): Regula las dimensiones del haz útil, se le denomina colimador. Se construye con una serie de placas metálicas (aluminio o cobre) con agujeros en el centro. Su propósito es absorber la radiación que no tiene dirección adecuada. • Foco: Se denomina también punto focal o blanco, al área (mm2) del ánodo donde chocan los electrones incidentes interactuando con la estructura atómica de este y en donde se generan los fotones de RX. Como el haz de electrones incide en un área muy pequeña, el calor generado en este punto es enorme, pudiendo llegar a fundirse el material del ánodo en este punto, por ello el foco debe tener un tamaño correspondiente a la carga que debe soportar. Los ánodos son giran a Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 161 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica velocidades de 3600 rpm para pistas focales de 21 cm. de longitud en tubos normales. En los supertubos, la velocidad de rotación aumenta a 10.800 rpm, con pistas focales de 53 cm. Cada exposición radiográfica exige del foco cierta carga durante un tiempo determinado, expresada en W/s o en unidades térmicas (UT), ya que la mayor parte de la energía se convierte en calor. La figura 166, muestra la relación entre la corriente del tubo IB y la corriente de filamento IF para una familia de curvas a diferentes KV y para un foco de 1mm x 1mm. De la grafica se concluye que mientras a 80 KV, el tubo soporta corrientes de 550 mA con corrientes de filamento de 6.2 A, a 150 KV, la máxima corriente del tubo se baja a 280 mA, para corriente de filamento de solo 5.4 A, esto para respetar la máxima carga térmica que puede soportar el ánodo. Para identificar los tubos de RX, se menciona en primer lugar el nombre patentado en forma abreviada, por ejemplo Ro para Rotalix, seguido de la máxima tensión permitida en KV, y a continuación la potencia de los focos, por ejemplo 12 KW para el foco fino y 27 KW para el grueso. Entonces el tubo queda identificado así: Ro125/12/27. IB (mA) Foco (1mmx1mm) IF (A) Figura 166. Relación IB versus IF de un tubo de RX comercial Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 162 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Es importante tener en cuenta que la capacidad de penetración del haz de RX se controla mediante los KV, es decir a más KV mayor penetración y la cantidad de la radiación, es decir el número de fotones de RX depende de IB, que a su vez depende de VF. La siguiente tabla muestra los KV, el tipo de material del ánodo, el tipo de fuente de RX y el promedio de energía de los fotones de acuerdo a la aplicación. 13.3 FUNCIONAMIENTO DEL EQUIPO DE RX La figura 167 muestra el diagrama de bloques funcional de un equipo de RX. Se alimenta de la red eléctrica de 60 Hz, ya sea en forma monofásica o en forma trifásica. Esto depende de la cantidad de KV requerido por el tubo. Por ejemplo para unidades de RX odontológicas, hasta 60 KV, se alimenta monofásicamente, y para equipos de radiología general, hasta 150 KV, se alimenta trifásicamente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 163 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica TRANSFORMADOR DE BAJA TENSIÓN CIRCUITO DE TEMPORIZACION (G) PARA EL FILAMENTO DE LA VALVULA CONTROL DE TEMPERATURA DEL ANODO RECTIFICADORA RED ELÉCTRICA MONOFASICA O TRIFASICA AUTO TRANSFORMADOR 1 X 120V/ 3 X 220 V / 60 Hz TRANSFORMADOR (A) DE ALT A TENSIÓN (B) RECTIFICADOR CON VALVULAS DE VACIO (E) TRANSFORMADOR DE BAJA TENSIÓN DEL FILAMENTO (C) CONTROL DE CORRIENTE DEL FILAMENTO (D) TUBO DE RAYOS X (F) Figura 167. Diagrama de bloques de un equipo de RX comercial La figura 168, muestra el plano electrónico básico de un equipo de RX monofásico, identificando la parte correspondiente con el diagrama de bloques. D C F G B E A Figura 168. Plano electrónico de un equipo de RX monofásico Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 164 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica A continuación se hará una breve descripción de la función de cada una de las partes que componen a un equipo de RX. 13.1 TRANSFORMADOR DE ALTA TENSIÓN El transformador es un dispositivo que se encarga de reducir o elevar el voltaje de corriente alterna que tiene a su entrada en otro diferente que entrega a su salida. Se compone de un núcleo de hierro sobre el cual se han arrollado varias espiras (vueltas) de alambre conductor, tal como se muestra en la figura 169. Figura 169. Constitución de un transformador Al conjunto de vueltas se les denominan bobinas y se les identifican como bobina primaria a aquella que recibe el voltaje de entrada y bobina secundaria a aquella que entrega el voltaje transformado. El principio de funcionamiento del transformador es el siguiente: • La Bobina primaria recibe un voltaje alterno que hará circular, por ella, una corriente alterna. • Esta corriente inducirá un flujo magnético en el núcleo de hierro. • Como el bobinado secundario está arrollado sobre el mismo núcleo de hierro, el flujo magnético circulará a través de las espiras de éste. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 165 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Al haber un flujo magnético que atraviesa las espiras del secundario, se generará por el alambre del secundario una tensión. En este bobinado secundario habría una corriente si hay una carga conectada. La razón de transformación del voltaje entre el bobinado primario y el secundario depende del número de vueltas que tenga cada uno y se puede calcular mediante la siguiente expresión: Vs = Ns x Vp / Np Un transformador puede ser elevador, cuando Ns es mayor que Np y reductor cuando Ns es menor de Np. En los equipos de RX, el transformador de alta tensión es elevador, ya que se encarga de elevar la baja tensión entregada por el autotransformador, a los niveles del voltaje (KV) requeridos para obtener el nivel de penetración de los RX requeridos de acuerdo al grosor de los tejidos que deben atravesar para llegar a la placa de radiografía. 13.2 AUTOTRANSFORMADOR El autotransformador es un transformador donde una parte del devanado es común tanto al primario como al secundario. El principio de funcionamiento es el mismo que el de el transformador común, entonces la relación de transformación entre las tensiones y las corrientes y el número de vueltas se mantiene. Las corrientes primaria y secundaria están en oposición y la corriente total que circula por las espiras en común es igual a la diferencia de la corriente del devanado de baja tensión y el devanado de alta tensión. Para que un autotransformador funcione adecuadamente, los dos devanados deben tener el mismo sentido de bobinado. Los autotransformadores tienen la ventaja sobre los transformadores comunes, de un peso y costo menor. Otra ventaja es la de no necesitar aislamiento entre los bobinados primario y secundario. Sin embargo esto trae la desventaja de que el bobinado primario no es independiente del secundario. Esto causa peligro para una persona, pues entre tierra y el hilo común del secundario y el primario, existe la tensión del primario. En los equipos de RX, se utiliza un autotransformador con taps que permita seleccionar diferentes niveles de tensión que alimentaran al devanado primario del transformador de alta tensión y así obtener diferentes niveles de KV DC de Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 166 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica acuerdo al tipo de placa de RX que se requiera tomar al paciente. La figura 170 muestra los autotransformadores reductores y elevadores respectivamente. AUTOTRANSFORMADOR REDUCTOR AUTOTRANSFORMADOR ELEVADOR Figura 170. Tipos de autotransformadores En los equipos de RX se emplean los autotransformadores reductores. 13.3 TRANSFORMADOR DE BAJA TENSIÓN DEL FILAMENTO DEL CATODO Es el encargado de alimentar en baja tensión el circuito de control de corriente de filamento del cátodo del tubo de RX. 13.4 TRANSFORMADOR DE BAJA TENSIÓN DEL FILAMENTO DE LAS VALVULAS RECTIFICADORAS Es el encargado de alimentar en baja tensión el circuito de control de corriente de filamento del cátodo de las válvulas rectificadoras. 13.5 CONTROL DE LA CORRIENTE DE FILAMENTO Aunque en la figura de la grafica 168 este control se propone por pasos y no lineal y se regula la corriente del filamento del cátodo del tubo de RX mediante el número de espiras del primario del transformador correspondiente con resistencias en serie, en los equipos de última generación se utiliza control de fase empleando tiristores, ya que este tipo de control es lineal y es mas eficiente. La figura 171, muestra el control de la corriente de filamento con tiristores. El voltaje RMS en el filamento esta determinado por el ángulo de disparo α de los tiristores mediante la siguiente ecuación: VRMS = Vm/√2 [1/π (π – α + (sen2α)/2]1/2 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 167 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica FORMA DE ONDA DEL VOLTAJE EN EL FILAMENTO (FILAMENTO) Figura 171. Control de corriente de filamento mediante control de fase 13.6 CIRCUITO DE TEMPORIZACION Es un circuito de control temporizado con característica ON/OFF (todo o nada) en donde se determina el tiempo de exposición, es decir durante cuanto tiempo el equipo producirá RX. Al terminarse el tiempo programado para la toma de la radiografía por parte del técnico radiólogo, el circuito de temporización abre un contacto normalmente cerrado que conecta al secundario del autotransformador con el primario del transformador de alta tensión y cesa entonces la radiación de RX. 13.7 CIRCUITO DE CONTROL DE LA TEMPERATURA DEL ANODO Es un circuito de control con característica ON/OFF (todo o nada), que abre un contacto normalmente cerrado que se encuentra en serie con el contacto normalmente cerrado del circuito temporizador y desconecta al primario del transformador de alta tensión cuando la temperatura de la placa del ánodo sobrepasa un valor predeterminado por el fabricante para protegerlo por exceso de carga térmica. 13.8 CIRCUITO RECTIFICADOR 13.8.1 VALVULAS RECTIFICADORAS DE VACIO En los equipos de RX, se utiliza como dispositivo rectificador a las válvulas rectificadoras de vacío, ya que estas soportan grandes tensiones de polarización inversa, algo que por ahora, los diodos semiconductores son incapaces de alcanzar. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 168 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La válvula rectificadora se denomina también válvula termoiónica que consiste en un componente electrónico basado en la propiedad que tienen los metales en caliente de liberar electrones desde su superficie. Se usó ampliamente en la electrónica analógica y digital antes de la invención del transistor, y sobrevive en aplicaciones específicas, como es el caso de los equipos de RX. La válvula termoiónica más simple está constituida por una ampolla de vidrio, similar a la de las lámparas de incandescencia, a la que se le ha practicado el vacío y en la que se hallan encerrados dos electrodos, denominados cátodo y ánodo, tal como se muestra en la figura 172, con su símbolo clásico. Figura 172. Válvula rectificadora de vacío Físicamente, el cátodo, consiste en un filamento de wolframio, recubierto por una sustancia rica en electrones libres, que se calienta mediante el paso de una corriente. El ánodo está formado por una placa metálica que rodea al filamento a una cierta distancia y a la que se aplica un potencial positivo. Por constar de dos electrodos a la válvula antes descrita se le denomina diodo. En tanto en cuanto que la función de cátodo es realizada directamente por el filamento, se trata de una válvula de caldeo directo. Cuando se quieren obtener mayores corrientes a través de la válvula y un aislamiento eléctrico entre la fuente de corriente de caldeo del filamento y la de ánodo-cátodo, se utiliza un cátodo independiente constituido por un tubito metálico revestido o "pintado" con algún material rico en electrones libres, como el óxido de torio, que rodea el filamento, aislado eléctricamente, pero muy Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 169 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica próximo a él para poder calentarlo adecuadamente. En este caso la válvula se denomina de caldeo indirecto, pudiendo entonces la corriente del caldeo ser incluso alterna. En este tipo de válvulas el filamento solo es el elemento calefactor y no se considera un electrodo activo. Al estar los filamentos aislados se pueden conectar juntos (en serie o paralelo) los filamentos de todas las válvulas del equipo, lo que no es posible con cátodos de caldeo directo. Si se agregan otros electrodos entre ánodo y cátodo - llamados rejillas - se puede controlar o modular el flujo de electrones que llegan al ánodo, de ahí la denominación de válvula. Debido al hecho de que la corriente por el interior de la válvula solo puede circular en un sentido, una de las aplicaciones de las válvulas termoiónicas es su utilización como rectificador, es decir que los electrones liberados por el cátodo caliente solo pueden llegar al ánodo cuando este es positivo con respecto a este. Con una corriente alterna aplicada a la válvula entre el cátodo y el ánodo, durante el semiciclo en que el ánodo es negativo no hay circulación de corriente y durante el semiciclo que es positivo si hay circulación de corriente. 13.8.2 RECTIFICADOR TRIFASICO DE MEDIA ONDA No se considerará en este apartado los rectificadores monofásicos de media onda y onda completa ya que están suficientemente explicados en la literatura de electrónica general, mas bien se estudiaran los rectificadores trifásicos. La figura 173 muestra como a partir de la red trifásica AC se rectifica y se entrega corriente continua a motores DC, hornos de inducción, hornos de fundición, procesos electrolíticos de galvanoplastia y tubos de RX. Las ventajas de los rectificadores trifásicos con respecto a los monofásicos son las siguientes: • Mayor potencia de salida • Mayor tensión DC a la salida • Menor rizado en la tensión de salida • Menores exigencias para el filtro de salida • Mejor factor de potencia Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 170 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 173. Concepción de un rectificador trifásico La figura 174 muestra un rectificador trifásico de media onda con carga resistiva. N Figura 174. Rectificador trifásico de media onda con carga resistiva Con respecto a la figura 174 se pueden hacer las siguientes observaciones: • El transformador empleado es del tipo estrella – estrella (Y-Y). • Un transformador trifásico equivale a conectar a 3 monofásicos. • El punto común de los arrollamientos secundarios es el neutro, N. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 171 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Si solo se usara un arrollamiento secundario, se tendría un rectificador monofásico de media onda. • El rectificador trifásico de media onda consiste en conectar tres rectificadores monofásicos de media onda en paralelo. • Cuando cualquiera de los rectificadores conduce a la carga le queda conectada la fase respectiva, por lo tanto en este tipo de rectificador, se trabaja con tensiones de fase. • Solo un rectificador conduce a la vez, ya que si lo hicieran dos o tres al mismo tiempo se presentaría un cortocircuito. La figura 175 muestra como se calcula el valor DC de la tensión de salida del rectificador de media onda con carga resistiva, donde VMF, es el voltaje pico del voltaje de fase del secundario del transformador de alta tensión. VMF VMF VDC = VMF VMF VMF Figura 175. Onda de salida del Rectificador trifásico de media onda con carga resistiva. Recordando que el valor DC de la tensión de salida de un rectificador monofásico de onda completa es 2VMF / π, entonces, la tensión de salida del rectificador trifásico de media onda es 1.3 veces mas grande, es decir, al Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 172 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica emplear un rectificador trifásico de media onda se logra un aumento del 30%, lo cual justifica utilizarlo. 13.8.3 RECTIFICADOR TRIFÁSICO DE ONDA COMPLETA La figura 176 muestra el circuito de un rectificador trifásico de onda completa, denominado también puente rectificador trifásico. Este circuito rectificador tiene las siguientes características: • Se emplean 6 rectificadores. • Dos rectificadores conducen al mismo tiempo y aplican a la carga tensiones de línea, no de fase, por lo tanto, el valor DC de la tensión en la carga será mayor que el producido por el puente rectificador de media onda. • Cuando se emplea transformador, el secundario se conecta en estrella, para aumentar las tensiones de línea. • Presenta menor tensión de rizado. • La frecuencia es 6 veces mayor que la de la red, es decir que en Colombia, la frecuencia de la onda de salida de este tipo de rectificador es de 360 Hz. Figura 176. Puente rectificador trifásico Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 173 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El proceso de conducción es el siguiente: 1) Cuando D1 conduce la corriente sale de la fase R, pasa por D1, atraviesa la carga y cuando retorna a través del diodo D5, la tensión aplicada a la carga es la tensión de línea VRS. Cuando retorna a través del diodo D6, la tensión aplicada a la carga será ahora la tensión de línea VRT. 2) Cuando D2 conduce la corriente sale de la fase S, pasa por D2, atraviesa la carga y cuando retorna a través del diodo D6, la tensión aplicada a la carga es la tensión de línea VST. Cuando retorna a través del diodo D4, la tensión aplicada a la carga será ahora la tensión de línea VSR. 3) Cuando D3 conduce la corriente sale de la fase T, pasa por D3, atraviesa la carga y cuando retorna a través del diodo D5, la tensión aplicada a la carga es la tensión de línea VTS. Cuando retorna a través del diodo D4, la tensión aplicada a la carga será ahora la tensión de línea VTR. La figura 177 muestra finalmente la tensión rectificada en la carga, con la información de que diodos conducen por cada intervalo y por lo tanto sirve para calcular el valor DC de la tensión de salida del puente rectificador trifásico con carga resistiva. VMF VDC = VRS VMF VMF Figura 177. Tensión de salida del puente rectificador trifásico Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 174 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Se puede concluir que la tensión DC del puente rectificador trifásico es el doble de la del rectificador trifásico de media onda con lo que se logra un aumento del 100%, lo cual justifica utilizarlo. 13.9 ESPECIFICACIONES TECNICAS DE LOS EQUIPOS DE RX COMERCIALES 13.9.1 EQUIPOS PORTATILES Diseñado para las áreas en radiología, salas de recién nacidos, salas de cirugía, emergencia, veterinaria. Fácil desplazamiento y operación. Las especificaciones son las siguientes: • Marca: Perlong Group • Modelo: PLX102 • Fuente de poder: 2.96KW • Tubo radiográfico: ánodo fijo • Rectificación de onda completa monofásica • Voltaje del tubo: 40~90KV • Corriente del tubo: 50~90KV 15mA, 50~90KV 30mA, 40~80KV 50mA • Tiempo de exposición: 50-90KV 15mA 0.1-6.3s, 50-90KV 30mA 0.1-6.3s, 40-80KV 50mA 0.1-1.5s • Fuente de alimentación: 110V/60Hz Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 175 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 13.9.2 EQUIPOS FIJOS Cuenta con un generador radiográfico digital de diseño compacto y de alto desempeño con sistema contactor SCR, sistema para protección de tubo de estado sólido y timer digital que contribuye a mejorar la calidad de la imagen, dando como resultado imágenes con alto contenido de detalles anatómicos. Este sistema puede ser utilizado en hospitales, clínicas, centros médicos, unidades de urgencias, salas de ortopedia y traumatología general, adulto y pediátrico. Las especificaciones son las siguientes: • Marca: AMERICOMP • Modelo: Spectra 325D • Capacidad de generación de rayos x desde 50mA hasta 300mA a 125Kvp Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 176 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Contactor SCR con sistema automático de seguridad (Back-up) electromagnético que abre y cierra el circuito a cero (0) voltaje, previendo cualquier daño por pico de voltaje en el tubo de rayos x. • Sistema de alarmas para técnicas erróneas de miliamperaje, kilovoltaje y tiempo de exposición, este sistema previene daños en el equipo por fallas en el suministro eléctrico, cortos circuitos o mal manejo del operario. • Sistema digital de mAs. Optimiza el tiempo del operario en la exposición de toma de estudios. • Sistema compensatorio de línea de 8 pasos, esta característica técnica permite operar el equipo en condiciones criticas de voltaje, pudiendo estabilizar la corriente exigida por el fabricante. • Selector de miliamperaje de 5 pasos, 2 de foco corto (50S,100S) y 3 para foco largo (150L,200L,300L). • Timer digital para el tiempo de exposición con 23 pasos de 1/120 a 6 segundos. Esta aplicación permite tomar estudios radiográficos a todo tipo de pacientes, incluso obesidad critica. • Selector de kilovoltaje de 40 a 125Kvp, ajustable en incrementos de 2 kilovotios. • Sistema para doble bucky, de mesa y de pared (soporte de tórax). • Panel de control de vinilo de alta resistencia fácil de limpiar. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 177 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14. EQUIPOS DE TOMOGRAFIA AXIAL COMPUTARIZADA Una de las aplicaciones más sobresaliente de los RX en imágenes médicas la constituye indudablemente la tomografía computada de RX. Tomografía viene del griego tomos que significa corte o sección y de grafía que significa representación gráfica. Por tanto tomografía es la obtención de imágenes de cortes o secciones de algún objeto. La palabra axial significa "relativo al eje". Plano axial es aquel que es perpendicular al eje longitudinal de un cuerpo. La tomografía axial computarizada o TAC, aplicada al estudio del cuerpo humano, obtiene cortes transversales a lo largo de una región concreta del cuerpo (o de todo él). Computarizar significa someter datos al tratamiento de una computadora. LA TAC es una exploración de rayos X que produce imágenes detalladas de cortes axiales del cuerpo. En lugar de obtener una imagen como la radiografía convencional, la TAC obtiene múltiples imágenes al rotar alrededor del cuerpo. Una computadora combina todas estas imágenes en una imagen final que representa un corte del cuerpo como si fuera una rodaja. Esta máquina crea múltiples imágenes en rodajas (cortes) de la parte del cuerpo que está siendo estudiada. Se trata de una técnica de visualización por rayos X. Se puede decir entonces, que es una radiografía de una fina rodaja obtenida tras cortar un objeto. En la radiografía se obtiene una imagen plana (en dos dimensiones) de un cuerpo (tridimensional) haciendo pasar a través del mismo un haz de rayos X. Entre las ventajas de la TAC se encuentra que es una prueba rápida de realizar, que ofrece nitidez de imágenes que todavía no se han superado con la resonancia magnética nuclear como es la visualización de ganglios, hueso, etc. y entre sus inconvenientes se cita que la mayoría de veces es necesario el uso de contraste intravenoso y que al utilizar rayos X, se reciben dosis de radiación ionizante, que a veces no son despreciables. Por ejemplo en una TAC abdominal, se puede recibir la radiación de más de 50 radiografías de tórax, el equivalente de radiación natural de más de cinco años. La figura 178, muestra el estudio completo de una tomografía computada, de donde se desprende el siguiente diagnostico: Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 178 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • Imagen A: Angio-Tac que demuestra disección de aspecto agudo de la aorta torácica descendente, con permeabilidad del falso lumen y flap de disección (flecha); • Imagen B: Sin uso de contraste se demuestra hemopericardio (flecha discontinua) y leve hemotórax (flecha continua), lo que traduce complicación por rotura; • Imagen C: Reconstrucción tridimensional de la aorta en toda su longitud, demostrando que el compromiso por el flap es sólo de aorta torácica descendente con extensión a segmento abdominal infrarrenal, por lo que constituye una disección tipo B complicada por rotura. Figura 178. Imágenes TAC de disección aguda complicada en aorta descendente (www.scielo.cl/scielo.php) Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 179 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14.1 PRINCIPIOS DE TOMOGRAFÍA AXIAL COMPUTARIZADA 14.1.1 CONCEPTO DE INTENSIDAD DE RADIACION (I) y ATENUACION (µ) La cantidad de radiación (I), de RX que penetra un tejido, depende del número atómico de los elementos químicos que lo componen. Materiales con número atómico grande absorberán, es decir, atenuaran una mayor radiación que los de menor número, por ser más densos. Es decir que los tejidos con mayor coeficiente de atenuación, µ, absorberán mayor radiación que los de menor coeficiente. Este comportamiento se refleja en la radiología convencional, en donde, la proyección de los objetos más densos (µ altos), como por ejemplo los huesos, impresionan menos la placa fotosensible, que los de bajo coeficiente de atenuación, por ejemplo los pulmones. De ahí que en la placa los huesos se vean blancos y los pulmones oscuros. La figura 179, muestra la relación entre las radiaciones de entrada y salida al tejido con el grosor de este y su coeficiente de atenuación, µ. HAZ INCIDENTE (Io eV) µ X (cm) I = I0 e - µx OBJETO (TEJIDO) HAZ EMERGENTE (ATENUADO) (I eV) Figura 179. Concepto de atenuación de RX en un tejido Como puede observarse, la radiación a la salida del tejido (I), depende de la intensidad de la radiación de entrada (I en eV), del espesor del tejido (x en cm) y del coeficiente de atenuación (µ). Este coeficiente de atenuación es una propiedad física de cada tejido y sus unidades son cm-1. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 180 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14.1.2 PRINCIPIO DE FUNCIONAMIENTO DE LA TOMOGRAFÍA COMPUTADA La figura 180 muestra la forma más sencilla de tomografía computarizada que consiste en el uso de un haz de rayos X (Io) finamente colimado y un único detector. La fuente de rayos X y el detector están conectados de tal modo que se mueven de forma sincronizada. Cuando el conjunto fuente-detector efectúa un barrido, o traslación, del paciente, las estructuras internas del cuerpo atenúan el haz de rayos X según sus respectivos valores de número atómico y densidad de masa. La intensidad de radiación detectada variará, formando un perfil de intensidad (I) llamado proyección. Al concluir la traslación, el conjunto fuentedetector regresa a su posición de partida, y el conjunto completo gira para iniciar una segunda traslación. Durante ésta, la señal del detector vuelve a ser proporcional a la atenuación del haz de rayos X de las estructuras anatómicas, de lo que se obtiene un segundo resultado de exploración. Figura 180. Principio de la Tomografía Computada Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 181 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Si se repite este proceso un número elevado de veces, se generarán numerosas proyecciones. Estas proyecciones no se perciben visualmente, sino que se almacenan en un computador. Después, se procesan y estudian sus patrones de superposición para reconstruir una imagen final de las estructuras anatómicas. La superposición de las proyecciones no se produce como podría imaginarse en primera instancia. La señal del detector durante cada traslación se registra en incrementos de un máximo de 1.000. El valor de cada incremento está relacionado con el coeficiente de atenuación de los rayos X que corresponde al trayecto total de la radiación por el tejido. Mediante el empleo de ecuaciones simultáneas se obtiene finalmente una matriz de valores representativa de la sección transversal de la estructura sometida a examen. A este principio de tomografía se le denomina de primera generación, ya que fue el primer sistema desarrollado en 1970, por G. N. Hounsfield. 14.1.3 GENERACIONES DE TOMOGRAFÍA COMPUTADA • PRIMERA GENERACIÓN: (Traslación – Rotación) El funcionamiento se basa en un tubo de Rx y un detector, este sistema hace el movimiento de translación rotación. Para obtener un corte tomográfico son necesarias muchas mediciones y, por tanto muchas rotaciones del sistema, lo que lleva a tiempos de corte muy grandes (superiores a 5 minutos). Se usó para tomografías de cráneo. La figura 181, muestra el principio de esta primera generación. Figura 181. Tomografía computada de primera generación Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 182 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • SEGUNDA GENERACIÓN: (Traslación – Rotación) En esta generación se utilizan varios detectores y un haz de RX en abanico, lo que aumentaba la radiación dispersa, con esto se consigue que el tiempo de corte se reduzca entre 20 y 60 seg. La figura 182, muestra el principio de esta segunda generación. Figura 182. Tomografía computada de segunda generación • TERCERA GENERACIÓN: (Rotación – Rotación) El tubo de RX y la matriz de detectores giraban en movimientos concéntricos alrededor del paciente. Como equipos de sólo rotación, los escáneres de tercera generación eran capaces de producir una imagen por segundo. El escáner de TC de tercera generación utiliza una disposición curvilínea que contiene múltiples detectores y un haz en abanico. El número de detectores y la anchura del haz en abanico, de entre 30 y 60° y el haz en abanico y la matriz de detectores permiten ver al paciente completo en todos los barridos. La disposición curvilínea de detectores se traduce en una longitud constante de la trayectoria del conjunto fuente-detector, lo que ofrece ventajas a la hora de reconstruir las imágenes. Esta característica de la matriz de detectores de tercera generación permite además obtener una Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 183 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica mejor colimación del haz de RX, con la reducción de la radiación dispersa. La figura 183, muestra el principio de esta tercera generación. Figura 183. Tomografía computada de tercera generación • CUARTA GENERACIÓN: (Rotación – Estacionaria) Los escáneres de cuarta generación poseen sólo movimiento rotatorio. El tubo de RX gira, pero la matriz de detectores no. La detección de la radiación se realiza mediante una disposición circular fija de detectores. El haz de rayos X tiene forma de abanico, con características similares a las de los haces usados en equipos de tercera generación. Estas unidades alcanzan tiempos de barrido de 1 segundo y pueden cubrir grosores de corte variables, así como suministrar las mismas posibilidades de manipulación de la imagen que los modelos de generaciones anteriores. La matriz de detectores fijos de los escáneres de cuarta generación no produce una trayectoria de haz constante desde la fuente a todos los detectores, sino que permite calibrar cada detector y normalizar su señal durante cada barrido. La figura 184, muestra el principio de esta cuarta generación. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 184 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Estacionario Figura 184. Tomografía computada de cuarta generación • QUINTA GENERACIÓN: (Estacionario – Estacionaria) En esta clase de TC hay múltiples fuentes fijas de RX que no se mueven y numerosos detectores también fijos. Son muy caros, muy rápidos y con tiempos de corte muy pequeños. No se emplearon ampliamente. La figura 185, muestra el principio de esta quinta generación. Figura 185. Tomografía computada de quinta generación Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 185 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica • SEXTA GENERACIÓN: Se basan en un chorro de electrones. Es un cañón emisor de electrones que posteriormente son reflexionados (desviados) que inciden sobre láminas de tungsteno. El detector esta situado en el lado opuesto del Gantry por donde entran los fotones. Consigue 8 cortes contiguos en 224 mseg. Apenas se utilizaron, eran muy costosos y enormes, poco útiles. La figura 186, muestra el principio de esta sexta generación. Figura 186. Tomografía computada de sexta generación • SEPTIMA GENERACIÓN: HELICOIDAL En estos sistemas el tubo de RX y los detectores se montan, sobre anillos deslizantes y no se necesitan cables para recibir electricidad o enviar información recibida. Esto permite una rotación completa y continua del tubo y detectores. La camilla de exploración, se desplaza con una velocidad constante. El haz de RX traza un dibujo en forma de hélice sobre la superficie del paciente, mientras se adquieren inmediatamente los datos de un volumen de su anatomía, por esto se denomina TC volumétrico o helicoidal. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 186 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Las imágenes o cortes axiales se reconstruyen a partir de los datos obtenidos en cada uno de los ciclos del TC helicoidal, también puede funcionar como un TC convencional. Fue introducida por Siemens en el año 1990, actualmente casi todos los equipos de TC que se venden son helicoidales, los tiempos de exploración son de 0.7 y 1 segundo por ciclo. La figura 187, muestra el principio de esta séptima generación. Figura 187. Tomografía computada de séptima generación (Helicoidal) Las características de la tomografía helicoidal son las siguientes: - Tiempos de corte superrápidos - Alta calidad de la imagen - Tubo de RX grande y eficiente - Detectores de estado sólido. Semiconductores muy eficientes. - Computadores con capacidad de trabajo en multitareas y procesamiento en paralelo. La tomografía helicoidal ha permitido la obtención de nuevas imágenes en los siguientes casos: - Detección de nódulos pulmonares - Colonoscopia virtual para detección no invasiva de pólipos. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 187 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica - Multifase y estudios de perfusión. - Angiografía periférica - Angiografía coronaria no invasiva La figura 188, muestra una colección de imagines tomadas con tomografía helicoidal en donde se aprecia la calidad y nitidez de estas. Figura 188. Imágenes obtenidas con tomografía helicoidal 14.2 COMPONENTES DE UN SISTEMA DE TOMOGRAFÍA COMPUTADA Sea cual sea el tipo de tomografía que se utilice, en su diseño cabe distinguir cinco componentes principales: el gantry, el computador de procesamiento de datos, la consola del operador, la mesa de paciente y la impresora láser. La figura 189, muestra el diagrama de bloques básico del sistema de tomografía computada, la figura 190, el esquema real y su distribución en la sala de radiología y la figura 191, un sistema comercial. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 188 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 189. Diagrama de bloques básico de un sistema de tomografía computada Gantry Impresora Laser Mesa paciente Consola Figura 190. Distribución en la sala de radiología del sistema de tomografía computada Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 189 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 191. Sistema comercial de tomografía computada 14.2.1 GANTRY Contiene un tubo de rayos X, la matriz de detectores, el generador de alta tensión y los colimadores. Estos subsistemas se controlan mediante órdenes electrónicas transmitidas desde la consola del operador, y transmiten a su vez datos al ordenador con vistas a la producción y análisis de las imágenes obtenidas. La figura 192, muestra la fotografía interna de un gantry, en donde la T señala al tubo de RX y la D a los detectores de RX. Tubo de rayos x. En la mayoría de los tubos se usan rotores de alta velocidad para favorecer la disipación del calor. Los escáneres de TC diseñados para la producción de imágenes con alta resolución espacial contienen tubos de RX con punto focal pequeño con tamaños de 0.5 x 1.5 mm y 1.0 x 2.5 mm. Los requerimientos de potencia son 120 KV con corrientes del tubo entre 200 y 500 mA, produciendo RX con energías entre 30 y 129 keV. Conjunto de detectores. Los primeros escáneres de TC tenían un solo detector. Los más modernos utilizan numerosos detectores, en disposiciones Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 190 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica que llegan hasta contener 2.400 elementos de dos categorías: detectores de centelleo y detectores de gas. Figura 192. Fotografía interna de un gantry de TC de cuarta generación Colimación. En TC a veces se utilizan dos colimadores. El primero se monta en la cubierta del tubo o en sus proximidades, y limita el área del paciente que intercepta el haz útil, determinando así el grosor del corte y la dosis de radiación recibida por el paciente. Este colimador prepaciente suele constar de varias secciones que permiten obtener un haz de rayos X casi paralelo. Un ajuste inapropiado de los colimadores prepaciente origina un exceso innecesario de dosis de radiación en el paciente durante la TC. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 191 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El segundo colimador (pospaciente), restringe el campo de RX visto por la matriz de receptores. Este colimador reduce la radiación dispersa que incide sobre los detectores. Generador de alta tensión. Todos los escáneres de TC funcionan con alimentación trifásica o de alta frecuencia (5 a 50 KHz). Así, admiten velocidades superiores del rotor del tubo de RX y los picos de potencia característicos de los sistemas pulsátiles. 14.2.2 CAMILLA DE PACIENTE Sostiene al paciente en una posición cómoda, está construida con un material de bajo número atómico, como fibra de carbono. Dispone de un motor que acciona la camilla con suavidad y precisión para lograr una posición óptima del paciente durante el examen, en particular en técnicas de TC espiral. Si la posición del paciente no es exacta, tal vez se efectúen barridos repetidos de un mismo tejido, o se dejen secciones anatómicas sin examinar. 14.2.3 COMPUTADOR La tomografía computarizada no sería posible si no se dispusiera de un computador digital ultrarrápido. Se requiere resolver simultáneamente del orden de 30.000 ecuaciones; por tanto, es preciso disponer de una máquina de gran capacidad. Con todos estos cálculos el ordenador reconstruye la imagen. La mayoría de los computadores requieren un entorno especial y controlado; en consecuencia, muchas instalaciones de TC deben disponer de una sala contigua dedicada al equipo informático. En la sala del computador se han de mantener condiciones de humedad y temperatura. 14.2.4 CONSOLA DE CONTROL Numerosos escáneres de TC disponen de dos consolas, una para el técnico que dirige el funcionamiento del equipo y la otra para el radiólogo que consulta las imágenes y manipula su contraste, tamaño y condiciones generales de presentación visual. La consola del operador contiene dispositivos de medida y control para facilitar la selección de los factores técnicos radiográficos adecuados, el movimiento mecánico del gantry y la mesa del paciente y los mandatos comunicados al computador para activar la reconstrucción y Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 192 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica transferencia de la imagen. La consola de visualización del médico acepta la imagen reconstruida desde la consola del operador y la visualiza con vistas a obtener el diagnóstico adecuado. 14.2.5 ALMACENAMIENTO DE IMÁGENES Existen numerosos formatos de imágenes útiles en el campo de la radiología. Los escáneres actuales almacenan los datos de las imágenes en discos duros del computador. 14.2.6 IMPRESORA LASER Una vez que el radiólogo ha procesado digitalmente las imágenes para efectuar un mejor diagnostico, puede imprimirlas para enviarlas al medico que las ha solicitado junto con su concepto especializado. 14.3 PRINCIPIOS DE LA RECONSTRUCCION DE LA IMAGEN Aunque la imagen obtenida en la pantalla del computador es bidimensional corresponde en la realidad a un volumen. El soporte donde se crea la imagen es una MATRIZ, que es un concepto abstracto y matemático. Esta matriz no se ve, se ve solo la imagen. La matriz es una rejilla cuadrada compuesta de un número variable de cuadrados pequeños, cada cuadrado recibe el nombre de PIXEL (dos dimensiones, 2D). Como la imagen obtenida es una representación bidimensional de un cierto volumen de tejido, esta matriz no es plana si no que tiene un espesor (ds). A este espesor se le denomina espesor de corte y lo determinan las dimensiones del colimador a la salida del tubo de RX. Ahora bien, examinando un solo pixel, como si se sacara de la matriz, se observa que el pixel tiene un espesor (espesor de corte fijado por los colimadores), pues bien al pixel más el espesor de corte se le denomina VOXEL (tres dimensiones, 3D). La figura 193, ilustra los conceptos expuestos anteriormente. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 193 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Pixel Figura 193. Concepto de matriz, píxel y voxel El tubo de RX gira alrededor del paciente y da una información a los detectores de RX, que mediante instrumentacion electrónica, las convierte en señales eléctricas, que se amplifican, se filtran y se digitalizan, asociando cada píxel a unas coordenadas espaciales (x, y, z), tal como se muestra en la figura194. I = I0 e - µx Detector de centelleo o de gas Multiplexor Convertidor de corriente en voltaje (Amplificador transconductan cia) Integrador Convertidor Analogo/ Al PC Digital Figura 194. Conversión de RX en señal eléctrica digitalizada Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 194 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica El computador después de computar toda la información, otorga un valor numérico a cada pixel (que se corresponde con el coeficiente de atenuación), a este número del pixel se le asigna un color en una escala de grises que va desde el blanco hasta el negro, teniéndose una amplia gama de grises capaz de representar cualquier imagen. Para crear la imagen, se necesita saber todos los coeficientes de atenuación de cada uno de los voxeles de la matriz del corte tomográfico. Este cálculo se hace por dos métodos, el iterativo y el analítico. 14.3.1 Método Iterativo: El computador va haciendo sumas verticales, horizontales y diagonales de la matriz, hasta que obtiene la coincidencia de todos los datos. No se puede reconstruir la imagen hasta que se tengan todos los datos, es decir el coeficiente de atenuación de cada voxel de la matriz. Se estiman las celdas de una matriz a partir de la suma de sus componentes medida en las proyecciones. Se supone la proyección como una suma ponderada de los elementos y se trata de estimar los pesos correspondientes. Se inicia asumiendo todas las celdas de la matriz en ceros y se toma la primera proyección que se reparte en partes iguales en todas las celdas. Posteriormente se compara el resultado de la suma en la dirección de la segunda proyección. Si hay diferencias se reparten equitativamente en las celdas correspondientes. Se continúa de la misma manera hasta considerar todas las proyecciones. Se finaliza así la primera iteración. El procedimiento se repite otra vez desde la primera iteración y se itera hasta obtener un resultado con la resolución numérica deseada. La figura 195, muestra la matriz y la formula para calcular el valor estimado del coeficiente de atenuación de cada voxel. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 195 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica j µij ∑ µij 1 N n+1 µij n = µij + ∑µij _ i ∑ µijn N Figura 195. Método de iteración para el cálculo del coeficiente de atenuación µij : Coeficiente de atenuación real a calcular µij : Sumatoria real de coeficientes en la proyección ∑ n+1 : iteración actual n : iteración anterior n+1 µij : Coeficiente estimado en la iteración actual n µij : Coeficiente estimado en la iteración anterior n ∑ µij : Sumatoria estimada de coeficientes de la iteración anterior N : Numero de coeficientes de atenuación en la proyección Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 196 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Se aplicará el método iterativo a una matriz 2x2 para el siguiente caso: µ11 µ12 µ21 µ22 Obsérvese que hay dos proyecciones verticales, dos horizontales y dos diagonales. En cada caso la suma total de atenuaciones corresponde a la suma de dos atenuaciones individuales de dos celdas. Paso 1: Asumir todas las celdas en ceros: 0 0 0 0 0 0 0 0 0 0 Paso 2: Iteración 1, proyección vertical Aplicando la formula de la figura 195 a la proyección vertical izquierda: µ11 = 0 + (11 – 0)/2 = 5.5 µ21 = 0 + (11 – 0)/2 = 5.5 Aplicando la formula de la figura 195 a la proyección vertical derecha: µ12 = 0 + (9 – 0)/2 = 4.5 µ22 = 0 + (9 – 0)/2 = 4.5 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 197 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La matriz después de esta primera iteración queda así: 10 11 9 10 5.5 4.5 10 5.5 4.5 10 Paso 3: Iteración 2, proyección horizontal: Aplicando la formula de la figura 195 a la proyección horizontal superior: µ11 = 5.5 + (12 – 10)/2 = 6.5 µ12 = 4.5 + (12 – 10)/2 = 5.5 Aplicando la formula de la figura 195 a la proyección horizontal inferior: µ21 = 5.5 + (8 – 10)/2 = 4.5 µ22 = 4.5 + (8 – 10)/2 = 3.5 La matriz después de esta segunda iteración queda así: 10 11 9 10 6.5 5.5 12 4.5 3.5 8 Paso 4: Iteración 3, proyección diagonal: Aplicando la formula de la figura 195 a la proyección diagonal derecha: µ12 = 5.5 + (13 – 10)/2 = 7 µ21 = 4.5 + (13 – 10)/2 = 6 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 198 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Aplicando la formula de la figura 195 a la proyección diagonal izquierda: µ11 = 6.5 + (7 – 10)/2 = 5 µ22 = 3.5 + (7 – 10)/2 = 2 La matriz después de esta tercera iteración queda así: 7 11 9 13 5 7 12 6 2 8 Obsérvese como con los valores hallados de atenuación para cada píxel de esta matriz cumple con la sumatoria total de cada una de las proyecciones, por lo tanto esta es la solución definitiva. En la realidad la radiación que llega a cada detector es la debida a la atenuación total de la trayectoria del haz. Esta se calcula de la siguiente manera: µT = ln (Io/I)/x, en donde Io, I, x, son valores conocidos del problema. Por lo tanto en el computador de procesamiento de datos se calcula cada µT correspondiente a su respectiva proyección y con el método iterativo, se calcula la atenuación µij de cada voxel de la matriz. 14.3.2 Método Analítico: Tiene varias posibilidades, tales como la transformada de Radon, la transformada de Fourier en 2D, pero la más usada es el método de retroproyección filtrada. El método analítico se trata de empezar a reconstruir la imagen según se van recibiendo los datos, así se crea una imagen unidimensional y se representa a continuación en la matriz, esto se hace sucesivamente con todos los disparos; después de todas las reconstrucciones se crea finalmente la imagen. Esta imagen es filtrada mediante un filtro KERNEL, que en realidad lo único que va a hacer es una superposición de una determinada curva, correspondiente a una determinada formula matemática Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 199 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica (filtro) a la curva obtenida mediante la adquisición de los datos de los detectores; esto es, multiplicando el valor obtenido por los detectores por un filtro Kelnel para así obtener el resultado. Su finalidad es resaltar los datos de la imagen que puedan tener alguna importancia diagnostica. Los filtros Kernel son formulas matemáticas y hay distintos tipos de filtros, se seleccionan dependiendo de lo que más interese ver. Los filtros más importantes son: • SHARP: Realza bordes de estructuras de muy distinto coeficiente de atenuación. • REALCE DE BORDES: Realza la diferencia entre bordes, realza más la diferencia de contraste entre estructuras de no muy distinto coeficiente de atenuación. • SUAVIZADO: Lo que hace es disminuir los artefactos debidos la ruido estático, va a limar diferencias. 14.4 CONSTRUCCIÓN DE LA ESCALA DE GRISES Una vez calculado el valor de la atenuación de cada voxel de la matriz de la imagen, se procede a calcular el número correspondiente en tomografía computada denominado valor TC, de la siguiente manera: Valor TC = (µcalculado – µagua)/ µagua x 1000 (Unidades Hounsfield, HU) Hay que tener en cuenta que esta escala consta de un número superior a 4.000 unidades HU, y que se representa en escala de tonalidades grises, de forma que el más denso (HU más alto) se aproxime al blanco, mientras que el menos denso (HU baja) se aproxime al negro. La figura 196, muestra la escala de unidades de Hounsfield, para la mayoría de tejidos del cuerpo humano. Obsérvese como el hueso compacto tiende a +1000 HU y corresponderá al blanco en la imagen y los pulmones tienden a – 900 HU y corresponderá al negro en la imagen de tomografía computada. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 200 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 196. Escala de atenuación en HU para los tejidos del cuerpo humano 14.5 CONCEPTO DE VENTANA Y CENTRO Ahora bien, el ojo humano no es capaz de distinguir más de 40 escalones de grises aproximadamente. Por tanto, nuestro ojo, si ve 100 unidades HU con la misma tonalidad de gris, creerá que todo lo que está en el rango entre 0 y 100 es de la misma materia, lo cual es grave; ya que para nuestra vista será lo mismo cartílago, hígado, intestino, etc, tal como se puede ve en la grafica 196, con los tejidos parenquimatosos. Afortunadamente existe un truco para que esto no ocurra así. Representar en escalones de gris, solamente la parte de la escala que interesa. Supóngase que se va a mostrar en el monitor de imágenes la parte correspondiente al rango entre 0 y +80. El gris medio corresponderá al 40; por encima de 80 todo será blanco y por debajo de 0 todo será negro. Ahora se pueden ver diferencias, entre cada dos unidades. A esta anchura o cantidad de valores HU, las cuales se pueden seleccionar libremente en la consola de control se le llama ventana. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 201 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Supóngase ahora que se requiere ver, con la ventana anterior de 80 HU, es la zona de grasa; pues simplemente se traslada esta, de forma que su límite superior será -20. Todo lo que tenga una HU superior a este valor, será blanco. El límite inferior será -100 y todo lo que esté por debajo de este valor será negro. Este truco de la ventana todavía es algo ambiguo, ya que sólo indica qué cantidad de unidades se verán en escalones de gris, pero no dice en qué zona de la escala está situado. Se requiere introducir otro concepto denominado centro o nivel. Este centro, o lo que es lo mismo el gris medio, va a indicar en qué valor HU se encuentra la mitad de la ventana. Resumiendo, cuando se representa la imagen en alguna parte del monitor, se indicaran dos valores: la ventana, que informa cuantas unidades CT se representará, y el centro, que indicará en qué parte de la escala se esta ubicado. La siguiente tabla sugiere los valores de centro y ventana para diferentes órganos: Región Ventana Centro Base de Cráneo 240 35 Cerebro 120 35 Abdomen 400 35 Columna Dorso Lumbar 450 40 Orbita 240 35 Pulmón 400 700 Pelvis Hígado/Páncreas Columna Cervical Silla Turca Oído Interno Extremidades 450 350 40 40 350 40 240 4000 350 35 300 40 Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 202 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica La figura 197, ilustra el concepto de centro y ventana, para una imagen de TC abdominal de hueso, intestino y pulmones. Hueso Intestino Pulmones Figura 197. Concepto de centro/ventana para tres órganos diferentes Se puede observar en la figura 197, que en el caso del hueso, el centro está ubicado en 1000 HU y el ancho de la ventana es de 2500 HU. Para el intestino, la calibración es de -50 HU/400 HU y para los pulmones -600 HU/1700 HU, comprobándose como con esta técnica de procesamiento digital de imágenes se resalta en la imagen lo que se quiere estudiar con más detalle. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 203 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14.6 FACTORES DE CALIBRACION DE UN TOMOGRAFO COMPUTADO Los valores que se pueden seleccionar en un Tomógrafo Computado son los siguientes: • Campo de medición (FOV): Existen dos tipos de campos el campo medido y el campo representado. Campo medido: es el tamaño de apertura en el gantry, esto es, preparar los detectores necesarios para hacer la medición, los demás detectores solo están preparados para recibir densidad aire. Si estos detectores recibieran RX aparecerían artefactos por fuera de campo. Campo de representación: se refiere a la parte del campo de medición que va a ser representada por el ordenador en el monitor. Una vez elegido el campo de medición ahora decidimos si se representa todo o una parte. El campo de representación debe ser lo más pequeño posible ya que determinara junto con la matriz el tamaño del pixel. • Tamaño de la matriz: Es la cuadricula donde se representa la imagen, su tamaño viene dado por el número de pixels e influye en la resolución espacial, a mayor tamaño mayor resolución • Grosor de corte: Es la tercera dimensión en un corte de un TC. Voxel = tamaño pixel + grosor de corte. Influye en la resolución espacial. A grosor de corte más fino mejor resolución espacial, por el contrario a cortes más finos mayor numero de cortes, mayor tiempo de reconstrucción, más ruido, y más calentamiento del tubo de RX. • Tiempo de corte: Es un valor que el técnico debe de valorar según sea el paciente y el estudio a realizar. Se puede acortar el tiempo de corte si el barrido del tubo de RX es incompleto o si la reconstrucción de la imagen se hace posterior a los cortes y no al mismo tiempo. • Kv y mAs: El Kv siempre es alto de 100 Kv a 150 Kv. El mA es lo único que se modifica en al practica para evitar el ruido. A mas mA menor ruido. • Punto focal • Algoritmo de reconstrucción: Filtros Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 204 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14.7 EQUIPOS COMERCIALES DE TOMOGRAFÍA COMPUTADA Las siguientes son las especificaciones técnicas de un equipo de tomografía computada de última generación: I. DESCRIPCIÓN: 1. Equipo de tomografía computarizada con un tiempo de rastreo o exploración de 0.5 segundos o menor en un giro de 360º o rotación 2. De 16 cortes o mayor 3.- Gantry 3.1 Con angulación de +/- 30º o mayor 3.2 Apertura de mínimo 70 cm. 4. Tubo de rayos X con capacidad de almacenamiento de calor en el ánodo de mínimo 5 MHU o mayor 5. Con un espesor de corte menor a 1 mm. 6. Reconstrucción de imagen en 1 segundo o menor o 1 corte por segundo 7. Matriz de reconstrucción de mínimo 512 x 512 elementos de imagen 8. Matriz de despliegue de 1024 x 1024 elementos de imagen o mayor 9. Monitor de 45.72 cm. o mayor o 18 pulgadas o mayor con una resolución de 1280 x 1024 10. capacidad de espiral o exploración de al menos 100 segundos y con una longitud de 100 cm. o mayor 11. Reconstrucción de imágenes MPR en tiempo real 12. Reconstrucción de conjuntos de cortes tridimensionales o 3D 13 Capacidad de almacenaje de 18 Gb o mayor 14. Disco óptico u óptico-magnético o CDR 15. El equipo debe incluir un programa de software para el mayor aprovechamiento del medio de contraste 16. Programas de software para la evaluación de imágenes espirales o helicoidales o volumétricos en angio CT o angiográficas y MIP 17. Software 17.1 Endoscopia virtual o navegador 17.2 Perfusión Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 205 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 17.3 Calcium scoring o smartscore o cardiac scoring 17.4 Programa para pulmón 17.5 Estudios cardiológicos; imágenes coronarias o cardiaco avanzado; función cardiaca o función ventricular 18. Posibilidad de realizar estudios o evaluación dinámica 19. Con salida DICOM 20. Consola del operador 21. Estación de trabajo o consola de postproceso II. ACCESORIOS: 1. Impresora en seco para película de 14” x 17” o 35 x 43 cm. 2. Inyector de medio de contraste para tomografía computarizada 3. Con unidad de energía ininterruptible UPS, para el respaldo del equipo de computo de al menos 30 min o mayor 4. Posibilidad de realizar intervenciones guiadas o floruro CT o modo de biopsia que incluya monitor dentro de la sala de examen o en el cuarto de examinación III. CONSUMIBLES: 1. Disco óptico u óptico magnético o CDR 2. Película para la impresora A continuación se describirá de manera resumida las características técnicas de los equipos de tomografía computada de los fabricantes líderes a nivel mundial de esta tecnología: 14.7.1 TOSHIBA – AQUILION 64 Para muchas publicaciones especializadas, este es el tomógrafo multicorte (multislice)más avanzado del mundo. Adquiere imágenes volumétricas a través de un detector Quantumde 64 filas. Posee un detector de 64 canales de adquisición reales, y algoritmo de reconstrucción 3D. Su detector produce alta velocidad, alta resolución de imagen, con muy buena resolución de bajo contraste a la dosis mas baja. Estas características hacen que sea muy versátil y sumamente aplicable en el ámbito del diagnóstico cardíaco y cardiovascular. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 206 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Permite la mejor visualización de las arterias coronarias y la obtención de cortes del corazón de forma sumamente veloz. Su tecnología le permite adquirir 64 cortes de 0.5mm de espesor por rotación y permite obtener una imagen isotrópica en cualquier región de la anatomía, de forma que, con la retención de la respiración del paciente tan solo por debajo de los diez segundos, ya habilita la posibilidad de adquisición de la misma. La figura 198, muestra al tomografo anteriormente descrito. Figura 198. Tomógrafo Computado Toshiba Aquilion 64 14.7.2 GENERAL ELECTRIC - LIGHTSPEED VCT La línea LightSpeed de G.E. Halthcare abarca diferentes modelos para cubrir las crecientes necesidades del desarrollo del diagnóstico por imágenes. Su denominación deviene de la especificación de Tomografía Computada Volumétrica. Este modelo se destaca por la utilización del detector V-Res™, que ofrece, al mismo tiempo, una amplia cobertura anatómica y alta resolución. Por cada rotación cubre 4 cm del cuerpo del paciente. Cuenta con 64 canales de rotación elevada para la obtención de datos volumétricos. Alcanza los 350 milisegundos por rotación. En cuanto a sus posibles aplicaciones, permite examinar órganos completos en menos de un segundo. También es altamente aplicable en cuestiones cardíacas, pudiendo analizar el corazón en solo cinco latidos. La figura 199, muestra al tomógrafo anteriormente descrito. Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 207 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica Figura 199. Tomógrafo Computado General Electric - Lightspeed VCT 14.7.3 PHILIPS MEDICAL SYSTEM – BRILLANCE CT La línea Brillance de Philips cuenta con un equipo estrella de 64 canales. Su tiempo de rotación es de 0.4 segundos y la adquisición de datos volumétricos es de 64 por 0.625 mm. La resolución de imagen isotrópica es de 0.34 mm. Su utilización permite la obtención de imágenes de alta resolución, con preponderancia en el área cardiaca y la evaluación general de las arterias coronarias. También es apto para estudios pulmonares. Ofrece un sistema denominado RapidView™ que posibilita el uso de una técnica de reconstrucción de imágenes de alta calidad en un tiempo extremadamente rápido. La figura 200, muestra al tomógrafo anteriormente descrito. Figura 200. Tomógrafo Computado Phillips – Brillance CT Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 208 UNIVERSIDAD NACIONAL ABIERTA Y A DISTANCIA – UNAD Instrumentación Médica 14.7.4 SIEMMENS - SOMATOM La línea Somatom tiene una característica saliente: el concepto Dual Source. Este concepto implica la utilización de dos fuentes de Rayos X combinadas con dos detectores al mismo tiempo. Las ventajas de este sistema es que permiten obtener el doble de resolución temporal, el doble de velocidad y reducir la dosis de exposición del paciente. Posee un tiempo de rotación de 0.33 segundos. Su sistema de obtención de imagen de alta resolución es el z-Sharp™, que permite esta aplicación también con dosis mínimas de exposición. La resolución de imagen isotrópica es de 0.24 mm. La figura 201, muestra al tomógrafo anteriormente descrito. Figura 201. Tomógrafo Computado Siemens – Somatom Jorge Eduardo Quintero Muñoz – jorgequintero@bioingenieros.com 209
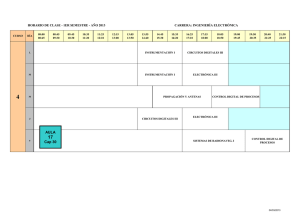




![Instrumentacion industrial[1]](http://s2.studylib.es/store/data/003358366_1-42b645bd6154f31d3364e8002ac0c8be-300x300.png)

