S4-MCS361
Anuncio

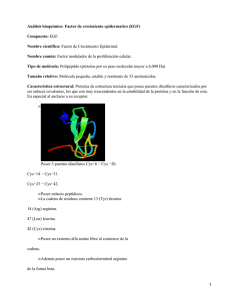
Papel del factor de crecimiento epidérmico (EGF) en la motilidad de las células GH3 cultivadas sobre diferentes proteínas de matriz extracelular (ECM) Azorín E., Solano-Agama C. and Mendoza-Garrido ME. CINVESTAV. Departamento de Fisiología, Biofísica y Neurociencias. México, D.F. INTRODUCCION La hipófisis es una glándula endocrina conformada por varios tipos celulares secretores (somatotropos, lactotropos, gonadotropos, tirotropos, adrenocorticotropos) y no secretores (células folículo estelares, así como endoteliales y macrófagos). El tejido hipofisiario mantiene un importante grado de plasticidad; de manera que, durante el desarrollo postnatal, la citoarquitectura de la glándula cambia para dar lugar a la estructura final y funcional presente en el adulto que se puede ver modificada en situaciones fisiológicas como la lactancia (4). La reorganización del tejido adenohipofisiario en la etapa postnatal, implica gran dinamismo en los procesos de adhesión, migración y señalización. Es gracias a la reorganización y diferenciación, que la adenohipófisis en la adultez se conforma de folículos en los que tanto células secretoras como no secretoras interaccionan estrechamente con factores parácrinos y con proteínas de la matriz extracelular (12,1). La composición de la matriz extracelular en la hipófisis es compleja y variable; conformada en general por glicoproteínas, proteoglicanos y proteínas fibrilares cuya proporción relativa varía de acuerdo con la circunstancia fisiológica. Tanto la ECM como los factores de crecimiento son cruciales para los fenómenos de migración. En este sentido, es bien conocido que el EGF induce re-arreglos en los procesos de adhesión y estimula la migración celular. De la misma forma en que estas proteínas tienen una función fisiológica, también pueden participar de manera muy importante en los procesos patológicos, de ahí la importancia de estudiarlos (8,5). En cuanto al EGF, la manera en la que responden las células adenohipofisiarias de rata a este factor varía de acuerdo con la etapa de desarrollo en que se encuentre el animal del que provienen. Las células infantiles se extienden y adhieren formando puntos focales de adhesión en respuesta al EGF, mientras su citoesqueleto de actina se organiza en fibras de estrés y se forman lamelipodios. Además, incrementan su tasa de migración. Lo anterior se observa cuando son cultivadas sobre colágena I (CI). La respuesta en cuanto a la migración de las células adultas es opuesta y no se observan cambios en el arreglo del citoesqueleto de actina (14,13). Por otro lado, Yarwood & Woodgett (2001) mostraron que la trascripción de genes relacionados con la arquitectura del citoesqueleto, síntesis proteica y ciclo celular inducida por el EGF se ve dramáticamente modificada por la composición de la ECM. La ECM comprende una gran familia de proteínas y de glicoproteínas dentro de las que predominan, las colágenas, las lamininas y los proteoglicanos. Las colágenas son un grupo de proteínas extracelulares que adquieren conformación de triple hélice. Estos trímeros se agregan en fibras, filamentos o redes para soportar y estabilizar a la membrana basal. Las colágenas fibrilares (I, II, III, V y XI) son sintetizadas como precursores que después de ser procesados en el espacio extracelular se sobreponen dando lugar a estructuras periódicas, constituidas por regiones densas y laxas que asemejan cuerdas rígidas con propiedades higroscópicas. Las colágenas de la membrana basal incluyen a diferentes moléculas conocidas en conjunto como colágenas tipo IV. Las colágenas tipo IV (CIV) están compuestas por tres cadenas organizadas en fibras elásticas. Estas proteínas forman redes irregulares y compactas, cuya expresión es tejido específica y varia a lo largo del desarrollo. Las CIV además de interaccionar entre sí, pueden formar uniones con heparina, heparán sulfato y laminina. Las células tumorales secretan grandes cantidades de laminina y su membrana basal esta compuesta únicamente por laminina (7,2). Las células GH3 han sido utilizadas como modelo para estudiar el comportamiento de células hipofisiarias. En 1968, Tashjian y cols. establecieron varias líneas celulares a partir de adenomas de ratas Wistar adultas. La clona GH3 se caracterizó por estar constituida por células redondas que crecen en cúmulos y secretan grandes cantidades de hormona de crecimiento (5µg/día). Más adelante se encontró que el citoesqueleto de actina de las células GH3 quiescentes se arregla en anillos corticales (3). Se ha documentado que la exposición de las células GH3 y sus subclonas a diferentes hormonas, así como al EGF, resulta en la inhibición parcial de la proliferación, aumento en la síntesis y secreción de prolactina, incremento en el número de canales de Ca2+ y a TRH (16). Así mismo las células GH3 cambian su morfología, de una forma redonda a una alargada, cuando son estimuladas con el EGF (6,11). La motilidad celular es un proceso cíclico que consta de 4 fases (adhesión, polarización, contractilidad y retracción). La adhesión, es determinada por la densidad de la ECM y la densidad y estado de activación de los receptores de adhesión; principalmente integrinas. La estabilidad de la interacción integrina-sustrato induce el reclutamiento de enzimas, proteínas adaptadoras y moléculas de señalización que favorecen el mantenimiento de la unión al mismo tiempo que se apagan las rutas de señalización activadas por mitógenos (MAPK) que ejercen una modulación negativa sobre la activación de integrinas. Estos cambios bioquímicos, propician que la célula alcance el grado de adhesión óptimo para que la forma de la célula cambie de redondeada a aplanada. El cambio morfológico (polarización) es el resultado de la activación de la fosfatidil inositol 3 cinasa (PI3K), las pequeñas GTPasas (Rho, Cdc42, Rac) y moléculas que se unen y regulan la organización dinámica de los componentes del citoesqueleto. De acuerdo con el modelo de tensegridad propuesto por Ingber, los puntos en los que la célula se ancla a la ECM generan fuerzas de compresión que son equilibradas con fuerzas de tensión generadas entre los filamentos del citoesqueleto. La relación de ambas fuerzas genera la tracción necesaria para que la célula pueda reptar sobre el sustrato. En el proceso de contractilidad, esta bien establecido que participa Rho activando a la cinasa dependiente de Rho (ROCK) la cual es capaz de inhibir a la fosfatasa de la cadena ligera de la miosina (MLCP) al mismo tiempo que activa a la cinasa de la cadena ligera de la miosina (MLCK) y fosforila a la cadena ligera de la miosina (LC20). Lo que pone de manifiesto que entre otros factores, la miosina II es una de las proteínas indispensables para la generación de tracción durante la motilidad de una célula (9,15). Dentro de los procesos de motilidad celular, se pueden distinguir: la migración que se refiere al desplazamiento de una célula sobre un sustrato sólido de ECM; o bien, la invasión en la cual se habla de un desplazamiento a través de la ECM y por consiguiente la degradación enzimática del sustrato. Tomando en consideración que durante los procesos de motilidad celular se observan cambios en la morfología, la organización del citoesqueleto de actina y el rearreglo de los procesos de adhesión (10). Así como, que el EGF induce la reorganización del citoesqueleto de actina, la formación de complejos de adhesión y el incremento en la migración celular en cultivo primario de células adenohipofisiarias infantiles de rata (14,13). En el presente trabajo se analizaron los cambios en la motilidad de las células GH3 por el estímulo con EGF en diferentes ECM y la relación de éste fenómeno con la activación de la vía MAPK/Erk. MATERIAL Y METODO La línea celular GH3, se mantuvo en medio Ham-F12 (Sigma) suplementado con 5% suero bovino fetal, 10% suero de caballo (GIBCO), 1 mM L-glutamina, NaHCO3 1.2 mg/ml y 1% de antibiótico (10 000 UI/ml penicilina y 10 000 µg/ml estreptomicina, Sigma) en condiciones de 95% de humedad a temperatura de 37 °C. Para excluir los efectos de los componentes del suero, se preparó un medio de composición definida (DEF): HAM-F12 suplementado con HEPES 10mM, L-glutamina 1 mM, antibiótico, NaHCO3 1.2 mg/ml, albumina 1 mg/ml, putresina 32 µg/ml, transferrina 5 µg/ml, insulina 5 µg/ml, triyodotironina 5 ng/ml, corticosterona 6 ng/ml, progesterona 60 ng/ml, selenito de sodio 2.9 µg/ml (Sigma). La suspensión celular de trabajo se obtuvo a partir de cultivos semi-confluentes incubados con una solución de EDTA 0.03% en PBS. La suspensión celular se centrifugó a 800 rpm y el botón celular se resuspendió en DEF. El número y viabilidad de las células en suspensión se determinó, por el método de exclusión con azul tripano. Visualización del citoesqueleto de actina y la vinculina Para visualizar la organización del citoesqueleto de actina así como el arreglo de la vinculina en los complejos de adhesión, se utilizó la técnica de citoquímica e inmunocitoquímica, respectivamente. Sobre vidrios cubiertos con las diferentes ECMs se sembraron 6x105 células en DEF con y sin EGF. Al completarse 48 horas de cultivo, las células se fijaron y permeabilizaron en un amortiguador estabilizador del citoesqueleto (PBS adicionado de MgCl2 5 mM, EGTA 3 mM). En seguida, se lavaron y se incubaron con un anticuerpo monoclonal contra vinculina 1.7 µg/ml (Sigma) el cual se detectó con un anticuerpo secundario fluoresceinado (Molecular Probes). La detección de actina-F se hizo con 1 µM de faloidina conjugada con rodamina (Sigma). Las laminillas se analizaron por microscopía confocal (Leica DM IRE2, Germany) con el objetivo de 60X haciendo cortes transversales de 0.5 µm de grosor. Ensayo de invasión Se sembraron 3x105 células en cámaras Boyden cuyo fondo había sido previamente tratado con ECM. Los cultivos se incubaron durante 48 horas en DEF, con y sin EGF 50 ng/ml (Boehringer). Las células que atravesaron la membrana cubierta con ECM se adhirieron a vidrios cubiertos con polilisina. Estas células, se fijaron y tiñeron para determinar la tasa de invasión. Para evaluar la participación de los principales activadores de LC20 en la capacidad invasiva de las células GH3, las células fueron tratadas durante 1 hora con inhibidores específicos de MLCK (ML7), de ROCK (Y27632) o de MEK (U0126). Análisis temporal de la activación de Erk y LC20 Para determinar el efecto de la ECM en la activación de la vía MAPK/Erk se colocaron 25x105 células previamente sincronizadas en el fondo de cajas Petri pretratadas con ECM; permitiendo la interacción de las células con la ECM por 50, 150 minutos o 24 horas. Para establecer el efecto modulador del EGF, se sembraron 25x105 células en cajas Petri de 66mm cuyo fondo había sido previamente tratado con ECM durante 24 horas. Al completarse el periodo de incubación, los cultivos se estimularon por 5, 10, 20, 30, 60 y 120 minutos con EGF. En todos los casos, se obtuvo el lisado celular total con el amortiguador de extracción RIPA-SDS, la cantidad de proteína se determinó con el método del ácido bisincronínico (BCA, Pierce). Las proteínas (50µg) se separaron en un SDS-page 15 % y se transfirieron a una membrana de PVDF (Amersham). Los sitios de unión inespecífica se bloquearon con leche descremada al 3 % (Upstate) en PBS. La detección de las fracciones fosforiladas se hizo con un anticuerpo que reconoce fosfo-p44/p42 MAPK 1:500 (Cell Signaling) y un anticuerpo contra la fosfoserina 19 de LC20 1:2500 (Chemicon) seguido de la incubación con un anticuerpo peroxidado de cabra contra raton 1:20000 (Pierce) o cabra contra conejo 1:8000 (Amersham Pharmacia Biotech). Después de detectar la proteina fosforilada, la membrana se lavo de anticuerpos (stripping) con una solución comercial (Pierce). La proteina total se detectó con un anticuerpo dirigido contra p44/p42 MAP Kinase 1:1000 (Cell Signaling) o LC20 sin fosforilar 1:1000 (Sigma) seguido de la incubación con el anticuerpo secundario peroxidado correspondiente. Las bandas de proteína se evidenciaron con ECL-Plus (Amersham Pharmacia Biothec) y su densidad se midió con el programa ImageQuant TL v.2003. RESULTADOS Con técnicas de citoquímica e inmunocitoquímica se observó la organización de actina y la localización de vinculina en presencia de diferentes ECM. Como se muestra en la figura 1, la morfología, la organización del citoesqueleto de actina y la distribución de vinculina de las células GH3 depende de la ECM. En CI se observó la formación de filopodios que se retraen después de la estimulación con EGF, mientras que en CIV y CIV/L las células están más aplanadas y no forman fibras de estrés. En CIV y CIV/L la vinculina se acumuló en las uniones célula-célula y mostró un patrón rayado asociado a puntos focales de adhesión cuando se agregó EGF. CI CIV CI + EGF CIV/L CIV + EGF CIV/L + EGF Fig 1. Efecto de ECM y EGF en la localización de actina-F (rojo) y vinculina (verde) en células GH3 Al analizar los efectos de la ECM y del EGF en la capacidad invasiva de las células GH3 encontramos que el tipo de ECM limita su capacidad invasiva (Fig.2). La CI, CI/F y CIV limitaron significativamente la capacidad invasiva de las células GH3. Mientras que el EGF moduló de manera diferencial la invasividad en función del tipo de ECM presente en el cultivo sugiriendo que la ECM activa ciertas señales bioquímicas que definen el efecto modulador ejercido por el EGF en una respuesta fisiológica como es la invasividad. De ahí que nos interesó entender como estaban siendo activadas y moduladas las señales bioquímicas involucradas en la motilidad celular por la ECM y el EGF. Al respecto, encontramos que la inhibición farmacologica de LMCK con ML7, MEK con U0126 y ROCK con Y27632 por si sola disminuyó significativamente la capacidad invasiva de las celulas GH3 en ausencia de ECM. Por otro lado, mostró que el EGF ejerce su efecto inhibitorio a través de MEK y ROCK (Fig. 3). El analísis temporal de la activación de Erk mostró que la activación de la vìa MAPK/Erk es rápida, sostenida y el nivel de activación de Erk varía deacuerdo con la ECM. DISCUSION El tamaño de una célula esta determinado por la interacción entre las integrinas con la matriz extracelular y las cascadas de señalización que con esto se inician que promueven la formación de puntos focales de adhesión y la polimerización de actina; cuya estabilidad a su vez depende de la formación de fibras de estrés y generación de tensión entre estas. Se detectó actina y mediante inmunocitoquimica se analizo la vinculina para caracterizar el arreglo del citoesqueleto de actina en las diferentes proteínas de matriz extracelular, así como la formación de puntos focales de adhesión. La organización del citoesqueleto cambia respecto de la matriz a la que están expuestas las células; en CI se pueden distinguir filopodios a nivel de sustrato. El estimulo con EGF indujo la retracción de los filopodios y la formación de un anillo cortical. En CIV, se observan placas de actina en el citoplasma a nivel del sustrato (invadipodia) que ante el estímulo con el EGF se reorganizan en anillos corticales, arcos y pequeñas fibras de estrés. Se han podido observar puntos focales de adhesión, en cultivos en ausencia de ECM. Como ya se mencionó, la estabilidad de los puntos focales de adhesión y las fibras de estrés dependen de la tensión generada entre filamentos de actina para lo que se requiere la fosforilacion de la cadena ligera de la miosina; se busca analizar la variación de esta fracción fosforilada por la presencia de las proteínas de matriz extracelular y del EGF. Se pretende relacionar estas observaciones con las cascadas de señalización involucradas en la fosforilacion de la cadena ligera de la miosina, las iniciadas por la interaccion de las integrinas con las proteínas de matriz extracelular y alguna de las vías inducidas por el receptor a EGF. El analisis electroforetico de proteinas fosforiladas en las diferentes ECM, muestra como el patron temporal de activacion de Erk y LC20 es varia en las distintas matrices analizadas. Siendo una activacion rapida, sostenida y ciclica que depende de la interaccion inicial con la ECM. La redistribución de la vinculina de las uniones célula-célula hacia los puntos focales de adhesión nos sugiere que el EGF esta modificando las señales bioquímicas que regulan la asociación de las células entre si y con el sustrato. El EGF al disminuir la asociación de las células con sus vecinas y al incrementar la asociación con el sustrato favorece la migración pero tal como lo muestran los resultados induce una disminución significativa de la capacidad invasiva. La organización del citoesqueleto de actina en anillos corticales y no en fibras de estrés indica que esta favorecida la generación de tensión en la periferia lo que provoca incremento en el aplanamiento de la célula y probablemente inhibe la secreción de metaloproteinasas y activa la señalización de cdc42. sugiere que el EGF esta modificando las señales bioquímicas que regulan la asociación de las células entre si y con el sustrato. El EGF al disminuir la asociación de las células con sus vecinas y al incrementar la asociación con el sustrato favorece la migración pero tal como lo muestran los resultados induce una disminución significativa de la capacidad invasiva. La organización del citoesqueleto de actina en anillos corticales y no en fibras de estrés indica que esta favorecida la generación de tensión en la periferia lo que provoca incremento en el aplanamiento de la célula y probablemente inhibe la secreción de metaloproteinasas y activa la señalización de cdc42. Al parecer la información bioquímica activada por la ECM define el tipo de respuesta que el EGF activará. REFERENCIAS Bello-Pineda J., Luna J., Romano M and Mendoza ME. 1999. Developmental changes in LH secretion by male pituitaries in vitro: from the infantile to adult period. J Endocrinol. 160:333-341 Belot N., Rorive S., Doyen I., Lefranc F., Bruyneel E., Dedecker R., Micik S., Brotchi J., Decaestecker C., Salmon I., Kiss R. and Camby I. 2001. Molecular Characterization of Cell Substratum Attachments in Human Glial Tumors Relates to Prognostic Features. GLIA. 36:375-390 Bissel M. and Radisky D. 2001. Putting Tumours in Context. Nature Rev. 1:46-54 Brown R. 1994. The pituitary gland and its hormones. Capitulo 3. En: An Introduction to Neuroendocrinology. Cambridge University Press. Pp. 30-37 Feldner J. and Brandt B. 2002. Cancer Cell Motility-On the Road from c-erbB-2 Receptor Steered Signaling to Actin Reorganization. Exp Cell Res. 272:93-108 Felix R., Meza U. and Cota G. 1995. Induction of Classical Lactotropes by Epidermal Growth Factor in Rat Pituitary Cell Cultures. Endocrinology 136: 939-946 Gonzales B., Solano-Agama M., Gonzales del Pliego M. and Mendoza-Garrido M. 2004. Differences in cell migration of cultured pituitary cells from infantile and adult rats: participation of the extracellular matrix and epidermal growth factor. Int J Devl Neuroscience 22: 231-239 Hackel P., Zwick E., Prenzel N and Ullrich A. 1999. Epidermal growth factor receptors: critical mediators of multiple receptor pathways. Curr Op Cell Biol. 11:184-189 Hapgood J., Libermann T., Lax I., Yarden Y., Schreiber A., Naor Z. and Schlessinger J. 1983. Monoclonal antibodies against epidermal growth factor receptor induce prolactin synthesis in cultured rat pituitary cells (GH3). PNAS 80:6451-6455 Johnson L., Baxter J., Vlodavsky I. and Gospodarowicz D. 1980. Epidermal growth factor and expression of specific genes: Effects on cultured rat pituitary cells are dissociable from mitogenic response. PNAS 77:394-398 Soji T., Sirasawa N., Kurono C., Yashiro T. and Herbert D. 1994. Immunohistochemical study of the post-natal development of the folliculo-stellate cells in the rat anterior pituitary gland. Tissue Cell. 26:1-8 Toral C., Solano-Agama M., Luna J., Romano M. and Mendoza-Garrido M. 2003. Epidermal Growth Factor Induces an Increase in Cell Adhesion and Arrangement of Actin Skeleton in Stress Fibres in Pituitary Cultured Cells From Infantile Rats but Not Adult Rats. J Cell Phys. 195:80-91 Yoneda M., Nishizaki T., Tasaka K., Kurachi H. and Miyake A. 2000. Changes in actin network during calcium-induced exocytosis in permeabilized GH3 cells: calcium directly regulates F-actin disassembly. J Endocr. 166:677-687