Virus de Hepatitis B y C en en el paciente TPH. 2009
Anuncio

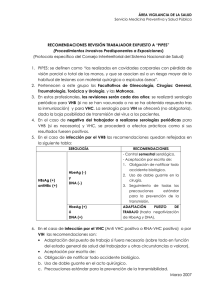
HEPATITIS B y C EN EL PACIENTE SOMETIDO A TRASPLANTE DE PROGENITORES HEMATOPOYÉTICOS Miguel Lanaspa Unitat de Patologia Infecciosa i Immunodeficiències de Pediatria Hospital Vall d’Hebron Octubre 2009 1 Hepatitis B 1. Introducción La incidencia de Hepatitis B ha disminuido considerablemente en nuestro medio con la introducción de medidas preventivas por lo que esta infección ya no es una prioridad de salud pública en los países desarrollados. En la población inmigrante, sin embargo, la prevalencia de infección (definida como HbsAg positivo en sangre) puede llegar a 5-15%, y la prevalencia de infección oculta o de infección resuelta puede ser incluso más elevada. En los pacientes inmunodeprimidos, estas entidades relacionadas con la hepatitis B pueden suponer un problema grave. En este protocolo se revisa el diagnóstico y el manejo de la infección por el virus de la hepatitis B (VHB) en el trasplante de progenitores hematopoyéticos. 2. Historia natural del VHB El VHB se contrae por vía sexual, por hemoderivados o por transmisión vertical. Después de un periodo de incubación entre 1 y 12 semanas, se inicia la replicación del virus en los hepatocitos que precede a la elevación de las transaminasas y al resto de clínica acompañante en un periodo de tiempo que varía desde pocos días a varias semanas. En esta fase de la enfermedad son positivos los siguientes maradores: HbsAg, HbeAg y DNA VHB. Posteriormente, según la respuesta inmunológica del paciente, la enfermedad se puede resolver clínicamente o cronificar, en una proporción mayor cuanto menor es la edad de adquisición del VHB. Los pacientes con infección crónica pueden presentan complicaciones hepáticas graves (cirrosis y carcinoma hepatocelular) en 15-40% de los casos. En los pacientes en los que la enfermedad está aparentemente resuelta (HbsAg negativo, transaminasas normales), el DNA del VHB puede persistir unido covalentemente al ADN de los hepatocitos. 2 3. Definiciones Hepatitis B crónica: Daño hepático con HbsAg positivo durante más de 6 meses. Portador inactivo: HbsAg positivo durante más de 6 meses, con transaminasas normales y DNA VHB negativo o inferior a 105 copias/ml. Hepatitis B oculta: Transminasas normales o anormales, HbsAg negativo, HbcAc positivo, DNA VHB positivo (en suero o en tejido hepático). Hepatitis resuelta: Historia de infección por VHB, HbcAc positivo, transminasas normales, HbsAg y DNA VHB negativos. Reactivación: Aumento de las copias de DNA VHB > a 1 logaritmo, o carga viral > 106 copias/ml, o positivación del DNA VHB, o aumento de transaminasas 5 veces superior al valor normal, o 3 veces superior al valor basal en pacientes portadores inactivos de HbsAg y en pacientes con infección oculta por VHB. Vacunado: HbsAc positivo. Puede ser inicialmente negativo pero positiviza con un booster. Resto de marcadores negativos. 4. Reactivación en el paciente hemato-oncológico En caso de inmunosupresión, el control inmunológico sobre la infección se pierde y el virus puede replicar de nuevo. La reactivación del VHB en pacientes hemato-oncológicos adultos que inician tratamiento con quimioterapia no es rara, pudiendo presentarla hasta un 50% de los portadores inactivos de HbsAg y un porcentaje menor de pacientes con hepatitis B oculta. Se presenta entre 4 y 36 semanas tras el inicio de la quimioterapia (media 16 semanas). Esta reactivación puede ser asintomática y transitoria, pero también puede presentarse con aumento de transminasas aislado, hepatitis fulminante y muerte (550% según las series). El aumento de transminasas ocurre entre pocos días y varias semanas después del aumento de la carga viral, pudiéndose observar un fenómeno de reconstitución inmune. El pronóstico hemato-oncológico de los pacientes empeora, además, por la necesidad de suspender la quimioterapia durante la reactivación. 3 Los factores de riesgo de reactivación son los siguientes: Marcadores serológicos: HbsAg (+), HbeAg (+), HbcAc (+) en ausencia de HbsAc. Quimioterapia: corticoides, antraciclinas, quimioterapia mieloablativa. Anticuerpos monoclonales: Rituximab, alentuzumab, infliximab. Enfermedad del injerto contra el huesped. Coinfecciones con otros virus hepatotropos. Sexo masculino. Menor edad. En el caso del TPH, el factor protector más importante es la presencia de HbsAc +/HbcAc en el donante. 5. Cribado de VHB y actitud en el TPH Es necesario determinar HbsAg, HbsAc y HbcAc en todos los donantes y receptores de progenitores hematopoyéticos. 1. Donante y/o receptor HbsAg (-), HbsAc (-), HbcAc (-): administrar al menos 2 dosis de vacuna previo a la extracción de progenitores o al inicio del acondicionamiento. Posteriormente administrar la tercera dosis a los 6 meses de la primera y comprobar si hay respuesta vacunal (15-60% en TPH). 2. Receptor HbsAg (+): Iniciar tratamiento antiviral. Monitorizar la carga viral y la ALT. Priorizar donantes HbsAc positivos. 3. Receptor HbcAc (+): Determinar DNA VHB. En caso de ser positivo iniciar tratamiento antiviral. En caso de ser negativo monitorizar la carga viral semanalmente y la ALT, especialmente si el donante es HbsAc positivo ya que la trasferencia de inmunidad adaptativa contra VHB es efectiva en las primeras semanas post TPH. 4. Receptor DNA VHB (+): Independientemente de los otros marcadores, iniciar tratamiento antiviral. 4 NOTAS: 1. En caso de ser HbsAc (-), se administrará una dosis de vacuna VHB siempre que sea posible como booster. Los pacientes que no presenten HbsAc tras el booster deberían ser vacunados (3 dosis) y valorar iniciar tratamiento antiviral ya que tienen mayor riesgo de reactivación de VHB, aunque la estrategia de tratamiento anticipado monitorizando la carga viral y la ALT también es válida. 2. En nuestro centro, la carga viral de VHB se expresa en unidades u, considerándose positiva una carga viral superior a 20 u. 6. Tratamiento El tratamiento de elección es lamivudina 3 mg/kg/día (máx. 100 mg/día). Se recomienda iniciarlo preferentemente 2-3 semanas antes del inicio de la quimioterapia, o lo antes posible en caso de tratamiento anticipado. La duración del tratamiento no está bien establecida, aunque se recomienda mantenerlo hasta 6 meses tras completar la quimioterapia, o incluso 12 meses si ha recibido rituximab, alentuzumab y en el TPH. Lamivudina suele ser bien tolerada y presenta una escasa toxicidad, pero puede provocar acidosis láctica con esteatosis hepática. El desarrollo de resistencias no es frecuente en pacientes con HbeAg negativo y suele ocurrir después de 12-15 meses de tratamiento con la selección de la mutación YMDD, que se puede genotipar en nuestro centro. En los pacientes con HbeAg positivo, el desarrollo de resistencias ocurre en el 15% de los casos tras un año de tratamiento y en el 38% de los pacientes tras dos años de tratamiento. En ese caso, el paciente presentará aumento de transaminasas y de DNA VHB a pesar del tratamiento. Los fármacos de segunda linea son tenofovir, adefovir y entecavir, activos frente a las cepas con la mutación YMDD. Interferon alfa, utilizado para controlar la infección crónica por VHB, puede empeorar el cuadro en el contexto de una reactivación ya que aumenta la respuesta inmunitaria contra VHB con el consecuente daño hepatocelular por lo que no se recomienda su uso. 5 7. Algoritmo 6 Hepatitis C 1. Complicaciones del TPH relacionadas con VHC Corto plazo El paciente con infección crónica por VHC sometido a un TPH suele presentar una elevación leve de la ALT en los primeros 3 meses post trasplante. El principal problema es la dificultad para diferenciar este cuadro de la enfermedad del injerto contra el huesped (EICH), incluso en presencia de afectación de otros órganos por lo que suele ser necesaria la realización de una biopsia hepática. Posteriormente, coincidiendo con la disminución de la inmunosupresión y la recuperación de la inmunidad celular, los pacientes pueden presentar una hepatitis tardía, clínicamente indistinguible del EICH hepático. El papel del VHC en el desarrollo de la enfermedad veno oclusiva hepática ha sido objeto de debate con estudios prospectivos con resultados discordantes. La mayoría no encontraba diferencias significativas entre el grupo de pacientes infectados con VHC y el grupo sin infección, y uno de ellos identifica la infección por VHC como factor de riesgo únicamente si se acompaña de elevación de transaminasas previas al TPH. Largo plazo La infección por VHC no ha sido considerada un problema importante en el contexto del TPH. Sin embargo, en estudios de seguimiento a largo plazo se ha podido evaluar los efectos de VHC en los pacientes trasplantados. En estos estudios no se asoció la infección por VHC con exceso de mortalidad a los 10 años, pero sí con evolución más precoz hacia la cirrosis. Así, el tiempo medio esperado hacia la cirrosis en estos pacientes es de 18 años, comparado con los 40 años de los pacientes no trasplantados. Los posibles factores que lo explican son el aumento de carga viral durante la inmunosupresión con el consecuente 7 daño hepático al recuperar la inmunidad, y la concomitancia de otros factores de riesgo de fibrosis hepática presentes en el paciente trasplantado (sobrecarga férrica, resistencia insulínica por corticoides, esteatosis hepática por nutrición parenteral total). 2. Cribado de VHC y actitud Es necesario determinar los anticuerpos totales anti-VHC en todos los donantes y receptores de progenitores hematopoyéticos y confirmar los resultados positivos con la detección de RNA-VHC. El manejo de la infección por VHC en el TPH ha sido objeto de escasos estudios. En el paciente pediátrico, además, no existe un consenso claro de indicaciones de tratamiento que debe ser individualizado. 1. Donante RNA-VHC (+): No es una contraindicación absoluta. Si es posible, priorizar un donante alternativo. En caso contrario, se puede administrar interferon alfa pegilado y ribavirina al donante para reducir la carga viral pretrasplante. 2. Receptor RNA-VHC (+): Es necesario realizar un Fibroscan y/o una biopsia hepática para valorar el grado de fibrosis. Dado que el tratamiento con interferon alfa pegilado y ribavirina presenta efectos secundarios hematológicos (especialmente anemia y trombocitopenia) entre otros, parece prudente postponer su administración unos meses en caso de cumplir criterios de tratamiento. Se ha probado la administración de ribavirina oral para prevenir la afectación hepática del post trasplante inmediato siendo el tratamiento bien tolerado y efectivo pero con series publicadas pequeñas. 3. Receptor Anticuerpos anti-VHC (+), RNA-VHC (-): Se trata de una infección por VHC curada y no es necesaria ninguna precaución suplementaria. 8 3. Algoritmo 9 Bibliografía 1. Lalazar G, Rund D, Shouval D. Screening, prevention and treatment of viral hepattitis B reactivation in patients with haematological malignancies. Br J Haematol 2007;136:699-712. 2. Kempinska A, Kwak EJ, Angel JB. Reactivation of hepatitis B infection following allogenic bone marrow transplantation in a hepatitis b-immune patient: case report and review of the literature. Clin Infect Dis 2005;41:1277-82. 3. Liang R. How I treat and monitor viral hepatitis B infection in patients receiving intensive immunosuppressive therapies or undergoing hematopoietic stem cell transplantation. Blood 2009;113(14):3147-53. 4. Carpenter PA, Huang M, McDonald GB. Activation of occult hepatitis B from a seronegative patient after hematopoietic cell transplant: a cautionary tale. Blood 2002;99(11):4245-6. 5. Orlando R, Tosone G, Tiseo D et al. Severe reactivation of hepatitis B virus infection in a patient with hairy cell leukemia: should lamivudine prophylaxis be recommended to HbsAg-Negative, Anti-HBc-Positive patients? Infection 2006;34(5):282-4. 6. Loomba R, Rowley A, Wesley R et al. Systematic review: the effect of preventive lamivudine on hepatitis B reactivation during chemotherapy. Ann Intern Med 2008;148:519-28. 7. Peffault de Latour R, Ribaud P, Robin M, Valla D, Marcellin P, Socié G et al. Allogeneic hematopoietic cell transplant in HCV-infected patients. J Hepatol. 2008;48(6):1008-17. 8. Francisci D, Aversa F, Coricelli V, Carotti A, Canovari B, Falcinelli F et al. Prevalence, incidence and clinical outcome of hepatitis B virus and hepatitis C virus hepatitis in patients undergoing allogeneic hematopoietic stem cell transplantation between 2001 and 2004. Haematologica. 2006;91(7):980-2. 9. Locasciulli A, Testa M, Valsecchi MG, Bacigalupo A, Solinas S, Tomas JF et al. The role of hepatitis C and B virus infections as risk factors for severe liver complications following allogeneic BMT: a prospective study by the Infectious Disease Working Party of the European Blood and Marrow Transplantation Group. Transplantation. 1999;68(10):148691. 10